26 липня, 2021
Профіль безпеки та переносимості біластину при хронічній кропив’янці у дітей
Хронічна кропив’янка (ХК) – захворювання, що вкрай негативно впливає на якість життя та щоденну діяльність дітей, погіршуючи сон та знижуючи продуктивність навчання у школі. Враховуючи тривалість лікування, хороша переносимість фармакологічних засобів має неабияке значення для досягнення успішного контролю симптомів захворювання та високої комплаєнтності лікування.
Кропив’янка (urticaria) – це розповсюджена хвороба, клінічними проявами якої є поява пухирів, ангіоневротичного набряку (ангіоедеми) або їх комбінації. Багато симптомів кропив’янки виникають перш за все через дію гістаміну на H1-рецептори. Згідно з доступними науковими даними останніх років, враховуючи механізм виникнення кропив’янки, тривале лікування H1-антигістамінними препаратами (АГП) має вирішальне значення при лікуванні кропив’янки.
Метою лікування ХК є досягнення повного контролю над її симптомами за допомогою препаратів з високим профілем безпеки, при цьому зберегти високий рівень якості життя кожного окремого пацієнта. Важливим аспектом лікування ХК у дітей є безперервність. Саме тому, враховуючи хороший профіль безпеки, мінімальні когнітивні та антимускаринові побічні ефекти і тривалу дію, як терапію першої лінії рекомендується використовувати АГП 2 покоління. Хоча багато клініцистів досі використовують для лікування дітей Н1-АГП 1 покоління, які мають виражену седативну дію, помилково припускаючи, що їх профіль безпеки є більш вивченим, у сучасних клінічних настановах наполегливо рекомендується не використовувати АГП 1 покоління для лікування кропив’янки у немовлят та дітей, натомість заохочується застосування сучасних АГП 2 покоління, які не мають седативного ефекту та антихолінергічної дії (T. Zuberbier et al., 2018).
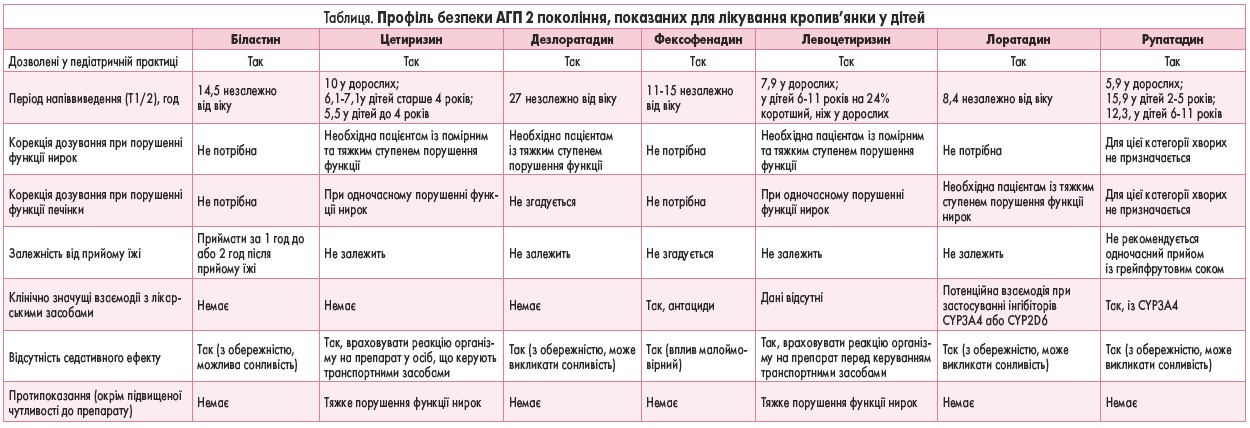
Для ефективного та безпечного використання АГП у клінічній практиці важливу роль відіграє розуміння фармакологічних характеристик окремих засобів. У таблиці наведено порівняння профілю безпеки біластину (Ніксар®) як найновішого АГП 2 покоління з іншими АГП 2 покоління.
Біластин (Ніксар®) – неседативний H1-АГП 2 покоління, який не проникає крізь гематоенцефалічний бар’єр (ГЕБ). Схвалений в Європі для лікування алергічного ринокон’юнктивіту (АРК) та кропив’янки у дорослих і дітей віком ≥6 років із масою тіла ≥20 кг (M. Rodriguez et al., 2020; C. Bachert et al., 2010; Medicines and Healthcare products Regulatory Agency (MHRA), 2018; Z. Novak et al., 2016). Нещодавно біластин також був затверджений у Мексиці для лікування дітей віком ≥2 років (M. Rodriguez et al., 2020).
Фармакологічні характеристики біластину
У дослідженнях in vitro біластин продемонстрував високу селективність/афінність до H1-антигістамінових рецепторів. При цьому H1-рецептори довго залишаються зв’язаними, що забезпечує високу тривалість дії препарату (N.G. Papadopoulos et al., 2020; M.K. Church et al., 2011; R. Bosma et al., 2018). Біластин швидко всмоктується після прийому (N. Jauregizar et al., 2009) та не взаємодіє суттєво із системою ферментів цитохрому Р450, що разом із відсутністю метаболізму в печінці мінімізує здатність препарату до міжлікарських взаємодій (X.Y. Wang et al., 2016; M.L. Lucero et al., 2012). Дослідження на здорових добровольцях показали, що відчутний ефект біластину виявляють вже через 1 годину, а його ефективність в усуненні свербежу краща, ніж у дезлоратадину (р<0,05) та рупатадину (р<0,01; R. Antonijoan et al., 2017). Висока спорідненість біластину до транспортних білків ГЕБ, зокрема Р-глікопротеїну (P-ГП), значно зменшує ймовірність седативного ефекту й впливу на центральну нервову систему (X.Y. Wang et al., 2016; M.L. Lucero et al., 2012). Позитронно-емісійний (ПЕТ) вимір окупації H1-рецепторів головного мозку демонструє, що здатність біластину зв’язуватися із церебральними Н1-гістаміновими рецепторами (H1RO) складає близько 0%, що дозволяє розглядати його як антигістамінний препарат, який не проникає до головного мозку (H. Kawauchi et al., 2019; M. Farre et al., 2014). Здатність окремих АГП зв’язуватися із церебральними Н1-гістаміновими рецепторами показана на рисунку.
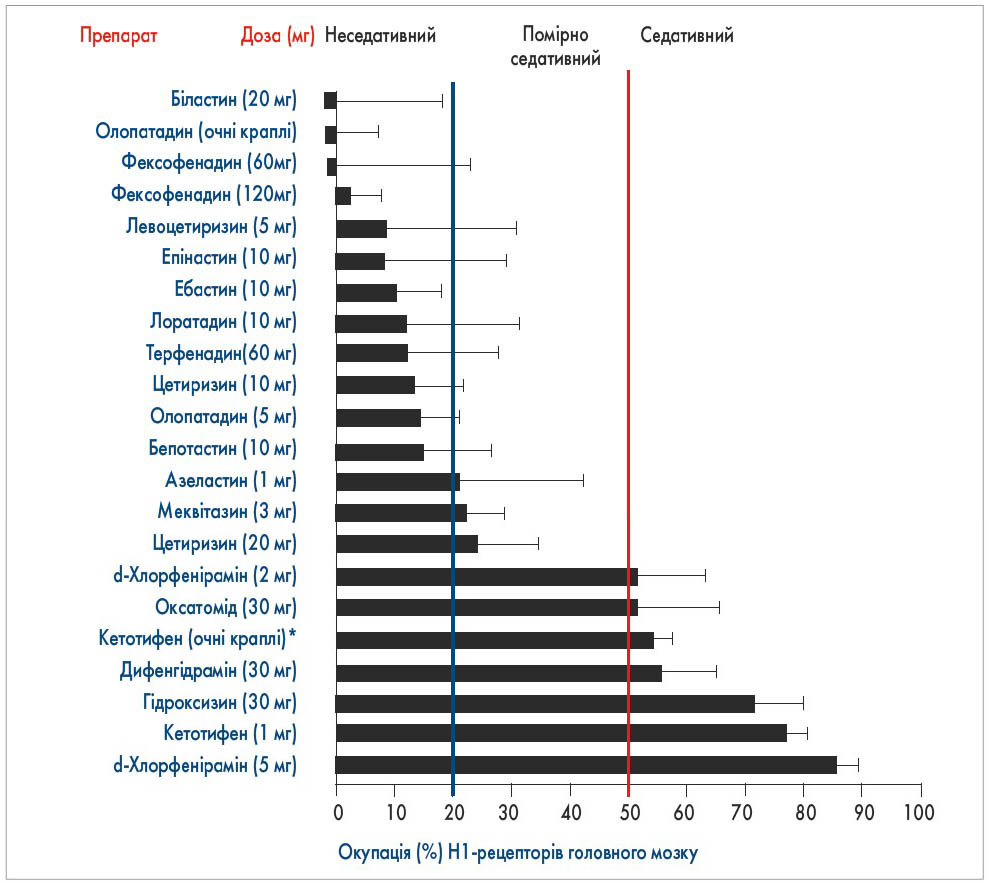 Рис. Окупація (%) Н1-рецепторів головного мозку пероральними антигістамінними препаратами
Рис. Окупація (%) Н1-рецепторів головного мозку пероральними антигістамінними препаратами
Ефективність біластину у дорослих
Ефективність біластину (Ніксар®) для лікування кропив’янки у дорослих була продемонстрована у рандомізованому клінічному дослідженні (T. Zuberbier et al., 2010). Так, біластин та левоцетиризин значно ефективніше, у порівнянні із плацебо, знижували середню загальну оцінку симптомів (total symptom score; TSS), кількість і максимальний розмір пухирів (p<0,001), а також достовірно покращували якість життя пацієнтів, що оцінювалася за допомогою дерматологічного індексу якості життя (The Dermatology Life Quality Index – DLQI): біластин -9,45±6,98 (р<0,001), левоцетиризин -8,94±6,53 (р<0,001) та плацебо -5,93±7,67.
Безпека біластину у дорослих
Біластин продемонстрував сприятливий профіль безпеки у рандомізованому клінічному дослідженні (РКД) та у дослідженнях реальної клінічної практики. Перш за все було відзначено відсутність седативного ефекту, як і очікувалося, для препарату з H1RO близько 0% (N.G. Papadopoulos et al., 2020; X.Y. Wang et al., 2016; H. Kawauchi et al., 2019). В огляді даних клінічних випробувань, опублікованих до 2011 року, M.K. Church та співавт. дійшли висновку, що біластин відповідає усім вимогам щодо тривалої, ефективної та безпечної терапії (M.K. Church et al., 2018). Відсутність впливу на центральну нервову систему та на інтервал QT у дорослих (B. Tyl et al., 2012; M.K. Church et al., 2018) зумовили проведення подальших досліджень дії препарату Ніксар® на дітей.
Ефективність та безпека біластину в педіатричній практиці
План педіатричних досліджень був розроблений відповідно до вимог Педіатричного комітету Європейського агентства з лікарських засобів (ЕМА; X.Y. Wang et al., 2016), згідно з яким серед АГП 2 покоління досліджували лише біластин та рупатадин .
Дозування біластину для дітей вивчали шляхом застосування напівмеханістичного підходу з метою прогнозування фармакокінетики біластину у дітей, припускаючи ту саму фармакодинаміку, що описана у дорослих. Доза біластину 10 мг/добу виявилася достатньою для підтримки інгібувального ефекту протягом усього інтервалу введення доз (24 год) у дітей від 2 до 12 років та забезпечувала системну експозицію і фармакодинамічні результати, еквівалентні дозі 20 мг у дорослих (V. Vozmediano et al., 2019).
Безпеку біластину в дозі 10 мг вивчали у рандомізованому контрольованому дослідженні із включенням 509 дітей із АРК або ХК віком 2-11 років. Статистично достовірної різниці у дітей без побічних реакцій з груп біластину та плацебо виявлено не було. Крім того, біластин продемонстрував порівнянні з плацебо результати за 4 параметрами педіатричного опитувальника якості сну (пов’язане зі сном порушення дихання, денна сонливість, хропіння та неуважність).
M. Rodriguez та співавт. провели оцінку результатів двох ретроспективних аналізів ФК та безпеки застосування біластину в дозі 10 мг/добу для терапії у дітей віком 6-11 років, хворих на АРК або ХК. Показники площі під кривою плазмової концентрації (AUC0-24) та максимальної концентрації в плазмі (Cmax) у дитячій (6-11 років) та дорослій групах виявилися дуже схожими: медіана AUC0-24 у педіатричній і дорослій групах становила 1045 (381) та 1121 (387) нг/год/мл відповідно, а медіана Cmax – 212,0 (123) та 232,5 (120) нг/мл відповідно; концентрація біластину в плазмі крові у дітей повністю збігалася з показниками дорослих, а співвідношення діти/дорослі для AUC0-24 та Cmax дорівнювали приблизно одиниці (0,93 та 0,91 відповідно). Ці результати свідчать на користь застосування біластину в дозі 10 мг у педіатричній практиці.
Статистично значущої різниці в частоті небажаних явищ у ході лікування у дітей, які отримували біластин або плацебо, не спостерігали. Найчастішими небажаними явищами, що виникали із частотою понад 5% в обох групах, були: головний біль (13,4 проти 12,6%), алергічний кон’юнктивіт (9,9 проти 9,4%), кашель (8,9 проти 7,9%), назофарингіт (7,9 проти 4,7%), фарингіт (7,4 проти 6,8%), алергічний риніт (6,4 проти 10,0%), підвищення температури тіла (5,0 проти 10,0%) та вірусна інфекція (4,5 проти 5,2%). Ці результати підтверджують, що профіль безпеки та переносимості біластину в дозі 10 мг у дітей подібний до такого плацебо (M. Rodriguez et al., 2020).
Таким чином, сучасний АГП Ніксар® (біластин) демонструє високу ефективність, швидкий початок і значну тривалість дії, а також хорошу переносимість дорослими та дітьми із мінімальним седативним ефектом і низькою схильністю до взаємодії з іншими препаратами.
Підготувала Ольга Нестеровська
Тематичний номер «Педіатрія» № 3 (59) 2021 р.