10 березня, 2026
Інтерферон a-2b як лікарський засіб противірусної дії широкого спектра для профілактики і лікування грипу та ГРВІ
 Небезпечні медичні та соціальні наслідки епідемій респіраторних вірусних інфекцій, зокрема грипу і COVID-19, спонукали провідні медичні асоціації світу переглянути рекомендації щодо їхньої профілактики і лікування. Через високий ризик госпіталізації та смерті від грипу в дітей Американська академія педіатрії (ААР) рекомендує щорічну вакцинацію проти грипу всім дітям без медичних протипоказань, починаючи з 6-місячного віку. Це є важливою стратегією захисту населення, а також зменшення загального тягаря респіраторних захворювань, коли коциркулюють інші віруси. В сезон варто якомога раніше вводити будь-яку ліцензовану вакцину проти грипу відповідно до віку та стану здоров’я, не надаючи переваги одному продукту чи формі над іншими.
Небезпечні медичні та соціальні наслідки епідемій респіраторних вірусних інфекцій, зокрема грипу і COVID-19, спонукали провідні медичні асоціації світу переглянути рекомендації щодо їхньої профілактики і лікування. Через високий ризик госпіталізації та смерті від грипу в дітей Американська академія педіатрії (ААР) рекомендує щорічну вакцинацію проти грипу всім дітям без медичних протипоказань, починаючи з 6-місячного віку. Це є важливою стратегією захисту населення, а також зменшення загального тягаря респіраторних захворювань, коли коциркулюють інші віруси. В сезон варто якомога раніше вводити будь-яку ліцензовану вакцину проти грипу відповідно до віку та стану здоров’я, не надаючи переваги одному продукту чи формі над іншими.
Противірусна хімієпрофілактика рекомендована для запобігання інфекції вірусом грипу як доповнення до вакцинації у певних осіб, особливо у дітей, які ще не були вакциновані, безсимптомних, але з високим ризиком ускладнень від грипу або імуноскомпрометованих.
Госпіталізованим дітям із підтвердженим грипом або грипоподібним захворюванням (лихоманка з кашлем або болем у горлі), з тяжким або прогресуючим перебігом або супутніми захворюваннями, що підвищують ризик ускладнень від грипу, незалежно від тривалості захворювання рекомендоване противірусне лікування. Його слід розпочати якомога швидше. Зокрема і в амбулаторних умовах – для дітей із симптомами грипу без високого ризику ускладнень, якщо це можливо, протягом 48 годин від початку захворювання. Для дітей із підозрою або з підтвердженням захворювання на грип також можна розглянути противірусне лікування, якщо вони контактують із дітьми до 6-місячного віку або з високим ризиком ускладнень [1].
Для специфічної терапії сезонного грипу застосовують інгібітор нейрамінідази озельтамівір [2]. Він впливає на поверхневий глікопротеїн нейрамінідази, пригнічує ферментативну активність, необхідну для брунькування новостворених віріонів із клітин. Це перешкоджає вивільненню потомства вірусу грипу з інфікованих клітин і зупиняє поширення інфекції на нові клітини. Слід зазначити, що нейрамінідаза вірусу грипу А більш чутлива до озельтамівіру, ніж нейрамінідаза вірусу грипу В, концентрація напівмаксимального інгібування (IC50) озельтамівіру для нейрамінідази вірусів грипу А може бути в межах 0,1-1,3 нмоль, тоді як для вірусів грипу В потрібно 2,6-8,5 нмоль [3]. І хоча у дітей озельтамівір зменшує інтенсивність симптомів грипу, кількість днів госпіталізації (p = 0,001), а також постінфекційні ускладнення (p = 0,005) [4], збільшення застосування озельтамівіру асоціюється із зростанням частоти побічних ефектів [5]. За даними систематичного огляду та метааналізу в амбулаторних пацієнтів, інфікованих грипом А, озельтамівір не знижував ризику госпіталізації, але збільшував кількість побічних ефектів, пов’язаних із шлунково-кишковим трактом [6].
Озельтамівір може застосовуватись лише у пацієнтів із грипом і не розглядається для профілактики та лікування інших гострих респіраторних вірусних захворювань, зокрема коронавірусної інфекції.
! Як відомо, на тяжкість гострої респіраторно-вірусної інфекції впливають такі фактори, як вірусна реплікація, адаптація хазяїна, сигналізація вродженого імунітету, наявний імунітет та вторинні інфекції [7], тому інтерферон розглядають як терапевтичну альтернативу для лікування респіраторно-вірусної інфекції, зокрема грипу і COVID‑19, через його широку противірусну активність [8].
Інтерферони типу I – це група противірусних цитокінів, які індукуються під час вірусної інфекції продуктами реплікації вірусу, такими як дволанцюгова (ds)РНК. Інтерферони виконують свої біологічні функції з допомогою зв’язування зі специфічними рецепторами клітинної поверхні. А це запускає внутрішньоклітинні сигнальні шляхи, переважно шлях JAK–STAT, який зрештою індукує експресію великої кількості генів, стимульованих інтерфероном (ISGs), що призводить до противірусної, антипроліферативної та імунорегуляторної активності у клітинах-хазяїнах. Так, під час грипу рівень інтерферону α‑2 зростає утричі [9].
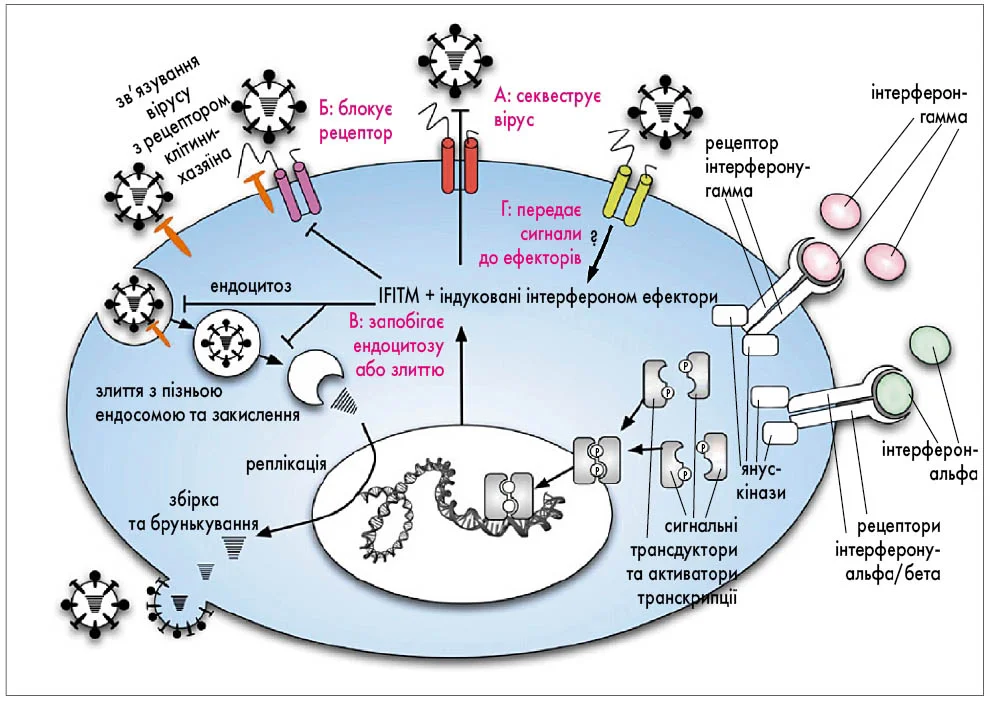
За допомогою функціонального геномного скринінгу з використанням siRNA було ідентифіковано, що індуковані інтерфероном трансмембранні білки (IFITM), зокрема IFITM1, IFITM2 та IFITM3, обмежують ранній етап реплікації вірусу грипу А. IFITM індукуються інтерферонами I та II типів. Водночас білок IFITM3 забезпечує базальну резистентність і є критично важливим для дії інтерферону. Білки IFITM демонструють противірусну активність проти кількох основних людських патогенів: пригнічують ранню реплікацію вірусу грипу А (H1N1), а також флавівірусів включно з вірусом Західного Нілу (WNV) та вірусом Денге (DNV), імовірно, між зв’язуванням вірусу з рецептором хазяїна та проникненням вірусного рибонуклеопротеїнового комплексу (vRNP) у цитозоль [10] (рис.).
Рис. Роль індукованих інтерфероном трансмембранних білків у противірусному захисті [10]
Через активацію сигнального шляху інтерферону І пригнічується реплікація респіраторно-синцитіального вірусу (RSV), зменшується RSV-індуковане запалення та окисний стрес [11].
Але потрібно враховувати, що чи не більшість вірусів розробила широкий спектр стратегій для блокування і перешкоджання шляху інтерферону. Так, відомо про порушення противірусного захисту під час грипу [12]. Загальні вірусні стратегії включають блокування індукції/експресії інтерферону, перехоплення рецепторного зв’язування інтерферону через вірусні рецептори – приманки інтерферону, порушення внутрішньоклітинного сигнального шляху інтерферону, безпосереднє зниження рівня експресії ISGs [13].
Гени, стимульовані інтерферонами I типу, та сигналізація, опосередкована інтерфероном, торпедуються коронавірусами, зокрема SARS-CoV‑2 [9, 14]. Тому коронавіруси (включно із SARS-CoV‑2) активно пригнічують вроджену імунну відповідь, опосередковану інтерфероном I типу. Наприклад, білки SARS-CoV‑2, такі як nsp1, nsp6, nsp13, ORF3a, M та ORF7b, можуть пригнічувати фосфорилювання STAT1 – ключового етапу сигналізації інтерфероном I типу [15, 16].
Порушення активності інтерферону I типу пов’язане з тяжким перебігом COVID‑19 [17]. Так, порівняно з госпіталізованими пацієнтами, у пацієнтів із легким перебігом COVID‑19 була більш виражена на ранніх стадіях противірусна імунна відповідь у верхніх дихальних шляхах, обумовлена вищою активністю NF-kB та ISGs [18]. У пацієнтів із загрозливим для життя COVID‑19 виявлено аутоантитіла проти інтерферону I типу (зокрема інтерферону α‑2b), що призводило до порушень сигналізації інтерферону I типу [19].
! Під час проведення фармакокінетичних досліджень застосування для профілактики і лікування гострої респіраторної вірусної інфекції назальної форми інтерферону α‑2b встановлено, що назальний спрей забезпечує захисний бар’єр у місці інфекції (носовій порожнині та ротоглотці). Це критично важливо, зокрема для профілактики і лікування коронавірусної інфекції, оскільки вірус SARS-CoV‑2 використовує рецептор ACE2, експресія якого найвища саме в носовій порожнині і знижується у нижніх дихальних шляхах [20].
Локальне введення спрея інтерферону α‑2b не призводить до системного впливу на організм через низьку загальну біодоступність, 97% вимірів концентрації інтерферону у зразках плазми крові демонстрували показники менші за нижню межу кількісного значення. Водночас експозиція інтерферону у змивах з носової порожнини зростала зі збільшенням введеної дози [20].
Концентрація інтерферону у носових змивах знижувалася експоненційно з часом відповідно до кінетичних процесів елімінації першого порядку [20].
Концентрація у змивах з носової порожнини основного фармакодинамічного індикатора індукованого інтерфероном білка‑10 (ІР‑10) – хемокіна, який індукується інтерфероном і може сприяти елімінації SARS-CoV‑2, була підвищена, зростала після введення спрея інтерферону α‑2b, досягаючи максимальних значень приблизно через 10 годин, а потім поверталася до базальних значень. Було виявлено достовірний кореляційний зв’язок між експозицією інтерферону і рівнем IP‑10 у носових змивах [20].
Слід зазначити, що концентрації інтерферону у носових змивах були значно вищими за EC50, а ступінь підвищення IP‑10 – приблизно однаковий, що може свідчити про досягнення плато насичення в цьому діапазоні дози – відповіді [20].
У зразках для полоскання ротоглотки не спостерігалося значної кореляції між експозицією інтерферону та рівнями IP‑10. Ймовірно, це пов’язано з тим, що середовище ротової порожнини більше зазнає впливу приймання їжі, пиття і ковтання слини, що призводить до вищої міжіндивідуальної варіабельності та швидшого напіврозпаду інтерферону [20].
Інтерферон α‑2b показав ефективність у профілактиці поширених вірусних респіраторних інфекцій у військових рекрутів. За результатами рандомізованого контрольованого дослідження встановлено, що низька доза рекомбінантного інтерферону α‑2b у формі назального спрея була ефективною для запобігання інфекціям, спричиненим вірусами грипу A, грипу B, парагрипу 1-3 та аденовірусу виду B [21].
В іншому дослідженні з профілактичною метою 1719 працівників сфери туризму отримували інтерферон α‑2b інтраназально щоденно 10 днів. Жодного випадку зараження SARS-CoV‑2 не було виявлено, тоді як серед 369 учасників дослідження, що не отримували профілактично інтерферон α‑2b, зареєстровано 39 випадків COVID‑19 (10,6%) [22].
! Інтерферон α‑2b вважається ідеальним для противірусної терапії широкого спектра, оскільки виявляє плейотропні ефекти, спрямовані на велику кількість стадій життєвого циклу вірусів, і активує відповідну імунну відповідь для очищення від вірусів незалежно від їхнього типу.
Його застосування асоціювалось із зниженням рівня біомаркерів запалення (інтерлейкіну‑6 та C-реактивного білка) [23]. Також інтерферон α‑2b підвищував, порівняно із арбідолом, відсоток CD8+ Т-клітин, що є сприятливим фактором, оскільки їхня низька кількість асоціювалась із тяжкими пошкодженнями легень [23].
За результатами багатьох досліджень встановлено, що застосування інтраназального інтерферону α‑2b пришвидшувало кліренс вірусу COVID‑19 [24]. Так, за результатами відкритого, проспективного когортного дослідження доведено, що застосування спрея інтерферону α‑2b скорочує час вірусного виділення варіанта SARS-CoV‑2 «Омікрон» (11,9 дня проти 12,58 відповідно в експериментальній та контрольній групах, р = 0,024). Найбільш ефективним було застосування спрея інтерферону α‑2b протягом трьох днів із моменту першого позитивного тесту на SARS-CoV‑2 (середній час вірусного виділення у пацієнтів цієї підгрупи становив у середньому 10,41 дня, що було суттєво менше порівняно із пацієнтами із підгрупи пізнього (> 3 дні) лікування – 13,56 дня, р < 0,000) [25]. Також було доведено, що спрей інтерферону α‑2b значно прискорював вірусний кліренс у вакцинованих учасників [25].
Обстеження 268 дітей віком від 1 до 14 років, інфікованих варіантом «Омікрон» SARS-CoV‑2, також показало, що назальний спрей інтерферону α‑2b покращував кліренс вірусу [26].
Хоча за результатами когортного дослідження 54 пацієнтів із помірним перебігом COVID‑19, які були госпіталізовані на початку пандемії 2020 р. та отримували потрійну комбінацію лікування, що включала інгаляційний інтерферон α‑2b (5 мільйонів МО, двічі на день), таблетки лопінавіру (500 мг, двічі на день) та гранули уміфеновіру (200 мг, тричі на день), не виявлено переконливих доказів щодо ключової ролі часу початку терапії у прогнозі помірно тяжкого перебігу [27], в особливо важких/критичних випадках застосування інтерферону α‑2b може сприяти одужанню і зниженню летальності (0,9% проти 32,1%) при COVID‑19 порівняно з тими, хто не отримував інтерферон [28].
Інтерферон α‑2b забезпечує високий ефект під час лікування дітей із вірусною пневмонією, покращуючи клінічні симптоми, зменшуючи запальну реакцію з хорошим профілем безпеки [29]. Введення інгаляційно високих доз інтерферону α‑2b пацієнтам із COVID‑19 значно зменшувало тяжкість пневмонії і потребу в штучній вентиляції легень [30].
За результатами рандомізованого, подвійного сліпого, плацебоконтрольованого дослідження спрея людського інтерферону α‑2b у здорових людей встановлено його безпечність під час введення через назальний і ротоглотковий шляхи. У дослідженні не було зафіксовано серйозних побічних явищ, не йшлося про припинення участі через побічні явища або необхідність корегування дози [20]. У деяких пацієнтів назальне введення інтерферону α‑2b асоціювалось із сухістю носоглотки та носовими кровотечами [21], закладеністю носа, головним болем, ринореєю [22], транзиторною лихоманкою, розладами травлення чи втомою [26]. Відсутність серйозних побічних ефектів є перевагою назальних форм порівняно з парентеральними, які можуть викликати грипоподібні симптоми та інші системні побічні реакції [25].
Препарат Лаферобіон® містить інтерферон α‑2b. У формі інтраназальних крапель і спрея він застосовується для профілактики, а у формі супозиторіїв – для лікування пацієнтів із тяжкими формами гострої респіраторно-вірусної інфекції.
За результатами проведеного в Україні дослідження встановлено, що використання препаратів інтерферону у формі супозиторіїв при неускладнених рецидивних ГРВІ порівняно з дітьми із контрольної групи сприяло скороченню тривалості підвищеної температури тіла (відповідно 3,9 ± 0,59 дня проти 4,8 ± 0,21 дня), інтоксикації (відповідно 4,1 ± 0,44 дня проти 5,6 ± 0,71 дня), катарального синдрому (відповідно 5,7 ± 0,82 дня проти 6,5 ± 0,32 дня), а також скороченню термінів прийому препаратів для симптоматичного лікування, зокрема жарознижувальних, в середньому на 1,4 дня. У дітей із основної групи швидше нормалізувався апетит (на 4,4 ± 0,42 дня проти 5,8 ± 0,51 дня), сон (4,7 ± 0,63 дня проти 5,9 ± 0,54 дня) та загальний стан (4,1 ± 0,62 дня проти 5,7 ± 0,65 дня у контрольній групі). Найважливішим результатом застосування супозиторіїв препарату Лаферобіон® стала відсутність у дітей із основної групи бактеріальних ускладнень й, відповідно, потреби у антибіотикотерапії, тоді як 20% дітей із контрольної групи отримували антибіотикотерапію через бактеріальний риносинусит або отит, затяжний бронхіт, в одному випадку – пневмонію [31].
Отже, препарат Лаферобіон® (інтерферон α‑2b) завдяки широкому спектру дії можна ефективно та безпечно використовувати для профілактики і лікування гострої респіраторної вірусної інфекції, зокрема грипу і коронавірусної інфекції.
Література
- Committee on Infectious Diseases. Recommendations for Prevention and Control of Influenza in Children, 2024-2025: Policy Statement. Pediatrics. 2024 Oct 1;154(4): e2024068507. doi: 10.1542/peds.2024-068507. PMID: 39183669.
- Jones J.C., Yen H.L., Adams P. et al. Influenza antivirals and their role in pandemic preparedness. Antiviral Res. 2023 Feb;210:105499. doi: 10.1016/j.antiviral.2022.105499. Epub 2022 Dec 23. PMID: 36567025; PMCID: PMC9852030.
- https://likicontrol.com.ua/%D1%96%D0%BD%D1%81%D1%82%D1%80%D1%83%D0%BA%D1%86%D1%96%D1%8F/?[14215].
- Jugulete G., Olariu M.C., Stanescu R. et al. The Clinical Effectiveness and Tolerability of Oseltamivir in Unvaccinated Pediatric Influenza Patients during Two Influenza Seasons after the COVID‑19 Pandemic: The Impact of Comorbidities on Hospitalization for Influenza in Children. Viruses. 2024 Oct 7;16(10):1576. doi: 10.3390/v16101576. PMID: 39459910; PMCID: PMC11512198.
- Tokunaga M., Kikuchi D., Noda A. et al. Trends in Anti-Influenza Drug Prescription and Adverse Drug Reaction Reporting After the Lifting of Oseltamivir Prescribing Restrictions in Pediatric Outpatients: An Ecological Study Using the MDV Analyzer® And the Japanese Adverse Drug Event Report Database. Drugs Real World Outcomes. 2024 Jun;11(2):177-184. doi: 10.1007/s40801-023-00414-x. Epub 2024 Jan 18. PMID: 38236514; PMCID: PMC11176281.
- Hanula R., Bortolussi-Courval E., Mendel A. et al. Evaluation of Oseltamivir Used to Prevent Hospitalization in Outpatients With Influenza: A Systematic Review and Meta-Analysis. JAMA Intern Med. 2024 Jan 1;184(1):18-27. doi: 10.1001/jamainternmed.2023.0699. Erratum in: JAMA Intern Med. 2024 Jan 1;184(1):121. doi: 10.1001/jamainternmed.2023.4905. Erratum in: JAMA Intern Med. 2024 Jan 1;184(1):115-116. doi: 10.1001/jamainternmed.2023.4708. PMID: 37306992; PMCID: PMC10262060.
…
31. Няньковський С.Л., Яцула М.С., Бережна І.Ю., Романів О.І. (2019) Ефективність та доцільність використання інтерферонів під час лікування рекурентної респіраторної вірусної інфекції у дітей. Здоров’я України, 3(50): 20-21 (https://health-ua.com/multimedia/userfiles/files/2019/Pediatria_3_2019/Pediatria_3_2019_str_19_21.pdf).
Повний список літератури – в редакції.
Ця інформація надана компанією ДП «СТАДА-Україна» в якості професійної підтримки фахівцям охорони здоров'я. Інформація, що стосується будь-якого продукту(ів), може не збігатися з інструкцією для медичного застосування препарату. Будь ласка, ознайомтеся з повним текстом інструкції для отримання точної інформації або даних щодо продуктів, які розглядають у цій публікації, до призначення.
HCP-LAF-01-26122025
Тематичний номер «Педіатрія» № 1 (82) 2026 р.



 Хайтович М.В.
Хайтович М.В.