25 березня, 2026
Взаємозв’язок гострих респіраторних інфекцій та атопічних захворювань у дітей: патогенетичні механізми і підходи до лікування
 Гострі респіраторні вірусні інфекції (ГРВІ) залишаються однією з найактуальніших проблем педіатричної практики: щорічно в Україні вони вражають понад 14 млн осіб, становлячи близько 90% усієї інфекційної захворюваності. Діти хворіють на ГРВІ в 3-7 разів частіше, ніж дорослі, однак медико-соціальне значення проблеми виходить за межі епізодичної захворюваності – накопичено переконливі докази того, що ГРВІ є важливим фактором ризику формування рецидивних, хронічних та алергічних захворювань у дітей зі спадковою схильністю до атопії. Цій темі присвячена доповідь Тетяни Рудольфівни Уманець, доктора медичних наук, головного наукового співробітника відділення імунозалежних станів, ревматичних та респіраторних хвороб у дітей ДУ «Всеукраїнський центр материнства та дитинства НАМН України», представлена в межах майстеркласу Української академії педіатричних спеціальностей «PedSMART Вакцинація».
Гострі респіраторні вірусні інфекції (ГРВІ) залишаються однією з найактуальніших проблем педіатричної практики: щорічно в Україні вони вражають понад 14 млн осіб, становлячи близько 90% усієї інфекційної захворюваності. Діти хворіють на ГРВІ в 3-7 разів частіше, ніж дорослі, однак медико-соціальне значення проблеми виходить за межі епізодичної захворюваності – накопичено переконливі докази того, що ГРВІ є важливим фактором ризику формування рецидивних, хронічних та алергічних захворювань у дітей зі спадковою схильністю до атопії. Цій темі присвячена доповідь Тетяни Рудольфівни Уманець, доктора медичних наук, головного наукового співробітника відділення імунозалежних станів, ревматичних та респіраторних хвороб у дітей ДУ «Всеукраїнський центр материнства та дитинства НАМН України», представлена в межах майстеркласу Української академії педіатричних спеціальностей «PedSMART Вакцинація».
Сучасна концепція взаємозв’язку між респіраторними інфекціями та атопічними захворюваннями ґрунтується на теорії подвійного удару (Wadhwa V., 2024): ГРВІ в ранньому дитячому віці у дітей із генетичною схильністю до атопії підвищують ризик маніфестації бронхіальної астми та негативно впливають на легеневу функцію. Аналіз даних 150 тис. дітей віком від 6 місяців до 5 років підтвердив достовірно підвищений ризик зниження легеневої функції та формування бронхіальної астми у віці 6-7 років після перенесеної інфекції нижніх дихальних шляхів (van Meel E.R., 2022), а окремий метааналіз розширив цей зв’язок до алергічного ринокон’юнктивіту та інших алергічних проявів (Kenmoe S., 2020). Показово, що взаємозв’язок не обмежується постнатальним періодом: респіраторна інфекція у матері під час вагітності підвищує ризик розвитку алергічного риніту (АР) у дитини, а перенесена інфекція верхніх дихальних шляхів у дітей до двох років асоціюється з подальшим формуванням АР (Chen J., 2023).
Імунологічні механізми взаємодії вірусної інфекції та алергічного запалення
Ключем до розуміння тяжкого і тривалого перебігу ГРВІ у дітей з атопією є імунологічні механізми. Повторні інфекції у таких дітей є наслідком значної дисфункції імунної системи, яка зачіпає не лише вроджені, а й адаптивні компоненти імунітету. Важливою ланкою є синергічна імунна відповідь: за умови одночасного впливу вірусної інфекції та алергенної експозиції виникає взаємне посилення обох патологічних процесів, що клінічно проявляється тривалішим і тяжчим перебігом ГРВІ (Wadhwa V., 2024).
Варто пам’ятати важливу деталь: діти зі схильністю до алергії мають вроджену незрілість вироблення інтерферону респіраторним епітелієм під час вірусної атаки. Ця незрілість створює сприятливі умови для активної вірусної реплікації та, як наслідок, загострення атопічного процесу. Паралельно відбувається посилення експресії молекул ICAM‑1 – молекул адгезії, які водночас є основним рецептором для риновірусу. Цей механізм забезпечує ефективне прикріплення вірусу до епітеліального шару та реалізацію його патогенної дії (Green R.J., 2015).
Ще одним важливим елементом патогенезу є вплив вірусу на експресію високоафінних рецепторів до специфічних IgE у сенсибілізованих дітей. За умови одночасної дії вірусу та алергену активується Th2-опосередковане запалення з посиленою продукцією інтерлейкінів 4 та 13, які пригнічують інтерферонну відповідь респіраторного епітелію і дендритних клітин, сприяючи вірусній реплікації та підтримуючи алергічне запалення. Так формується патологічне зачароване коло, в якому інфекційний та алергічний процеси постійно посилюють один одного (Schatz M., 2018).
Клінічні прояви та лікувальна тактика у дітей з атопією на тлі ГРВІ
Практичне значення описаних механізмів проявляється в конкретних клінічних ситуаціях. Найчастіший сценарій – риновірусна інфекція у пацієнта з алергічним ринітом, за якої формується змішана форма захворювання з затяжним і тяжчим перебігом та суттєво гіршою відповіддю на традиційну антиалергічну терапію, що необхідно враховувати під час планування лікування (De Corso E., 2020; Smulders T., 2024).
Патогенетичним підґрунтям алергічної симптоматики, що розвивається або посилюється на тлі вірусної інфекції, є активація базофілів і мастоцитів із вивільненням гістаміну – ключового медіатора ранньої фази алергічної відповіді. Доведено, що респіраторна вірусна інфекція у дітей з атопією призводить до підвищення концентрації гістаміну й еозинофілів і при АР, і при бронхіальній астмі, а також їхньому поєднанні. Саме ця ланка патогенезу обґрунтовує застосування антигістамінних препаратів у дітей з алергічними захворюваннями на тлі ГРВІ. Важливо наголосити: йдеться виключно про дітей з атопічною патологією, оскільки у здорових дітей антигістамінні препарати при ГРВІ не мають доказової бази і можуть навіть завдавати шкоди (Kudryavtseva A.V., 2019; Bezirganoglu H., 2022).
Антигістамінні препарати нового покоління є засобами першої лінії у лікуванні АР та гострої кропив’янки. На відміну від препаратів першого покоління з їхньою холінолітичною активністю, кардіотоксичністю і ризиком тахіфілаксії, синтезована у 2010 р. молекула біластину не проникає через гематоенцефалічний бар'єр, що забезпечує відсутність седативного та інших системних побічних ефектів. Оригінальним препаратом біластину в Україні є Ніксар®, порівняльний аналіз якого з іншими антигістамінними засобами підтверджує суттєво нижче проникнення в тканини головного мозку (Wise S.K., 2023).
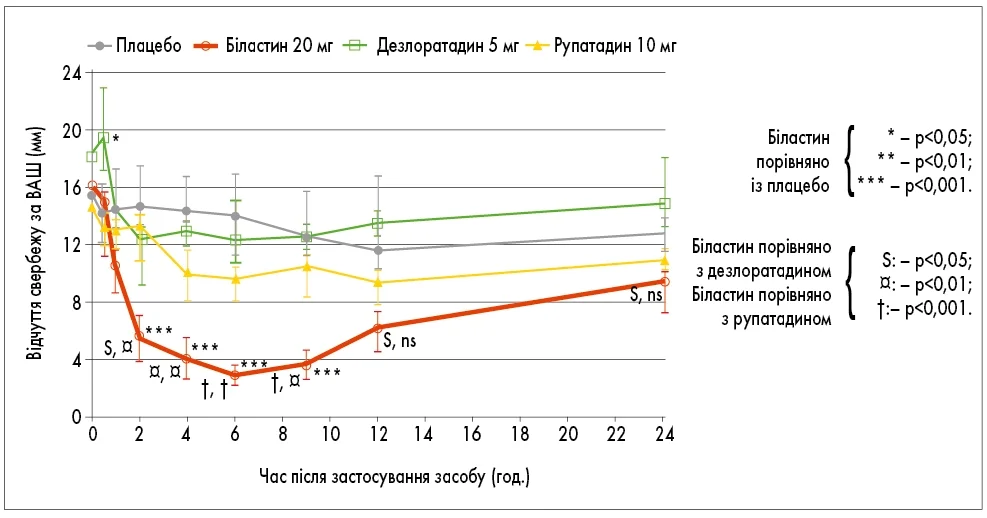
Клінічна ефективність препарату Ніксар® підтверджена щодо обох показань. При алергічному риніті ефект розвивається через 1 годину та підтримується 24 години, забезпечуючи одноразовий прийом на добу. При гострій кропив'янці біластин у дозі 20 мг суттєво пригнічував свербіж і утворення пухирів, перевершуючи дезлоратадин, рупатадин і плацебо, тоді як два останні препарати від плацебо не відрізнялися (рис. 1; Antonijoan R., 2017).
Рис. 1. Біластин у дозі 20 мг суттєво зменшив відчуття свербежу порівняно з дезлоратадином у дозі 5 мг, рупатадином у дозі 10 мг і плацебо протягом 2-12 год.
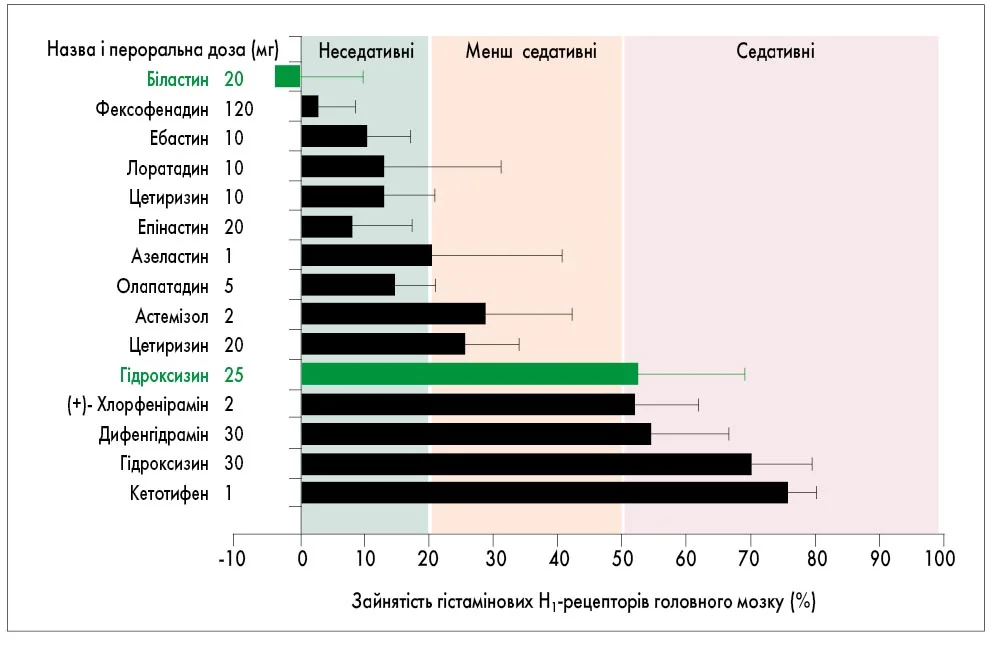
Щодо впливу на центральну нервову систему, дослідження позитронно-емісійної томографії показали, що зайнятість H1-рецепторів мозку на тлі біластину 20 мг була порівнянною з плацебо і значно нижчою, ніж під час застосування гідроксизину 25 мг (рис. 2; Jauregui I., 2016).
Рис. 2. Зайнятість гістамінових H1-рецепторів головного мозку (середній відсоток ± стандартне відхилення) антигістамінними препаратами
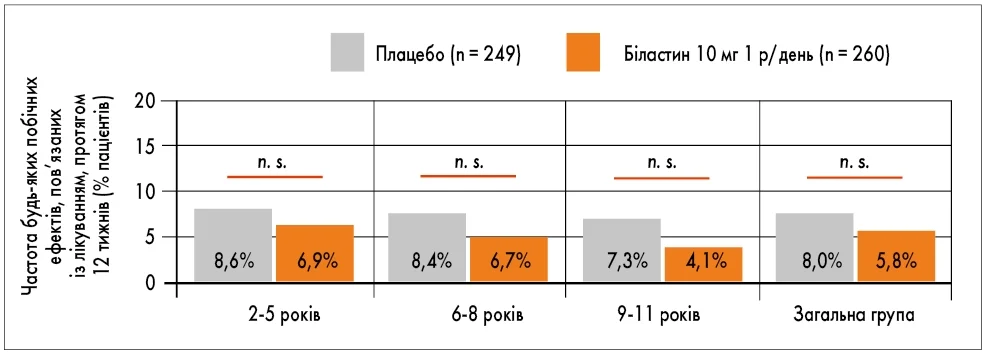
Безпечність у педіатричній популяції підтверджена в рандомізованому подвійному сліпому дослідженні III фази за участі 509 дітей віком 2-11 років: біластин 10 мг був порівнянний із плацебо за частотою побічних ефектів протягом 12 тижнів (рис. 3; Novak Z., 2016; Kuna P., 2016).
Рис. 3. Біластин у дітей від 2 до 11 років був подібним до плацебо щодо частоти побічних ефектів протягом 12 тижнів лікування
Отже, діти з атопічними захворюваннями та з групи ризику щодо атопії мають підвищену схильність до ГРВІ, а на тлі вірусної інфекції відбувається патогенетично обґрунтоване посилення алергічного запалення. Саме тому ведення таких пацієнтів потребує комплексного підходу, що включає адекватний контроль алергічного компонента – зокрема застосування препарату Ніксар® при алергічному риніті та гострій кропив’янці.
Підготував Максим Голуб
Тематичний номер «Педіатрія» № 1 (82) 2026 р.