16 грудня, 2021
Коморбідна патологія та її роль у клінічному перебігу подагри
 28-30 жовтня відбувся Національний конгрес ревматологів України, під час якого було висвітлено різноманітні аспекти діагностики та новинки в галузі лікування ревматологічних захворювань. Доповідь на тему «Коморбідна патологія та її роль у клінічному перебігу подагри» представила професор кафедри терапії, кардіології та сімейної медицини ФПО Дніпровського державного медичного університету, доктор медичних наук Ганна Петрівна Кузьміна.
28-30 жовтня відбувся Національний конгрес ревматологів України, під час якого було висвітлено різноманітні аспекти діагностики та новинки в галузі лікування ревматологічних захворювань. Доповідь на тему «Коморбідна патологія та її роль у клінічному перебігу подагри» представила професор кафедри терапії, кардіології та сімейної медицини ФПО Дніпровського державного медичного університету, доктор медичних наук Ганна Петрівна Кузьміна.
Вважають, що найпоширенішою формою запального артриту на сьогодні є подагричний. Згідно зі статистичними даними, в Європі його частота становить 0,9-2,5%, а в США – 3,9%.
Рекомендації Європейської протиревматичної ліги (EULAR, 2018) окреслили діагностичну цінність клінічних алгоритмів і способів візуалізації, як-от виявлення кристалів сечової кислоти в синовіальній рідині, ультразвукове дослідження та двоенергетична комп’ютерна томографія.
Ключовим у настанові є розширення показань для початку уратознижувальної терапії (УЗТ) у пацієнтів із подагрою. Велике значення надається призначенню алопуринолу як засобу першої лінії для всіх пацієнтів, яким необхідна УЗТ, включаючи осіб із хронічною хворобою нирок (ХХН). Окрім того, розширено рекомендації стосовно того, кому потрібно визначати HLA-B*5801 до початку застосування алопуринолу.
В настанові рекомендовано застосовувати цільову стратегію з УЗТ для всіх пацієнтів із подагрою, ґрунтуючись на даних останніх клінічних випробувань. Стратегія ведення передбачає початок прийому уратознижувального препарату в низькій дозі та подальше її підвищення з метою досягнення й підтримки рівня уратів у сироватці <6 мг/дл для оптимізації результатів лікування на відміну від стратегії фіксованих доз.
Автори пояснюють, що такий алгоритм сприяє зниженню ризику розвитку побічних ефектів, пов’язаних із лікуванням, як-от гіперчутливість і ймовірність загострень.
Серед інших змін у рекомендаціях EULAR такі:
- показання для початку УЗТ були розширені, тому пацієнтів із нечастими або першими загостреннями подагри можна розглядати, якщо вони також мають помірну чи тяжку ХХН (стадія >3), виражену гіперурикемію (урати сироватки >9 мг/дл) або камені в нирках;
- умовна рекомендація не починати УЗТ пацієнтам без супутніх захворювань, у яких уперше виникло загострення подагри;
- наполеглива рекомендація застосовувати протизапальні профілактичні засоби, як-от колхіцин, нестероїдні протизапальні препарати або преднізолон, протягом щонайменше 3-6 міс (не менш як 3 міс у разі початку УЗТ) з постійною оцінкою й подовжувати профілактику за потреби, якщо в пацієнта повторно виникають загострення.
За результатами досліджень, проведених у Великій Британії (2020), найпоширенішими коморбідними патологіями при подагрі були артеріальна гіпертензія – АГ (57%), гіперхолестеринемія (28%), цукровий діабет – ЦД (12%), ішемічна хвороба серця (14%), хронічна серцева недостатність (1%), ХХН стадії 3b або вище (4%).
Нині можна чітко стверджувати, що подагра є незалежним фактором ризику серцево-судинних захворювань (ССЗ), як-от ішемічна хвороба серця, серцева недостатність, інсульт, АГ; метаболічного синдрому (МС), оскільки спричиняє розвиток ЦД 2 типу та пов’язана з усіма компонентами МС; захворювань нирок, адже відіграє безпосередню роль у початку та прогресуванні ХХН. У пацієнтів із ХХН середнього й тяжкого ступенів поширеність подагри зростає в 10 разів.
Важливим моментом є наявність нових асоціацій подагри з іншими супутніми захворюваннями (анемією, фібриляцією передсердь, обструктивним апное уві сні, остеопорозом, венозною тромбоемболією й еректильною дисфункцією).
Доречним буде згадати дослідження, яке описує схему чутливості різних наборів шкали генетичного ризику коморбідної патології та різних локусів сечової кислоти. Саме за результатами такого аналізу виділено неплейотропні та плейотропні локуси уратів. Неплейотропні локуси уратів сироватки крові (т. зв. транспортери уратів) асоціюються з подагрою, але не з коморбідною патологією серцево-судинної системи. Плейотропні локуси асоціюються як із подагрою, так і з АГ, гіперхолестеринемією тощо. Існує теорія, що плейотропні ефекти локусів уратів сироватки крові пояснюють зв’язок між подагрою та коморбідною патологією незалежно від рівня сечової кислоти крові.
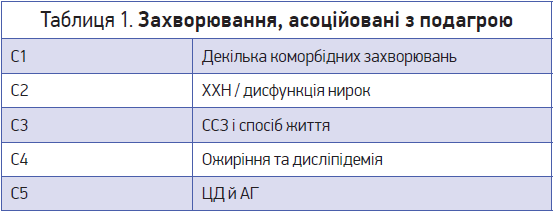
На основі даних зазначеного дослідження проаналізовано коморбідні захворювання, асоційовані з подагрою. Було встановлено п’ять основних кластерів, які описано в таблиці 1.
Показано, що подагра вдвічі частіше розвивається в осіб з анемічним синдромом. Окрім того, анемія була пов’язана з 1,7-разовим збільшенням ризику розвитку подагри після корегування клінічних факторів ризику, а також перебігу анемії та подагри. У багатофакторному логістичному регресійному аналізі, який вивчав зв’язок між анемією та гіперурикемією, анемія була пов’язана з дворазовим збільшенням ризику гіперурикемії у хворих на ХХН. Істотний зв’язок між анемією та гіперурикемією (навіть після корегування швидкості клубочкової фільтрації) свідчить про те, що між цими двома станами існує прямий зв’язок. Анемія збільшує ризик розвитку гіперурикемії в людей віком >65 років, хворих на ЦД й АГ.
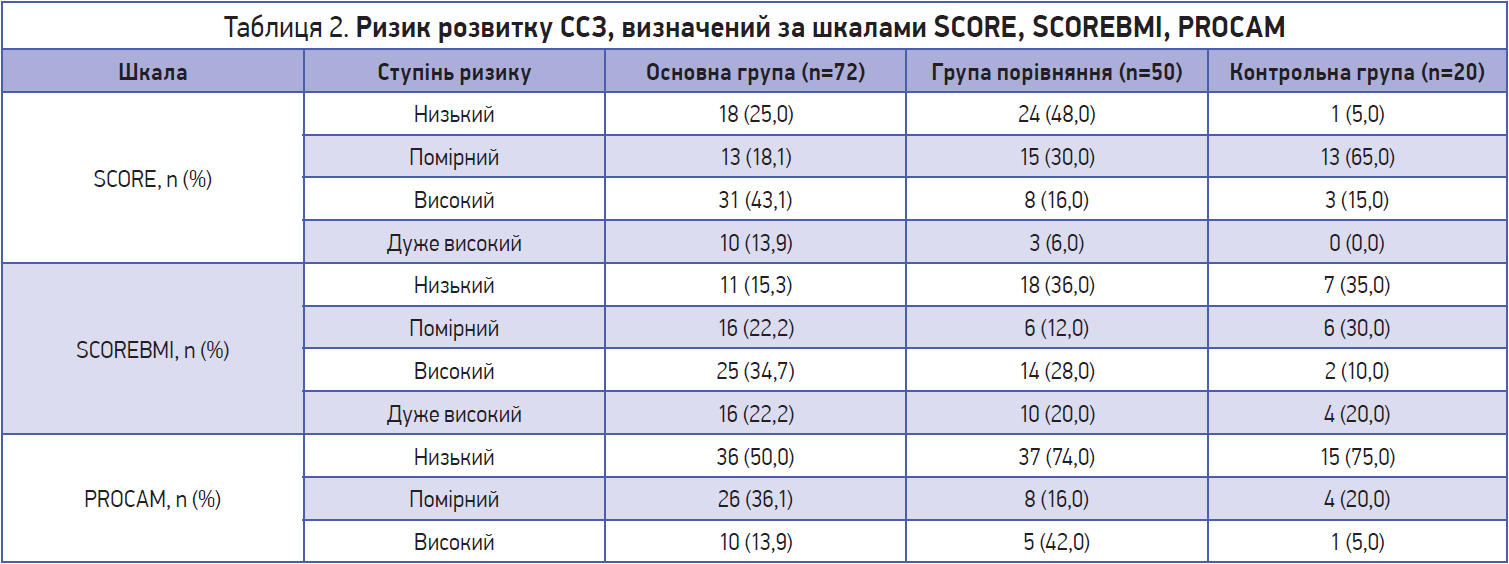
Важливим є визначення ризику розвитку ССЗ у досліджуваних груп хворих за шкалами SCORE, SCOREBMI, PROCAM (табл. 2). Згідно зі шкалою PROCAM, встановлено прямий зв’язок ризику з віком дебюту (rs=0,32; p<0,05) і тривалістю подагри (rs=0,43; p<0,05).
Асоціація між концентрацією феритину й сироватковим рівнем сечової кислоти при подагрі свідчить про те, що залізо може відігравати важливу роль у патогенезі захворювання. Зростання рівня феритину в міжнападному періоді подагри свідчить про ризик розвитку загострення подагричного артриту, тобто накопичення заліза в тофусах.
Фактори, які впливають на прихильність пацієнтів до довготривалої УЗТ, можна розподілити на дві групи: GP‑фактори та пов’язані безпосередньо з пацієнтом. До GP‑факторів належать розуміння стану та підходу до лікування; регулярний моніторинг; постійний діалог із пацієнтом; низька / висока ймовірність старту/продовження тривалої УЗТ; сприйняття подагри як гострого, персистентного та хронічного процесу; ідея допустимої кількості загострень; загальне зберігання медикаментів; бажання самостійного управління; зміна симптомів (частоти, тяжкості, впливу).
Натомість факторами, пов’язаними з пацієнтом, вважаються надто велика розбіжність між клінічною практикою та потенційними можливостями щодо лікування подагри. Згідно із проведеним дослідженням, 30% пацієнтів отримують УЗТ, а 40% – підтримувальну УЗТ.
Нині стало можливим впливати на такі фактори ризику подагри, як пуриновий катаболізм, туморлітичний синдром, харчування (вживання свинини, телятини, морепродуктів, напоїв із фруктозою, пива, дистильованого спирту), чоловіча стать, вік, ожиріння, анемія, походження, генетичні особливості, кліренс нирок (зниження за допомогою ацетилсаліцилової кислоти, циклоспорину), захворювання нирок.
Глобальною проблемою охорони здоров’я стала коронавірусна хвороба (COVID‑19). Нестача знань про вірус пояснює значну кількість пропозицій щодо потенційних мішеней для застосування того або іншого препарату. Представлено п’ять клінічних випадків впливу біополімерів у ділянці сідниць у пацієнтів, у яких розвинувся ятрогенний алогеноз. Хворі мали неспецифічні симптоми (головний біль, кашель без задишки й артралгії) з позитивним результатом тесту на SARS-CoV‑2 та лікувалися колхіцином. Їхні близькі контакти мали симптоми від легких до тяжких; троє з них померли.
Висновки
Поширеність подагри, АГ, МС неухильно зростає, причому з однаковою швидкістю. Новим незалежним предиктором виникнення подагри є анемічний стан, який поряд з ожирінням і ЦД належить до факторів серцево-судинного ризику. Коморбідна патологія пов’язана зі спалахами подагри. Перебіг подагри в пацієнтів із МС відрізняється більшою кількістю уражених суглобів за весь час хвороби, частотою та тривалістю загострень на рік. Ба більше, рецидив загострення у 80% пацієнтів із подагрою відбувається протягом року після першого нападу. Лише третина пацієнтів досягає цільового рівня сечової кислоти протягом 12 міс.
Підготувала Ольга Забродська