9 березня, 2026
Підходи до менеджменту пацієнта з анемічним синдромом у практиці лікаря загальної практики – сімейної медицини
Автори: О. М. Радченко, д.м.н., ДНП «Львівський національний медичний університет ім. Данила Галицького», Університетська клініка, кампус 2; О. В. Федик, PhD, ДНП «Львівський національний медичний університет ім. Данила Галицького»; О. С. Романишин, Університетська клініка, кампус 2

Анемічний синдром (АС) належить до найчастіших патологічних синдромів у клініці внутрішніх хвороб [1-3]. Лише через залізодефіцитну анемію (ЗДА) страждають 1,2 млрд людей на планеті, в т. ч. 14% дорослого населення США та 84% вагітних [1, 4]. Досить часто анемію випадково виявляють в амбулаторних чи стаціонарних пацієнтів, коли їм рутинно виконують загальний аналіз крові, тобто первинна діагностика АС є надзвичайно простою, однак його повна ліквідація неможлива без установлення причини і впливу на нього; це переважно тривалий і кропіткий процес [5].
АС – це не звичайне лабораторне зниження показників гемоглобіну та/або еритроцитів, а системний синдром, що має дуже важливе значення [6], оскільки часто проявляється неспецифічними скаргами, які стають підставою для пошуку інших хвороб (втома, зниження працездатності, слабкість, головні болі, пришвидшене серцебиття), а також приховує прояви важливих та тяжких процесів, не має гострих виражених скарг, може перебігати тривалий час безсимптомно й непомітно для пацієнта; водночас це незалежний предиктор погіршення перебігу всіх наявних гострих і хронічних хвороб, у найкращому разі фігуруючи в діагнозі як «супутні хвороби» й залишаючись поза увагою як лікарів, так і пацієнтів.
Лікар сімейної медицини – загальної практики є центральною фігурою, яка часто першою має справу з діагностикою причин і проявів АС, відповідає за своєчасну та точну нозологічну ідентифікацію, що дозволяє уникнути тривалих і часто неефективних емпіричних схем лікування. Ефективний сучасний менеджмент пацієнта з АС потребує переходу від застарілих алгоритмів до використання біомаркерів та ефективних сучасних засобів лікування АС.
Поширеність АС відрізняється в різних групах населення, є найбільшою серед жінок та осіб старечого віку [1]. Згідно із критеріями Всесвітньої організації охорони здоров’я (ВООЗ), серед жінок АС діагностується за умов умісту гемоглобіну <120 г/л (під час вагітності – <110 г/л), а серед чоловіків – <130 г/л. Однак проблема полягає у тому, що такі норми були встановлені за визначенням у венозній крові, тоді як у капілярній цей показник має бути на 10-20% вищим, ніж у венозній. Отже, легкий ступінь АС часто є недодіагностованим і прихованим, а пацієнти звертаються до лікаря в заавансованій стадії.
Анемія може розвинутися в будь-якому віці людини, причому не лише за наявності патологічних станів, а й за певних фізіологічних обставин: під час вагітності, лактації, періодів інтенсивного росту в дітей та підлітків, у дівчат пубертатного віку чи жінок у клімактеричному періоді, коли інтенсифікується кровотворення, втрачається кров або збільшується потреба в залізі.
Залежно від контингенту, від 50 до 80% АС зумовлені недостатністю заліза [7], тобто ЗДА є найчастішим представником АС. Вітчизняні нормативні документи щодо діагностики та лікування залізодефіцитного АС містять наказ Міністерства охорони здоров’я України № 709 від 02.11.2015 «Про затвердження та впровадження медико-технологічних документів зі стандартизації медичної допомоги при залізодефіцитній анемії».
Діагностика АС
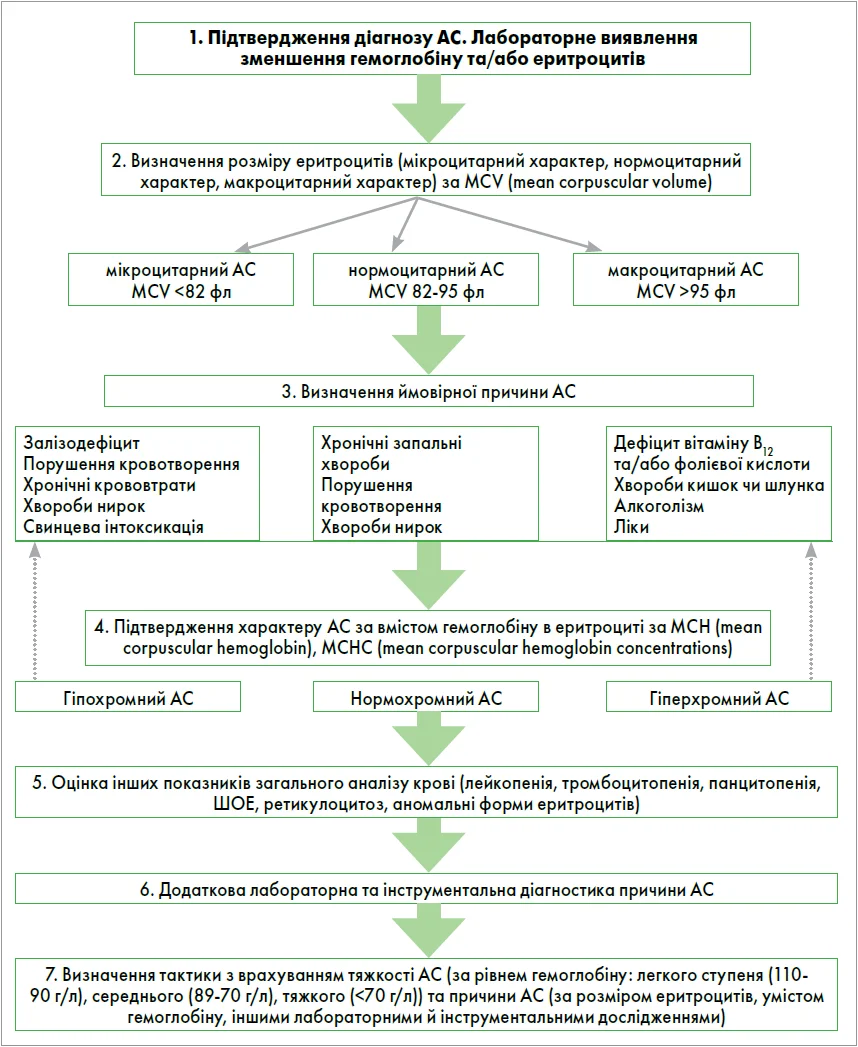
З огляду на величезну кількість хвороб і станів, які можуть бути причинами АС, алгоритм діагностичного пошуку потребує певної послідовності з вирішенням конкретних діагностичних завдань на кожному етапі пошуку. Діагностичний алгоритм АС наведено на рисунку.
Після виявлення зменшення гемоглобіну та/або еритроцитів діагностичний процес найкраще розпочинати з визначення розміру еритроцитів (мікроцитарний, нормоцитарний та макроцитарний АС), що раніше проводилося візуально, а тепер визначається за показником MCV (mean corpuscular volume) (табл. 1): мікроцитарний (MCV <82 фл), нормоцитарний (MCV 82-95 фл), макроцитарний АС (MCV >95 фл). Це дозволяє передбачити ймовірну причину АС (табл. 2). Саме основні причини АС зумовлюють провідні клінічні прояви, відрізняються за умов мікро-, нормо- і макроцитарних АС, мають визначальне значення для стратегії та тактики лікування, його ефективності. Однак у певних випадках основні причини АС можуть не зазнавати корекції, що зумовлюватиме вкрай низьку ефективність лікування АС.
|
Таблиця 1. Референтні значення показників |
||
|
Показник |
Розшифровка |
Референтне значення (норма) |
|
MCV |
Mean corpuscular volume |
82-92 фл (10-15/л) |
|
MCH |
Mean corpuscular hemoglobin |
27-33 пг |
|
MCHC |
Mean corpuscular hemoglobin concentrations |
31-36 г/дл, або 20-22 ммоль/л |
|
RDW-CV |
Red cell distribution width |
11,5-14,5% |
|
Колірний показник |
0,86-1,05 |
|
|
Залізо сироватки |
чол. 14,3-26,9; жін. 10,7-25,1 мкг/л |
|
|
Феритин сироватки |
≥16 нг/мл |
|
|
Загальна залізозв’язувальна здатність сироватки крові |
<71,6 ммоль/л |
|
|
Насичення трансферину (<20%) |
>20% |
|
|
Розчинні рецептори до трансферину sTfR |
чол. <5,0; жін. <4,4 мг/л |
|
|
Цинковий протопорфірин крові |
19-38 мкмоль/ммоль гему |
|
|
Ретикулоцитарний гемоглобін-еквівалент (Ret-He) |
≥28 пг |
|
|
Еритропоетин крові |
чол. 3,5-17,6; жін. 3,7-19,4 мОд/л |
|
|
Вітамін В12 крові |
300-500 пг/мл |
|
|
Фолієва кислота крові |
3-17 нг/мл |
|
|
Метилмалонова кислота крові |
73-271 нмоль/л |
|
|
Таблиця 2. Основні причини мікроцитарного, нормоцитарного та макроцитарного АС |
|
Причини мікроцитарного АС |
|
|
Причини нормоцитарного АС |
|
|
Причини макроцитарного АС |
|
Такі самі причини АС підтверджуються за оцінкою хромії (інтенсивності забарвлення) еритроцитів візуально або за вмістом гемоглобіну в еритроциті згідно із MCH (mean corpuscular hemoglobin) та МСНС (mean corpuscular hemoglobin concentrations) і колірним показником. Мікроцитарні анемії зазвичай є гіпохромними, нормоцитарні – нормохромними, а макроцитарні – гіперхромними.
Клінічна діагностика АС розпочинається зі збору анамнезу. Слід приділити особливу увагу характеру харчування (вегетаріанство, веганство, різні дієти, тривалі й часті суворі пости, низький матеріальний стан), прийому лікарських засобів, впливу ймовірних шкідливих професійних чинників (бензол, свинець, фарби), наявності осередків хронічних інфекцій, шлунково-кишкових хвороб (Helicobacter pylori) та оперативних втручань в анамнезі. Вкрай важливого значення набуває гінекологічний анамнез у жінок, оскільки кожна вагітність та лактація пов’язані з підвищеними потребами в залізі, що не компенсуються їжею та навіть харчовими добавками.
Клінічні прояви АС представлені низкою неспецифічних і специфічних синдромів, які можуть бути в різноманітних комбінаціях та вираженості [7-9]. До них належать загальний неспецифічний АС (гіпоксичний), а також сідеропенічний (дефіцит заліза), фунікулярний мієлоз (демієлінізація аксонів), гемолітичний та жовтяничний синдроми (скорочення тривалості життя еритроцитів), імуносупресивний (лейкопенія) і психоневрологічний синдроми тощо.
Скарги та об’єктивні прояви клінічних синдромів анемій
До скарг пацієнта як проявів загального АС належать слабкість, млявість, зменшення фізичної активності, задишка, пришвидшене серцебиття, сонливість удень і безсоння вночі, погіршення уваги та концентрації, роздратованість і нервозність [8]. Часто також виникають головні болі (частіше ввечері), запаморочення. Об’єктивні прояви загального АС: блідість шкіри та слизових, вушних раковин, тахікардія, низький артеріальний тиск.
Скарги пацієнта внаслідок сидеропенічного синдрому проявляються насамперед стосовно шкіри, волосся, нігтів (лущення та сухість шкіри, випадіння і ламкість волосся, ламкість нігтів), слизових оболонок (сухість), язика (блідість, атрофічний глосит), глотки (утруднене ковтання), тріщин у куточках рота (ангулярний стоматит), спотворення сприйняття смаку та запахів (pica chlorotica). Об’єктивні прояви сидеропенічного синдрому: блакитний відтінок склер, описаний Вільямом Ослером у 1908 р., унаслідок порушення гідроксилювання проліну та лізину; лущення й сухість шкіри, тьмяне і ламке сухе волосся; койлоніхії, розшарування та смугастість нігтів; гладкий язик з атрофованими сосочками (часто – із тріщинами); бліді ясна (нерідко – гіпертрофовані); множинний карієс, стерта і темна емаль зубів; хейліт; прояви гастриту А, атрофічного езофагіту, часті інфекції; розлади емоційної та інтелектуальної сфер [7]. Часто сидеропенічний синдром поєднується з інфікованістю Helicobacter pylori, отже, і з розвитком хронічного гастриту В і виразки шлунка чи дванадцятипалої кишки.
Особливості підходів до діагностики АС у практиці лікаря загальної практики – сімейної медицини
- нерідко в практиці сімейного лікаря спостерігається невідповідність між вираженими об’єктивними ознаками тяжкої анемії та відносно задовільним самопочуттям пацієнта. Це пояснюється тим, що організм тривалий час може компенсувати дефіцит гемоглобіну завдяки активації адаптаційних механізмів, які насамперед залучають серцево-судинну та кровотворну системи. При легких і хронічно прогресувальних формах анемії забезпечення тканин киснем частково підтримується за рахунок підвищення активності еритроцитів і збільшення проникності капілярів для газообміну. Основна роль у цих компенсаторних реакціях (а згодом і у відновленні нормального складу крові) належить кістковому мозку. У разі швидкого розвитку анемії чи тривалого її існування компенсаторні можливості виснажуються і на перший план виходять клінічні прояви гіпоксії з порушеннями функції центральної нервової системи та серця. Такі пацієнти скаржаться на головний біль, запаморочення, слабкість, шум у вухах, зниження пам’яті або біль у ділянці серця, тахікардію та виражену задишку;
- для сімейного лікаря критично важливо завжди шукати першопричину АС, особливо хронічну приховану крововтрату в чоловіків (виразки шлунка, кишок, пухлини кишок, геморой) та в жінок без менструації (виразки і пухлини кишок), що переважно потребує застосування ендоскопічного обстеження;
- вкрай важливою для сімейного лікаря є потреба розмежування ЗДА (істинне виснаження запасів заліза) та анемії хронічного захворювання (АХЗ) (залізообмежувальна анемія запалення). АХЗ – адаптивна відповідь на запалення [10]. Центральним регулятором є гепсидин – пептид, що синтезується в печінці під впливом інтерлейкіну‑6, зв’язується з білком-експортером феропортином, спричиняючи його деградацію. Це зумовлює блокування виходу заліза з макрофагів ретикулоендотеліальної системи та пригнічення абсорбції заліза в кишечнику. Внаслідок цього залізо в організмі стає недоступним для еритропоезу. В пацієнтів літнього віку з поліморбідністю та субклінічним запаленням феритин може бути хибно нормальним або підвищеним. У таких випадках емпіричне призначення перорального заліза переважно неефективне, а лікування ним супроводжується побічними ефектами;
- виключення зловживання алкоголем та ятрогенного компонента в пацієнтів із макроцитарним АС (MCV >100 фл) може становити труднощі, адже ґрунтується переважно на ретельному опитуванні. Зокрема, тривалий прийом метформіну (>4 роки), який є препаратом першої лінії для лікування цукрового діабету 2 типу, може порушувати абсорбцію вітаміну В12 на рівні клубової кишки [11]. Сімейний лікар повинен включати щорічний скринінг рівня вітаміну В12 до менеджменту пацієнтів, що приймають метформін. Також інгібітори протонної помпи, які широко застосовуються за умов лікування хронічних гастритів В, С і під час використання нестероїдних протизапальних препаратів, знижують кислотність шлунка, що перешкоджає вивільненню вітаміну В12 із харчових білкових комплексів і може зумовити АС.
Підходи до діагностики АС мають бути економічно обґрунтованими та спрямованими на пошук конкретної причини в кожному випадку [12]. Мікроцитарний характер АС насамперед потребує діагностики ЗДА. Діагностичні показники обміну заліза наведено в таблицях 1, 3. Феритин сироватки – чутливий і високоспецифічний показник умісту заліза в організмі, що зберігається у вигляді феритину (внутрішньоклітинне депо) в ретикулоендотеліальній системі. Феритин крові знижується задовго до появи клінічних симптомів дефіциту заліза, згодом знижується гемоглобін і лише потім виникають клінічні прояви. Однак феритин сироватки одночасно є гострофазовим показником, тому може підвищуватися за умов фебрильних станів, запальних хвороб, хвороб печінки та злоякісних пухлин. В таких пацієнтів дефіцит заліза може бути наявним навіть за умов високих рівнів феритину (до 50-60 нг/мл).
Збільшення ширини розподілу еритроцитів (RDW) – особливо корисний маркер діагностики ранньої фази анемії (латентний дефіцит), оскільки в осіб із дефіцитом заліза спостерігається підвищення RDW уже тоді, коли MCV усе ще є нормальним.
Розчинний рецептор трансферину (sTfR) також відіграє важливу діагностичну цінність. Кількість sTfR зростає, коли еритроїдні клітини мають брак заліза. Оскільки sTfR не є прозапальним білком гострої фази, його підвищення чітко корелює з реальною нестачею заліза. Розрахунок індексу sTfR/log (феритин) є найнадійнішим маркером верифікації змішаного характеру анемії. Ретикулоцитарний гемоглобін-еквівалент (Ret-He) вважається критичним показником, що відображає постачання заліза до кісткового мозку за останні 3-4 дні. Його зниження <28 пг – найточніший індикатор функціонального дефіциту заліза, що дозволяє рано оцінити ефективність терапії (через 7-10 днів), а також диференціювати ЗДА від АХЗ.
|
Таблиця 3. Діагностичні показники обміну заліза |
|
Загальний аналіз крові: зменшення гемоглобіну й еритроцитів; перевага мікроцитів (MCV <82 фл) і зсув кривої розподілу еритроцитів Прайс – Джонса вліво (збільшення RDW – ширина розподілу еритроцитів); зменшення колірного показника <0,8 (гіпохромія еритроцитів); анізоцитоз і пойкілоцитоз. Можуть бути також лейкопенія, нейтропенія, відносний лімфоцит. Збільшення ШОЕ |
|
Збільшення RDW (ширини розподілу еритроцитів) (≥14,5%) |
|
Зменшене залізо сироватки (<12,5 мкг/л) |
|
Зменшений феритин сироватки (<16 нг/мл) |
|
Збільшена загальна залізозв’язувальна здатність сироватки крові (>71,6 ммоль/л) |
|
Зменшений відсоток насичення трансферину (<20%) |
|
Підвищення розчинних рецепторів до трансферину sTfR, що визначається імунохімічними методами за допомогою автоматичних аналізаторів – у жінок >4,4, в чоловіків >5,0 мг/л |
|
Зниження ретикулоцитарного гемоглобінового еквівалента (Ret-He) <28 пг |
|
Первинна діагностика причинного патологічного стану – хронічної крововтрати (метрорагії, геморой, виразки), гіпоацидного гастриту чи гастриту А, вагітності, ХХН зі зменшенням продукції еритропоетину, інтоксикації свинцем тощо |
Діагностика макроцитарного АС, третина випадків якого зумовлена дефіцитом вітамінів В12 та В9 (фолієвої кислоти), розпочинається із загального аналізу крові, зміни якого досить характерні (табл. 4). Для точного підтвердження В12-дефіциту на ранніх та субклінічних стадіях доцільним буде визначення метилмалонової кислоти, підвищення якої є високоспецифічним маркером дефіциту вітаміну В12 і дозволяє чітко відмежувати його від фолатної недостатності. Причиною макроцитарного АС може бути гіпотиреоїдизм (слід перевірити тиреотропний гормон, який не має бути підвищеним).
|
Таблиця 4. Діагностичні показники макроцитарної анемії |
|
Загальний аналіз крові: зменшення гемоглобіну й еритроцитів, макроцитоз (MCV >95 фл), переважання великих еритроцитів, зсув кривої Прайс – Джонса вправо; поява мегалоцитів і мегалобластів; збільшення колірного показника >1,0 (гіперхромія); залишки ядер у вигляді тілець Жоллі та Кебота. Лейкопенія, тромбоцитопенія; нейтропенія зі зсувом вправо (поява гігантських гіперсегментованих нейтрофілів); моноцитопенія та відносний лімфоцитоз, еозинопенія. Зменшення кількості ретикулоцитів у період ремісії. Анізоцитоз, пойкілоцитоз. Збільшення ШОЕ |
|
Зменшений уміст вітаміну В12 у крові (<200 пг/мл; оптимальний рівень становить 300-500 пг/мл) |
|
Зменшений уміст фолієвої кислоти в крові (<3,0 нг/мл; норма становить 3-17 нг/мл) |
|
Підвищення метилмалонової кислоти (норма – 73-271 нмоль/л); у пацієнтів літнього віку не має діагностичної цінності |
|
Біопсія кісткового мозку – мегалобластний тип кровотворення |
|
Первинна діагностика причинного патологічного стану – гастриту А, глистної інвазії, патології кишок, алкоголізму, вагітності, гіпотиреоїдизму, застосування ліків (метформін, барбітурати, гідроксисечовина, колхіцин, зидовудин, 6-меркаптопурин, оральні контрацептиви, сульфасалазин, тріамтерен, сульфаніламіди, цитостатики) |
Діагностика нормоцитарного АС потребує визначення кількості еритропоетину (має бути в нормі) та виключення прихованих дефіцитів заліза й вітамінів В12 і В9 (табл. 5, 6).
|
Таблиця 5. Діагностичні показники нормоцитарної анемії |
|
Загальний аналіз крові: зменшення гемоглобіну й еритроцитів, нормоцитоз (MCV 82-95 фл), нормохромія, колірний показник 0,9-1,0. Можуть бути зміни форми зрілих еритроцитів (шистоцитоз – мікроангіопатичний гемоліз, пов’язаний із тромбоцитопенічною пурпурою, гемолітико-уремічним синдромом, ДВЗ-синдромом; серпоподібні клітини, еліптоцити); якщо кількість ретикулоцитів <100 000/мл, це свідчить про порушення продукції еритроцитів. Збільшення ШОЕ |
|
Нормальний уміст еритропоетину (норма для чоловіків становить 3,5-17,6, для жінок – 3,7-19,4 мОд/л) |
|
Первинна діагностика ХХН, тривалого хронічного запального процесу, особливо гнійного, злоякісних пухлин, автоімунних процесів, гіпотиреоїдизму |
|
Таблиця 6. Орієнтовні діагностичні критерії АС за даними гемоцитограми (модифіковано за [13]) |
|||||
|
Анемія |
Залізодефіцитний |
Мегалобластний |
Гіпопластичний |
Гемолітичний |
АС хронічної хвороби |
|
Показник |
|||||
|
Еритроцити |
N, ↓ |
↓ |
↓↓ |
↓ |
↓ |
|
MCV |
N, ↓ |
↑ |
N, ↑ |
N, ↓,↑ |
N, ↓ |
|
RDV |
↑ |
↑ |
↑ |
N, ↑ |
N, ↑ |
|
MCH |
↓ |
↑ |
N |
N ↓ |
N, ↓ |
|
MCHC |
↓ |
N |
N |
N, ↓ |
N, ↓ |
|
Морфологія еритроцитів |
гіпохромія, пойкілоцитоз |
гіперхромія, макроцитоз, мегалоцитоз, пойкілоцитоз |
нормохромія |
нормохромія, гіпохромія, патологічні форми |
нормохромія, гіпохромія |
|
Елементи ядра в еритроцитах |
(–) |
(+) |
(+) |
(–), (+) |
(–) |
|
Ретикулоцити |
N, ↓ |
↓ |
↓↓ |
↑↑ |
N, ↓ |
|
Тромбоцити |
N, ↑ |
N, ↓ |
↓↓ |
N, ↓ |
N, ↑ |
|
Лейкоцити |
N |
N, ↓ |
↓↓ |
N, ↓,↑ |
N, ↑ |
|
Особливості лейкограми |
немає |
гіперсегментація ядер нейтрофілів |
гранулоцитопенія |
немає |
немає |
|
ШОЕ |
N |
N |
↑↑ |
N, ↑ |
N, ↑ |
|
Примітки: N – нормальний; ↓ – знижений; ↓↓ – значно знижений; ↑ – підвищений; ↑↑ – значно підвищений; (–) – відсутній, (+) – наявний. |
|||||
Підходи до лікування
Лікування пацієнта з АС на перший погляд є легким завданням, однак насправді – це цілісна багатокомпонентна програма менеджменту, що визначається встановленням причин анемії у кожному конкретному випадку. Слід пам’ятати, що досить часто одночасно існують декілька різних причин АС. У пацієнтів із хронічною патологією корекція АС є не просто лікуванням синдрому, а прогностично значущим менеджментом. Лікування має бути індивідуалізованим з огляду на новітні дані про метаболізм заліза [14, 15], а також комплексним і раціональним.
Дієтотерапія має допоміжне значення, оскільки з їжі всмоктується тільки 10-20% заліза – в найдоступнішій формі (у вигляді гему) міститься у воловому м’ясі; у печінці, яйцях, рибі (у вигляді гемосидерину). Необхідно обмежити продукти, які погіршують усмоктування заліза: молоко, чай, кава, лужні мінеральні води, кукурудза, рис. Однак сімейний лікар повинен наголосити на тому, що лише продуктами харчування, харчовими добавками з умістом заліза чи вітамінними/вітамінно-мінеральними комплексами з додатками заліза не можливо це ліквідувати.
Феротерапія (табл. 7) має призначатися тільки після встановлення остаточного діагнозу, адже просто зменшення гемоглобіну не є показанням для препаратів заліза, оскільки може утруднити подальшу діагностику. Залізо використовується в медицині з прадавніх часів. Уже в XVII ст. англійський лікар Томас Сиденгам (1624-1689) уперше застосував ліки із залізних спилків на рейнському вині.
|
Таблиця 7. Правила феротерапії |
|
Обирати препарат заліза з доведеною ефективністю |
|
Перевага надається пероральним формам заліза |
|
Препарат має містити достатню дозу заліза та речовини, які покращують його всмоктування |
|
Препарат має характеризуватися хорошою переносимістю та не спричиняти побічних ефектів; переносимість різних солей є індивідуальною |
|
Достатня тривалість терапії препаратом заліза (до 4-6 міс) |
|
Приймати препарат натще (за 30 хв до споживання їжі), запиваючи водою чи соком; не запивати зеленим чаєм |
На ринку є препарати двовалентного заліза у вигляді органічних (глюконат або фумарат), неорганічних (сульфат чи хлорид) солей і тривалентного заліза у вигляді органічних (сукцинат) й органічних (гідроксид у комплексі з полімальтозою) солей. Розрахунок дози має бути тільки за елементарним залізом. Рекомендації ВООЗ із дозування за елементарним залізом: анемія легкого ступеня – 60 мг елементарного заліза на добу; середнього та тяжкого ступенів – 120 мг елементарного заліза на добу.
Якщо хворий не може переносити таке лікування внаслідок захворювання шлунково-кишкового тракту, доцільно призначити залізо у формі капсул сповільненого виділення. Це лікування продовжують ще протягом декількох місяців після усунення анемії для адекватного відновлення запасів заліза в організмі. Варто досягти нормального рівня феритину в сироватці. Стандартний щоденний прийом перорального заліза зумовлює значне підвищення гепсидину, що блокує подальше всмоктування заліза наступного дня. Сучасний протокол передбачає прийом 100-200 мг елементарного заліза через день (альтернувальний режим). Це дозволяє рівню гепсидину знизитися в «день відпочинку», максимізуючи фракцію абсорбції наступної дози та покращуючи комплаєнс.
Рішення про використання внутрішньовенного заліза (заліза карбоксимальтоза, заліза ізомальтозат) є обґрунтованим у практиці сімейного лікаря. Внутрішньовенна терапія – це терапія вибору, а не лише резерв, коли діагностовано АХЗ або змішану форму з високим рівнем гепсидину чи якщо в пацієнта наявний синдром мальабсорбції або коли пероральна терапія неефективна (відсутність зростання гемоглобіну на ≥10 г/л за 4 тиж або позитивної динаміки Ret-He).
Показання для парентального введення препаратів заліза:
1) наявність психічної хвороби, що робить таблетоване лікування неможливим;
2) пухлина чи спайки стравоходу або кардіального відділу шлунка;
3) патологія тонкої кишки: резекція значної ділянки (>60 см) кишки, запальний чи пухлинний процес у кишках, трофічна ентеропатія;
4) гострий запальний або виразковий процес у травному каналі, особливо в період загострення.
Сторонні ефекти парентеральної терапії:
1) часті алергічні реакції у вигляді кропив’янки, лихоманки; анафілактичних реакцій;
2) часті флебіти;
3) висока ймовірність інфільтратів, абсцесів, пігментація шкіри в місці ін’єкцій;
4) розвиток гемосидерозу за умов помилкового діагнозу дефіциту заліза.
Ранній моніторинг ЗДА: контроль Ret-He через 7-14 днів після початку терапії. Його зростання – найшвидший і найнадійніший індикатор правильної відповіді на лікування. Контроль Hb через 4-6 тиж. Очікуваний мінімальний приріст Hb становить 10 г/л. Відсутність такої динаміки потребує негайного перегляду діагнозу (резистентність, АХЗ, прихована крововтрата). Терапія ЗДА має тривати щонайменше 3 міс після нормалізації Hb для повного відновлення депо (феритин >50 мкг/л).
Причини неефективного лікування ЗДА:
1) відсутність дефіциту заліза (помилковий діагноз);
2) неправильно обрана форма препарату чи неадекватні дози заліза;
3) ігнорування хворим програми лікування;
4) втрати крові, що тривають (невиявлені джерела кровотечі, частіше – в травному каналі);
5) пригнічення еритропоезу в результаті інфекції, запалення або нерозпізнаного пухлинного росту;
6) недостатнє всмоктування заліза;
7) недостатня тривалість лікування;
8) одночасний прийом засобів, які зменшують усмоктування заліза;
9) одночасне існування ЗДА з іншими АС (В12-дефіцитною, фолієводефіцитною);
10) рідкісна форма ЗДА (ізольований легеневий сидероз і синдром Гудпасчера).
При виявленні макроцитарного АС сімейний лікар повинен спочатку виключити В12-дефіцит і провести пункцію кісткового мозку до призначення замісної терапії. За підтвердження діагнозу спочатку слід призначити вітамін В12, лише потім – фолієву кислоту для запобігання маскуванню неврологічних ускладнень. При легких формах або фармакологічно індукованому дефіциті ефективними є високі пероральні дози В12 (1000-2000 мкг).
Особливості діагностики та лікування АС за умов інших патологічних станів і хвороб
Анемія та дефіцит заліза є невід’ємною частиною патогенезу хронічної серцевої недостатності (ХСН). Скринінг дефіциту заліза (феритин <100 або 100-300 мкг/л при НТ <20%) слід проводити всім пацієнтам із ХСН зі зниженою фракцією викиду. Внутрішньовенне залізо показано цим хворим незалежно від наявності анемії для зменшення госпіталізацій та покращення функціонального класу.
Анемія при хронічній хворобі нирок (ХХН) переважно є результатом дефіциту еритропоетину та проявом АХЗ. Згідно із протоколом, перший крок – корекція дефіциту заліза (майже завжди внутрішньовенним залізом). Еритропоез-стимулювальні агенти призначаються лише після забезпечення адекватних запасів заліза та при Hb <100 г/л [15].
Анемія у вагітних потребує активної профілактики. За неефективності перорального заліза внутрішньовенне (після I триместру) є безпечною та високоефективною стратегією, що дозволяє швидко досягти цільових показників гемоглобіну, а також знизити ризики, пов’язані з тяжкою анемією.
Активне використання маркерів (Ret-He) для подолання гепсидинового блоку, застосування альтернувальних схем перорального дозування та своєчасна ініціація внутрішньовенного заліза в пацієнтів із ХСН та ХХН підвищують ефективність лікування. Комплексний та сучасний підхід гарантує не лише корекцію гемоглобіну, а й значне покращення якості життя і зниження смертності серед найуразливіших груп пацієнтів.
Наводимо клінічний випадок складного для діагностики АС, який, імовірно, змінив свій характер. Особливість клінічного випадку – пацієнтка страждала на ЗДА 25 років, але останнім часом з’явилися виражені болі в епігастрії та навколо пупка з набряковим синдромом без значних змін сечі, проте з ознаками мальдигестії та кахексії. АС був тяжкого ступеня, гіпохромного мікроцитарного характеру зі збільшенням ширини розподілу та значним зниженням параметрів обміну заліза. Однак нетиповими для ЗДА були тромбоцитоз і лейкоцитоз; низькі рівні загального холестерину та загального білірубіну, високий уміст С-реактивного білка. Під час комп’ютерної томографії (КТ) із контрастуванням виявлено зміни слизової оболонки клубової, сліпої та висхідної кишок, ілеоцекальну лімфаденопатію, асцит, випіт у малому тазі. З огляду на тромбоцитоз, який часто є паранеопластичною реакцією, випіт у черевну порожнину, болі не можна виключати паранеопластичний, автоімунний та залізодефіцитний характери анемії, що посилює прояви АС і робить малоефективним лікування.
Клінічний випадок
Пацієнтка Б., 66 років, пенсіонерка, надійшла до університетської лікарні ДНП «Львівський національний медичний університет ім. Данила Галицького» 19.11.2025 зі скаргами на виражену загальну слабкість, набряки нижніх кінцівок, сильні болі в епігастрії та навколо пупка, пришвидшене серцебиття, задишку при навантаженні, покашлювання.
Хворіла на виразку шлунка з 1998 р., щодо пенетрацї якої у 2000 р. проведено резекцію шлунка за Більрот‑2. Після оперативного втручання діагностовано ЗДА, яку неодноразово лікувала в стаціонарі (2007, 2011 рр., тричі в 2015 р.). Погіршення стану розпочалося поступово (≈6 міс тому, коли з’явилися болі в животі та посилилася слабкість). Лікувалася амбулаторно – без ефекту. Анамнез: працювала із формальдегідом і миш’яком (на пенсії – з 2015 р.). Спадковість не обтяжена; алергологічний, епідеміологічний, гінекологічний анамнези – б/о. Курить. Має автоімунний тиреоїдит; ендопротезування лівого кульшового суглоба.
Об’єктивно: температура тіла 36,6 °C. Загальний стан тяжкий. Свідомість ясна, орієнтація в просторі та часі збережена. Поза Ромберга: похитування. Астенічна, шкіра бліда із жовтуватим відтінком. Слизові оболонки бліді. Набряки на ногах до рівня колін. М’язи дряблі. Лімфатичні вузли не збільшені. Тремор пальців рук відсутній. Дихання носом вільне, частота дихання 16/хв. Над легенями коробковий перкуторний звук. Дихання везикулярне, в нижніх відділах – поодинокі сухі свистячі хрипи. Пульс 76 уд./хв, ритмічний, задовільного наповнення; артеріальний тиск 130/80 мм рт. ст. Тони серця послаблені. Частота серцевих скорочень 76 уд./хв. Прослуховується систолічний шум. Ліва межа відносної серцевої тупості зміщена вліво на 0,5 см. Живіт звичайної форми, бере участь в акті дихання. Підшкірні вени не розширені. Пальпаторно біль в епігастрії та навколо пупка. Печінка виступає з-під краю реберної дуги на 1 см. Селезінка не пальпується. Випорожнення 1 р/добу. Нирки не пальпуються, симптом Пастернацького (–) з обох боків.
Попередній діагноз: хронічна ЗДА тяжкого ступеня, хронічний бронхіт курця.
Обстеження. Загальний аналіз крові (18.11.2025): лейкоцити 24 г/л; еритроцити 2,3 т/л; рівень гемоглобіну (Hb) 40 г/л; гематокрит (НСТ) 16,4%; середній обсяг еритроцитів (MCV) 71,3 фл; середній рівень гемоглобіну в еритроциті (MCH) 17,4 пг; середня еритроцитарна концентрація гемоглобіну (MCHC) 244 г/л; ширина розподілу еритроцитів (RDW-CV) 19,5%; тромбоцити 575 г/л; еозинофіли 1, паличкоядерні нейтрофіли 4, сегментоядерні нейтрофіли 86, лімфоцити 6, моноцити 3; ШОЕ 45 мм/год.
Загальний аналіз крові (26.11.2025): рівень Hb 63 г/л; еритроцити 2,6 т/л; КП 0,7; тромбоцити 454 г/л; лейкоцити 9,2 г/л; сегментоядерні нейтрофіли 65; еозинофіли 3; лімфоцити 20; моноцити 10; анізоцитоз (+++); пойкілоцитоз (+); гіпохромія (++); ШОЕ 38 мм/год.
Загальний аналіз крові (01.12.2025): рівень Hb 94 г/л; еритроцити 3,7 т/л; КП 0,8; лейкоцити 8,4 г/л; ШОЕ 35 мм/год; паличкоядерні нейтрофіли 4; сегментоядерні нейтрофіли 75; лімфоцити 17; моноцити 4; анізоцитоз (+).
Загальний аналіз сечі (01.12.2025): питома вага 1015; білок 0,033; рН 5,5.
Обмін заліза (18.11.2025): залізо 1,9 мкг/л (норма для жінок 6,6-26,0); феритин 4,6 нг/мл (норма ≥16); трансферин 2,67 г/л (норма 2,0-3,6 г/л).
Біохімічний аналіз крові (18.11.2025): білірубін 3,1 мкмоль/л; альбумін 27,66 г/л; загальний білок 62,4 г/л; глюкоза 5,3 ммоль/л; холестерин загальний 2,4 ммоль/л; креатинін 66 мкмоль/л; сечовина 4,3 ммоль/л; сечова кислота 194 ммоль/л; K+ 4,8 ммоль/л; Na+ 139 ммоль/л; амілаза 27 Од (норма); АЛТ 9 Од; АСТ 5 Од; лужна фосфатаза 141 Од/л (норма для жінок <98); ГГТП 20 Од (норма); СРБ 70,8 мг/л; ревматоїдний фактор 12,64 МО/мл (норма); АСЛО 242 МО/л (норма <200).
Коагулограма (18.11.2025): протромбіновий індекс 5%; протромбіновий час 11,7 с; загальний фібриноген 4,84 г/л; МНВ 1,09; D-димер 1,52.
Гормони (18.11.2025): ТТГ 6,8 мМО/л (норма – до 4,05); антитіла до тиреопероксидази >3000 (норма – до 20 МО/мл).
ЕКГ: синусовий ритм; частота серцевих скорочень 80 уд./хв; електрична вісь серця горизонтальна. Зміни за типом атеросклеротичного кардіосклерозу.
ЕхоКГ (05.12.2025): мітральна недостатність 1,5 (+); трикуспідальна недостатність 1,5 (+); легенева гіпертензія (–). Рідини в порожнині перикарда не виявлено. Розміри камер і товщина стінок у нормі. Загальна скоротлива здатність лівого шлуночка (ЛШ) знижена, є зони гіпокінезу. Початкові ознаки систолічної дисфункції ЛШ. Легка мітральна недостатність. Аортальний клапан: стулки ущільнені. Трикуспідальна недостатність легка.
КТ із внутрішньовенним контрастуванням йогексолом (20.11.2025): щитоподібна залоза – обидві частки збільшені, без вузлів і патологічного контрастування. Помірна центролобулярна емфізема верхніх часток обох легень; незначний апікальний пневмофіброз; легеневі артерії помірно розширені. Стравохід: не розширений, стінка не потовщена. Післяоперативний гастроєюноанастомоз функціонує, стінки не змінені. Стінки товстої кишки помірно потовщені, вираженіше – в ділянці сліпої (СК), висхідної та термінального відділу клубової кишок, із контрастним підсиленням слизової оболонки. Виражена периколічна тяжистість навколо СК, візуалізація її купола утруднена. Визначаються дрібні дефекти по стінці СК, заповнені повітрям, не виключено виразки. Гаустрація висхідної кишки згладжена. Апендикс – 8 мм, у просвіті – повітря. Хід судин брижі не змінений. Черевний стовбур і брижові судини контрастуються рівномірно; брижа та сальники помірно ущільнені. Підшлункова залоза з ознаками ліпоматозу. Печінка не збільшена. Портальна вена – 13 мм, печінкові вени без змін; жовчні протоки не розширені. Холедох – 7 мм, без конкрементів; жовчний міхур без змін. Селезінка збільшена; структура не змінена; селезінкова вена – 9 мм, без дефектів. Наднирковики типового положення та форми – без утворень. Нирки типового положення, розмірів і форми. В паренхімі обох нирок – дрібні прості кісти (2-8 мм). Виділення контрасту своєчасне; ЧМС не розширена. У малому тазі – значні артефакти від металевої конструкції ендопротеза лівого кульшового суглоба. Рекомендовано УЗД матки та яєчників. Асцит. У малому тазі – вільна рідина розміром 90×25 мм. Парагепатично та параспленічно – незначна кількість рідини завтовшки до 7 мм. Периколічно на рівні селезінкового кута 19×13 мм. Лімфатичні вузли заочеревинного простору та малого таза не збільшені. Ілеоцекальні лімфатичні вузли з активним накопиченням контрасту розміром до 18 мм.
Висновки: стан після оперативного лікування шлунка – потовщення стінок термінального відділу клубової кишки, сліпої та висхідної кишок. Ілеоцекальна лімфаденопатія (НВК? Лімфома?). Асцит. Церебральна мікроангіопатія. Гіперплазія обох часток щитоподібної залози. Центролобулярна емфізема обох легень. Плевральний випіт (гідроторакс). Прості кісти обох нирок.
Клінічний діагноз: ЗДА тяжкого ступеня. Хвороба оперованого шлунка. Стан після резекції шлунка за Більрот‑2 (2000 р.). Анастомозит. Больовий синдром. Хронічний коліт, стадія загострення. НВК? Лімфома? Астенічний синдром. Вторинна білкова недостатність. Синдроми мальабсорбції та мальдигестії. Дефіцит маси тіла. Автоімунний тиреоїдит; гіпотиреоз. ІХС: стабільна стенокардія напруги, І ФК; дифузний кардіосклероз. Атеросклероз аорти. Набуті недостатності мітрального та тристулкового клапанів. Систоло-діастолічна дисфункція ЛШ. Хронічний бронхіт курця, катарально-гнійний; емфізема легень; пневмосклероз; легенева недостатність І ст. Остеохондроз хребта; остеопороз; сколіоз грудного відділу хребта. Множинні ліпоми кінцівок.
Особливості менеджменту пацієнтки. З огляду на виявлені зміни кишок усмоктування заліза в пацієнтки, ймовірно, практично відсутнє (відсутність шлунка, ентерит). Лікування АС полягало в застосуванні парентерального заліза (Fe-карбоксимальтози, Fe(ІІІ)-гідроксид-сахарозний комплекс) та еритроцитарної маси, що комбінували зі спазмолітиками, інгібітором протонної помпи, прокінетиком, альбуміном із фуросемідом, антибіотиком. Однак остаточна причина АС залишилася тільки гіпотетичною.
Висновки
АС належить до найчастіших патологічних синдромів у клініці внутрішніх хвороб і загальної практики. Лікар сімейної медицини часто першим має справу з діагностикою причин і проявів АС, відповідає за своєчасну та точну нозологічну ідентифікацію. Клінічні прояви АС часто є невираженими, маскуються іншими ураженнями, потребують додаткового обстеження залежно від імовірного його походження. Найтяжчими для діагностики є випадки поєднаного генезу АС.
Список літератури знаходиться в редакції.
Медична газета «Здоров’я України 21 сторіччя» № 2 (613), 2026 р



 Радченко О.М.
Радченко О.М.