27 грудня, 2021
Застосування N-ацетилцистеїну при COVID-19: що відомо на кінець 2021 року?
Коронавірусна хвороба (COVID-19) спричинила справжню кризу системи охорони здоров’я в усьому світі. Оскільки препаратів, прицільно спрямованих на лікування COVID-19, дотепер не існує, основною стратегією фармакотерапії цієї хвороби наразі є переосмислення та перепозиціонування наявних медикаментів з іншими показаннями, які можуть бути потенційно здатними пришвидшувати одужання пацієнтів або запобігати прогресуванню хвороби до тяжкого гострого респіраторного дистрес-синдрому (Wong K.K. et al., 2021).
N‑ацетилцистеїн являє собою відомий муколітичний препарат з антиоксидантною та протизапальною дією (Landini G. et al., 2016). Цей засіб застосовується в клінічній практиці впродовж декількох декад для лікування низки респіраторних патологічних станів, зокрема бронхіту і гострого респіраторного дистрес-синдрому. Муколітична дія N‑ацетилцистеїну опосередкована наявністю вільної сульфгідрильної групи, яка сприяє руйнуванню дисульфідних зв’язків перехресно зв’язаних глікопротеїнів матриксу слизу, знижуючи в’язкість останнього (Aldini G. et al., 2018). Своєю чергою, антиоксидантна ефективність N‑ацетилцистеїну вважається наслідком його здатності реагувати з вільними радикалами (-OH, -CO3, -NO2), відновлювати ушкоджені структури клітин і бути посередником у реакції біосинтезу глутатіону (Samuni Y. et al., 2013). За рахунок останньої властивості N‑ацетилцистеїн здатен підсилювати ефективність антимікробної терапії інфекцій дихальних шляхів, покращуючи наслідки лікування (Blasi F. et al., 2016).
Продовжує зростати також база даних щодо власної антимікробної дії N‑ацетилцистеїну та його здатності руйнувати біоплівки. Описано схожий вплив щодо таких бактерій, як Escherichia, Pseudomonas, Staphylococcus, Acinetobacter, Haemophilus і Klebsiella (Landini G. et al., 2016; Rodríguez-Beltrán J. et al., 2015; Goswami M., Jawali N., 2010; Domenech M., García E., 2017).
Ще в 1997 р. S. De Flora та співавт. продемонстрували, що пероральне застосування N‑ацетилцистеїну в дозі 600 мг 2 р/добу достовірно покращувало клітинний імунітет в осіб похилого віку, «переключаючи» його від анергії (відсутності реакції на сторонні речовини, бактерії та віруси) до нормоергії.
Нещодавно було також запропоновано застосовувати N‑ацетилцистеїн як допоміжний препарат у стандартній схемі медичної допомоги при COVID‑19, оскільки цьому медикаменту притаманні необхідні в цьому випадку ефекти (муколітичний, антиоксидантний, імуномодулювальний та протизапальний), а також сприятливе співвідношення користь/ризик (Jorge-Aarón R.-M., Rosa-Ester M.-P., 2020; Poe F. L., Corn J., 2020; Der Kinderen D. J., Koten J. W., 2020).
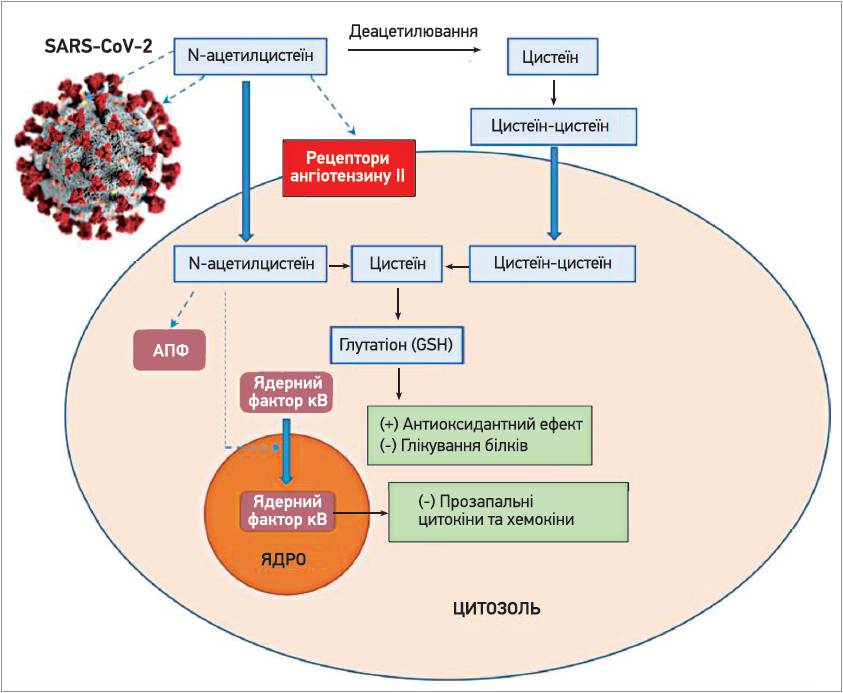
K. K. Wong і співавт. (2021) виокремлюють 6 основних потенційних механізмів дії N‑ацетилцистеїну при COVID‑19 (рис. 1):
1. За даними попередніх випробувань, на потрапляння вірусних глікопротеїнів до клітини впливає тіоло-дисульфідний баланс на поверхні вірусу та на поверхні клітини організму-господаря. Руйнування дисульфідних зв’язків під дією N‑ацетилцистеїну змінює структуру білків, які взаємодіють між собою, порушуючи в такий спосіб афінність рецепторів та інфекційність вірусу.
2. За рахунок того ж руйнування дисульфідних зв’язків N‑ацетилцистеїн порушує третинну структуру рецептора ангіотензину II, запобігаючи зв’язуванню ангіотензину із цими рецепторами. Цей ефект має протекторну дію щодо запалення та фіброзу легень.
3. Сульфгідрильна група N‑ацетилцистеїну пригнічує ангіотензинперетворювальний фермент (АПФ), знижуючи вироблення ангіотензину ІІ. Наслідком цього в легенях людини є обмеження надходження вірусу до клітин, оскільки воно розпочинається із прикріплення спайк-білка до АПФ на поверхні альвеолоцитів.
4. Зазначена антиоксидантна дія N‑ацетилцистеїну протидіє окисному стресу, запобігає глікозилюванню білків, реалізуючи профілактичну дію щодо респіраторного дистрес-синдрому, легеневої недостатності. На тлі антиоксидантного впливу N‑ацетилцистеїну підсилюється активність низки сигнальних молекул (білок тол-подібного рецептора 7, мітохондріальний противірусний сигнальний білок) і зростає вироблення інтерферону 1 типу, основною функцією якого є збільшення експресії генів, що відповідають за противірусну активність клітин організму-господаря.
5. N‑ацетилцистеїн індукує синтез глутатіону, а також сульфіду водню, послаблюючи індуковане кінцевим продуктом глікування (метилгліоксалем) глікування білків і додаткове глікозилювання. Ці ефекти зумовлюють зниження інфекційності вірусу SARS-CoV‑2 та зменшення вираженості асоційованих із ним патологічних станів.
6. N‑ацетилцистеїн пригнічує активацію ядерного фактора κB, блокуючи експресію прозапальних цитокінів і хемокінів, рівні яких корелюють з тяжкістю перебігу та показниками смертності при низці вірусних інфекцій дихальних шляхів.
Рис. 1. Схема потенційних ефектів N-ацетилцистеїну при COVID-19
Численні дослідження іn vitro довели, що N‑ацетилцистеїн є перспективною молекулою для лікування вірусних хвороб дихальної системи. Так, у клітинах, інфікованих вірусом грипу H5N1, N‑ацетилцистеїн протидіяв цитопатичному впливу вірусу й апоптозу клітин, знижував уміст прозапального інтерлейкіну‑6 (Geiler J. et al., 2010). В іншому дослідженні було продемонстровано здатність N‑ацетилцистеїну підвищувати вміст вірус-специфічних цитотоксичних T‑лімфоцитів і концентрацію інтерферону-γ (Boon A. C. et al., 2002). В клітинній лінії Vero, інфікованій свинячим штамом грипу H1N1, N‑ацетилцистеїн пригнічував реплікацію вірусу (Garigliany M. M.O., Desmecht D. J., 2011), а в культурі клітин бронхіального епітелію, інфікованих респіраторно-синцитіальним вірусом, окрім того, відновлював кількість рухомих війчастих клітин (Mata M. et al., 2012).
Сприятливі результати було отримано і в дослідженнях іn vivo, в яких N‑ацетилцистеїн продемонстрував здатність підвищувати виживаність при інтраназальному введенні летальної дози вірусу грипу A, підсилювати дію рибавірину (Ghezzi P., Ungheri D., 2004; Ungheri D. et al., 2000), зменшувати вираженість набряку легень та запальної відповіді, а також знижувати активність прозапальних цитокінів у промивних водах, одержаних за допомогою бронхоальвеолярного лаважу (Zhang R. H. et al., 2014).
Що стосується клінічних випробувань N‑ацетилцистеїну при респіраторних захворюваннях, то рандомізоване контрольоване дослідження довело, що тривалий прийом цього препарату супроводжується достовірним зменшенням частоти виникнення грипу та грипоподібних інфекцій порівняно із плацебо (25 проти 79%) (De Flora S. et al., 1997). Продемонстровано також підвищення загальної антиоксидантної здатності на тлі N‑ацетилцистеїну в пацієнтів із позагоспітальною пневмонією (Zhang Q. et al., 2018). Лікування пероральним N‑ацетилцистеїном у дозі 600 мг 2 р/добу супроводжувалося меншою частотою виникнення пневмоній порівняно із плацебо (26,6 проти 46,6%), асоційованих зі штучною вентиляцією легень, меншою тривалістю перебування у відділенні інтенсивної терапії та стаціонарного лікування загалом, більшою часткою повного одужання (Sharafkhah M. et al., 2018).
Схожі результати було отримано і в ретроспективному двоцентровому когортному дослідженні, під час якого порівнювалися результати лікування пацієнтів за допомогою стандартної схеми та стандартної схеми в поєднанні з пероральним прийомом N‑ацетилцистеїну в дозі 600 мг 2 р/добу протягом 14 днів. Додавання до схеми терапії N‑ацетилцистеїну супроводжувалося достовірно нижчою частотою прогресування до тяжкої дихальної недостатності та меншими показниками 14-, 28-денної смертності. Додаткові сприятливі ефекти: зниження кількості лейкоцитів, С‑реактивного білка, D‑димерів, лактатдегідрогенази. Аналіз за допомогою методу багатоваріантної логістичної регресії виявив, що нетяжкий перебіг хвороби та застосування N‑ацетилцистеїну були незалежними предикторами 28-денної виживаності (Assimakopoulos S. F. et al., 2021).
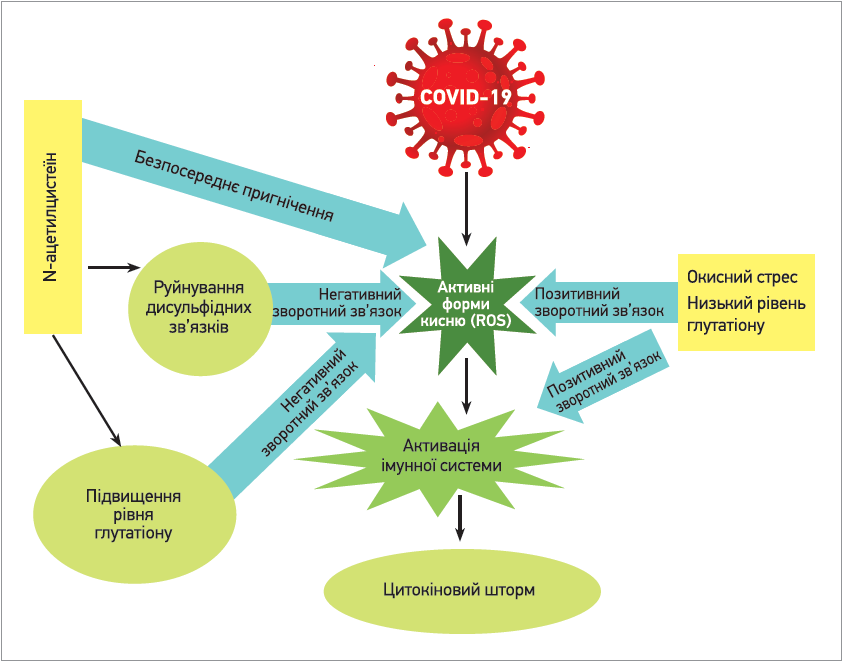
Наявні на сьогодні дослідження N‑ацетилцистеїну при COVID‑19 переважно є невеликими. Додавання N‑ацетилцистеїну, аторвастатину та івермектину до стандартної терапії COVID‑19 здатне зменшити смертність, не збільшуючи водночас кількості побічних ефектів (Bhattacharya R. et al., 2020). Однак з огляду на вищезазначені ефекти N‑ацетилцистеїну Z. Shi та C. A. Puyo (2020) пропонують використовувати цей препарат як профілактичний імуномодулятор під час пандемії. Аналогічну думку мають R.-M. Jorge-Aaron, M.-P. Rosa-Ester (2021), які рекомендують профілактичний пероральний прийом N‑ацетилцистеїну лікарям, котрі часто контактують з носіями SARS-CoV‑2. N‑ацетилцистеїн здатен запобігати розвитку цитокінового шторму – однієї з основних небезпек для пацієнтів з COVID‑19 (рис. 2) (Mohanty R. R. et al., 2021).
Рис. 2. Потенційні механізми впливу N-ацетилцистеїну на цитокіновий шторм
Цікаво, що N‑ацетилцистеїн впливає також і на згортання крові, що особливо важливо при COVID‑19. Завдяки пригніченню вивільнення еластази та зниженню активності нейтрофілів цей препарат має потенціал запобігання тромботичним ускладненням (Wong K. K. et al., 2021).
Препарат N‑ацетилцистеїну Асиброкс (компанія World Medicine) представлений у формі шипучих таблеток по 200 або 600 мг. Основним показанням до застосування Асиброксу є лікування гострих і хронічних захворювань бронхолегеневої системи, що супроводжуються підвищеним утворенням мокротиння. Однак не варто вважати, що Асиброкс – це винятково муколітик. Дослідження всіх рівнів (in vitro, in vivo та клінічні) демонструють, що діюча речовина Асиброксу (N‑ацетилцистеїн) – це потужний імуномодулятор, протизапальний та антиоксидантний засіб, а також препарат із потенційним антибактеріальним і антитромботичним ефектом. Зазначені властивості обумовлюють доцільність включення Асиброксу до комплексної терапії COVID‑19.
Висновки
1. За відсутності препаратів прицільної дії лікування COVID‑19 передбачає переосмислення та використання добре вивчених препаратів із протизапальними, імунотропними й антиоксидантними властивостями.
2. N‑ацетилцистеїну притаманні відмінний профіль безпеки та висока ефективність у лікуванні хвороб дихальної системи, що обумовило науковий інтерес до цього препарату при COVID‑19.
3. Доведені in vitro та in vivo ефекти N‑ацетилцистеїну забезпечують цьому препарату гідне місце серед медикаментів для комплексної терапії COVID‑19.
4. На фармацевтичному ринку N‑ацетилцистеїн представлений, зокрема, препаратом Асиброкс (компанія World Medicine).
Медична газета «Здоров’я України 21 сторіччя» № 22 (515), 2021 р.