24 квітня, 2026
Нові можливості відновлення когнітивних функцій у загальній медичній практиці: синергія холіну, гінкго білоба та біоенхансерів
 Погіршення розумової діяльності, що визначається терміном «когнітивні порушення» (послаблення пам’яті, уваги, швидкості мислення, гостроти емоційного сприйняття), в наш час перестають бути ознакою винятково літнього віку. Через вплив хронічного стресу, перевантаження інформацією, перевтоми, серцево-судинні захворювання, наслідки вірусних інфекцій (зокрема, COVID‑19) стан когнітивного дефіциту дедалі частіше діагностують в осіб активного віку. Пацієнти з відповідними скаргами зустрічаються в практиці лікарів майже всіх спеціальностей. Подальший розвиток когнітивних порушень не лише суттєво погіршує якість життя хворого, а й спричиняє інвалідизацію, лягає тяжким тягарем на родину та систему охорони здоров’я.
Погіршення розумової діяльності, що визначається терміном «когнітивні порушення» (послаблення пам’яті, уваги, швидкості мислення, гостроти емоційного сприйняття), в наш час перестають бути ознакою винятково літнього віку. Через вплив хронічного стресу, перевантаження інформацією, перевтоми, серцево-судинні захворювання, наслідки вірусних інфекцій (зокрема, COVID‑19) стан когнітивного дефіциту дедалі частіше діагностують в осіб активного віку. Пацієнти з відповідними скаргами зустрічаються в практиці лікарів майже всіх спеціальностей. Подальший розвиток когнітивних порушень не лише суттєво погіршує якість життя хворого, а й спричиняє інвалідизацію, лягає тяжким тягарем на родину та систему охорони здоров’я.
На початковому етапі розвитку когнітивного дефіциту мозок ще має високий ресурс для відновлення своїх функцій. Саме тому питання адекватної нейропротекторної підтримки легких порушень та профілактики їхнього прогресування є критично важливими. Сьогодні когнітивні порушення – це не діагноз літнього віку, а щоденний виклик для лікаря, що потребує ефективних, безпечних та доступних методів терапії.
Холінергічна теорія порушення когнітивних функцій та уповільнення нейрорегенерації значною мірою пов’язує їхній розвиток із дефіцитом ацетилхоліну (АЦХ). АЦХ – ключовий нейромедіатор, що відповідає за пам’ять, увагу та швидкість мислення (Hasselmo M., 2006; Wurtman R., 2021). Холінергічна теорія базується на основі кореляції між рівнем АЦХ у мозку та когнітивними здібностями. Цей факт обґрунтовує застосування як симптоматичної терапії деменції нейродегенеративного генезу інгібіторів холінестерази (ферменту, що руйнує АЦХ) (NICE Guideline, 2024; Liu et al., 2025; Singh R. et al., 2026).
Підвищення рівня АЦХ можна досягти іншим шляхом – замість гальмування руйнації можна підвищити синтез цього важливого нейромедіатора. Цей шлях можливо реалізувати призначенням екзогенних холіновмісних сполук.
Холін – біологічно активна речовина (БАР), яка є головним компонентом для синтезу АЦХ. Вона надходить до організму людини з їжею, а також синтезується de novo, переважно в печінці. Одночасно холін є найважливішим компонентом фосфоліпідів мембран нервових клітин і клітинних органел (Blusztajn J., 2012; Amenta F. et al., 2012; Cucinotta D., 2018; Guan F. et al., 2024). За рахунок участі в синтезі сфінгомієліну холін відіграє певну роль у процесах мієлінізації нервових волокон. Отже, можна стверджувати, що холін є важливим субстратом для забезпечення нейропластичності – здатності мозку змінювати свою структуру та функцію у відповідь на новий досвід або ушкодження. Відповідно до холінергічної гіпотези цілком обґрунтованою видається пропозиція використання холіновмісних сполук як одного з напрямів корекції когнітивних порушень при хронічній церебральній недостатності. На відміну від використання інгібіторів ацетилхолінестерази призначення препаратів холіну – це перехід від простої стимуляції мозку до його структурно-функціональної регенерації. Це забезпечення нейронів одночасно як «паливом», так і «будівельним матеріалом» (Moreno H., 2021).
Холіновмісні препарати патогенетично обґрунтовані при станах, які супроводжуються як гострою, так і хронічною ішемією мозку. Це можуть бути порушення мікроциркуляції, пов’язані з атеросклерозом, артеріальною гіпертензією, цукровим діабетом, віковими змінами. В умовах хронічного стресу та порушень сну високий ризик ішемічного стану головного мозку наявний навіть у молодому працездатному віці. Стрес діє через активацію системи «гіпоталамус – гіпофіз – наднирники», що супроводжується постійним викидом кортизолу і катехоламінів, які, своєю чергою, сприяють вазоконстрикції та розвитку ендотеліальної дисфункції. Надлишок кортизолу сприяє розвитку нейрозапалення, безпосередньо ушкоджує клітини гіпокампа – центру пам’яті та навчання, що є прямою причиною когнітивного дефіциту. Сон – це не просто відпочинок, а активний процес відновлення мозку. Під час глибокого сну мозок очищується від метаболічного «сміття», відбувається процес консолідації пам’яті. Хронічне недосипання зумовлює накопичення білка бета-амілоїду, що є характерним для хвороби Альцгеймера, прискорює ураження дрібних судин головного мозку (Arias-Carrión O., 2025; Shlomi-Loubaton S. et al., 2025; Joshi S. et al., 2026). Пацієнт при цьому скаржиться на туман у голові, зниження концентрації, сповільнення швидкості реакції, складність засвоєння нової інформації, швидку втомлюваність під час розумової діяльності. Доцільність використання екзогенних холіновмісних сполук є визнаним патогенетично обґрунтованим напрямом лікування станів, що спричиняють когнітивний дефіцит. Їхнє призначення особливо важливо в період реабілітації після судинних катастроф, при хронічних ішемічних станах, постковідних порушеннях (Mukaetova-Ladinska E. et al., 2021; Reuben D. et al., 2024; Sohn M. et al., 2025; Kim H. et al., 2025; Cepeda-Pineda D. et al., 2025).
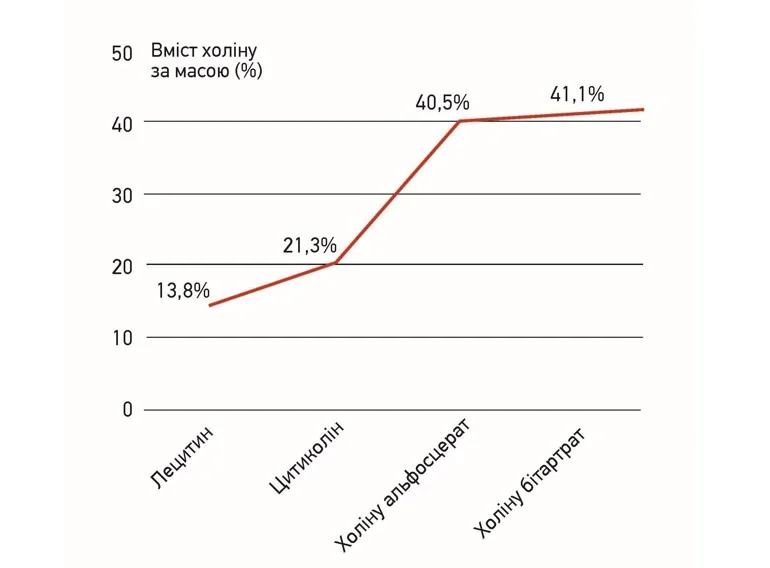
Результати лікування початкових стадій когнітивних порушень за допомогою холіновмісних сполук свідчать про суттєві відмінності в їхній ефективності залежно від особливостей хімічної будови. Важливою характеристикою є відсоткова частка вільного холіну в структурі молекули (її умовно можна охарактеризувати як «питому холіноємність» речовини). Наприклад, лецитин у дозі 100 мг – джерело холіну в 13,8 мг, що є найнижчим показником. Використання 100 мг цитиколіну забезпечує 21,3 мг холіну, а холіну альфосцерат ≈40,5 мг холіну – майже вдвічі більше. Ще вищу «холіноємність» має холіну бітартрат – 41,2% (рис. 1).
Рис. 1. Характеристика за масою холіновмісних сполук, представлених на фармацевтичному ринку України
Суттєво збільшити позитивний вплив холіну бітартрату на когнітивну функцію можна за рахунок синергізму зі сполуками, які впливають на інші патогенетичні ланки.
Порушення мікроциркуляції та активація ПОЛ – процеси, що прискорюють виникнення когнітивного дефіциту при хронічній ішемії. Навіть якщо в організмі достатньо холіну, через проблеми з належною мікроциркуляцією він не доходить до нейронів у потрібній концентрації. Синтез АЦХ – це енерговитратний процес, який гальмується в умовах гіпоксії. Щоб вижити, нейрон вимикає «другорядні» функції, першими страждають когнітивні (пам’ять, увага). Ішемія активує утворення вільних радикалів, які буквально «роз’їдають» фосфоліпідний шар мембран. Формується хибне коло: мозок руйнує власні мембрани, щоб отримати холін, а вільні радикали, що утворюються під час руйнації, ще більше прискорюють цей розпад (Wurtman R., 2021). Отже, для посилення позитивної дії холіну бітартрату на когніцію при хронічних ішемічних станах, цілком логічно поєднати його з БАР, яка здатна покращувати стан мікросудин і чинить антиоксидантну дію. Цим вимогам повністю відповідає стандартизований екстракт гінкго білоба.
Гінкго білоба як рослинний лікарський препарат давно завоював популярність у неврології завдяки поєднанню БАР, котрі забезпечують різноманітні фармакологічні ефекти: вазотропний (вазорегулюючий та антиагрегантний), антиоксидантний, мембраностабілізуючий, нейромедіаторний, нейротрофічний (Tan M. et al., 2015; Liu H. et al., 2020; Ge W. et al., 2021).
Флавоноїдні глікозиди гінкго (кверцетин, кемпферол, ізорамнетин) діють як м’які вазодилататори й антиагреганти. Вони стимулюють синтез оксиду азоту (NO), що розширює дрібні артерії та покращує капілярний кровоток, сприяють підвищенню тонусу вен, покращуючи в такий спосіб кровопостачання головного мозку, особливо в зонах ішемії. Одночасно ці сполуки знижують ризик мікротромбозів капілярів шляхом гальмування фактора активації тромбоцитів (PAF), що перешкоджає їхній агрегації. Їм також притаманна протинабрякова дія: зміцнення стінки капілярів, зменшення їхньої проникності критично важливі для запобігання мікронабряку мозкової тканини при ішемії.
Кверцетин і кемпферол забезпечують потужний подвійний антиоксидантний ефект гінкго. Як прямий антиоксидант кверцетин миттєво нейтралізує вільні радикали, що захищає мембрани нейронів від деструкції. Як непрямий антиоксидант він активує власну ендогенну систему ферментативного захисту клітини від ПОЛ. Кверцетин зв’язує іони металів (заліза та міді), які є каталізаторами продукції найнебезпечніших гідроксильних радикалів. Він активує ядерний фактор Nrf2, який є «головним вимикачем» антиоксидантної відповіді в геномі клітини. Це змушує нейрон синтезувати захисні білки. Навіть коли молекула кверцетину вже вивелася з організму, активовані ним ферменти продовжують захищати мозок від окиснювального стресу (Nowak A. et al., 2021; Sforzini L. et al., 2022).
Кемпферол, окрім прямої нейтралізації вільних радикалів, проявляє виражену непряму антиоксидантну активність, підтримуючи цілісність мітохондрій та стимулюючи синтез нейротрофічного фактора мозку (BDNF). Це створює синергію з холіном бітартратом: поки холін надає матеріал для побудови нейронних мембран, кемпферол забезпечує цей процес необхідною енергією та нейротрофічною підтримкою.
Наявні в гінкго терпенові лактони чинять на нервову тканину прямий нейропротекторний вплив: підвищують стійкість нейронів до дефіциту кисню, збільшують щільність рецепторів до АЦХ та дофаміну, що робить нейрон чутливішим до сигналів медіаторів (Li S. et al., 2023).
Слід підкреслити, що вищезазначені фармакологічні ефекти притаманні саме стандартизованому екстракту гінкго, котрий містить 24% флавонглікозидів. Саме флавонглікозиди (флавоноїди, які зв’язані з молекулами цукрів) є гарантами фармацевтичної якості та надійного терапевтичного ефекту препарату. Вільні флавоноїди дуже уразливі до окислення під час зберігання, погано розчиняються у воді, легко руйнуються в шлунку. На відміну від них флавонглікозиди стабільні при зберіганні, не руйнуються в кислому середовищі шлунка.
Поєднання холіну бітартрату та гінкго білоба є своєрідним біохімічно-фармакологічним тандемом. Холіну бітартрат забезпечує синтез медіатора АЦХ, постачає фосфоліпіди для «ремонту» ушкодженої мембрани нейронів і клітинних органел. Флавонглікозиди гінкго покращують стан судинного русла, що забезпечує доставку холіну до мозку (через судини), підвищують чутливість рецепторів до новоутвореного АЦХ, зупиняють процеси ПОЛ, що запобігає повторному руйнуванню щойно відновленої мембрани і в такий спосіб допомагає стабілізації ефекту холіну бітартрату (Zhang J. et al., 2020; Kennedy D. et al., 2023). На жаль, використовувати цей тандем із максимальною користю заважають помірна біодоступність холіну бітартрату та низька біодоступність флавонглікозидів гінкго.
Біодоступність – це термін, яким позначають кількість лікарської речовини (ЛР), що доходить до місця її дії в організмі людини. Слід підкреслити, що біодоступність – це поняття суттєво ширше, ніж просто відсоток всмоктування ЛР у шлунково-кишковому тракті (ШКТ). Для запобігання потенційній шкоді, яку можна завдати вживанням невідомої чужорідної речовини (ЧР), у процесі еволюції у нашому організмі була створена розгалужена «система безпеки». Мета її діяльності – максимально зменшити кількість ЧР, котра може досягти клітин життєво важливих внутрішніх органів, насамперед ЦНС.
Ця «система безпеки» діє декількома шляхами:
- перешкоджає всмоктуванню ЧР у ШКТ (всмоктуються лише ліпофільні сполуки; деякі речовини всмоктуються за допомогою спеціальних переносників);
- активно метаболізує ЧР у печінці (тобто перетворює їх на інші хімічні сполуки, які не здатні взаємодіяти з органами-мішенями та швидко виводяться з організму;
- забезпечує низьку чутливість рецепторів до ЧР;
- створює механізми запобігання проникненню ЧР крізь клітинні мембрани;
- створює спеціальні біологічні бар’єри, які запобігають можливості впливу ЧР на «керівні органи» (гематоенцефалічний (ГЕБ), гематоофтальмічний бар’єри).
Сукупність біологічних і біохімічних перешкод в організмі людини, які обмежують шлях ЛР від місця введення до органа-мішені, об’єднується поняттям «фармакологічні бар’єри». Результат такої «захисної діяльності» фармакологічних бар’єрів – ситуація, коли нові синтетичні ЛР і БАР, отримані з рослин, чудово працюють в умовах in vitro та не мають клінічно значущого ефекту in vivo. Так, значна частина молекул БАР гінкго білоба інактивується в кишечнику (пресистемний бар’єр), метаболізується в печінці до неБАР (печінковий бар’єр або ефект першого проходження) і не досягає системного кровотоку. Отже, та частка БАР гінкго, що пройшла вищезазначені бар’єри, має подолати найскладнішій з них – ГЕБ. Для цього БАР повинні мати певну спорідненість із транспортними системами ГЕБ. Що вищою є ця спорідненість, то більше молекул БАР пройде крізь ГЕБ і дістанеться органа-мішені (в нашому випадку – нейронів головного мозку).
Отже, діє на нейрони та формує клінічний ефект суттєво менша кількість молекул БАР, ніж міститься в рекомендованій дозі екстракту гінкго. Підвищення дози не вирішує проблеми – більша доза пов’язана з більшою імовірністю розвитку побічної дії та збільшує вартість лікарського препарату. Перспективним шляхом підвищення клінічної ефективності ліків без збільшення їхньої дози є використання явища біоенхансменту.
Біоенхансмент (англ. bioenhancement, біопідсилення) – це фармакологічний феномен, завдяки якому певна речовина (біоенхансер) здатна докорінно змінювати фармакокінетику, значно підвищувати біодоступність та біологічну активність іншої лікарської сполуки за їхнього комплексного введення. В сучасній медицині цей підхід розглядається як стратегічний шлях подолання «фармакологічних бар’єрів».
Упровадження принципу біоенхансменту у схеми лікування неврологічних пацієнтів надає такі переваги:
- можливість досягнення клінічного ефекту при менших дозах основного препарату (наприклад, холіну);
- зменшення токсичного навантаження на печінку за рахунок використання менших доз, що особливо важливо для літніх пацієнтів із коморбідністю;
- стабільність плазмової концентрації – біоенхансери допомагають уникнути «пікових» коливань концентрації ліків, забезпечуючи більш плавний та тривалий терапевтичний вплив;
- економічна доцільність – підвищення ефективності кожної одиниці активної речовини робить терапію раціональнішою та доступнішою.
Термін «біоенхансер» уперше використали індійські вчені (Atal C. et al., 1981) в публікації результатів досліджень, присвячених фармакологічному вивченню алкалоїду чорного перцю піперину. За результатами експериментів виявлено, що додавання незначної кількості піперину значно підвищує концентрацію інших ліків у крові. Відкриття не було випадковим. Учені звернули увагу на давні тексти Аюрведи, де в >200 рецептах ліків використовувався склад «Трікату» (суміш чорного перцю, довгого перцю та імбиру). «Трікату» додавали до ліків не для смаку, а для того, щоб допомогти основному компоненту краще працювати. Подальші дослідження (Atal C. et al., 2016) довели, що піперин здатен не просто допомагати, а радикально змінювати фармакокінетику деяких ЛР і підвищувати їхній рівень у плазмі крові на 30-200%. Це відкриття стало дійсно революційним, показало шлях до створення сучасних комплексних препаратів із підвищеною біодоступністю. Пізніше була продемонстрована ще виразніша дія піперину як біоенхансера – за комплексного введення він підвищував біодоступність куркуміну на 2000% (!) (Shoba G. et al., 1998).
Піперин сьогодні називають золотим стандартом біоенхансерів. Завдяки проведеним фундаментальним дослідженням Shoba G. і співавт. (1998), Khajuria A. та співавт. (2002), Han H.K. (2011), Raghunath I. та співавт. (2024) встановлені основні механізми його здатності докорінно змінювати кінетику призначених сполук.
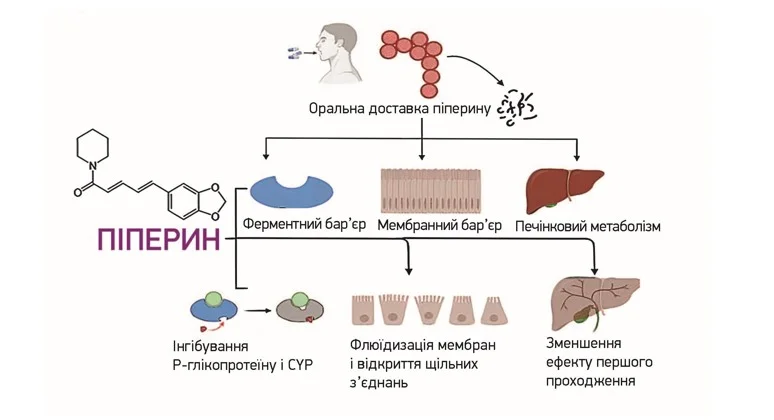
Піперин діє у такий спосіб (рис. 2):
- збільшує абсорбцію ЛР у ШКТ за рахунок посилення локального кровотоку та зміни конформації епітеліальних клітин кишечнику;
- пригнічує ферменти, що відповідають за глюкуронізацію ЛР у печінці (з’єднання із глюкуроновою кислотою перетворює ЛР на водорозчинні сполуки, які швидко та легко виводяться з організму із сечею або жовчю, – відбувається передчасна інактивація нейропротекторних молекул);
- модулює активність P-глікопротеїну (білка-насоса, без якого неможливі подолання ГЕБ і підвищення внутрішньоклітинної концентрації холіну та БАР гінкго).
Власна терапевтична активність піперину є корисним доповненням його функції провідника для інших ЛР.
Рис. 2. Основні напрями дії піперину як біоенхансера
Піперину притаманні:
- антиоксидантна дія (інгібує ПОЛ і підтримує рівень ендогенного глутатіону в тканинах мозку);
- антидепресивна дія (за рахунок інгібування МАО підвищує рівень медіаторів серотоніну та дофаміну);
- протизапальна дія (пригнічує експресію прозапальних цитокінів IL‑1, IL‑6, TNF, що є ключовим чинником у сповільненні процесів вторинної нейродегенерації при ішемії) (Mao Q. et al., 2011; Wattanathorn J. et al., 2008; Subramanian V. et al., 2015).
Наявні фармакологічні властивості піперину дозволяють прогнозувати синергічний вплив на ЦНС при комбінованому застосуванні з вазотропними та нейротропними засобами, а саме із холіновмісною сполукою та гінкго білоба (Singh A. et al., 2011).
Цікаво, що на можливість піперину та кверцетину, який є в гінкго білоба, працювати в тандемі, підсилюючи всмоктування один одного, звернули увагу вже в першій науковій роботі, присвяченій біоенхансерам (Atal C. et al., 1981). У подальших дослідженнях підтверджено суттєво вищу експозицію активних речовин гінкго білоба в плазмі крові при комбінації з піперином (Bi et al., 2019; Kesarwani K., Gupta R., 2013).
Комбінація холіну бітартрату, БАР з екстракту гінкго білоба та піперину сприяє формуванню стійкого терапевтичного відгуку в пацієнтів із когнітивним дефіцитом унаслідок хронічної ішемії за рахунок фармакологічного синергізму і феномену біоенхансменту. Додавання до комбінації біоенхансера піперину – це не просто допоміжний механізм, а інструмент оптимізації фармакотерапії, що дозволяє при використанні звичайних пероральних доз досягати цільових рівнів холіну і флавонглікозидів гінкго в органи‑мішені та максимально реалізувати нейропластичну дію холіну бітартрату й вазоактивний і антиоксидантний потенціал екстракту гінкго білоба.
Лікарські засоби на основі холіновмісних сполук і гінкго білоба зазвичай є монопрепаратами. Поєднання холіновмісної сполуки та екстракту гінкго білоба на світовому фармацевтичному ринку представлено у формі комплексних дієтичних добавок (БАД).
Гінкго білоба в поєднанні з вітамінами групи В і магнієм – класична комбінація, яка найчастіше представлена в аптечному асортименті. Різні варіанти такої комбінації зазвичай вважаються корисними та безпечними. Проте, як і з будь-яким «активним коктейлем», існують певні нюанси. Так, магній – досить «егоїстичний» мінерал. Його великі дози можуть сповільнювати всмоктування деяких речовин у шлунку. Якщо в складі комплексу є магнію оксид (найдешевша форма), він може діяти як легкий антацид, змінюючи кислотність шлунка, що потенційно впливає на швидкість вивільнення активних глікозидів гінкго. Магній (особливо у формі цитрату або оксиду) має легку послаблюючу дію. Гінкго білоба містить терпени, які можуть подразнювати слизову оболонку шлунка. Поєднання цих двох компонентів у деяких пацієнтів спричиняє дискомфорт у животі, метеоризм або діарею. Вітаміни групи B є одними з найалергенніших. За рахунок стимулюючої дії на ЦНС комбінація вітамінів групи В із гінкго в чутливих людей або при прийомі ввечері може зумовлювати тривожність чи безсоння. Певні комбіновані добавки «гінкго + вітаміни B + Mg» містять всього потроху, тобто такі дози компонентів, яких недостатньо для терапевтичного ефекту (Katzung B. et al., 2024). Більшість цих комбінацій розрахована на синергічну дію компонентів, але жодна не використовує компоненти, здатні до феномену біоенхансменту для підсилення терапевтичного ефекту.
Демацит Холін
Демацит Холін – комбінація, що містить холіну бітартрат і стандартизовані екстракти гінко та чорного перцю.
Стандартизовані екстракти – це витяжки з рослин, які містять суворо визначену та незмінну кількість головної активної речовини в кожній капсулі чи таблетці. Вони докорінно відрізняються від звичайних фітопрепаратів. Це вкрай важливо підкреслити, бо відтворення очікуваної терапевтичної дії можливо лише за умови використання високотехнологічної комбінації, де кожен відсоток активної речовини працює на результат.
Використання нативної рослинної сировини («аптечної трави») не гарантує стабільного вмісту БАР, оскільки їхня концентрація в рослині коливається залежно від вегетаційного періоду, кліматичних умов та способу зберігання. На противагу цьому, стандартизовані комплекси проходять процес високотехнологічного очищення та молекулярного контролю. Екстракт гінкго білоба із фіксованим вмістом (24% флавонглікозидів та 6% терпенових лактонів) має виражені антиоксидантні й вазотропні властивості. Додавання стандартизованого 95% піперину до фіксованої дози БАР гінкго створює умови для «фармакологічного прориву». Жорстка стандартизація дозволяє перетворити варіабельну природну субстанцію на високоточний фармакологічний інструмент із передбачуваною біодоступністю та чітким дозуванням. Для лікаря-практика саме стандартизована комбінація є гарантією того, що пацієнт отримає терапевтичну дозу нейропротектора, вазопротектора, антиоксиданта та біоенхансера в кожній капсулі. Це мінімізує ризик побічних ефектів від баластних речовин і забезпечує відтворюваність результатів, продемонстрованих у клінічних дослідженнях.
Отже, в арсеналі інструментів фармакологічного впливу на когнітивні функції в асортименті аптек наявні холіновмісні препарати для монотерапії та комплексні засоби. Комбінація холіну бітартрату, гінкго та піперину (стандартизований комплексний засіб Демацит Холін) за рахунок синергії активних речовин сприяє відновленню структури нейронів і синаптичного зв’язку, покращенню мозкового кровотоку та захисту від гіпоксії, із покращеною доставкою активних компонентів до цілі за рахунок властивостей піперину як біоенхансера.
Комбінація фармакологічних властивостей складових Демацит Холіну дозволяє зробити новий крок у стратегії збереження важливих когнітивних функцій – пам’яті, уваги, швидкості мислення, гостроти емоційного сприйняття в осіб працездатного віку, які тривалий час перебувають в умовах хронічного стресу, тривожності, порушення сну, фізичної та емоційної перевтоми. В таких умовах наразі, на жаль, знаходиться більшість населення нашої країни. Але якщо в молодому віці наявні достатньо великі компенсаторні можливості організму, то в осіб віком >40 років Демацит Холін можна розглядати як засіб, який допомагає підтримувати когнітивні функції.
Позитивний вплив складових Демацит Холіну на нейропластичність і мікроциркуляцію є доцільним за ознак легкої та помірної когнітивної дисфункції, що виникає на тлі стресу, перевтоми, порушень сну і вікових змін когніції. В умовах, у яких сьогодні перебуває практично вся країна, така підтримка особливо актуальна для збереження гостроти мислення. Схожі симптоми також характерні для пацієнтів із хронічною ішемією головного мозку, зокрема при атеросклерозі, артеріальній гіпертензії, цукровому діабеті, а також судинних і вегетативних розладах.
Збереження когнітивних можливостей – важлива складова якості життя людини в будь-якому віці. Саме тому Демацит Холін заслуговує на широку апробацію та подальший аналіз застосування в умовах реальної клінічної практики.
Список літератури знаходиться в редакції.
Медична газета «Здоров’я України 21 сторіччя» № 6 (617), 2026 р



 Бездітко Н.В.
Бездітко Н.В.