2 березня, 2026
Подвійні антагоністи рецепторів орексину як перспективний напрям лікування хронічних порушень сну
Сон – це короткочасне звільнення від тягаря життя.
А. Шопенгауер
 Без сумнівів, сон – це фундаментальна біологічна необхідність, зіставна з потребою в їжі чи воді. Однак для мільйонів людей у всьому світі, котрі страждають через симптоми інсомнії (безсоння), як-от труднощі із засинанням, підтриманням сну або невідновлювальний чи неякісний сон, дні та ночі можуть бути постійною боротьбою, що значною мірою впливає на психічне і фізичне здоров’я, погіршує якість життя, а також сприяє розвитку коморбідної патології. Наслідки інсомнії виходять далеко за межі впливу на окремого індивіда, оскільки можуть чинити каскадний ефект на домогосподарства, роботодавців і світову економіку [1].
Без сумнівів, сон – це фундаментальна біологічна необхідність, зіставна з потребою в їжі чи воді. Однак для мільйонів людей у всьому світі, котрі страждають через симптоми інсомнії (безсоння), як-от труднощі із засинанням, підтриманням сну або невідновлювальний чи неякісний сон, дні та ночі можуть бути постійною боротьбою, що значною мірою впливає на психічне і фізичне здоров’я, погіршує якість життя, а також сприяє розвитку коморбідної патології. Наслідки інсомнії виходять далеко за межі впливу на окремого індивіда, оскільки можуть чинити каскадний ефект на домогосподарства, роботодавців і світову економіку [1].
За різними даними, розлади сну охоплюють ≈50% населення світу; водночас лабораторно підтверджена клінічна чи хронічна інсомнія зустрічається лише в 6-23%. Ця різниця, найімовірніше, пов’язана з тим, що більшість пацієнтів не приділяє належної уваги цій патології, отже, часто займається самолікуванням. Слід зазначити, що ризик хронічної інсомнії є вищим у жінок, осіб літнього віку, людей, які працюють позмінно, осіб із сімейним анамнезом безсоння або коморбідними соматичними чи психічними розладами. Додатковими чинниками ризику розвитку цього захворювання є належність до негроїдної раси, низький соціально-економічний статус і служба в армії [2, 3].
Для переважної верстви населення нашої країни, що має справу з порушеннями сну під час повномасштабного вторгнення, вченими України сформульовано нове поняття – «бойове безсоння», яке поєднує порушення нічного та денного функціонування, котре виникає в умовах хронічної або гострої бойової загрози, незалежно від того, перебуває людина безпосередньо на передовій чи в тилу, під обстрілами або в стані тривожного очікування. Бойове безсоння може мати різні клінічні прояви – від затримки засинання, жахів і частих пробуджень до повної втрати відчуття сну, емоційного паралічу та вираженого денного виснаження [4].
За тривалістю інсомнія може бути хронічною (Chronic Insomnia Disorder), що має тривалість симптомів ≥3 міс із порушенням якості чи кількості сну та денними наслідками, або короткочасною (Short-term Insomnia Disorder) тривалістю <3 міс.
Нижче наведено чинні діагностичні критерії хронічної інсомнії згідно з ICSD‑3 (International Classification of Sleep Disorders, Third Edition – Міжнародна класифікація порушень сну, 3-тя редакція) (рис. 1) [13].
 Рис. 1. Діагностичні критерії хронічного безсоння
Рис. 1. Діагностичні критерії хронічного безсоння
Безперечним є той факт, що розуміння величезних суспільних наслідків хронічних порушень сну має вирішальне значення з метою визначення можливостей для масштабованих втручань, спрямованих на позитивний вплив на здоров’я, добробут і продуктивність людей, а також на користь суспільства загалом [1].
Підходи до лікування хронічного безсоння передбачають як фармакологічні, так і нефармакологічні методики. Лікарям слід обов’ язково враховувати супутні захворювання, які можуть сприяти порушенням сну в кожного конкретного пацієнта. Адекватна терапевтична корекція цих захворювань має вирішальне значення для ефективного вирішення проблеми інсомнії [7, 8].
Нефармакологічні методи. Як перша лінія терапії безсоння рекомендується когнітивно-поведінкова терапія, що на відміну від лікарських засобів, які зазвичай призначаються від безсоння, має мінімальний ризик побічних ефектів [9]. Водночас, поєднуючи в собі когнітивну терапію, поведінкові методи, як-от обмеження сну та контроль стимулів, з освітніми стратегіями, включаючи гігієну сну і тренінги з релаксації [7], з огляду на обмеженість часу в більшості пацієнтів цей метод може мати низький рівень комплаєнсу.
Фармакологічні методи. Фармакологічна корекція інсомнії може застосовуватися в пацієнтів, які не реагують на нефармакологічну терапію або в котрих симптоми є тяжкими [10]. Обирати лікарський засіб слід індивідуально відповідно до симптомів конкретного пацієнта, крім того, необхідно враховувати будь-які супутні захворювання [8]. Загальновідомо, що більшість снодійних препаратів дозволені лише для короткочасного застосування, вони можуть мати серйозні побічні ефекти та спричинити залежність [7, 11]. Призначаючи снодійні засоби молодим й активним пацієнтам, також слід брати до уваги високу ймовірність появи денної сонливості, що надзвичайно важливо для автомобілістів та осіб, умови праці котрих потребують уваги [12]. Ліки, котрі використовуються для лікування безсоння, можна класифікувати на такі, що схвалені Управлінням з контролю за якістю продуктів харчування та лікарських засобів США (FDA) для цього стану, а також ті, які використовуються поза показаннями [7]. Водночас не всі препарати від безсоння, схвалені FDA, схвалено Європейським агентством з лікарських засобів (EMA), тому вони можуть бути недоступними в Європі та в Україні [13].
Препарати, схвалені FDA для лікування безсоння [7, 13]:
- бензодіазепіни (тріазолам, флуразепам, темазепам, квазепам, естазолам);
- небензодіазепінові снодійні, т. зв. Z-препарати (золпідем, залеплон, зопіклон, есзопіклон);
- агоністи рецепторів мелатоніну (рамелтеон);
- селективні антагоністи рецепторів гістаміну H1 (доксиламін, доксепін);
- подвійні антагоністи рецепторів орексину (суворексант, лемборексант, даридорексант, ворнорексант).
Препарати, що також використовуються для лікування порушень сну, але можуть бути офіційно не схвалені FDA саме для безсоння [7]:
- інші бензодіазепіни;
- мелатонін (швидкого вивільнення – доступний в Україні як у складі лікарських засобів, так і в дієтичних добавках; мелатонін пролонгованої дії схвалено EMA для лікування безсоння в пацієнтів віком >55 років);
- седативні антидепресанти;
- атипові антипсихотичні засоби;
- деякі антигістамінні препарати;
- деякі засоби, що впливають на рецептори γ-аміномасляної кислоти (ГАМК).
Упродовж останнього десятиріччя увагу клініцистів усього світу привертає значна ефективність у лікуванні проявів інсомнії нового класу лікарських засобів – подвійних антагоністів рецепторів орексину. У 2014 році FDA схвалило перший препарат із цієї групи – суворексант [14].
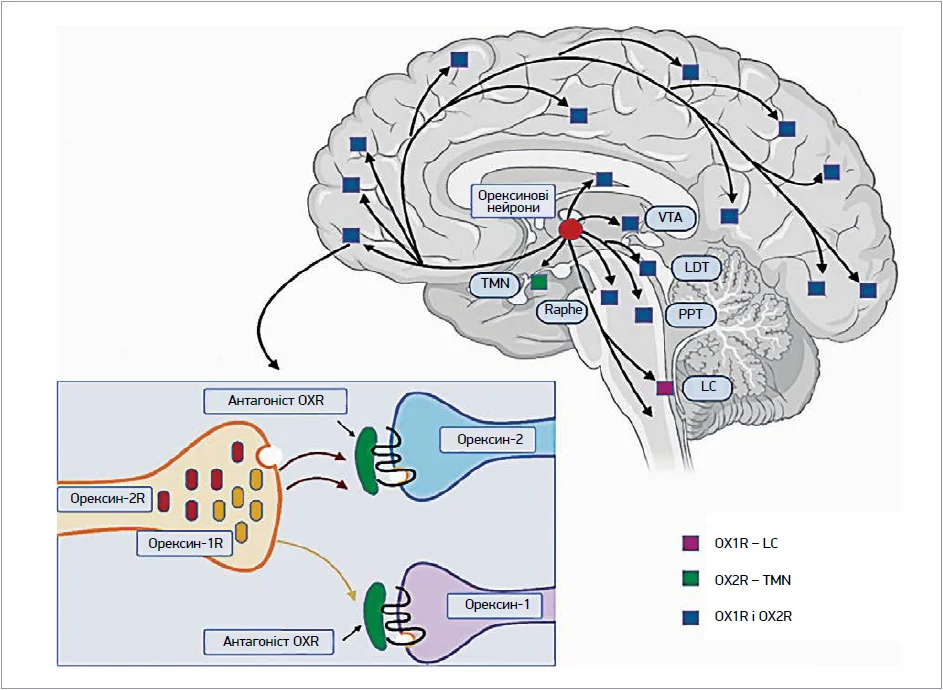
Орексинова система включає два нейропептиди – орексин‑1 і орексин‑2, які зв’язуються з двома типами рецепторів (OX1R, OX2R). Ці рецептори переважно розташовані в гіпоталамусі – ділянці мозку, відповідальній за підтримку неспання. Коли орексинові пептиди зв’язуються із цими рецепторами, вони сприяють збудженню та пригнічують сон. Подвійні антагоністи орексинових рецепторів (dual orexin receptor antagonists, DORA) реалізують свій терапевтичний ефект шляхом блокування сигналів, відповідальних за активацію неспання, а не шляхом прямої індукції сну, як це відбувається в разі застосування бензодіазепінів або небензодіазепінових агоністів рецепторів ГАМК. Отже, DORA блокують взаємодію між орексиновими пептидами та їхніми рецепторами (рис. 2).
Інгібуючи цей шлях, такі сполуки знижують сигнали пробудження, що підтримують неспання. Отже, DORA можуть допомогти спричинити сон і підтримувати його безперервність [15].
Слід звернути увагу, що на сьогодні серед препаратів цієї групи поки лише даридорексант схвалений ЕМА. Препарат дозволено для лікування безсоння в дорослих із тривалістю симптомів щонайменше 3 міс, крім того, він демонструє клінічно значущий вплив на денне функціонування [7].
За роки спостережень накопичується вагома доказова база ефективності DORA: наприклад, метааналіз 4 рандомізованих клінічних досліджень включав 2271 пацієнта з діагнозом безсоння, які отримували даридорексант у дозах 5, 10, 25 або 50 мг чи плацебо. Результати показали, що даридорексант у дозах 25 і 50 мг достовірно покращував показники, пов’язані з безсонням, порівняно із плацебо. Через 1 міс лікування доза 50 мг продемонструвала виражену короткострокову ефективність зі значним зменшенням часу неспання після засинання – Wake After Sleep Onset (WASO); стандартизована різниця середніх значень (Standardized Mean Difference, SMD) становила -0,62, латентності сну (LPS; SMD -0,36) та денної сонливості (SMD -0,37), а також зі збільшенням загальної тривалості сну (TST; SMD 0,45), у всіх випадках p<0,001. Зазначені покращення зберігалися протягом 3 міс, при цьому доза 50 мг продовжувала демонструвати кращі результати порівняно з дозою 25 мг за всіма оцінюваними параметрами. На 3-му місяці лікування спостерігалося зниження WASO та LPS (обидва SMD -0,53), збільшення TST (SMD 0,35) та покращення денного функціонування, оціненого за допомогою опитувальників Insomnia Daytime Symptoms та Impacts (SMD -0,31). Доза 25 мг також забезпечувала статистично значущі, хоча і менш виражені, покращення за тими самими показниками. Клінічний ефект спостерігався вже на 1-2-й день лікування, причому доза 50 мг забезпечувала найстабільніші результати. Найчастіше повідомляли про такі побічні ефекти, як назофарингіт, втома та головний біль. Загалом даридорексант добре переносився в усіх досліджуваних режимах [16].
Для оцінки довгострокової безпеки та переносимості даридорексанту проведено подвійне сліпе плацебо-контрольоване дослідження, в якому взяли участь 804 пацієнти, з яких 801 хворий отримав щонайменше одну дозу досліджуваного лікування – даридорексант у дозах 10, 25 або 50 мг чи плацебо. Період лікування тривалістю 40 тиж завершувався 7-денним періодом «вимивання» на прийомі плацебо. Результати продемонстрували покращення параметрів сну та денного функціонування з найвираженішим ефектом при застосуванні дози 50 мг. Даридорексант достовірно збільшував суб’єктивно оцінену тривалість сну та покращував денне функціонування, при цьому найсильніший ефект спостерігався на 12-му тижні (збільшення TST на 20,4 хв; 95% довірчий інтервал (ДІ) 4,2-36,5) і зберігався до 36-го тижня (збільшення TST на 17,8 хв; 95% ДІ від -0,4 до 35,9). Також було зафіксовано покращення за всіма шкалами опитувальників Insomnia Daytime Symptoms та Impacts порівняно із плацебо. Частота побічних ефектів була схожою в усіх групах лікування; найпоширенішим із них виявився назофарингіт. Інші небажані явища, зокрема падіння, головний біль і сонливість, реєструвалися менш ніж у 3% пацієнтів, тоді як запаморочення та втома – менш ніж у 2% хворих будь-якої групи. Протягом 12 міс застосування даридорексанту така терапія була безпечною і добре переносилася та не спричиняла денної сонливості наступного дня, розвитку толерантності, рикошетного безсоння, залежності чи синдрому відміни за жодної з досліджуваних доз. Отримані результати підтверджують доцільність використання даридорексанту для довготривалого лікування безсоння [17].
На прикладі даридорексанту не викликає сумнівів клінічно доведена ефективність у лікуванні безсоння, безпека та можливість тривалого застосування (за потреби) цього класу препаратів. Що стосується інших представників DORA в світі, то узагальнено наявні наразі часткові дані (табл.).
|
Таблиця. Основні DORA, наявні у світі [18] |
||||
|
Препарат |
Суворексант |
Лемборексант |
Даридорексант |
Ворнорексант |
|
Рік схвалення FDA |
2014 |
грудень 2019 |
січень 2022 (США та ЄС) |
серпень 2025 (Японія) |
|
Період напіврозпаду, год |
12 |
17-19 |
8 |
1,5-3 (досліджується) |
|
Тmax, год |
2 |
1-3 |
1-2 |
1,5-3 |
|
Ефективне дозування згідно з дослідженнями |
5-20 мг |
5-10 мг |
25-50 мг |
5-10 мг |
|
Клінічна ефективність |
безсоння |
безсоння |
безсоння, покращення денного функціонування |
безсоння |
|
Основні протипоказання |
Нарколепсія, печінкова недостатність |
|||
|
Побічні явища |
астенія, ксеростомія, надмірна денна сонливість, сонний параліч, гіпнагогічні галюцинації, катаплексія та суїцидальні думки |
сонливість, денні функціональні порушення, сонний параліч, гіпнагогічні / гіпнопомпічні галюцинації, симптоми, схожі на катаплексію, парасомнії |
когнітивні порушення, тахіфренія, розлад харчової поведінки, пов’язаний зі сном, гіперчутливість, ксеростомія, пришвидшене серцебиття |
сонливість, назофарингіт |
Отже, DORA відрізняються між собою за низкою показників. Із клінічного погляду коротший період напіврозпаду, властивий ворнорексанту, може надати низку клінічних переваг для пацієнтів, у т. ч. у вигляді повної відсутності денної сонливості.
Що стосується майбутнього цього класу препаратів в Україні, то відповідно до оновлених у 2023 році та чинних європейських настанов із лікування безсоння [13] подвійні антагоністи орексинових рецепторів можуть застосовуватися протягом періоду до 3 міс. В окремих випадках лікування може бути продовжене до 1 року, однак переваги та можливі ризики такої терапії слід обговорювати з кожним пацієнтом індивідуально [7]. Потенційно в найближчій перспективі в арсеналі клініцистів нашої країни може з’явитися ще один клас препаратів для лікування інсомнії, що мають доведену клінічну ефективність, незначні протипоказання та побічні явища порівняно із вже зареєстрованими лікарськими засобами, котрі можуть призначатися на триваліший термін.
Список літератури знаходиться в редакції.
Медична газета «Здоров’я України 21 сторіччя» № 1 (612), 2026 р



 Кравчун П.П.
Кравчун П.П.
 Дунаєва І.П.
Дунаєва І.П.