24 квітня, 2021
Діабетична ретинопатія – зона відповідальності офтальмолога чи ендокринолога?
За підсумками Всеукраїнського офтальмологічного марафону (9 березня)
Розмежувати «сфери впливу» в медицині досить складно. Діагностика й лікування більшості нозологій – не «соло», а «дует» або навіть «ансамбль» фахівців різних спеціальностей, адже передбачає міждисциплінарний підхід і постійну взаємодію. Чимало точок дотику й між офтальмологією й ендокринологією. Зокрема, йдеться про цукровий діабет (ЦД), насамперед 2 типу, й одне з його ускладнень – діабетичну ретинопатію (ДР).
9 березня в рамках Всеукраїнського офтальмологічного марафону, що було організовано Всеукраїнським альянсом офтальмологів, провідні експерти згаданих галузей – Оксана Петрівна Вітовська, доктор медичних наук, професор кафедри офтальмології Національного медичного університету ім. О. О. Богомольця (м. Київ), та Любов Костянтинівна Соколова, доктор медичних наук, керівник відділу діабетології ДУ «Інститут ендокринології та обміну речовин ім. В. П. Комісаренка» (м. Київ) – проаналізували сучасні підходи до діагностики порушень вуглеводного обміну, стратегії лікування й можливості фармакотерапії.
 Захід відбувся онлайн у форматі панельної дискусії: до 2-годинного обговорення проблематики та 4 презентованих клінічних випадків долучилися всі охочі слухачі. Найважливіші тези, що прозвучали під час цього надзвичайно цікавого та змістовного ефіру, наведено нижче.
Захід відбувся онлайн у форматі панельної дискусії: до 2-годинного обговорення проблематики та 4 презентованих клінічних випадків долучилися всі охочі слухачі. Найважливіші тези, що прозвучали під час цього надзвичайно цікавого та змістовного ефіру, наведено нижче.
Отже, питання в студію!
Поширеність ЦД і ДР
? Наскільки поширеним є ЦД залежно від географічного регіону? Чи відображає офіційна статистика реальну ситуацію?
Нині людство переживає пандемію коронавірусної хвороби (COVID‑19). Проте, як влучно зазначили спікерки, це не єдина пандемія. Величезних масштабів набула проблема ЦД: його поширеність зростає на всіх континентах (і це без урахування недіагностованих випадків).
У Європі розповсюдженість ЦД у 2014 р. оцінювали в 7,9%, при цьому очікується зростання показника до 10,3% у 2035 р. (у Північній Америці – 11,4 та 12,5%, у Південно-Східній Азії – 8,3 та 10,1% відповідно). В Україні кількість хворих на ЦД наразі сягає 1,5 млн. Фахівці припускають, що насправді порушення вуглеводного обміну мають 3 млн осіб, що вдвічі перевищує офіційну статистику та є зіставним показником із даними європейських країн.
Істотно збільшується у світовому масштабі й кількість випадків ДР. Існує т. зв. правило третини: кожен 3-й пацієнт із ЦД має ДР. У 2015 р. із 415 млн хворих на ЦД у світі в 145 млн осіб (35%) виявляли ДР, із них 45 млн мали загрозу втрати зору (кожен 10-й хворий на діабет). Прогнозують, що у 2045 р. кількість пацієнтів із ЦД зросте до 642 млн, із ДР – до 224 млн, із ризиком втратити зір – до 79 млн.
В Україні офіційно зареєстровано приблизно 300 тис. пацієнтів із ДР. І якщо застосувати правило третини та врахувати кількість хворих на діабет, то можемо говорити про те, що кожний 2-й випадок патології не діагностований. За останні 40 років питома вага хворих на офтальмодіабет у структурі первинної інвалідності за зором в Україні збільшилася в 9 разів. Серед людей з інвалідністю через офтальмодіабет 50% – сліпі та слабкозорі особи.
ЦД і принципи діагностики
? Яке дослідження краще виконувати за наявності підозри на ЦД – пероральний глюкозотолерантний тест (ПГТТ) або визначення рівня глікозильованого гемоглобіну (HbA1c)?
Нерідко пацієнти звертаються до фахівців іншого профілю з приводу ускладнень (наприклад, до офтальмолога з проявами ДР), не підозрюючи, що вже тривалий час страждають на ЦД 2 типу. Тому лікарі всіх спеціальностей повинні зберігати настороженість щодо ЦД і в разі підозри рекомендувати проведення ПГТТ, оцінку рівня HbA1c або консультацію ендокринолога.
Показник HbA1c ≥6,5% – достатній аргумент для встановлення діагнозу ЦД (додаткові тести не потрібні). Рівень HbA1c <6,5% не гарантує відсутність порушень вуглеводного обміну, пацієнту варто визначити концентрацію глюкози натще.
Якщо в пацієнта HbA1c <6,5%, порушена глікемія натще (ПГН) >7 ммоль/л або ПГТТ >11,1 ммоль/л, верифікують ЦД 2 типу.
Якщо HbA1c <6,5%, а ПГН <7 ммоль/л, пацієнта скеровують до ендокринолога та призначають йому ПГТТ.
? Порушена толерантність до глюкози → ЦД 2 типу. Як часто спостерігається трансформація?
Рівень HbA1c 6,5% – гранична межа, котру можна трактувати як ЦД; при цьому в лікуванні можна обмежитися зміною способу життя, посиленням фізичної активності, правильним харчуванням, обійтися без пероральних цукрознижувальних засобів або призначити тільки метформін.
Як свідчать дані літератури, в 30% хворих порушення вуглеводного обміну прогресує в класичний ЦД 2 типу без етапу предіабету.
? Коли та для чого визначають індекс НОМА?
Індекс НОМА відображає наявність інсулінорезистентності (ІР). Розрахунок індексу НОМА проводиться за формулою: інсулін натще × глюкоза натще / 22,5. Референсні значення – 0-3,0.
Експерти наголосили, що цей параметр оцінюють здебільшого в клінічних дослідженнях. У реальній щоденній практиці його варто визначати в пацієнтів із надмірною вагою / ожирінням, які мають недостатню мотивацію знижувати масу тіла. Адже, як вдало зазначила Л. К. Соколова, «цифри в червоній рамочці в результатах досліджень стимулюють хворих до дії краще, ніж слова лікаря».
? Кому з пацієнтів слід рекомендувати генетичні дослідження?
Генетичні дослідження актуальні за умови обтяженого сімейного анамнезу щодо ЦД – коли хворіє один із батьків або декілька близьких родичів: батько, сестра та ін. Вони дають змогу виявити мутації генів, які зумовлюють специфічні типи ЦД (класифікують як MODY). Серед варіантів хвороби найпоширеніші MODY2 та MODY3.
MODY3 – ЦД 1 типу, що маніфестує в дорослому віці (15-35 років) або під час вагітності. Для цього варіанта діабету характерні глюкозурія, нормальні показники С‑пептиду (підшлункова залоза функціонує, відзначається варіабельність рівнів глікемії), хороша відповідь на застосування препаратів сульфонілсечовини (зокрема, гліклазиду). Проте надалі порушення прогресують і зумовлюють потребу в інсулінотерапії.
? Яка середня тривалість життя пацієнтів із ЦД 1 типу, що маніфестував у ранньому дитинстві?
«Усе залежить від своєчасності діагностики, лікування й мотивації пацієнта суворо дотримуватися рекомендацій, досягти компенсації. Хворі, котрі мають декомпенсацію ЦД, зазвичай помирають у молодому віці від порушення ниркової функції та прогресування хронічної хвороби нирок. Середня тривалість життя пацієнтів, які досягають стану компенсації ЦД і підтримують його, така сама, як у загальній популяції», – прокоментувала Л. К. Соколова.
ЦД і вагітність
? Як часто у вагітних діагностується гестаційний ЦД?
За інформацією американських науковців, у 10%. За даними вітчизняної статистики (принаймні, офіційної), показники значно нижчі.
Варто зауважити, що вагітність – стан фізіологічної ІР. ЦД частіше дебютує в II-III триместрах, коли ІР сягає максимуму. Усім вагітним показаний ПГТТ на 24-28-му тижні вагітності.
Кожна наступна вагітність підвищує вірогідність розвитку порушень вуглеводного обміну.
? Після пологів параметри вуглеводного обміну нормалізуються чи порушення прогресують?
Якщо це гестаційний ЦД, часто після пологів показники повертаються до нормальних значень. Однак ризик розвитку ЦД 2 типу в такої пацієнтки залишається підвищеним, тому вона має перебувати під наглядом сімейного лікаря, що 3 роки виконувати ПГТТ і контролювати рівень HbA1c.
За появи патологічних змін, типових для предіабету, обстеження варто проводити частіше – щороку, щоби своєчасно зафіксувати розвиток ЦД 2 типу.
ЦД і сучасні підходи до лікування
Лікування ЦД має бути комплексним, із корекцією факторів ризику, зміною способу життя та призначенням адекватної фармакотерапії (пероральні цукрознижувальні засоби, інсулін).
? Кетодієта при ЦД: модне віяння чи дієва стратегія харчування?
На переконання Л. К. Соколової, кетодієта не має становити основу життя. Її призначають на нетривалий час (до 1 міс), а перед початком обов’язково відстежують стан нирок, адже прийом великої кількості білкової їжі асоціюється з ризиком появи ниркової дисфункції та погіршення хронічної хвороби нирок. Краще не повністю відмовлятися від вуглеводів, а значно обмежити їх споживання.
? Чи потрібні фізичні навантаження хворим на ЦД?
«Так, так і ще раз так! Дані про їхню ефективність містяться в доказових джерелах, рекомендаціях, неодноразово перевірені й підтверджені життям. Але маються на увазі не прогулянки в легкому режимі, а щонайменше 30-40 хв інтенсивних фізичних навантажень щодня, – наголосила Любов Костянтинівна. – Навіть якщо людина тільки питиме воду, проте не посилить фізичної активності, досягти покращення перебігу ЦД і знизити вагу не вдасться».
? Які замінники цукру рекомендуються пацієнтам із ЦД?
Спікерки підкреслили, що зазвичай радять віддавати перевагу рослинним препаратам, як-от стевія. Натомість небезпечними вважають продукти, що містять фруктозу. Останні здатні провокувати посилення ІР.
? До яких цільових рівнів потрібно знижувати глюкозу крові?
В ідеалі – до нормальних значень. Проте слід усвідомлювати: що старший вік пацієнта та що вираженіша декомпенсація, то помітніше цільові значення зсуваються в бік вищих показників.
? Коли переходити на інсулінотерапію?
У випадках, коли пероральна цукрознижувальна терапія не забезпечує терапевтичного ефекту.
? З якого віку в лікуванні ЦД дозволяється використовувати інсулінову помпу?
Від народження, якщо батьки обізнані, як за нею доглядати. У рекомендаціях Американської діабетичної асоціації (ADA, 2021) вказано, що при терапії дітей/підлітків із ЦД слід розглядати можливість застосування інсулінової помпи як фізіологічного та зручного способу лікування.
? Кому інсулінова помпа протипоказана?
Це технологічний пристрій, який може застосовуватися кожним, хто поінформований про правила використання й обслуговування, мотивований їх дотримуватися.
ЦД і порушення зору
? На якому етапі пацієнта з ЦД повинен оглянути офтальмолог?
У разі ЦД 2 типу в 15-40% випадків ознаки ДР фіксуються на етапі встановлення діагнозу. В останній редакції рекомендацій ADA (2021) наголошується, що пацієнт із ЦД 2 типу повинен бути оглянутий офтальмологом одразу після встановлення діагнозу.
При цьому, як показують дані Всесвітньої організації охорони здоров’я (ВООЗ), лише 50% хворих на ЦД, які потребують консультації офтальмолога, звертаються до спеціаліста. Серед пацієнтів, які пройшли офтальмологічне обстеження, адекватне лікування отримують менше половини. На жаль, в Україні ситуація видається гіршою. На часі імплементація на державному рівні сучасних програм скринінгу, розроблених ВООЗ, Міжнародною діабетичною федерацією, безумовно, з урахуванням тих напрацювань, які вже є в Україні.
? На які показники офтальмологу варто звернути особливу увагу?
Передусім на рівень артеріального тиску (АТ), HbA1c (вихідний), швидкість зниження HbA1c на тлі лікування.
Чітких рекомендацій стосовно поняття «швидкість зниження» концентрації HbA1c немає; отримані дані трактуються індивідуально в кожному випадку. Коли офтальмолог спостерігає швидке прогресування в пацієнта змін очного дна (дрібних крововиливів, розширення вен сітківки, інтраретинальних судинних аномалій, діабетичного макулярного набряку – ДМН та ін.), для ендокринолога це може вказувати на надмірно швидку компенсацію ЦД у хворого, що асоціюється з численними ризиками.
? З якою періодичністю хворі на ЦД з адекватним контролем захворювання повинні проходити повторний огляд у офтальмолога?
- ДР відсутня, непроліферативна ДР (легкого ступеня) – 1 раз на 1-2 роки (залежить від супутніх факторів ризику).
- Непроліферативна ДР (легкого ступеня) – 1 раз на 6-12 міс.
- Непроліферативна ДР (середнього ступеня) – 1 раз на 3-6 міс.
- Непроліферативна ДР (тяжкого ступеня) – 1 раз на 2-3 міс.
- Наявність ДМН – щомісяця або частіше (до стабілізації процесу за допомогою лазерної чи фармакотерапії; надалі частота спостереження залежить від того, який препарат використовується, в середньому 1 раз на 3 міс).
? Ведення пацієнтів із ДМН: що говорять рекомендації?
Відповідно до настанов EURETINA (Schmidt-Erfurth U. et al., 2017), у пріоритеті анти-VEGF‑терапія, що має переваги порівняно з лазерною терапією щодо структурних змін і гостроти зору.
За вихідної найкраще скорегованої гостроти зору (BCVA) ≥69 букв (≥20/40 за таблицею Снеллена) всі засоби з анти-VEGF‑активністю мають рівнозначну ефективність. У разі ДМН і вихідної BCVA <69 букв (≥20/50 за таблицею Снеллена) препаратом вибору є афліберсепт (рівень доказів А). Він виявився ефективнішим за бевацизумаб після 2 років лікування та за ранібізумаб – після 1 року лікування.
? Чи потрібно офтальмологу відтерміновувати початок анти-VEGF‑лікування, очікуючи нормалізації показників вуглеводного обміну, найперше глікемії?
Ні, оскільки концентрація HbA1c жодним чином не корелює з ефектами та прогнозом інтравітреальної анти-VEGF‑терапії.
Корекція ендокринних і офтальмологічних порушень має відбуватися паралельно, а не послідовно!
? Анти-VEGF‑терапія та лазерні втручання: як поєднувати?
Спочатку застосовується анти-VEGF‑терапія, щоб усунути ДМН, а потім здійснюється лазерне лікування. За наявності макулярного набряку лазерна терапія може призвести до його посилення.
? Які показники вуглеводного обміну потрібно контролювати перед проведенням офтальмологічних оперативних втручань у пацієнтів із ЦД?
Рівень глікемії натще, постпрандіальний рівень глюкози, адже моніторинг тільки показника HbA1c не забезпечить об’єктивного уявлення про ситуацію.
ЦД, ДР і фенофібрат
? Яке місце в терапії ДР посідає фенофібрат?
Фенофібрат (Трайкор®, Abbott) продемонстрував хороші результати у випробуваннях ACCORD Eye та FIELD.
У дослідженні ACCORD Eye оцінювали вплив фенофібрату на прогресування ДР. Майже 1600 пацієнтів із ЦД 2 типу розподілили на групи прийому симвастатину + фенофібрату чи симвастатину + плацебо. ДР діагностувалася в кожного 2-го пацієнта (в 99% випадків – непроліферативна форма). Фенофібрат знижував ризик прогресування ДР у пацієнтів із ЦД 2 типу: в загальній популяції обстежуваних – на 40%, серед хворих із діагностованою ДР – на 57%. Терапія забезпечувала ефективність незалежно від рівнів тригліцеридів (ТГ) і холестерину ліпопротеїнів високої щільності (ХС ЛПВЩ).
В офтальмологічному субдослідженні FIELD (n=1012) вивчали, чи зменшує тривале лікування фенофібратом імовірність прогресування ДР і потребу в лазерному втручанні в пацієнтів із ЦД 2 типу порівняно з групою плацебо. Фенофібрат на 31% знижував необхідність проведення першої лазерної терапії при ДР. Лікування фенофібратом допомогло зменшити загальну кількість курсів лазерної хірургії ДР на 37%.
Як показало субдослідження FIELD, фенофібрат істотно (на 79%) знижував ризик прогресування ДР, а також імовірність виникнення серйозної патології сітківки (на 34%).
Загальне зниження частоти прогресування ДР на тлі застосування фенофібрату, за даними описаних спостережень, становило 60%.
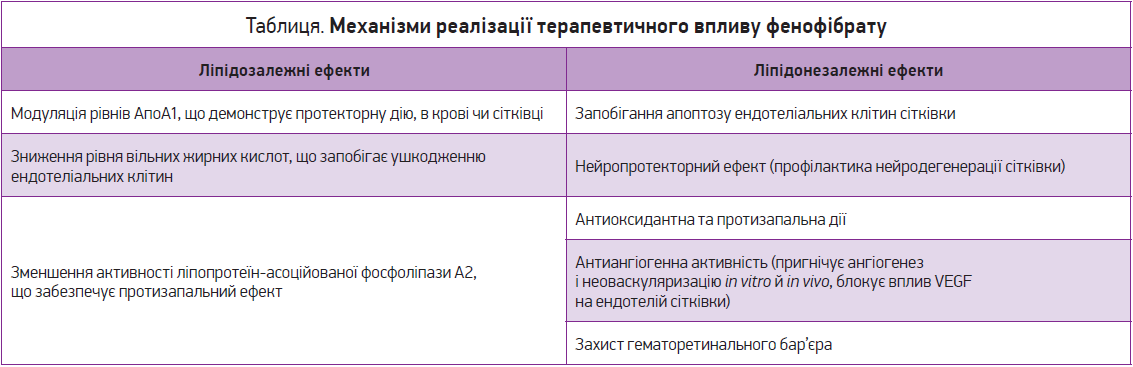
? Завдяки яким механізмам реалізується терапевтичний вплив фенофібрату?
Позитивні ефекти фенофібрату реалізуються шляхом ліпідозалежних і ліпідонезалежних механізмів (табл.).
В яких рекомендаціях/протоколах як терапевтична опція при ДР пропонується призначення фенофібрату?
Останні рекомендації ADA (2021), як і попередні версії, наголошують, що препаратом для зниження ризику прогресування ДР є саме фенофібрат.
? Офтальмолог чи ендокринолог: хто повинен зробити перший крок до призначення фенофібрату?
Слід розуміти, з якою метою призначається фенофібрат – не суто як ліпідознижувальний препарат (до речі, основна точка його прикладання – ТГ, а не загальний холестерин, холестерин ліпопротеїнів низької щільності чи ХС ЛПВЩ), а для сповільнення прогресування ДР, що реалізується за рахунок ліпідонезалежних механізмів. Підвищені показники ТГ – додатковий аргумент на користь призначення препарату Трайкор® 145 мг. Він допомагає вбити декількох зайців одразу: сповільнює прогресування ДР, впливає на концентрацію ТГ, запобігає ускладненням, зумовленим швидкою компенсацією ЦД.
Перший поштовх до використання фенофібрату повинні дати офтальмологи, спираючись на дані про зміни очного дна. Завдання ендокринологів – проаналізувати ліпідний профіль. А на основі отриманих даних фахівці спільно приймають рішення.
Якщо йдеться про нормалізацію тільки ліпідних параметрів, краще вибрати статини.
? На який термін призначається Трайкор® 145 мг?
Відповідно до результатів досліджень FIELD та ACCORD Eye, використання фенофібрату протягом менш ніж 8 міс недоцільне: суттєві розбіжності в ефективності лікування спостерігалися після цього періоду. До того ж ДР є хронічним захворюванням, яке прогресує. Тому, як у випадку з антигіпертензивною терапією, слід уживати формулювання «тривале» лікування, бо психологічно воно сприймається легше, ніж «пожиттєве».
? Які переваги властиві препарату Трайкор® 145 мг із точки зору клініцистів і пацієнтів?
Насамперед Трайкор® 145 мг (Abbott) – єдиний таблетований препарат із неанти-VEGF‑активністю, що доведено сповільнює прогресування ДР. Він підходить для лікування ДР будь-якої стадії. Має простий і зручний режим використання – по 1 таблетці 1 раз на день.
? Чи потрібно оцінювати перед призначенням фенофібрату рівні печінкових ферментів аспартатамінотрансферази й аланінамінотрансферази?
Перед використанням статинів, фібратів бажано визначити вказані параметри, щоб виключити можливі протипоказання до застосування.
? Чи існують вікові обмеження стосовно застосування фенофібрату?
Ні, жодних обмежень такого роду для дорослих осіб рекомендації не містять. Даних щодо застосування у віці до 18 років немає.
ЦД й інші офтальмологічні порушення
? Якими симптомами з боку органа зору, крім ДР, супроводжується ЦД?
За даними літератури, у 80% пацієнтів із ЦД виникають прояви синдрому сухого ока (ССО). Йому притаманні відчуття дискомфорту («піску» в очах), нечіткість зору («дивлюся – все розмите, а після кліпання очима картинка покращується») тощо. Така нестабільність зору вказує на погіршення якості слізної плівки, негативно впливає на гостроту зору.
? Якої тактики дотримуватися в лікуванні ССО?
Комбінованого підходу: використовувати сльозозамінники + контролювати фактори ризику (в усіх хворих на ЦД, не тільки з офтальмологічними порушеннями!) + приймати антиоксиданти.
«На українському ринку представлений величезний асортимент сльозозамінників. Для мене хорошим вибором є гіалуронат натрію без консервантів, фосфатів і з високим коефіцієнтом зволоження, – поділилася досвідом О. П. Вітовська. – Зважайте й на величезну роль у нормалізації функції ендотелію, захисті нейронів, покращенні гостроти зору, зниженні АТ прийому вітамінів та антиоксидантів. У численних роботах показано, що астаксантин, вітаміни С, D, Е, В1, В12, фолієва кислота, лютеїн забезпечують виражений позитивний вплив і покращують відповідь пацієнта на терапію ДР».
ЦД і COVID‑19
? Підвищення рівня глюкози в крові після COVID‑19. Що робити?
Ймовірні кілька сценаріїв. По-перше, гіперглікемія може бути наслідком прямої дії вірусу (прогресування вуглеводних порушень характерне для багатьох вірусних інфекцій, коронавірус не є винятком). SARS-CoV‑2 тропний до β-клітин підшлункової залози, здатний спровокувати маніфестацію автоімунних процесів, які перебували в «сплячому стані», зокрема патологію щитоподібної залози, ЦД.
По-друге, транзиторну гіперглікемію може зумовити застосування глюкокортикоїдів на тлі середньотяжкого/тяжкого перебігу COVID‑19. Тому спікерки порадили спостерігати: якщо після відміни стероїдів і одужання рівень глюкози в крові нормалізується, не варто призначати додаткових обстежень і ліків; коли ж гіперглікемія зберігається тривало, необхідно застосовувати цукрознижувальну терапію й розглядати ситуацію як випадок виявленого ЦД.
Завершуючи ефір, експерти вкотре акцентували увагу на необхідності тісної та постійної співпраці: «Ендокринолог і офтальмолог повинні працювати в тандемі й обговорювати призначення фармакотерапії. Не варто перетягувати ковдру на себе. Краще виважено підійти до діагностики й лікування ЦД і ДР, спільними зусиллями вибрати оптимальну тактику».
Дізнатися більше про здоров’я очей від провідних експертів:
https://www.youtube.com/channel/UCKgI48EJHQ0U6VLIUWr6bvA
Підготувала Олександра Марченко
Медична газета «Здоров’я України 21 сторіччя» № 6 (499), 2021 р.