12 травня, 2026
Віковий андрогенодефіцит у контексті «doublepause»: сучасний погляд на сексуальне благополуччя подружньої пари
У статті феномени «couplepause» та «doublepause» розглядаються як наслідок взаємопов’язаних клінічних станів – менопаузи в жінок і вікового гіпогонадизму в чоловіків, – що істотно впливають на сексуальне здоров’я пари. Показано, що віковий андрогенодефіцит у чоловіків часто залишається недодіагностованим, попри те що саме сексуальні порушення (еректильна дисфункція, зниження лібідо, рідші спонтанні ерекції) найчастіше стають приводом для звернення до уролога чи андролога. Узагальнено актуальні рекомендації щодо діагностики та ведення вікового гіпогонадизму в чоловіків. Висвітлено роль тестостерон-замісної терапії (ТЗТ) як ключового чинника відновлення сексуальної функції чоловіка, якості життя та стосунків пари.
Ключові слова: віковий гіпогонадизм, андрогенодефіцит, couplepause, doublepause, еректильна дисфункція, замісна терапія тестостероном, трансдермальний гель тестостерону.
У зв’язку зі старінням популяції та збільшенням частки осіб середнього й старшого віку, що зумовлює тривалий пострепродуктивний період життя, особливого клінічного значення набувають менопаузальні зміни в жінок та віковий андрогенодефіцит/гіпогонадизм у чоловіків як прояви вікового згасання гонадної функції. Менопауза у жінок (зазвичай віком 45-55 років) та поступове вікове зниження рівня тестостерону в чоловіків після 50 років супроводжуються широким спектром соматичних, психоемоційних і когнітивних симптомів та суттєво знижують якість життя [1, 2]. У такій ситуації доцільно розглядати ці вікові зміни не тільки з позицій індивідуального здоров’я, а й крізь призму взаємодії партнерів у парі.
Терміни «сouplepause» (парна пауза) та «doublepause» (подвійна пауза) – це відносно нові, але вже описані в літературі поняття, які фокусують увагу на парі, а не лише окремо на жінці чи чоловіку. Термін «couplepause» запропонований E.A. Jannini та R.E. Nappi як нова парадигма для опису сексуальної дисфункції в періоди менопаузи й андропаузи з фокусуванням на парі як цілісній одиниці [3]. Менопауза в жінки та зростання частоти еректильної дисфункції (ЕД) й андрогенодефіцитних станів у чоловіка разом формують підґрунтя для «couplepause». Тому «парна пауза» має розглядатися в контексті того, що вікові гормональні зміни та сексуальні розлади в одного з партнерів неминуче позначаються на поведінці, сексуальності та самооцінці іншого, а отже, лікування лише одного партнера є недостатнім і потенційно неефективним [3].
«Doublepause» – це подальший розвиток концепції «couplepause», коли клінічно значущі вікові гормональні зміни одночасно присутні в обох партнерів [4]. Сексуальні дисфункції виникають у двох напрямках: жіночі (генітоуринарний менопаузальний синдром, гіпоактивний розлад сексуального бажання) і чоловічі (ЕД, зниження лібідо, гіпогонадизм). Іншими словами, «doublepause» – це «подвійна пауза» сексуальності: естроген-дефіцитна пауза в жінки та андроген-дефіцитна пауза в чоловіка, що прогресивно посилює сексуальні та психоемоційні проблеми пари (зменшення частоти статевих актів, збільшення конфліктів, зниження прихильності до терапії в обох партнерів) [3].
У реальній практиці ведення пацієнтів старших вікових груп часто клінічний фокус зміщений лише на менопаузу жінки, тоді як «друга половина» – віковий андрогенодефіцит чоловіка – лишається поза увагою. Сексуальні труднощі пари переважно інтерпретують крізь призму менопаузального генітоуринарного синдрому, тоді як внесок вікових гормональних змін чоловіка часто залишається недостатньо оціненим [3, 5, 6].
У цьому контексті зростає потреба у своєчасному виявленні та корекції вікового андрогенодефіциту в чоловіків, для якого характерні певна неспецифічність і поліморфізм клінічних проявів, що часто ускладнює діагностику та призводить до її відтермінування.
Віковий андрогенодефіцит у чоловіків як недооцінений компонент проблеми сексуального благополуччя пари
Віковий гіпогонадизм – це клінічно та біохімічно підтверджений стан у чоловіків старшого віку, що характеризується зниженням рівня сироваткового тестостерону порівняно з референтними значеннями в молодих здорових чоловіків. Він проявляється симптомами дефіциту тестостерону, значним погіршенням якості життя та несприятливим впливом на функціонування багатьох органів і систем [7]. Частіше гіпогонадизм виявляють у літніх чоловіків, пацієнтів з ЕД, ожирінням, супутніми захворюваннями та ускладненим спадковим анамнезом [8]. Інтенсивність клінічних проявів гіпогонадизму не завжди корелює з рівнем андрогенів у крові.
У дорослих чоловіків домінуючими симптомами гіпогонадизму є сексуальні розлади (ЕД, зниження лібідо та зменшення частоти нічних/ранкових ерекцій), загальна втома, порушення концентрації, уваги, підвищена пітливість, погане самопочуття та депресивний настрій [9]. При фізикальному обстеженні в таких пацієнтів частими знахідками є збільшення жирової та втрата м’язової маси, зменшення волосяного покриву на тілі, гінекомастія, зменшення розміру яєчок. Гіпогонадизм також пов’язаний з анемією, нижчими відповідно до віку концентраціями простат-специфічного антигену (ПСА) та зниженою мінеральною щільністю кісток [10].
У чоловіків середнього та старшого віку саме порушення сексуальної функції – зниження лібідо, ЕД, рідші спонтанні та ранкові ерекції – найчастіше стають первинним приводом для звернення до уролога або андролога. Натомість загальні симптоми, такі як хронічна втома, зниження настрою чи збільшення маси тіла, часто залишаються поза увагою та сприймаються пацієнтами як неминучі вікові зміни, а не як можливі прояви дефіциту тестостерону, пов’язаного із віком [11].
У цьому аспекті важливо розуміти, що за такими, на перший погляд, ізольованими порушеннями статевої функції, як ЕД, у значної частки пацієнтів стоїть системний стан – віковий гіпогонадизм, який потребує цілеспрямованого діагностичного пошуку, а не лише симптоматичної корекції ЕД. Саме тому сексуальні розлади доцільно розглядати як терапевтичне вікно для своєчасного виявлення та корекції вікового андрогенодефіциту. Слід зазначити, що цей стан також може бути однією з причин субоптимальної відповіді на інгібітори фосфодіестерази 5 (іФДЕ‑5) у пацієнтів з ЕД, що обґрунтовує необхідність оцінки андрогенного статусу в цій категорії хворих [12].
У чоловіків із гіпогонадизмом низький рівень тестостерону асоціюється не лише з порушеннями сексуальної функції, а й зі зниженням самооцінки, відчуття маскулінності та впевненості в собі; ці психосоціальні зміни супроводжуються емоційною відстороненістю та погіршенням якості стосунків із партнеркою [13, 14]. У рамках концепцій «couplepause» та «doublepause» наголошується, що такі психоемоційні наслідки андрогенодефіциту не є виключно індивідуальною проблемою чоловіка, а неминуче відображаються на якості інтимної та емоційної взаємодії в парі, підсилюючи загальний тягар вікових змін в обох партнерів [3, 4].
Відповідно до сучасних гайдлайнів Європейської асоціації урології (ЄАУ, 2026) та Європейського товариства менопаузи й андропаузи (2023), рівень загального тестостерону <12 нмоль/л (3,5 нг/мл) за наявності відповідних симптомів (особливо ЕД та зниження лібідо) вважається пороговим значенням для встановлення діагнозу вікового гіпогонадизму [15, 16].
Терапія тестостероном: практичні аспекти
ТЗТ все частіше визнається ключовим методом лікування вікового гіпогонадизму в чоловіків і спрямована на відновлення фізіологічних рівнів тестостерону, що відповідають середньо-нормальним значенням для молодих чоловіків (Salonia A. et al., 2023). Відповідно до актуальних клінічних рекомендацій США (Американська урологічна асоціація) та Канади (Канадська урологічна асоціація), цільові рівні загального тестостерону на фоні проведення ТЗТ мають бути в діапазоні 14,0-17,0 та 15,6-20,0 нмоль/л відповідно (Carolyn A. et al., 2019; Grober E.D. et al., 2021).
У керівництві ЄАУ щодо розладів сексуальної функції для лікування легкої ЕД у чоловіків із лабораторно підтвердженим андрогенодефіцитом ТЗТ розглядається як терапія першої лінії, тоді як при більш тяжких формах ЕД або недостатній відповіді на монотерапію іФДЕ‑5 доцільним є поєднання її із ТЗТ [16]. В останній редакції гайдлайну ЄАУ (2026) щодо вибору препаратів для ТЗТ у пацієнтів із віковим гіпогонадизмом вказано, що гелі тестостерону та ін’єкційні препарати тривалої дії є оптимальними щодо профілю безпеки (рівень доказовості 1а) [15]. Експерти також вказують, що при призначенні ТЗТ чоловікам групи високого ризику засобом вибору має бути трансдермальний гель тестостерону, а не препарати тривалої дії.
До абсолютних протипоказань ТЗТ відносять місцево-поширений або метастатичний рак передміхурової залози (ПЗ), злоякісні новоутворення грудної залози, бажання пацієнта зберегти фертильність, гематокрит ≥54% та неконтрольовану або важко контрольовану застійну серцеву недостатність (ЄАУ, 2026). До відносних обмежень зазвичай відносять підвищений вихідний гематокрит (приблизно 48-50%), виражені симптоми нижніх сечових шляхів, а також обтяжений сімейний анамнез щодо венозної тромбоемболії [16].
Вибір препарату для ТЗТ: чому трансдермальний гель тестостерону є оптимальним
Трансдермальний гель тестостерону розглядається як одна з найбільш фізіологічних форм замісної терапії, оскільки дозволяє відтворити відносно стабільний добовий профіль рівня тестостерону без виражених піків і спадів, властивих деяким ін’єкційним формам. У клінічних дослідженнях показано, що за щоденного нанесення гелю рівні загального та вільного тестостерону швидко досягають нормального діапазону й зберігаються в межах цільових значень упродовж тривалого часу [17, 18]. Важливою перевагою гелю є простота титрування дози: корекція добової кількості препарату (збільшення або зменшення дози) дозволяє індивідуально підібрати режим, досягаючи концентрацій тестостерону посередині фізіологічного діапазону. Крім того, у разі небажаних явищ або зміни клінічної ситуації терапію гелем можна швидко припинити, що забезпечує додатковий рівень безпеки для пацієнта [19].
Доведена ефективність гелю тестостерону
Дані рандомізованих і спостережних досліджень свідчать, що застосування гелю тестостерону в чоловіків з андрогенодефіцитом сприяє збільшенню сексуального потягу, частоти ерекцій і загальної сексуальної активності. У пацієнтів, які отримували гель, відзначено позитивний вплив на еректильну функцію, а також на самооцінку, енергійність і показники якості життя [19, 20].
Окремі дослідження показали також збільшення м’язової маси, зменшення жирової тканини й покращення силових показників на фоні тривалої терапії трансдермальним тестостероном, що додатково вказує на його роль як системної замісної гормонотерапії у чоловіків із гіпогонадизмом [18].
Посилення ефекту іФДЕ‑5 при додаванні гелю тестостерону
У чоловіків з андрогенодефіцтом та ЕД, які демонструють неповну або відсутню відповідь на терапію іФДЕ‑5, додавання ТЗТ може суттєво підвищити ефективність лікування. У рандомізованих дослідженнях за участю пацієнтів із низьким рівнем тестостерону, які не відповідали на силденафіл, комбіноване застосування гелю тестостерону та силденафілу приводило до значного покращення еректильної функції за шкалою Міжнародного індексу еректильної функції (IIEF) порівняно з монотерапією іФДЕ‑5 [21, 22].
Серцево-судинна безпека та моніторинг терапії
Хоча ТЗТ у чоловіків із віковим гіпогонадизмом пропонує значні переваги, такі як покращення сексуальної функції, настрою, м’язової маси тощо, занепокоєння щодо кардіоваскулярної безпеки традиційно стримувало її використання. У цьому контексті ключове значення мають дані дослідження TRAVERSE (TheRapy for Assessment of long-term Vascular events and Efficacy ResponSE in hypogonadal men), яке надало переконливі докази щодо серцево-судинної безпеки ТЗТ у відповідно відібраних пацієнтів [23]. Це найбільше рандомізоване плацебо-контрольоване дослідження, сфокусоване на оцінці впливу тестостерону на частоту великих серцево-судинних подій і стан ПЗ. У ньому взяли участь понад 5200 чоловіків віком 45-80 років із гіпогонадизмом та наявним або високим ризиком серцево-судинних захворювань, які були рандомізовані для щоденного застосування 16,2 мг/1 г гелю тестостерону (Андрожель) або плацебо.
У дослідженні TRAVERSE доза трансдермального гелю титрувалася з метою підтримання рівня тестостерону в межах 350-750 нг/дл, а первинною кінцевою точкою був комбінований показник великих серцево-судинних подій (MACE: серцево-судинна смерть, нефатальний інфаркт міокарда, нефатальний інсульт). Було показано, що ТЗТ не поступається плацебо щодо частоти MACE, тобто не асоціюється зі зростанням ризику основних серцево-судинних ускладнень у цій популяції.
Разом із тим рекомендованим є ретельний моніторинг безпеки при призначенні ТЗТ [24], який включає:
- визначення рівня тестостерону до початку лікування та під час терапії для уникнення як недостатньої, так і надмірної експозиції;
- контроль гематокриту (із припиненням або зменшенням дози при перевищенні рекомендованих меж);
- оцінку ПСА та стану ПЗ (згідно вікових рекомендацій);
- моніторинг артеріального тиску, набряків, симптомів серцево-судинної декомпенсації.
Препарат Андрожель: характеристика, режим дозування та особливості застосування
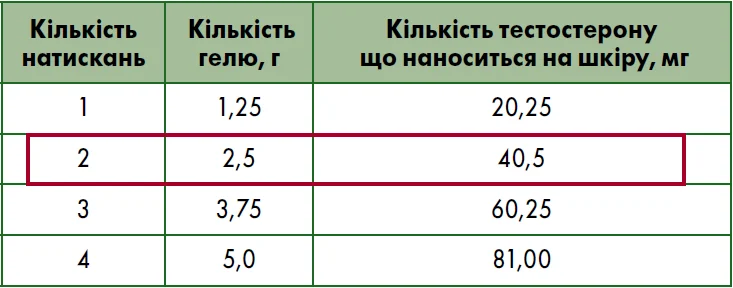
В Україні топічний тестостерон у формі гелю представлений препаратом Андрожель гель для зовнішнього застосування 16,2 мг/1 г. Така форма випуску дозволяє гнучко підбирати дозу шляхом зміни кількості натискань помпи. Рекомендована доза становить два натискання дозуючого пристрою (40,5 мг тестостерону) один раз на добу, бажано в один і той самий час, вранці [24].
Після всмоктування через шкіру тестостерон дифундує у системний кровотік із відносно постійною концентрацією протягом 24-годинного циклу.
Рівень тестостерону у крові збільшується з першої години нанесення, досягаючи рівноважного значення вже з другої доби. Після цього добові зміни концентрації тестостерону мають схожу амплітуду зі змінами, характерними для циркадного ритму секреції ендогенного тестостерону. Таким чином, черезшкірний шлях застосування дозволяє уникнути пікових підйомів концентрації препарату у крові, які виникають після ін’єкцій, і супрафізіологічних концентрацій стероїду в печінці при пероральному прийомі.
Доза Андрожелю коригується залежно від цільового рівня тестостерону в сироватці (зазвичай 350-750 нг/дл, або ≈12,1-26,0 нмоль/л) і клінічної відповіді.
Перед початком ТЗТ усім пацієнтам необхідно пройти повне обстеження для виключення раку ПЗ. У пацієнтів, які отримують тестостерон, необхідно регулярно й ретельно перевіряти стан ПЗ і грудних залоз відповідно до рекомендованих методик (пальцеве ректальне дослідження, визначення рівня ПСА у сироватці крові) щонайменше один раз на рік, а у пацієнтів літнього віку та осіб із факторами ризику (клінічними й сімейними) – два рази на рік.
Клінічний сценарій ведення пари з віковим гіпогонадизмом у чоловіка та менопаузою в жінки («doublepause»)
Середньостатистична пара, чоловік 56 років і дружина 51 року, звернулася зі скаргами на погіршення якості сексуального життя, зниження частоти статевих контактів та зростання напруження у стосунках. Жінка перебуває на менопаузальній гормональній терапії з частковим контролем вазомоторних симптомів і порушень сну, однак відзначає зниження сексуального бажання, пов’язане не лише із власними фізіологічними змінами, а й із зменшенням ініціативи з боку чоловіка. Чоловік скаржиться на прогресивне зниження сексуального потягу, проблеми з ерекцією під час статевого акту, загальну втому, зниження працездатності, дратівливість і пригнічений настрій. На фоні цих змін обидва повідомляють про напруженість у стосунках і поступове віддалення, уникнення статевих контактів та зростання конфліктів, які вони самі пов’язують із «віком».
При обстеженні чоловіка була виключена соматична патологія та прийом ліків, що могли спричиняти вищезазначені скарги. Проведено лабораторну діагностику, зокрема визначено рівень загального тестостерону – 9,0 нмоль/л. Виявлене зниження цього показника нижче референтного порога 12 нмоль/л у поєднанні з типовими клінічними проявами дало підстави встановити діагноз вікового гіпогонадизму.
Після проведення детального обстеження та виключення протипоказань, під час бесіди з пацієнтом (на якій була присутня дружина) були обговорені можливості ТЗТ: очікувані переваги та потенційні ризики, доступні форми тестостерону (ін’єкційні, трансдермальні) і раціональність вибору гелю тестостерону як зручної, керованої та добре вивченої форми замісної гормонотерапії. Було прийнято рішення розпочати ТЗТ із призначення Андрожель гелю в початковій дозі: 40,5 мг тестостерону (два натискання дозатора) один раз на добу вранці з подальшою корекцією відповідно до цільових рівнів. Пацієнту було надано інформацію стосовно техніки нанесення гелю, правил гігієни та заходів запобігання вторинній експозиції тестостерону для партнерки.
На контрольному візиті через 3 міс від початку лікування пацієнт відзначив відновлення сексуального бажання, поліпшення якості ерекції, збільшення енергійності та покращення настрою; дружина відмітила поліпшення відносин, емоційної близькості, а також збільшення частоти та задоволеності статевими контактами. Після контрольного обстеження відповідно до плану моніторингу пацієнтів, які отримують ТЗТ, лікування було продовжено.
Отже, менопауза у жінок та віковий гіпогонадизм у чоловіків мають розглядатися не як ізольовані стани, а як взаємопов’язані компоненти сексуального здоров’я пари. Своєчасна діагностика вікового андрогенодефіциту на підставі поєднання симптомів і зниженого рівня тестостерону, а також його корекція за допомогою ТЗТ, зокрема з використанням трансдермального гелю тестостерону, сприяє не лише відновленню лібідо та еректильної функції, а й покращенню енергійності, настрою та самооцінки, що є критично важливим для якості взаємин у парі. У контексті «doublepause» це доповнює ефекти менопаузальної терапії у жінки, дозволяючи покращити сексуальну активність обох партнерів і зменшити сумарний тягар вікових гормональних змін.
Література
- Yildirim F., Duman N.B., Kulakaз О. The Effect of Menopause on the Sexual Functions and Marital Adjustment of the Spouses. J Midlife Health. 2023 Jul-Sep;14(3):170-175. doi: 10.4103/jmh.jmh_90_23. Epub 2023 Dec 30. PMID: 38312762; PMCID: PMC10836430.
- https://uroweb.org/news/late-onset-hypogonadism-loh-what-does-that-mean-for-a-man
- Jannini E.A., Nappi R.E. Couplepause: A New Paradigm in Treating Sexual Dysfunction During Menopause and Andropause. Sex Med Rev. 2018 Jul;6(3):384-395. doi: 10.1016/j.sxmr.2017.11.002. Epub 2018 Jan 19. PMID: 29371146.
- Giraldi A., Nappi R.E., Palacios S., Reisman Y., Jannini E.A. From couplepause to doublepause: the impact of midlife physical, psychological, and social changes on the sexual life of aging couples. Sex Med Rev. 2024 Jun 26;12(3):346-354. doi: 10.1093/sxmrev/qeae016. PMID: 38515320.
- Serge Rozenberg, Rossella E. Nappi, Katrin Schaudig, Emmanuele A Jannini, Annamaria G E Giraldi, Couplepause: deconstructing sick menopause and andropause during midlife, The Journal of Sexual Medicine, Volume 20, Issue 11, November 2023, Pages 1270-1273.
- Jannini E.A. et al. Deconstructing sick menopause and andropause during midlife. J Sex Med. 2023.
- Wang C., Nieschlag E., Swerdloff F. et al. Investigation, treatment, and monitoring of late-onset hypogonadism in males: ISA, ISSAM, EAU, EAA, and ASA recommendations. Eur Urol. 2009;1:121-130. doi: 10.1016/j.eururo.2008.08.033.
- Mulligan T., Frick M.F., Zuraw Q.C. et al. Prevalence of hypogonadism in males aged at least 45 years: the HIM study. Int J Clin Pract. 2006;60:762-769. doi: 10.1111/j.1742-1241.2006.00992.x.
- Isidori A.M., Aversa A. et al. Adult- and late-onset male hypogonadism: the clinical practice guidelines of the Italian Society of Andrology and Sexual Medicine (SIAMS) and the Italian Society of Endocrinology (SIE). J Endocrinol Invest. 2022 Dec;45(12):2385-2403.
- Salonia A., Rastrelli G., Hackett G., Seminara S.B., Huhtaniemi I.T., Rey R.A. et al. Paediatric and adult-onset male hypogonadism. Nat Rev Dis Primers. 2019;5(1):38. doi: 10.1038/s41572-019-0087-y.
- Corona G., Rastrelli G., Vignozzi L., Mannucci E., Maggi M. How to recognize late-onset hypogonadism in men with sexual dysfunction. Asian J Androl. 2012 Mar;14(2):251-9. doi: 10.1038/aja.2011.138. Epub 2012 Jan 30. PMID: 22286862; PMCID: PMC3735094.
- Buvat J., Montorsi F., Maggi M., Porst H., Kaipia A., Colson M.H., Cuzin B., Moncada I., Martin-Morales A., Yassin A., Meuleman E., Eardley I., Dean J.D., Shabsigh R. Hypogonadal men nonresponders to the PDE5 inhibitor tadalafil benefit from normalization of testosterone levels with a 1% hydroalcoholic testosterone gel in the treatment of erectile dysfunction (TADTEST study). J Sex Med. 2011 Jan;8(1):284-93.
- Aceves-Martins M., Quinton R., Brazzelli M., Cruickshank M., Manson P., Hudson J., Oliver N., Hernandez R., Aucott L., Wu F., Dhillo W.S., Bhattacharya S., Gillies K., Jayasena C.N.; NIHR Testosterone Efficacy & Safety (TestES) Consortium. Identifying the outcomes important to men with hypogonadism: A qualitative evidence synthesis. Andrology. 2022 May;10(4):625-641. doi: 10.1111/andr.13156. Epub 2022 Feb 8. PMID: 35064779; PMCID: PMC9487983.
- Corona G., Mannucci E., Lotti F., Boddi V., Jannini E.A., Fisher A.D., Monami M., Sforza A., Forti G., Maggi M. Impairment of couple relationship in male patients with sexual dysfunction is associated with overt hypogonadism.
J Sex Med. 2009 Sep;6(9):2591-600. - https://uroweb.org/guidelines/sexual-and-reproductive-health/chapter/male-hypogonadism.
- Salonia A., Boeri L., Capogrosso P., Corona G., Dinkelman-Smith M., Falcone M., Gьl M., Kadioğlu A., Martinez-Salamanca J.I., Minhas S., Serefoğlu E.C., Verze P., Cocci A., Fuglesang Jensen C., Kalkanli A., Morgado L.A., Milenkovic U. & Russo G. (2025). EAU Guidelines on Sexual and Reproductive Health. In EAU.
- Swerdloff R.S., Wang C., Cunningham G., Dobs A., Iranmanesh A., Matsumoto A.M., Snyder P.J., Weber T., Longstreth J., Berman N. Long-term pharmacokinetics of transdermal testosterone gel in hypogonadal men. J Clin Endocrinol Metab. 2000 Dec;85(12):4500-10. doi: 10.1210/jcem.85.12.7045. PMID: 11134099.
- Lakshman K.M., Basaria S. Safety and efficacy of testosterone gel in the treatment of male hypogonadism. Clin Interv Aging. 2009;4:397-412. doi: 10.2147/cia.s4466. Epub 2009 Nov 18. PMID: 19966909; PMCID: PMC2785864.
- Shoskes J.J., Wilson M.K., Spinner M.L. Pharmacology of testosterone replacement therapy preparations. Transl Androl Urol. 2016 Dec;5(6):834-843.
doi: 10.21037/tau.2016.07.10. PMID: 28078214; PMCID: PMC5182226. - Rizk P.J., Kohn T.P., Pastuszak A.W., Khera M. Testosterone therapy improves erectile function and libido in hypogonadal men. Curr Opin Urol. 2017 Nov;27(6):511-515. doi: 10.1097/MOU.0000000000000442. PMID: 28816715; PMCID: PMC5649360.
- Shabsigh R., Kaufman J.M., Steidle C., Padma-Nathan H. Randomized study of testosterone gel as adjunctive therapy to sildenafil in hypogonadal men with erectile dysfunction who do not respond to sildenafil alone. J Urol. 2008;179 (5 Suppl): S97-S102. doi: 10.1016/j.juro.2008.03.145.
- Greenstein A., Mabjeesh N.J., Sofer M. et al. Does sildenafil combined with testosterone gel improve erectile dysfunction in hypogonadal men in whom testosterone supplement therapy alone failed? J Urol. 2005;173:530-2.
doi: 10.1097/01.ju.0000149870.36577.05. - Hackett G.I. Long Term Cardiovascular Safety of Testosterone Therapy: A Review of the TRAVERSE Study. World J Mens Health. 2025 Apr;43(2):
282-290. - https://compendium.com.ua/dec/270202.
Підготувала Марія Ареф’єва
Тематичний номер «Урологія. Нефрологія. Андрологія» № 1 (40), 2026 р.