11 лютого, 2023
Застосування фіксованої комбінації кеторолаку трометаміну та компонентів зі спазмолітичною дією (Неоспастил®) для лікування ниркової кольки після проведення дистанційної літотрипсії
у порівнянні з препаратом метамізолу в комбінації з компонентами зі спазмолітичним ефектом
Автори: С.О. Возіанов, академік НАМН України, д. мед. н., професор, завідувач кафедри урології Національного університету охорони здоров’я України ім. П.Л. Шупика, завідувач відділу рентген-ендоурології та літотрипсії, директор ДУ «Інститут урології ім. акад. О.Ф. Возіанова НАМН України», президент Асоціації урологів України, А.О. Юрах, к. мед. н., старший науковий співробітник відділу ендоскопічної урології та літотрипсії, О.О. Шевчук, к. мед. н., завідувач відділення ендоскопічної урології та літотрипсії, ДУ «Інститут урології ім. акад. О.Ф. Возіанова НАМН України», м. Київ
Мета дослідження. Оцінити ефективність, безпечність застосування й переносимість нового лікарського засобу Неоспастил®, розчину для ін’єкцій (фіксована комбінація кеторолаку трометаміну та компонентів зі спазмолітичним типом дії), для усунення больового синдрому у випадку ниркової кольки після проведення дистанційної літотрипсії у порівнянні із застосуванням комбінованого лікарського засобу метамізолу натрію.
Матеріали та методи. До участі в дослідженні було залучено 60 пацієнтів, по 30 осіб у досліджуваній і контрольній групах. Для усунення больового синдрому в досліджуваній групі пацієнтам внутрішньом’язово вводили 2 мл розчину для ін’єкцій Неоспастил® (фіксована комбінація кеторолаку трометаміну 15 мг/мл, пітофенону гідрохлориду 5 мг/мл і фенпіверинію броміду 0,05 мг/мл), а в контрольній групі – внутрішньом’язово 2 мл розчину для ін’єкцій Спазмалгон® (фіксована комбінація метамізолу натрію моногідрату 500 мг/мл, пітофенону гідрохлориду 2 мг/мл і фенпіверинію броміду 0,02 мг/мл). Рівень болю оцінювали за допомогою анкетування та цифрової рейтингової шкали (ЦРШ) на 0‑й, 20‑й, 40‑й хвилинах і через 1 та 8 год після введення лікарського засобу.
Результати. Згідно з отриманими результатами, Неоспастил® був ефективним (досягнення цільового рівня інтенсивності болю за 10‑бальною ЦРШ 0-3 бали через 40 хв після застосування препарату) у 83,5% випадків, а комбінований препарат метамізолу натрію (Спазмалгон®) – у 60,0% (p=0,045). Необхідність додаткового знеболення впродовж 8 год після використання лікарського засобу в досліджуваній групі виникла у 26% хворих, а в контрольній – у 40% (p=0,27).
Застосування комбінованого препарату кеторолаку (Неоспастил®) у досліджуваній групі супроводжувалося кращою динамікою зниження інтенсивності больових відчуттів: порівняно з контрольною групою рівень болю був достовірно нижчим через 20 хв (p=0,002), 40 хв (p=0,025) та через 8 год (p=0,0004) після знеболення. Через 1 год після введення препаратів значущої відмінності між показниками рівня болю (p=0,43) і динаміки його інтенсивності (p=0,14) у пацієнтів двох груп не спостерігалося. В обох групах було виявлено по 4 випадки, які виділялися із загальної вибірки. У цих пацієнтів больовий синдром виявляв високу резистентність до обох досліджуваних препаратів, а фрагменти ниркових каменів відзначалися у вічку сечоводу.
Висновки. Застосування фіксованої комбінації кеторолаку трометаміну та компонентів зі спазмолітичним типом дії (препарат Неоспастил®) у дозі 2 мл продемонструвало високу ефективність у досягненні знеболення при нирковій кольці після проведення дистанційної літотрипсії й мало переваги над комбінованим препаратом, до складу якого входив метамізол натрію.
Ключові слова: ниркова колька, дистанційна літотрипсія, знеболення, кеторолак, метамізол, Неоспастил®.
Дистанційна літотрипсія – ефективний малоінвазивний і безпечний метод лікування сечокам’яної хвороби. Однак фрагменти каменя, виходячи природним шляхом, можуть зумовлювати ниркові кольки, і, як наслідок, такі пацієнти потребують проведення знеболення. Патогенез болю при цьому такий самий, як і при нирковій кольці, і потребує відповідного лікування. Достатньо часто з метою знеболення в таких випадках застосовують лікарські засоби диклофенаку натрію, що демонструють високу ефективність у купіруванні больового синдрому. Разом із тим його призначення може призводити до значного зменшення фільтрації сечі ниркою у стані обструкції, що, у свою чергу, веде до сповільнення просування каменів по сечоводу.
Призначення монотерапії спазмолітиками не розглядається як достатньо результативне, оскільки не впливає на простагландиновий механізм формування болю. Водночас із патогенетичної точки зору застосування при нирковій кольці комбінацій нестероїдних протизапальних препаратів (НПЗП) зі спазмолітиками може бути значно ефективнішим за монотерапію як знеболювальними, так і спазмолітичними засобами.
Однією з найбільш часто використовуваних фіксованих комбінацій в Україні є комбінація метамізолу натрію (анальгіну) із засобами спазмолітичної дії (пітофенону гідрохлорид і фенпіверинію бромід). Однак метамізол натрію (анальгін), який у такому випадку є основним знеболювальним компонентом, заборонений або обмежений у використанні у близько 70 країнах світу (більшість економічно розвинених європейських держав і США) з огляду на високий ризик виникнення такого ускладнення, як агранулоцитоз [1]. В Україні метамізол натрію та препарати, до складу яких він входить, дозволені до застосування, але не всі вони відпускаються за рецептом, що може призводити до їх частого використання й розвитку ускладнень. До останнього часу вищезгаданим комбінованим препаратам метамізолу, зокрема в купіруванні ниркової кольки, на ринку України не було альтернативи. Тому поява нового комбінованого препарату Неоспастил® з основним знеболювальним компонентом кеторолаку трометаміном, застосування якого не асоціюється з високим ризиком розвитку агранулоцитозу, була з ентузіазмом сприйнята урологічною спільнотою.
Мета дослідження полягала в оцінці ефективності, безпечності застосування та переносимості препарату Неоспастил® (комбінація кеторолаку трометаміну з пітофенону гідрохлоридом і фенпіверинію бромідом), розчин для ін’єкцій, по 2 мл в ампулі, виробництва ПрАТ «Фармацевтична фірма “Дарниця”» (Україна) для усунення больового синдрому у випадку ниркової кольки після проведення дистанційної літотрипсії у порівнянні із застосуванням комбінації метамізолу натрію з пітофенону гідрохлоридом і фенпіверинію бромідом (лікарський засіб Спазмалгон®, розчин для ін’єкцій, по 2 мл в ампулі, виробництва АТ «Софарма», Болгарія).
Матеріали та методи
У дослідження включали пацієнтів віком від 18 до 65 років обох статей з індексом маси тіла 18-35 кг/м2, які перебували на стаціонарному лікуванні в ДУ «Інститут урології НАМН України» у зв’язку з проведенням їм дистанційної літотрипсії із приводу сечокам’яної хвороби, що мали напад ниркової кольки з інтенсивністю болю >4 балів за 10‑бальною цифровою рейтинговою шкалою (ЦРШ).
Дизайн дослідження включав дві групи: досліджувану, пацієнтам якої у випадку ниркової кольки одноразово внутрішньом’язово вводили 2 мл Неоспастил®, розчин для ін’єкцій (фіксована комбінація кеторолаку трометаміну 15 мг/ мл, пітофенону гідрохлориду 5 мг/ мл і фенпіверинію броміду 0,05 мг/мл), та контрольну, у якій для знеболення застосовували 2 мл Спазмалгон®, розчин для ін’єкцій (фіксована комбінація метамізолу натрію моногідрату 500 мг/ мл, пітофенону гідрохлориду 2 мг/мл і фенпіверинію броміду 0,02 мг/мл). Подальше знеболення обома препаратами проводилося «на вимогу», але з дотриманням інтервалу не менше 8 год і не більше двох днів поспіль. За більш ранньої необхідності повторного знеболення внутрішньом’язово вводили диклофенак натрію. Розподіл за групами здійснювався шляхом рандомізації. Наявність і локалізація конкрементів підтверджувалася даними ультразвукового дослідження (УЗД) зі щоденним моніторингом.
У дослідження не включали осіб з обтяженим алергологічним анамнезом, із дегенеративними захворюваннями центральної нервової системи, відомими психічними розладами, діагностованим цукровим діабетом або вираженою гіперглікемією, онкологічною патологією ІІ-ІІІ клінічної групи, з ерозивно-виразковими захворюваннями шлунково-кишкового тракту, некоригованою артеріальною гіпертензією й іншими протипоказаннями до призначення досліджуваних препаратів.
Інтенсивність болю визначали за ЦРШ на час призначення препарату, через 20, 40 хв, 1 та 8 год після його введення. Проводили оцінку тривалості нападу болю та необхідності додаткового знеболення. Також здійснювали аналіз динаміки інтенсивності болю у відповідні часові інтервали. Загальне враження пацієнта щодо якості знеболення за першу добу й за весь курс лікування оцінювали шляхом анкетування. Розташування уламків каменя у сечоводі протягом періоду лікування хворого встановлювали за допомогою щоденного УЗД-моніторингу.
Знеболювальну дію препарату вважали достатньою при зниженні інтенсивності болю до 0-3 балів на період 40 хв – 8 год після його введення й за відсутності потреби в додатковому знеболенні протягом цього часу.
Отримані дані обробляли методами непараметричної статистики за допомогою ПЗ Statistica 10, Stat Soft, Tusla, OK, USA та Medcalc 20, Med Calc Software LTD. Використовували U-критерій Манна – Уітні (Mann – Whitney U-test) для порядкових величин і χ2 Пірсона – для категоріальних.
Результати дослідження та їх обговорення
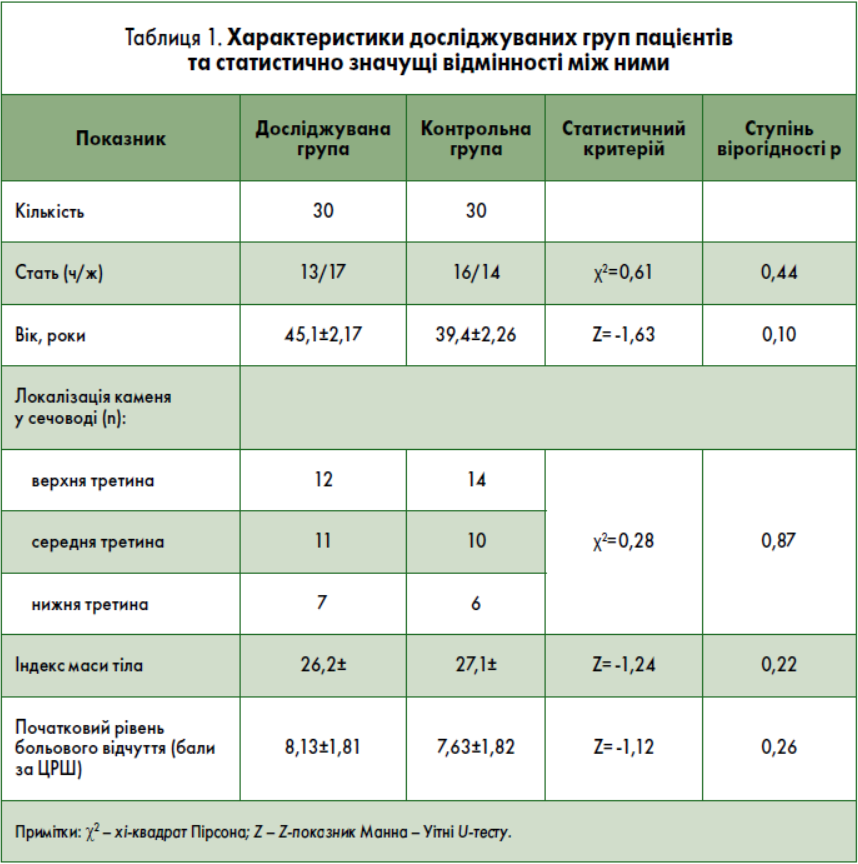
Характеристики обох груп наведені у табл. 1. Між групами не спостерігалося статистично значущих відмінностей за статтю, віком, локалізацією каменя, масово-ростовим індексом, початковим рівнем больового відчуття.
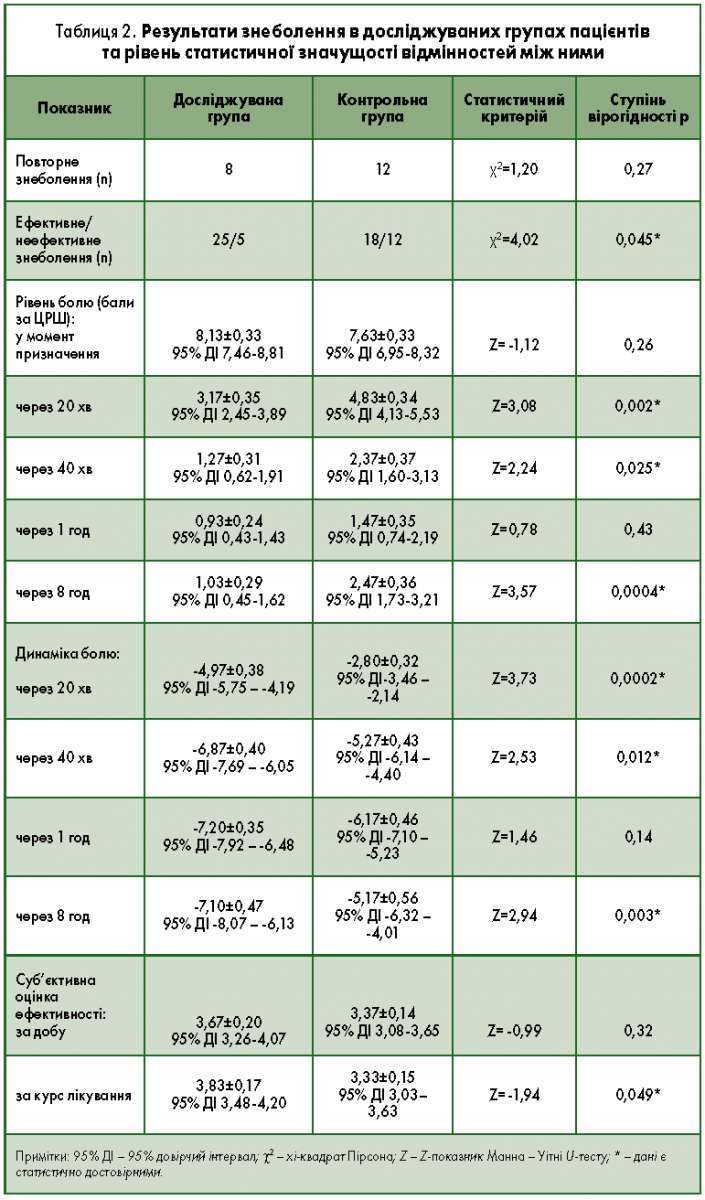
Досліджувані препарати знижували вираженість больового синдрому, однак рівень впливу був різним за окремими оцінюваними параметрами для обох груп (табл. 2). Зокрема, у досліджуваній групі ефективність препарату, визначена зниженням рівня болю до 0-3 балів за ЦРШ, спостерігалася у 25 (83,3%) пацієнтів, натомість як у контрольній групі препарат, згідно із встановленим критерієм, був ефективним у 18 (60%) випадків. Така відмінність між групами була статистично значущою (χ2=4,02; p=0,045), що свідчило про вищу ефективність препарату Неоспастил®. Необхідність у додатковому знеболенні протягом перших 8 год виникла в досліджуваній групі у 8 (26,7%) пацієнтів, а в контрольній – у 12 (40,0%) осіб, що значущо не відрізнялося (χ2=1,20; p=0,27). За результатами аналізу суб’єктивної оцінки якості знеболення: у досліджуваній групі за першу добу лікування пацієнти оцінили досліджуваний препарат на 3,67±0,20 (95% довірчий інтервал [ДІ] 3,26-4,07), а за курс лікування – на 3,83±0,17 (95% ДІ 3,48-4,20) бала за 5‑бальною шкалою. Дещо гірші результати були отримані в контрольній групі: 3,37±0,14 (95% ДІ 3,08-3,65) та 3,33±0,15 (95% ДІ 3,03-3,63) відповідно. При цьому відмінність між групами хворих при оцінці якості знеболення за першу добу була недостовірною (z= -0,99; p=0,32), а при оцінці за курс лікування Неоспастил® отримав статистично підтверджений кращий результат (z= -1,94; p=0,049), ніж лікарський засіб порівняння.
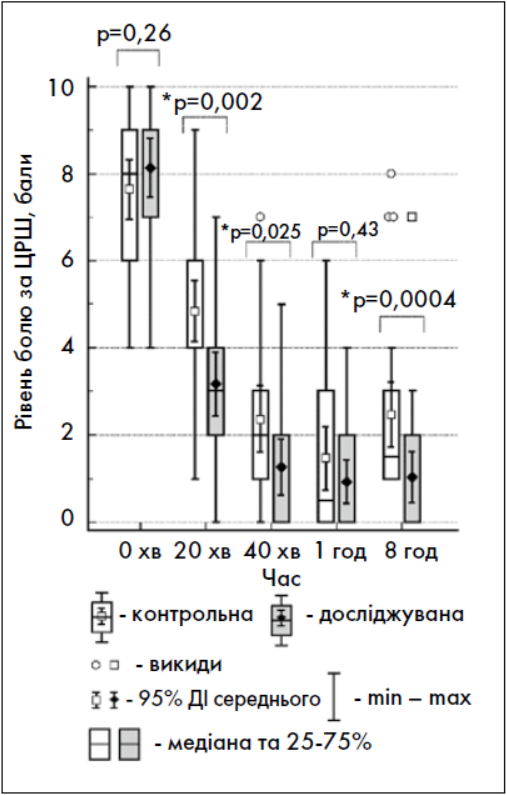
Оцінюючи динаміку інтенсивності болю (рис. 1), дослідники встановили, що у групі пацієнтів, яким застосовували Неоспастил®, спостерігалася достовірно менша інтенсивність болю на 20‑й (Z=3,08; p=0,002), 40‑й хвилині (Z=2,24; p=0,025) та через 8 год (Z=3,57; p=0,0004) після призначення препарату. Однак через 1 год після введення препаратів значущих відмінностей між результатами у двох групах пацієнтів виявлено не було (Z=0,78; p=0,43). Подібні дані (рис. 2) спостерігалися і при оцінюванні динаміки інтенсивності болю відносно початкового рівня (табл. 2). Із цього можна зробити висновок, що знеболювальний ефект після введення комбінованого препарату з метамізолом натрію наставав дещо пізніше і спадав швидше, ніж при знеболенні із застосовуванням нової комбінації кеторолаку зі спазмолітиками.
Рис. 1. Порівняння інтенсивності болю в досліджуваній і контрольній групах у різні часові інтервали після призначення досліджуваних препаратів
Рис. 2. Динаміка інтенсивності болю відносно початкового рівня в досліджуваній і контрольній групах у різні часові інтервали після призначення досліджуваних препаратів
Також було виявлено чотири випадки викидів (із загальною для досліджуваних сукупностей тенденцією) як в одній, так і в іншій групі пацієнтів: вони характеризувалися високою резистентністю больового синдрому до лікування досліджуваними препаратами. Більш глибокий аналіз даних випадків виявив, що у всіх хворих камені локалізувалися в інтрамуральному та передміхуровому відділах сечоводу і больовий синдром носив характер вираженого болісного імперативного позиву до сечовипускання з відсутнім або незначним болем у проекції нирки. Статистичний аналіз цих випадків не проводився у зв’язку з малою їх кількістю.
За час проведення дослідження в учасників не було зафіксовано жодного випадку значущих побічних ефектів при введенні досліджуваного та контрольного препаратів.
Неоспастил® і Спазмалгон® за своїм складом відрізнялися не лише знеболювальними компонентами (кеторолаку трометамін і метамізол натрію відповідно), а й також дозами складових із спазмолітичним типом дії (пітофенону гідрохлорид 5 мг/мл і фенпіверинію бромід 0,05 мг/мл проти пітофенону гідрохлориду 2 мг/мл і фенпіверинію броміду 0,02 мг/ мл відповідно). Тому розбіжності у їхній ефективності та дії можна пояснити як відмінністю знеболювальної дії кеторолаку трометаміну й метамізолу натрію, так і можливістю більш вираженого впливу комбінації з кеторолаком на спазматичний компонент болю.
Кеторолак, що входить до складу Неоспастилу, є одним із найбільш ефективних НПЗП. При цьому, за даними окремих досліджень, знеболення при його застосуванні може наставати вже на 15‑й хвилині після введення і триває не менше 6-8 год, а за силою аналгезії його можна порівняти із введенням 10 мг морфіну [2]. Висока ефективність кеторолаку при нирковій кольці була доведена V. Wood et al. [3]. У цьому дослідженні знеболення після введення 30 мг кеторолаку було зіставним із застосуванням 50 мг опіоїдного анальгетика меперидину. Останні дослідження свідчать, що застосування 10 мг кеторолаку достатньо ефективно знижує вираженість больового синдрому при нирковій кольці в 97% випадків [4]. Враховуючи, що максимальна добова доза препарату становить 90 мг (для літніх людей – 60 мг) за тривалості дії 6-8 год, можливим є використання кеторолаку в адекватній знеболювальній дозі до 3 разів на добу.
Анальгін (метамізол) також є ефективним знеболювальним засобом, який має столітній досвід клінічного використання. Незважаючи на заборону та обмеження використання у 70 країнах світу, він до сих пір призначається для екстреної медичної допомоги при нирковій кольці у Німеччині, Іспанії, Італії та деяких інших економічно розвинених країнах [1]. Численні дослідження [5, 6] показали його ефективність, проте для отримання ефекту, порівнянного з опіатами, однократна доза метамізолу має становити не нижче 2-2,5 г [7]. Останнім часом його дозування було переглянуте: тепер при внутрішньом’язовому введенні максимальну добову дозу рекомендовано обмежити 1 г, а разову – 500 мг [8]. Це унеможливлює застосування високих доз препарату, особливо при неоднократному знеболенні протягом доби. Щодо механізму дії цього препарату, то, як не дивно, до останнього часу він був вивчений недостатньо й відносився до НПЗП. Проте у зв’язку із тим, що на початку століття було виявлено циклооксигеназу 3‑го типу (ЦОГ‑3, дериват ЦОГ‑1), а саме у тканинах спинного й головного мозку за гематоенцефалічним бар’єром, метамізол був визнаний одним із препаратів, здатним її інгібувати. Частково він інгібує і периферичну ЦОГ‑1, але практично не впливає на ЦОГ‑2, а отже, не проявляє протизапальних властивостей [9].
Враховуючи дані вищевказаних літературних джерел, особливо щодо високої знеболювальної ефективності кеторолаку при нирковій кольці [2-4], отримані у цьому досліджені результати є очікуваними.
Синергізм НПЗП зі спазмолітиком пітофеноном був показаний у дослідженні S.K. Kulkarni et al. [10], що доводить доцільність створення комбінованих препаратів.
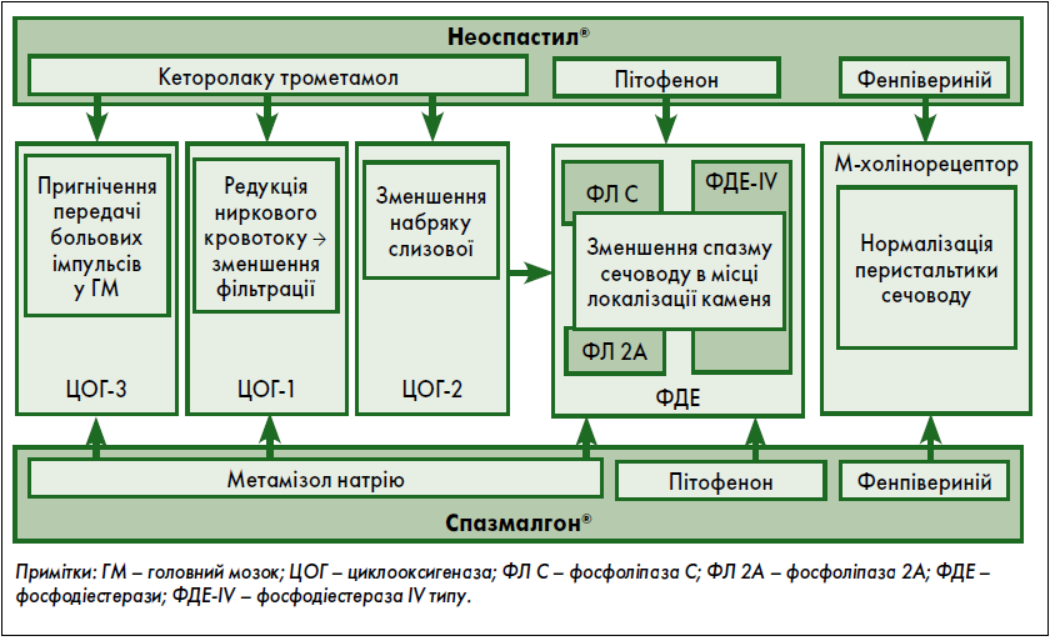
Патогенетичне лікування після проведення дистанційної літотрипсії має включати у себе поєднання знеболення та експульсивної (літокінетичної) терапії. У таку схему вписуються обидва препарати, проте Неоспастил® має певні переваги (рис. 3). Кеторолак є класичним НПЗП, здатним інгібувати як ЦОГ‑1, так і ЦОГ‑2 [11], на відміну від метамізолу, який є неопіатним анальгетиком без вираженого протизапального ефекту (слабко впливає на ЦОГ‑2) [12]. Таким чином, перший буде зменшувати прояви запалення, у тому числі набряк слизової сечоводу в зоні локалізації каменя (де закономірно виникає запальний процес), що полегшить просування останнього по сечоводу. Кеторолак є одним із найефективніших інгібіторів ЦОГ‑1, натомість як інгібуюча дія метамізолу на ЦОГ‑1 значно менша [11, 13]. Саме блокування ЦОГ‑1 приводить до зменшення фільтрації сечі у блокованій нирці й перериває патогенетичне коло розвитку ниркової кольки [14, 15]. Тому лікування з використанням препаратів кеторолаку є більш наближеним до патогенетичного. Здатність кеторолаку інгібувати ЦОГ‑2 веде до зниження тонусу сечоводу, що відбувається опосередковано через зменшення синтезу простагландинів, фосфоліпази A2 та активності аденілатциклазної системи [16]. Натомість метамізол виявляє прямі міотропні спазмолітичні властивості за рахунок пригнічення активності фосфоліпази С [17]. Центральні знеболювальні ефекти обох препаратів ґрунтуються на ймовірному інгібуванні ЦОГ‑3 й активації канабіноїдної системи [12].
Рис. 3. Схема дії досліджуваних препаратів при патогенетичному лікуванні ниркової кольки
Таким чином, застосування комбінації кеторолаку з компонентами спазмолітичної дії (Неоспастил®) добре вписується у патогенетичну схему лікування ниркової кольки й має переваги над традиційною терапією комбінованими препаратами метамізолу.
Перспективи подальших досліджень
Вплив Неоспастилу на відходження каменів із сечоводу та ефективність знеболення препаратом при каменях у його інтрамуральному відділі потребує подальшого вивчення на значно більших вибірках пацієнтів.
Висновки
- Комбінація кеторолаку трометаміну з пітофенону гідрохлоридом і фенпіверинію бромідом (Неоспастил®) продемонструвала виражений знеболювальний ефект у пацієнтів із нирковою колькою, що розвивалася після дистанційної літотрипсії.
- Комбінація кеторолаку трометаміну з пітофенону гідрохлоридом і фенпіверинію бромідом (Неоспастил®) у дозі 2 мл продемонструвала вищу ефективність у досягнені достатнього рівня знеболення (0-3 бали за ЦРШ), ніж комбінація метамізолу натрію з пітофенону гідрохлоридом і фенпіверинію бромідом (Спазмалгон®) у дозі 2 мл.
- У суб’єктивній оцінці знеболювального ефекту за першу добу лікування не спостерігалося значущих відмінностей між препаратами, проте за весь курс терапії хворі оцінили знеболювальний ефект комбінації з кеторолаку трометаміном вище, ніж комбінованого лікарського засобу з метамізолом натрію.
- За рахунок наявності протизапального ефекту кеторолаку трометаміну Неоспастил® може мати переваги над комбінованими препаратами метамізолу завдяки впливу на простагландиновий механізм формування болю при нирковій кольці.
- Відсутність метамізолу в новому комбінованому препараті знімає ряд обмежень на його використання й зменшує потенційні ризики розвитку ускладнень.
Література
- Lutz M. Metamizole (Dipyrone) and the Liver: A Review of the Literature. J Clin Pharmacol. 2019;59(11):1433-42.
- Anthony D., Jasinski D.M. Postoperative pain management: morphine versus ketorolac. J Perianesth Nurs. 2002;17(1):30-42.
- Wood V.M., Christenson J.M., Innes G.D., Lesperance M., McKnight D. The NARC (nonsteroidal anti-inflammatory in renal colic) trial. Single-dose intravenous ketorolac versus titrated intravenous meperidine in acute renal colic: a randomized clinical trial. Cjem. 2000;2(2):83-9.
- Eidinejad L., Bahreini M., Ahmadi A., Yazdchi M., Thiruganasambandamoorthy V., Mirfazaelian H. Comparison of intravenous ketorolac at three doses for treating renal colic in the emergency department: A noninferiority randomized controlled trial. Acad Emerg Med. 2021;28(7):768-75.
- Stankov G., Schmieder G., Zerle G., Schinzel S., Brune K. Double-blind study with dipyrone versus tramadol and butylscopolamine in acute renal colic pain. World J Urol. 1994;12(3):155-61.
- Edwards J.E., Meseguer F., Faura C., Moore R.A., McQuay H. J. Single dose dipyrone for acute renal colic pain. Cochrane Database Syst Rev. 2002;2002(4): CD003867-CD.
- Muriel C., Ortiz P. Efficacy of two different intramuscular doses of dipyrone in acute renal colic. Cooperative Study Group. Methods Find Exp Clin Pharmacol. 1993;15(7):465-9.
- Інструкція для медичного застосування лікарського засобу Анальгін-Дарниця. Державний реєстр лікарських засобів України: Департамент фармацевтичної діяльності. Державний експертний центр Міністерства охорони здоров’я України; 2021 [17.10.2021]. Available from: http://www.drlz.com.ua/ibp/lz_www.nsf/id/B9190E521F03FF6AC225866A00381F33/$file/UA32220202_5A53.mht.
- Chandrasekharan N.V., Dai H., Roos K.L., Evanson N.K., Tomsik J., Elton T.S. et al. COX‑3, a cyclooxygenase‑1 variant inhibited by acetaminophen and other analgesic/antipyretic drugs: cloning, structure, and expression. Proc Natl Acad Sci USA. 2002;99(21):13926-31.
- Kulkarni S.K., Patil C. S., Jain N. K., Singh A. Modulatory effect of diclofenac on antispasmodic effect of pitofenone in cholinergic spasm. Indian J Exp Biol. 2004;42(6):567-9.
- Warner T.D., Giuliano F., Vojnovic I., Bukasa A., Mitchell J. A., Vane J. R. Nonsteroid drug selectivities for cyclo-oxygenase‑1 rather than cyclo-oxygenase‑2 are associated with human gastrointestinal toxicity: a full in vitro analysis. Proc Natl Acad Sci USA. 1999;96(13):7563-8.
- Jasiecka A., Maślanka T., Jaroszewski J.J. Pharmacological characteristics of metamizole. Polish Journal of Veterinary Sciences. 2014;17(1):207-14.
- Warner T.D., Mitchell J.A. Cyclooxygenases: new forms, new inhibitors, and lessons from the clinic. Faseb j. 2004;18(7):790-804.
- Perlmutter A., Miller L., Trimble L.A., Marion D.N., Vaughan E.D. Jr., Felsen D. Toradol, an NSAID used for renal colic, decreases renal perfusion and ureteral pressure in a canine model of unilateral ureteral obstruction. J Urol. 1993;149(4):926-30.
- Zwergel U.E., Zwergel T.B., Neisius D.A., Ziegler M. Effects of prostaglandin synthetase inhibitors on the upper urinary tract. Experimental studies on isolated preparations and urodynamic measurements in men. Urol Res. 1990;18(6):429-33.
- Davidson M.E., Lang R. J. Effects of selective inhibitors of cyclo-oxygenase‑1 (COX‑1) and cyclo-oxygenase‑2 (COX‑2) on the spontaneous myogenic contractions in the upper urinary tract of the guinea-pig and rat. Br J Pharmacol. 2000;129(4):661-70.
- Gulmez S.E., Gurdal H., Tulunay F. C. Airway smooth muscle relaxations induced by dipyrone. Pharmacology. 2006;78(4):202-8.