Шляхи покращення ефективності ерадикації Helicobacter pylori : місце пантопразолу
Відкриття мікроорганізму Helicobacter pylori (Нр) і визначення його ролі в етіології багатьох захворювань не тільки органів травлення, а й інших органів та систем організму, дозволило здійснити значний науковий прорив у медицині та дало підстави говорити про можливість виліковування та профілактики низки захворювань шлунка та дванадцятипалої кишки [9, 31].
Сучасні дослідження Нр-інфекції відбуваються у двох основних напрямах:
- вивчення ролі мікроорганізму в етіології та патогенезі різноманітних захворювань внутрішніх органів [23, 28, 39];
- пошук оптимальних схем антимікробної фармакотерапії, що максимально ефективно приводили б до ерадикації Нр [31].
Чому пошуку оптимальних схем ерадикації Нр приділяється настільки значна увага медичної спільноти?
Не є секретом, що останніми роками відзначено наростання кількості невдач під час проведення ерадикаційної терапії [5, 6, 15]. Більш ніж 25-річний досвід лікування гелікобактерної інфекції показав, що ерадикація стає все більш складним завданням, оскільки мікроорганізм швидко набуває стійкості до антибактеріальних препаратів. Незадовільні результати класичних ерадикаційних схем змушують проводити повторні курси лікування, у зв’язку з чим існує потреба не тільки у пошуку нових ефективних схем ерадикації Нр першої лінії, що оптимально працюють в умовах високої антибіотикорезистентності, а й в розробленні нових підходів до проведення антигелікобактерної терапії, що впливали б на різні ланки патогенезу гелікобактерної інфекції.
Однак для розв’язання цього завдання слід звернути увагу на низку проблем, пов’язаних з успішним проведенням ерадикації Нр.
- По-перше, кількість антибактеріальних фармакопрепаратів, до яких чутливий мікроорганізм (макроліди – кларитроміцин, напівсинтетичні пеніциліни – амоксицилін, тетрацикліни – тетрациклін, похідні імідазолу – метронідазол та ін., фторхінолони – левофлоксацин, нітрофурани – фуразолідон та препарати вісмуту), є обмеженою.
- По-друге, Нр властивий швидкий розвиток вторинної резистентності до антибактеріальних засобів, зокрема до метронідазолу, кларитроміцину та левофлоксацину [2, 16, 24, 31].
- По-третє, екологічна ніша Нр (поверхня слизової оболонки шлунка) не сприяє як оптимальному здійсненню ефектів антибактеріальних препаратів, так і реалізації імунної відповіді. Це пов’язано з тим, що хлористоводнева кислота частково призводить до інактивації імуноглобулінів [41] та руйнує навіть кислотостійкі антибактеріальні препарати. Зокрема, у кислому середовищі шлунка руйнується до 20% кларитроміцину, амоксициліну та метронідазолу [22, 38]. Крім того, в умовах кислого середовища шлунка ускладненим є потрапляння антибактеріальних препаратів у слиз та слизову оболонку [26].
На цей час виділяють кілька основних напрямів у розв’язанні наведених вище проблем.
- Визначення чутливості Нр до найбільш часто вживаних антибактеріальних препаратів.
- Розроблення й апробація нових антибактеріальних препаратів, до яких буде чутливий Нр.
- Подолання резистентності Нр шляхом збільшення кількості антибактеріальних препаратів у схемі ерадикації Нр або подовження тривалості застосування антигелікобактерних схем.
- Досягнення потужного кислотосупресивного ефекту при застосуванні інгібіторів протонної помпи (ІПП).
Визначення чутливості Нр in vitro до найбільш часто вживаних препаратів є обмеженим для широкого застосування у повсякденній медичній практиці більшості країн. В Україні такі дослідження виконувалися у великих клінічних центрах Харкова, Львова та Києва [1, 2, 9].
Однак на цей час вказаний метод, як правило, використовується у вигляді скринінгових програм із метою визначення змін чутливості Нр до антибактеріальних препаратів і подальшого розроблення нових підходів до антигелікобактерної фармакотерапії [9]. Це зумовлюється як високою вартістю самого дослідження, що потребує спеціальних поживних середовищ для вирощування культури Нр, так і потребою в спеціальному лабораторному обладнанні із створенням мікроаерофільних умов для культивації мікроорганізму [1, 2, 8, 10].
Синтез будь-яких нових антибактеріальних препаратів, зокрема антигелікобактерних, є тривалим і вартісним. Виходячи з цього, слід відзначити, що найближчим часом оптимізація схем ерадикації Нр базуватиметься на розробленні нових комбінацій уже відомих антибактеріальних препаратів з антигелікобактерною активністю [31].
Останнім часом у схемах антигелікобактерної фармакотерапії почали використовувати рифабутин та левофлоксацин [31].
Левофлоксацин (присутній на фармацевтичному ринку України як торгова марка Леваксела) є антибіотиком з групи фторхінолонів, широкий спектр дії якого забезпечується взаємодією з внутрішньоклітинними і мембранними структурами різних мікроорганізмів (як аеробних, так і анаеробних). Левофлоксацин має високу біодоступність, легко всмоктується з шлунково-кишкового тракту та проникає в різні тканини, виводиться переважно нирками, його застосування характеризується мінімальними побічними ефектами й обмеженнями (дитячий вік, вагітність).
Обмежене застосування левофлоксацину з науковою метою при ерадикації Нр було і раніше, але зараз препарат включено в найавторитетніші міжнародні рекомендації, зокрема й схеми Маастрихтського консенсусу. Терапія на основі левофлоксацину сприяє успішній ерадикації Hp у 81-87% випадків.
Зокрема у дослідженні, проведеному E.G. Giannini та співавт. (2006), у якому застосовували схему на основі левофлоксацину, рівень ерадикації при 7-денному режимі терапії 2-ї лінії становив 84%. За даними J.P. Gisbert і співавт., у 64 пацієнтів з виразковою хворобою та функціональною диспепсією первинне призначення левофлоксацину дало змогу досягти ерадикації Hp у 88,5 і 84,4% випадків при аналізі популяції пацієнтів (PP) та популяції ITТ-аналізу відповідно. В інших подібних дослідженнях, проведених у різних країнах, були отримані порівнянні результати.
Таким чином, Леваксела може бути досить ефективним засобом не тільки в схемах так званої терапії порятунку, а й як препарат 1-ї лінії в комбінації з одним з інгібіторів протонної помпи й амоксициліном. Єдиним обмеженням залишається небажаність призначення левофлоксацину в дитячому та підлітковому віці (до 18 років). При коротких курсах лікування Леваксела є відносно безпечним і зручним у застосуванні препаратом.
Однак у разі подальшого підвищення резистентності Hp до левофлоксацину можна очікувати зниження ефективності такої схеми.
Що ж стосується рифабутину, то, ураховуючи епідемічну ситуацію, що склалася в Україні з туберкульозом, його використання рекомендується тільки у випадках призначення «терапії порятунку».
Слід зазначити, що дослідження, проведені безпосередньо в Україні, продемонстрували поширеність резистентності до кларитроміцину, хоча водночас за рівнем антигелікобактерної активності він перевищує інші препарати групи макролідів. Це робить його єдиним лікарським засобом з цієї групи, рекомендованим для лікування гелікобактерної інфекції.
Бактеріостатичний ефект кларитроміцину (Фроміліду) пов’язаний з блокадою синтезу білка за рахунок зворотного зв’язування з 23S-субодиницею рибосоми, що призводить до утворення неповноцінних білкових молекул і загибелі клітини. Однак у разі досягнення у вогнищі інфекції концентрації, яка в 2-4 рази перевищує мінімальну інгібуючу, він може чинити і бактерицидну дію, що, можливо, обумовлює його дозозалежний ефект при антигелікобактерній терапії. Крім цього, кларитроміцин володіє і певною протизапальною активністю, яка пояснюється його здатністю пригнічувати продукцію прозапальних і стимулювати синтез протизапальних цитокінів.
Після перорального прийому кларитроміцин швидко всмоктується в шлунково-кишковому тракті. За даними B. Sullivan та співавт. (2002), кларитроміцин забезпечує майже на 30% вищу частоту ерадикації Нр порівняно з азитроміцином. 90% Нр пригнічується вже при застосуванні кларитроміцину (Фроміліду) у мінімальній концентрації, а його біодоступність із підвищенням дози зростає.
Фромілід має ліпофільні властивості і добре проникає в шлунковий сік. Біотрансформується в печінці за допомогою цитохрому Р450. Препарат стійкий до впливу соляної кислоти шлункового соку, але ефективний тільки проти тих мікроорганізмів, які здатні до поділу.
Нові дані про антигелікобактерну активність кларитроміцину були отримані після відкриття феномену бактеріальних біоплівок. Біоплівка є динамічною сукупністю мікроорганізмів, що перебувають у синтезованому ними полімерному матриксі і тісно пов’язані з поверхнею під ним. Найважливішою функцією такої системи є захист бактеріальних клітин від реакцій імунної системи макроорганізму та дії несприятливих факторів зовнішнього середовища, зокрема антибіотиків.
Як і більшість бактерій у своєму середовищі існування, Hp формує біоплівки на слизовій оболонці шлунка. Саме цим феноменом можна частково пояснити високу стійкість цього мікроорганізму до багатьох антибіотиків. Кларитроміцин (Фромілід) має здатність руйнувати матрикс бактеріальних біоплівок, що значно підвищує їх проникність для інших антибактеріальних засобів.
Наш багаторічний досвід застосування Фроміліду в складі антигелікобактерної терапії свідчить не тільки про його високу клінічну ефективність і стабільну ерадикаційну активність, а й про хорошу переносимість препарату та мінімальну частоту розвитку диспепсичних розладів.
Крім того, в останні роки подолання можливої резистентності Нр до антигелікобактерних препаратів вже при першому зверненні хворого рекомендують розпочинати ерадикацію Нр з чотирикомпонентних схем на основі вісмуту субцитрату [4, 11, 19, 31].
Водночас у значної кількості фахівців виникли нові запитання, пов’язані з ерадикацією Нр. Одним із таких питань є ефективність ерадикаційної терапії залежно від вибору ІПП [31].
Чому кислотоінгібіція є важливим компонентом у контексті ефективності ерадикаційної антигелікобактерної фармакотерапії?
Вибір ІПП може впливати на ефективність ерадикаційної терапії, що було підтверджено в проведених метааналізах.
Так, наприклад, є дані досліджень in vitro, які демонструють, що рабепразол має більш виражену активність проти росту і рухливості кларитроміцин-резистентних штамів Нр, ніж інші ІПП [42]. За даними тих самих авторів, прийом рабепразолу в зниженому дозуванні (10 мг 2 рази добу) дозволяє досягти результатів ерадикації від 75 до 89%.
Метааналіз ефективності різних ІПП (омепразолу, лансопразолу, рабепразолу й езомепразолу) у потрійній терапії Нр був проведений у 2005 році в Барселоні, Іспанія [44]. Результати виявилися такими: ефективність ерадикації Нр при застосуванні омепразолу і лансопразолу – 74,7% і 76%, омепразолу і рабепразолу – 77,9% і 81,2%, омепразолу і езомепразолу – 87,7% і 89%, лансопразолу і рабепразолу – 81% і 85,7%. Тобто ефективність ерадикації Нр залежно від обраного ІПП виявилася різною.
Нещодавно було опубліковано результати метааналізу, у якому досліджувалася ефективність рабепразолу і езомепразолу порівняно з ІПП першого покоління в ерадикації Нр [36]. Автори дійшли висновку, що рабепразол та езомепразол виявляють більшу ефективність в ерадикаційних схемах, ніж ІПП першого покоління. Висновки про ефективність езомепразолу є неоднозначними, оскільки цей препарат застосовувався в подвійній дозі (40 мг) в порівнянні з рабепразолом в дозі 10-20 мг. Автори метааналізу стверджують, що рабепразол та езомепразол показують більшу ефективність у схемах ерадикаційної терапії, ніж ІПП першого покоління.
Для ефективної антигелікобактерної фармакотерапії необхідно, щоб внутрішньошлунковий рН був >5,0 не менше ніж 8 год на добу. При цьому концентрація антибактеріальних препаратів у шлунку збільшується на 15-20%, а їхня бактерицидна дія починає реалізовуватися безпосередньо в шлунку [9, 18, 35]. Крім того, слід враховувати, що ІПП мають діяти максимально ефективно в нічний час [37].
Експериментальним шляхом було встановлено, що чутливість Нр до кларитроміцину, амоксициліну та тетрацикліну залежить від рівня шлункового рН. Зокрема, мінімальна чутливість Нр до вищеназваних антибіотиків буде при рН середовища від 1,0 до 5,0. Водночас при збільшенні рН середовища від 5,5 до 7,0 спостерігається збільшення чутливості Нр до кларитроміцину, амоксициліну та тетрацикліну [25, 32].
Відомо, що за рахунок збільшення внутрішньошлункового рН зменшується руйнація антигелікобактерних препаратів, таких як метронідазол та кларитроміцин, що збільшує їх вміст у просвіті шлунка та підвищує їх концентрацію у слизовій оболонці шлунка [22, 38].
Тому підтримання високих значень внутрішньошлункового рН є необхідним чинником для проведення ефективної ерадикації Нр [27].
Для досягнення високих значень внутрішньошлункового рН навіть пропонується використання збільшених доз ІПП. Зокрема, у низці досліджень, де використовувались подвійні стандартні дози омепразолу разом з антибіотиками, було встановлено пряму залежність успішності ерадикації Нр від дози ІПП [30, 44].
Встановити безпосередню залежність успішності ерадикації Нр від рівня кислотоінгібіції вдалося і в дослідженні M. Sugimoto, T. Furuta та співавт. (2007). Виявлено, що у хворих, у яких вдалося досягнути елімінації Нр, медіана добового внутрішньошлункового рН була вірогідно більшою (6,4 [5,0-7,6]), ніж у хворих із неуспішною ерадикацією Нр (5,2 [2,2-6,2]). Подальші дослідження виявили взаємозв’язок між кислотосупресією та активністю ізоензиму СYP2С19 в обстежених пацієнтів [40].
Метаболізм ІПП відбувається в печінці за участю двох ізоформ цитохрому Р450 – СYР2С19 і СYРЗА4, які забезпечують окислення СН3 – групи піримідинового циклу, атома сірки молекули омепразолу і його аналогів до гідроксисульфонів [33, 34]. Саме тому кислотоблокуючий ефект ІПП залежатиме від активності ізоензиму СYP2С19. Генний поліморфізм СYP2С19 поділяє людську популяцію на три фенотипові підгрупи: швидкі метаболізатори, проміжні метаболізатори та повільні метаболізатори [29]. На думку низки дослідників, 2/3 представників білої раси відносяться до швидких метаболізаторів і саме тому у таких пацієнтів ефективність ерадикації Нр може знижуватися аж до 20% [43]. Тож застосування езомепразолу і рабепразолу як препаратів, чий кислотоблокуючий ефект не буде залежати від активності цитохрому Р450, рекомендоване Маастрихтським консенсусом V для переважного використання в ерадикаційних схемах у пацієнтів в Європі і Північній Америці, де відзначена висока поширеність саме швидких метаболізаторов ІПП [31].
Однак у клінічній практиці не було б доречним нехтувати використанням пантопразолу в ерадикаційних схемах, адже цьому препарату також притаманний шлях метаболізму, що відбувається через кон’югації (сульфатування) майже без участі ізоферментів СYP2С19 та CYP3A4. За рахунок цього, по-перше, забезпечується постійна величина його біодоступності вже після першого прийому, а по-друге, пантопразол має найменший серед інших ІПП вплив на метаболізм інших лікарських засобів [17, 20].
На кафедрі внутрішньої та сімейної медицини Вінницького національного медичного університету ім. М.І. Пирогова накопичений значний досвід вивчення кислотосупресивної дії сучасних ІПП, зокрема пантопразолу [12, 13, 14].
Саме тому метою роботи було вивчення показників добового внутрішньошлункового рН під час проведення ерадикації Нр трикомпонентною схемою (пантопразол + кларитроміцин + амоксицилін) у пацієнтів із кислотозалежними захворюваннями стравоходу, шлунка та дванадцятипалої кишки з успішною ерадикацією Нр і проведення порівняльного аналізу результатів експрес-гастро-рН-моніторингу у пацієнтів з успішною та неуспішною ерадикацією Нр.
Матеріали та методи. Було обстежено і проліковано 15 хворих (9 чоловіків і 6 жінок) на кислотозалежні захворювання стравоходу, шлунка та дванадцятипалої кишки, інфікованих Нр (основна група).
Середній вік пацієнтів основної групи склав 38,7±3,6 року, зріст 170,7±2,2 см, маса тіла 69,9±3,3 кг. Пацієнтам цієї групи була призначена трикомпонентна антигелікобактерна фармакотерапія: пантопразол (Нольпаза) 0,04 г × 2 рази на добу + кларитроміцин 0,5 г × 2 рази на добу + амоксицилін 1,0 г × 2 рази на добу.
Експрес-гастро-рН-моніторинг і добовий гастро-рН-моніторинг проводився на 6,7±0,3 добу застосування трикомпонентної схеми ерадикації Нр.
Контрольний дихальний уреазний тест із 13С-міченою сечовиною (IRIS, Wagner, Німеччина), який виконувався через 4 тижні після завершення лікування, у всіх пацієнтів групи був негативним.
Крім того, ми проаналізували результати експрес-гастро-рН-моніторингу 10 хворих (5 чоловіків і 5 жінок) на кислотозалежні захворювання стравоходу, шлунка і дванадцятипалої кишки, інфікованих Нр, із невдалим результатом антигелікобактерної терапії (контрольна група).
Середній вік пацієнтів контрольної групи становив 46,4±5,8 року, зріст 169,6±2,1 см, маса тіла 68,8±2,6 кг. Пацієнти цієї групи отримували такі ІПП: омепразол – 3 хворих, лансопразол – 4 пацієнти, езомепразол – 1 хворий, рабепразол та пантопразол по 1 пацієнту відповідно.
Трикомпонентна антигелікобактерна фармакотерапія у цих хворих складалась з ІПП (стандартна доза) × 2 рази на добу + кларитроміцин 0,5 г × 2 рази на добу + амоксицилін 1,0 г × 2 рази на добу.
Експрес-гастро-рН-моніторинг проводився на 6,5±0,4 добу застосування трикомпонентної схеми ерадикації Нр.
Контрольний дихальний уреазний тест із 13С-міченою сечовиною (IRIS, Wagner, Німеччина), який виконувався через 4 тижні після завершення лікування, у пацієнтів цієї групи виявися позитивним.
Експрес-гастро-рН-моніторинг та добовий гастро-рН-моніторинг проводився з використанням ацидогастрографа АГ-1рН-М та гастроентерологічної електродної системи. Експрес-гастро-рН-моніторинг виконувався пацієнтам згідно з методикою, розробленою професором В.М. Чернобровим [3].
Під час статистичної обробки отриманих результатів використовувалися середня арифметична і стандартна похибка середньої арифметичної, які розраховувались за відомими формулами [7].
Обробка отриманих результатів проводилась на комп’ютері з ліцензованим програмним забезпеченням Windows XP Home Edition (№ ліцензії C4CGH-PRWGG-WPBF4-PJVRM-F339W), Office 2002 Word, Excel (№ ліцензії XST36-B8T7W-9CFV-9C9Y8-MJ226; № продукту 54521-750-6140064-17681).
Результати дослідження. Під час аналізу результатів добового гастро-рН-моніторингу у хворих основної групи встановлено, що комплекс показників добового внутрішньошлункового рН при проведенні антигелікобактерної фармакотерапії становив: min pH 1,8±0,29, max рН 8,1±0,19, Х рН 5,4±0,33, Mo рН 5,8±0,57 та Me pH 5,4±0,41.
Результати аналізу добового гастро-рН-моніторингу (рис. 1) показали, що за добу кількість вимірювань із внутрішньошлунковим рН≥3,0 складала 85,2±5,0% від всіх вимірювань внутрішньошлункового рН протягом всього дослідження, що становило 20,4±1,2 год.
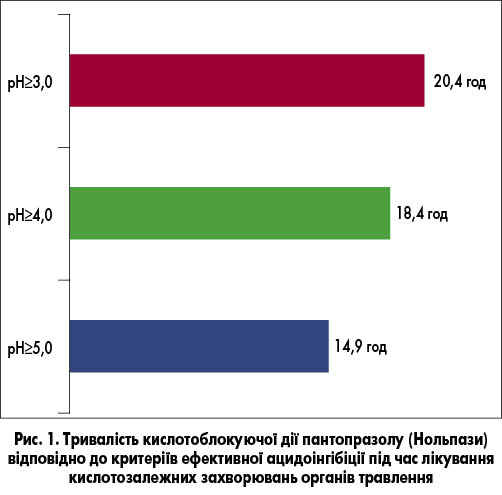
Під час дослідження кількості вимірювань із внутрішньошлунковим рН≥4,0 встановлено, що за добу їх відсоток складав 76,0±6,59% від усіх вимірювань внутрішньошлункового рН протягом всього дослідження, що становило 18,4±1,6 год.
У ході аналізу результатів добового гастро-рН-моніторингу кількість вимірювань внутрішньошлункового рН≥5,0 складала 62,4±7,91% від усіх вимірювань внутрішньошлункового рН, що становило 14,9±1,9 год.
Оцінюючи нічний період (22:00-07:00) добового гастро-рН-моніторингу у хворих з успішною ерадикацією Нр, ми встановили, що показники внутрішньошлункового рН під час проведення антигелікобактерної фармакотерапії становили: min pH 2,9±0,49, max рН 7,7±0,31, Х рН 5,3±0,43, Mo рН 5,6±0,61 та Me pH 5,1±0,49.
Відсоток вимірювань із внутрішньошлунковим рН≥3,0 за нічний період складав 81,9±7,5% від усіх вимірювань внутрішньошлункового рН цього періоду, що становило 7,4±0,7 год.
При визначенні кількості вимірювань із внутрішньошлунковим рН≥4,0 встановлено, що за нічний період вони склали 72,9±7,79% від усіх вимірювань внутрішньошлункового рН цього періоду, що становило 6,6±0,7 год.
За результатами аналізу нічного періоду добового гастро-рН-моніторингу було встановлено, що кількість вимірювань внутрішньошлункового рН≥5,0 склала 62,5±8,79% від усіх вимірювань внутрішньошлункового рН цього періоду, що становило 5,6±0,8 год.
Таким чином, пантопразол (Нольпаза) забезпечує достатній кислотоінгібуючий ефект (внутрішньошлунковий рН≥5,0 підтримувався 14,9±1,9 год) впродовж доби. Такий рівень кислотосупресії є достатнім для забезпечення успішної ерадикації Нр. Це дозволяє рекомендувати застосування Нольпази у схемах для проведення антигелікобактерної терапії.
Слід зазначити, що добовий гастро-рН-моніторинг є золотим стандартом вивчення ефективності тих чи інших кислотоблокуючих препаратів. Однак його широке використання обмежене низкою причин, зокрема певною незручністю для хворого, тривалістю дослідження, раціональністю використання обладнання.
Тому для практичних гастроентерологів було б важливим вивчити можливість застосування більш швидкої та простої у виконанні, але достатньо інформативної методики внутрішньошлункової рН-метрії для оцінки ефективності кислотоблокуючої дії ІПП та можливості прогнозування за її результатами успішності ерадикації Нр. Такою методикою є експрес-гастро-рН-моніторинг.
У ході порівняльного оцінювання результатів експрес-гастро-рН-моніторингу у хворих основної та контрольної групи ми встановили певні відмінності секреції хлористоводневої кислоти на тлі прийому ІПП в цих групах обстежуваних. Зокрема, при введенні рН-мікрозонду у шлунок (згідно з методикою експрес-гастро-рН-моніторингу) ми з’ясували, що у хворих основної групи, які отримували в лікувальній схемі пантопразол (Нольпазу), що привело в результаті до успішної ерадикації у порівнянні з пацієнтами контрольної групи, ерадикація у яких виявилася неуспішною, внутрішньошлунковий рН (рис. 2) був вірогідно більшим (р<0,01) в кардіальному відділі, тілі й антральному відділі шлунка на глибині вимірювання 40, 43, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60 см (6,7±0,24; 6,3±0,26; 6,3±0,37; 6,3±0,47; 6,3±0,45; 6,2±0,44; 6,2±0,44; 6,2±0,39; 6,1±0,42; 6,1±0,42; 6,2±0,41; 6,3±0,37; 6,2±0,36; 6,2±0,38; 6,2±0,39; 6,2±0,38; 6,3±0,39; 6,3±0,29 проти 5,3±0,58; 4,8±0,59; 4,7±0,6; 4,1±0,73; 4,1±0,73; 3,9±0,73; 4,0±0,72; 3,9±0,42; 4,0±0,57; 3,9±0,37; 3,9±0,32; 4,1±0,57; 4,1±0,78; 4,0±0,8; 4,0±0,79; 4,0±0,77; 4,1±0,77; 4,3±0,79 відповідно).
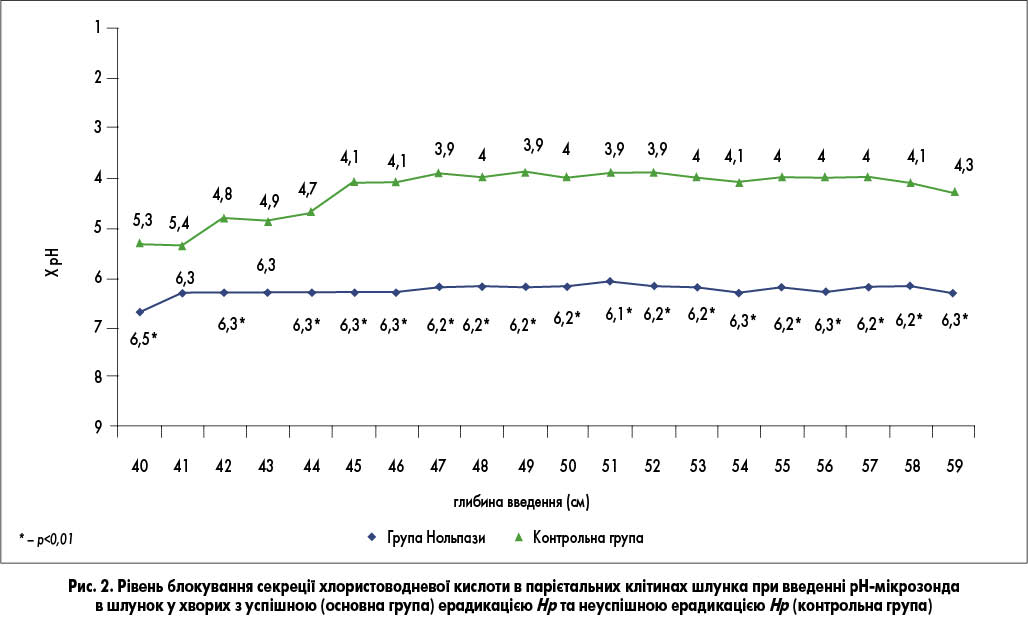
Отримані результати засвідчили, що пантопразол (Нольпаза) у пацієнтів основної групи приводив до потужного блокування секреції хлористоводневої кислоти в парієтальних клітинах шлунка.
При проведенні вимірювань рН під час виведення рН-мікрозонда зі шлунка (рис. 3) встановлено, що внутрішньошлунковий рН в основній групі порівняно з контрольною групою був також вірогідно більшим (р<0,05) в тілі та кардіальному відділі шлунка на глибині вимірювання рН 54, 52, 51, 50, 49, 48, 47, 46, 45, 44, 43, 42, 41, 40 см (6,1±0,44; 6,1±0,46; 6,1±0,47; 6,0±0,48; 5,9±0,5; 6,0±0,5; 5,9±0,51; 5,9±0,5; 5,9±0,42; 6,0±0,42; 6,1±0,46; 6,1±0,47; 6,1±0,36; 6,3±0,38 проти 4,2±0,8; 4,1±0,8; 4,0±0,8; 3,9±0,8; 4,1±0,77; 4,1±0,73; 4,0±0,72; 4,0±0,72; 4,1±0,7; 4,1±0,7; 4,0±0,77; 4,1±0,7; 4,2±0,78; 4,3±0,8).
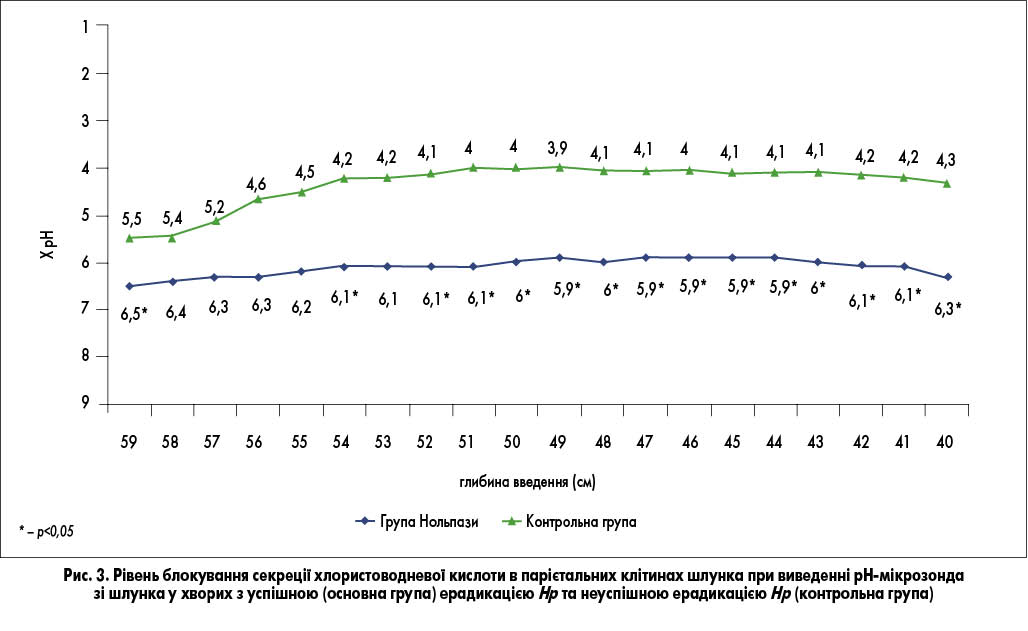
Порівняння комплексу показників експрес-гастро-рН-моніторингу у пацієнтів основної та контрольної груп (табл.) показало, що у хворих із неуспішною ерадикацією Нр (контрольна група) спостерігалися вірогідно менші (р<0,01) показники внутрішньошлункового рН порівняно з пацієнтами з успішною ерадикацією Нр (основна група).
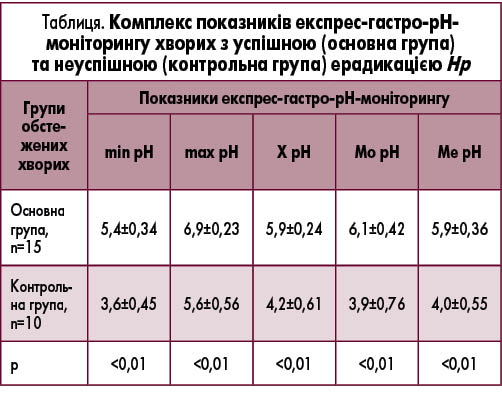
Таким чином, ми встановили, що за результатами експрес-гастро-рН-моніторингу у хворих з успішною ерадикацією Нр спостерігалося більш потужне блокування секреції хлористоводневої кислоти, ніж у хворих із невдалим лікуванням Нр, що забезпечувалося застосуванням в ерадикаційній схемі препарату пантопразол (Нольпаза).
Отримані нами дані підтверджують необхідність контролю ефективності кислотосупресивної фармакотерапії для прогнозування успішності антигелікобактерної терапії та можливості проведення вчасної корекції схеми лікування.
Висновки
- Успішність проведення ерадикації Нр залежить від значень внутрішньошлункового рН під час проведення антигелікобактерної фармакотерапії.
- Підтримання рівня внутрішньошлункового рН≥5,0 впродовж 14,9±1,9 год на добу є достатнім для успішної ерадикації Нр у пацієнтів із кислотозалежними захворюваннями стравоходу, шлунка та дванадцятипалої кишки.
- Експрес-гастро-рН-моніторинг може бути використаний як скринінгова методика для контролю ефективності антисекреторної дії блокаторів секреції хлористоводневої кислоти та прогнозування успішності проведення антигелікобактерного лікування.
- Пантопразол (Нольпаза) в дозі 0,04 г × 2 рази на добу забезпечує достатнє блокування секреції хлористоводневої кислоти для проведення успішної ерадикації Нр.
Література
- Бабак М.О., Фадєєнко Г.Д. Порівняльна ефективність потрійних схем антигелікобактеріальної терапії у хворих з виразкою дванадцятипалої кишки, асоційованою з резистентними штамами Helicobacter pylori // Сучасна гастроентерологія. – 2002. – № 1 (7). – С. 39-41.
- Вдовиченко В.І., Демидова А.Л. Динаміка резистентності штамів Helicobacter pylori до антибіотиків та ефективність лікування виразкової хвороби дванадцятипалої кишки // Сучасна гастроентерологія. – 2006. – № 4 (30). – С. 55-59.
- Внутрішньопорожнинна рН-метрія шлунково-кишкового тракту / за ред. В.М. Чернобрового. – Вінниця, 1999. – 80 с.
- Зак М.Ю. Динаміка серологічних та морфологічних показників атрофічного гастриту в результаті ерадикації Helicobacter pylori // Сучасна гастроентерологія. – 2013. – № 3 (71). – С. 53-57.
- Ивашкин В.Т., Лапина Т.Л. Гастроэнтерология: нацинальное руководство. – М.: ГЭОТАР-Медиа, 2008. – С. 255-258.
- Кучерявый Ю.А. Как повысить эффективность лечения язвенной болезни / Ю.А. Кучерявый // Consilium Medicum Ukraina. – 2011. – № 12. – С. 36-42.
- Колде Я.К. Практикум по теории вероятностей и математической статистике. – М.: Медицина, 1991. – 157 с.
- Новицький А.О. Оптимізація мікробіологічного виявлення Helicobacter pylori: автореф. дис. … канд. мед. наук: [спец.] 03.00.07 «Мікробіологія»; Вінниц. НМУ. – Вінниця, 2015. – 16 с.
- Передерий В.Г., Ткач С.М., Кузенко Ю.Г., Скопиченко С.В. Кислотозависимые заболевания. Современные подходы к диагностике, лечению и ведению больных с ГЭРБ, пептическими язвами, НПВП-гастропатиями, функциональной диспепсией и другими гиперсекреторными заболеваниями. – К.: ООО «Тиса ЛТД», 2008. – 425 с.
- Передерій В.Г. Бактеріологічний метод визначення чутливості Helicobacter pylori до антибактеріальних препаратів // Сучасна гастроентерологія. – 2011. – № 3. – С. 7-10.
- Палій І.Г., Заїка С.В. Деякі аспекти лікування гастроезофагеальної рефлюксної хвороби // Український терапевтичний журнал. – 2005. – № 4. – С. 71-75.
- Палій І.Г., Заїка С.В., Чернова І.В. Порівняння впливу S-ізомеру пантопразолу («Ультера»), омепразолу та лансопразолу за результатами добового гастро-рН-моніторингу пацієнтів з пептичними ерозивно-виразковими захворюваннями шлунка та дванадцятипалої кишки // Сучасна гастроентерологія. – 2010. – № 5 (55). – С. 90-97.
- Палій І.Г., Заїка С.В., Колісник С.П., Вавринчук В.В., Салабай І.О. Роль інноваційної форми пантопразолу в лікуванні хворих на НПЗП-гастропатію // Сучасна гастроентерологія. – 2012. – № 1 (63). – С. 88-93.
- Палій І.Г., Вавринчук В.В., Салабай І.О., Заїка С.В. Сучасні вимоги до проведення ерадикації Helicobacter pylori у хворих з ерозивно-виразковими пошкодженнями шлунка та дванадцятипалої кишки // Сучасна гастроентерологія. – 2010. – № 4 (54). – С. 111-119.
Повний список літератури, що включає 44 джерела,
знаходиться в редакції.
СТАТТІ ЗА ТЕМОЮ Гастроентерологія
Метаболічноасоційована жирова хвороба печінки (МАЖХП) є однією з найактуальніших проблем сучасної гепатології та внутрішньої медицини в цілому. Стрімке зростання поширеності ожиріння та цукрового діабету (ЦД) 2 типу в популяції призвело до істотного збільшення кількості хворих на МАЖХП, яка охоплює спектр патологічних станів від неускладненого стеатозу до алкогольної хвороби печінки та цирозу, що розвиваються на тлі надлишкового нагромадження ліпідів у гепатоцитах. ...
Інфекція Helicobacter pylori (H. pylori) офіційно визнана інфекційним захворюванням і включена до Міжнародної класифікації хвороб (МКХ) 11-го перегляду, тому рекомендовано лікувати всіх інфікованих пацієнтів. Проте, зважаючи на широкий спектр клінічних проявів, пов’язаних із гастритом, викликаним H. pylori, лишаються специфічні проблеми, які потребують регулярного перегляду для оптимізації лікування. ...
Відтворення майбутнього здорової нації – один з найважливіших сенсів існування теперішнього покоління. День боротьби з ожирінням нагадує нам про поширеність цього проблемного явища і важливість попередження його наслідків. Ожиріння може мати вплив на різні аспекти здоров'я, включаючи репродуктивне....
Вивчення клініко-патогенетичних особливостей поєднаного перебігу остеоартрозу (ОА) у хворих із метаболічними розладами, які характеризують перебіг метаболічного синдрому (МС), зокрема цукровим діабетом (ЦД) 2 типу, ожирінням (ОЖ), артеріальною гіпертензією (АГ), є актуальним, оскільки це пов’язано з неухильним збільшенням розповсюдженості цього захворювання, недостатньою ефективністю лікування, особливо за коморбідності з іншими захворюваннями, які патогенетично пов’язані з порушеннями метаболічних процесів. ...




