Тактика ведения больных с хронической сердечной недостаточностью на этапе первичной медицинской помощи
 ХСН является конечной стадией практически всех кардиоваскулярных заболеваний. С практической точки зрения, ХСН – это синдром, для которого характерны определенные симптомы (одышка, отеки лодыжек, утомляемость) и клинические признаки (набухание шейных вен, мелкопузырчатые хрипы в легких, смещение верхушечного толчка влево, увеличение печени), возникшие в результате нарушения структуры или функции сердца.
ХСН является конечной стадией практически всех кардиоваскулярных заболеваний. С практической точки зрения, ХСН – это синдром, для которого характерны определенные симптомы (одышка, отеки лодыжек, утомляемость) и клинические признаки (набухание шейных вен, мелкопузырчатые хрипы в легких, смещение верхушечного толчка влево, увеличение печени), возникшие в результате нарушения структуры или функции сердца.
Распространенность ХСН в общей популяции составляет 1,5-2%, среди взрослого населения, по данным статистики разных стран, – от 1,5 до 5,5%, а среди лиц старше 70 лет – ≥10%. Несмотря на значительные успехи в лечении сердечно-сосудистых заболеваний, распространенность ХСН не только не снижается, но и неуклонно возрастает. Около 50% пациентов с ХСН имеют диастолический вариант синдрома, при котором систолическая функция левого желудочка (ЛЖ), оцениваемая прежде всего по его фракции выброса (ФВ), остается сохраненной. Значительную часть этой когорты больных составляют женщины с артериальной гипертензией (АГ), ожирением и фибрилляцией предсердий. Лидирующие позиции в структуре причин ХСН занимают ишемическая болезнь сердца (ИБС), способствующая развитию ХСН в 60-75% случаев, а также АГ, вследствие которой ХСН возникает у 75-80% больных. Важными факторами риска развития ХСН являются сахарный диабет 2 типа и кардиомиопатии.
Медицинскую помощь больным с ХСН предоставляют на трех уровнях здравоохранения: первичном – семейные врачи, участковые терапевты, вторичном – специализированная кардиологическая амбулаторная и стационарная помощь, третичном – специализированные центры и НИИ. Важное, часто – решающее, значение в диагностике, адекватной терапии и профилактике осложнений у больных с ХСН имеет тактика врача общей практики – семейной медицины. Нередко ему приходится принимать решения в условиях ограниченных диагностических ресурсов, что повышает значение правильной интерпретации общеклинических данных (жалоб пациента, анамнеза, физикального обследования), способствующей своевременному установлению правильного диагноза. На любом этапе предоставления медицинской помощи формулировка диагноза ХСН должна соответствовать терминологии действующих классификаций.
Какие классификации ХСН используются в клинической практике?
 В Украине применяются 3 клинические классификации ХСН, существенно дополняющие друг друга. Одна из них, созданная Н. Д. Стражеско и В. Х. Василенко при участии Г. Ф. Ланга и утвержденная на ХII Всесоюзном съезде терапевтов (1935 г.), основана на функционально-морфологических принципах оценки состояния больного (табл. 1).
В Украине применяются 3 клинические классификации ХСН, существенно дополняющие друг друга. Одна из них, созданная Н. Д. Стражеско и В. Х. Василенко при участии Г. Ф. Ланга и утвержденная на ХII Всесоюзном съезде терапевтов (1935 г.), основана на функционально-морфологических принципах оценки состояния больного (табл. 1).
Для описания выраженности симптомов ХСН в динамике традиционно используют классификацию ХСН по функциональным классам (ФК) Нью-Йоркской ассоциации сердца (NYHA). Именно на основании этой классификации отбирали больных для участия в большинстве рандомизированных исследований по ХСН. У больных с I ФК отсутствуют какие-либо симптомы, связанные с заболеванием сердца; больные со II, III или IV ФК имеют, соответственно, незначительные, умеренные или выраженные симптомы ХСН (табл. 2). Существуют ориентировочные соответствия стадий и ФК ХСН:
 I стадия соответствует II ФК (на фоне адекватного лечения – I ФК);
I стадия соответствует II ФК (на фоне адекватного лечения – I ФК);
IIа стадия соответствует III ФК (на фоне адекватного лечения – II ФК, иногда I ФК);
IIб стадия соответствует IV ФК (на фоне адекватного лечения – III ФК, иногда II ФК);
III стадия соответствует IV ФК (иногда, на фоне адекватного лечения, – III ФК).
И наконец классификация ХСН по вариантам в зависимости от результатов эхокардиографического (ЭхоКГ) исследования ФВ ЛЖ – со сниженной (<40%) и сохраненной (≥40%) ФВ ЛЖ.
Какую классификацию необходимо использовать для формулировки диагноза ХСН?
При формулировке диагноза необходимо использовать все 3 классификации и указывать клиническую стадию ХСН, состояние ФВ ЛЖ сердца и ФК ХСН по классификации NYHA, отражающий функциональные возможности пациента.
Какой объем обязательных диагностических мероприятий должен быть проведен больным с ХСН на этапе оказания первичной медицинской помощи?
Согласно унифицированному клиническому протоколу по ведению пациентов с ХСН врачам первичного звена здравоохранения необходимо выполнить следующий обязательный объем клинико-диагностического обследования:
- Клинический осмотр пациента (детальный сбор жалоб и анамнеза, оценка этиологических факторов и данных физикального обследования).
- Общий анализ крови (эритроциты, гемоглобин, гематокрит, тромбоциты, лейкоциты, СОЭ).
- Общий анализ мочи.
- Биохимические исследования: содержание в крови калия, натрия, креатинина, мочевины, глюкозы, билирубина, печеночных ферментов, расчет скорости клубочковой фильтрации (СКФ) по формулам EPI-CKD или MDRD.
- Регистрация электрокардиографии (ЭКГ) в 12 отведениях.
- ЭхоКГ.
- Рентгенография грудной клетки.
Дополнительные исследования по показаниям:
- Кардиоспецифические ферменты.
- Международное нормализованное отношение.
- Общий белок крови.
- Гликированный гемоглобин.
- Содержание в крови мочевой кислоты.
- Уровень тиреотропного гормона в крови.
Диагностика ХСН, особенно на ранних стадиях, может быть сопряжена с определенными трудностями. Обычно больной обращается за медицинской помощью именно из-за возникновения у него симптомов, многие из которых имеют низкую специфичность и не позволяют с уверенностью отличить ХСН от других сердечно-сосудистых заболеваний. Такие характерные симптомы, как ортопноэ и ночные приступы сердечной астмы, встречаются гораздо реже, особенно у больных с начальными стадиями ХСН. Многие клинические признаки ХСН обусловлены задержкой жидкости и также неспецифичны, к примеру периферические отеки, которые могут иметь внесердечные причины. Кроме того, признаки, связанные с задержкой жидкости, достаточно быстро исчезают при приеме диуретиков, поэтому они могут отсутствовать у больных, получающих диуретическую терапию. Симптомы и клинические признаки ХСН особенно трудно выявлять и, что не менее важно, правильно трактовать у больных пожилого возраста, у пациентов с ожирением и заболеваниями легких. Поэтому большое значение в диагностике ХСН имеет тщательный сбор анамнеза.
Маловероятно развитие сердечной недостаточности у лиц без сколько-нибудь значимого повреждения сердца, в то время как при наличии такового (особенно ранее перенесенного инфаркта миокарда) вероятность наличия ХСН существенно повышается. Это подчеркивает важность выявления у больного структурных или функциональных нарушений, которые объясняют имеющиеся симптомы ХСН и служат своего рода гарантией правильной диагностики.
Лечение этого заболевания носит постоянный характер, при этом регулярно осуществляется контроль клинического состояния пациента и переносимости им лечения. Стандарты терапии пациентов с ХСН и сохраненной ФВ ЛЖ сердца не разработаны, стратегия лечения таких больных основана на соблюдении ряда принципов.
Каковы принципы лечения больных с сохраненной ФВ ЛЖ сердца?
- Адекватное лечение основного заболевания.
- Адекватное лечение сопутствующих заболеваний.
- Симптоматическая терапия, направленная на устранение симптомов и нарушений кровообращения, вызванных ХСН.
- Лечение отечного синдрома (признаков гиперволемии).
Основные цели терапии больных ХСН на этапе оказания первичной медицинской помощи?
- Уменьшение симптомов ХСН и повышение качества жизни пациента.
- Улучшение прогноза – профилактика осложнений и преждевременной смерти.
Какие мероприятия предусмотрены для пациента на этапе оказания первичной медицинской помощи?
- Обучение пациента (разъяснение особенностей течения ХСН и роли модификации образа жизни; обучение контролю факторов риска развития ХСН и ее осложнений: объяснение необходимости отказа от алкоголя, курения, контроля массы тела, соблюдения диетического режима, измерения диуреза и т. д.; обсуждение необходимости приема конкретных лекарственных препаратов с информированием об их эффектах, в том числе о возможных побочных действиях; ответы на вопросы пациента).
- Мероприятия немедикаментозного характера.
- Назначение медикаментозного лечения.
Какие фармакотерапевтические средства обязательно должны быть назначены пациентам с ХСН и какова тактика их применения?
Все лекарственные средства для лечения ХСН можно разделить на две основные категории соответственно степени доказанности их влияния на прогноз:
- препараты, применяемые у всех больных и доказавшие способность снижать уровень смертности;
- препараты, применяемые в особых клинических ситуациях.
К средствам, доказавшим способность снижать смертность от ХСН, относятся ингибиторы ангиотензинпревращающего фермента (иАПФ), сартаны (блокаторы рецепторов ангиотензина II – БРА II), β-адреноблокаторы (β-АБ) и антагонисты минералокортикоидных рецепторов (АМР).
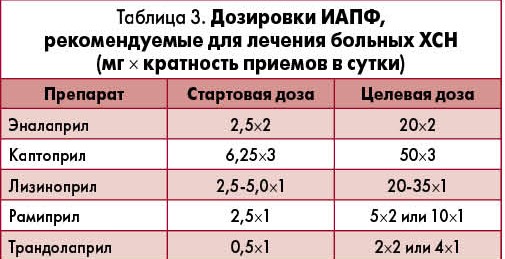 ИАПФ. Они, безусловно, относятся к препаратам первой линии в лечении больных ХСН (табл. 3). ИАПФ благоприятно воздействуют на клиническую симптоматику, качество жизни, замедляют прогрессирование болезни, улучшают его прогноз. Доказана способность иАПФ снижать риск смерти больных ХСН на 23%. Положительные эффекты иАПФ не зависят от возраста больных, сохраняются в большинстве клинических ситуаций и при любой степени тяжести ХСН. ИАПФ эффективны как на начальном этапе развития ХСН, включая бессимптомную дисфункцию ЛЖ, так и в самых поздних стадиях декомпенсации.
ИАПФ. Они, безусловно, относятся к препаратам первой линии в лечении больных ХСН (табл. 3). ИАПФ благоприятно воздействуют на клиническую симптоматику, качество жизни, замедляют прогрессирование болезни, улучшают его прогноз. Доказана способность иАПФ снижать риск смерти больных ХСН на 23%. Положительные эффекты иАПФ не зависят от возраста больных, сохраняются в большинстве клинических ситуаций и при любой степени тяжести ХСН. ИАПФ эффективны как на начальном этапе развития ХСН, включая бессимптомную дисфункцию ЛЖ, так и в самых поздних стадиях декомпенсации.
Кому и в какой дозировке назначают иАПФ при ХСН?
ИАПФ показаны всем больным с клиническими проявлениями ХСН (II-IV ФК) со сниженной (<40%) ФВ ЛЖ при отсутствии противопоказаний и, как правило, в сочетании с β-адреноблокаторами. Вначале назначают минимальную дозу, затем производят ее титрование путем повышения на величину стартовой дозы не чаще чем каждые 2 нед. Чем раньше начато лечение, тем больше шансов добиться благоприятного эффекта и продлить жизнь пациентов.
Побочные эффекты возникают на фоне приема иАПФ достаточно редко. Повышение уровня креатинина возможно у 5-15% больных ХСН и связано с основным механизмом действия иАПФ – блокадой влияния ангиотензина II на уровень почечной фильтрации. При этом может развиваться функциональная почечная недостаточность, что опасно у больных с исходной гипонатриемией. Однако при медленном титровании доз иАПФ стойкая высокая азотемия и усугубление почечной недостаточности встречается лишь у 1-2% декомпенсированных больных.
У пациентов с ХСН важно определение СКФ, так как иАПФ могут негативно влиять на этот показатель, особенно в условиях назначения больших доз без титрования и наличия у препарата только одного почечного пути выведения. При СКФ <60 мл/мин дозу иАПФ следует уменьшить наполовину, а при <30 мл/мин – на 3/4. СКФ <15 мл/мин является критерием отмены иАПФ . При патологии почек возможно применение иАПФ, имеющих два пути выведения из организма (почки/печень): фозиноприла (50/50), спираприла (50/50), рамиприла (70/30), трандолаприла (30/70). Дозы этих препаратов нужно корригировать лишь при снижении СКФ до менее чем 30 мл/мин.
При появлении на фоне приема иАПФ упорного кашля их заменяют на БРА II, которым не свойственно развитие этого осложнения. Абсолютными противопоказаниями к назначению иАПФ являются непереносимость (ангионевротический отек), двусторонний стеноз почечных артерий, беременность. Непереносимость при применении рекомендованных доз иАПФ не превышает 0,4%.
Титрование дозы иАПФ – процесс индивидуальный, так как у каждого пациента имеется свой дозовый оптимум и максимум лекарственных средств. Использование комбинации иАПФ с другими нейрогормональными ингибиторами (β-АБ, АМР) позволяет достигать у подавляющего числа больных ХСН благоприятного эффекта с меньшим риском нежелательных явлений, свойственных максимальным дозам препаратов. Однако будет ошибкой ограничиваться минимальными дозами иАПФ , если пациент хорошо их переносит и его артериальное давление (АД) находится в пределах нормальных значений, без резкого снижения.
Блокаторы β-адренергических рецепторов. Рациональным обоснованием применения β-АБ в лечении ХСН является блокада симпатико-адреналовой системы (САС), которая у больных с декомпенсацией находится в состоянии хронической гиперактивации и определяет плохой прогноз (высокую смертность). Активность САС прогрессивно нарастает параллельно увеличению тяжести ХСН, причем начиная со II стадии или II ФК преобладающими становятся негативные дезадаптирующие свойства катехоламинов. В связи с этим применение β-АБ наиболее целесообразно и эффективно у пациентов с клинически выраженной ХСН.
Доказано, что гиперактивация САС способствует достоверному увеличению риска как внезапной смерти, так и смерти от прогрессирования декомпенсации. Поэтому основная цель применения β-АБ в лечении больных с ХСН – улучшение прогноза и снижение смертности. Кроме того, β-АБ уменьшают степень ремоделирования сердца, т. е. оказывают кардиопротекторное действие, позволяющее замедлять прогрессирование декомпенсации и снижать число госпитализаций. Главным же негативным свойством, препятствующим в течение многих лет включению β-АБ в перечень препаратов первой линии для лечения ХСН, считался их отрицательный инотропный эффект, который, по мнению многих кардиологов и терапевтов, приводил к ухудшению течения заболевания. Сегодня доказана двухфазность влияния β-АБ на центральную гемодинамику у больных ХСН. Действительно, в первые две недели терапии этими препаратами сердечный выброс может снижаться (как за счет уменьшения собственно сократимости, так и в результате снижения частоты сердечных сокращений – ЧСС), а клинические проявления ХСН – даже несколько нарастать. Но затем, в результате уменьшения тахикардии, а следовательно, и снижения потребления миокардом кислорода, кардиомиоциты восстанавливают свою сократимость, и сердечный выброс начинает расти. Причем некоторые β-АБ (карведилол) при длительном применении могут позволить добиваться большего роста ФВ, чем положительные инотропные агенты (в частности, сердечные гликозиды).
Кому и в какой дозировке назначают β-АБ при ХСН?
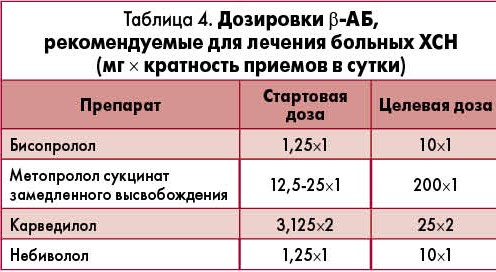 Блокаторы β-адренергических рецепторов назначают в сочетании с иАПФ , а при непереносимости последних – с БРА II, всем больным с клиническими проявлениями ХСН (II-IV ФК) со сниженно (<40%) ФВ ЛЖ при отсутствии противопоказаний. Лечение β-АБ начинают с 1/8 целевой дозы (стартовая доза), увеличивая ее на величину (или удвоенную величину) стартовой дозы не чаще 1 раза в 2 нед, а при плохой переносимости и резком снижении АД или ЧСС – 1 раз в месяц. Как и в случае с иАПФ , необходимо помнить, что у каждого больного своя оптимальная дозировка β-АБ, которая определяется снижением ЧСС до уровня <70 уд./мин. Только снижение ЧСС определяет эффективность лечения. На каждые 5 ударов снижения ЧСС достигается 18% снижения риска смерти больных ХСН (табл. 4).
Блокаторы β-адренергических рецепторов назначают в сочетании с иАПФ , а при непереносимости последних – с БРА II, всем больным с клиническими проявлениями ХСН (II-IV ФК) со сниженно (<40%) ФВ ЛЖ при отсутствии противопоказаний. Лечение β-АБ начинают с 1/8 целевой дозы (стартовая доза), увеличивая ее на величину (или удвоенную величину) стартовой дозы не чаще 1 раза в 2 нед, а при плохой переносимости и резком снижении АД или ЧСС – 1 раз в месяц. Как и в случае с иАПФ , необходимо помнить, что у каждого больного своя оптимальная дозировка β-АБ, которая определяется снижением ЧСС до уровня <70 уд./мин. Только снижение ЧСС определяет эффективность лечения. На каждые 5 ударов снижения ЧСС достигается 18% снижения риска смерти больных ХСН (табл. 4).
АМР. Негативная роль вторичного гиперальдостеронизма при ХСН известна давно. Начиная с середины 60-х годов XX ст. спиронолактон в дозах 100-300 мг/сут успешно применялся в комплексной диуретической терапии тяжелой ХСН как калийсберегающий диуретик. Спиронолактон рассматривался именно в качестве надежного партнера тиазидных и петлевых диуретиков. Препарат назначали при обострении явлений декомпенсации в течение 1-3 нед, после достижения компенсации доза препарата уменьшалась. Сегодня спиронолактон назначают начиная с дозы 25 мг/сут (целевая – 50 мг/сут) в комбинации с другими нейрогормональными модуляторами для лечения ХСН. Одновременно используется высокоселективный АМР эплеренон (стартовая и целевая дозы аналогичны дозам спиронолактона и составляют 25 и 50 мг в сутки соответственно). У препарата отсутствуют побочные эффекты в виде гинекомастии и нарушений менструального цикла, он реже вызывает ухудшение функции почек и гиперкалиемию.
Кому показаны АМР при ХСН?
АМР (спиронолактон и эплеренон) рекомендуются для лечения больных, имеющих клинические проявления ХСН (II-IV ФК) с ФВ ЛЖ сердца <35%. Их назначают на фоне приема иАПФ (а при их непереносимости – БРА II) и β-АБ.
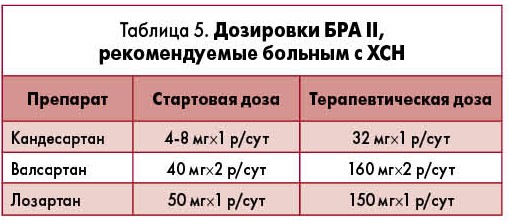 Блокаторы рецепторов АТ II. Появление второго класса блокаторов ренин-ангиотензин-альдостероновой системы (РААС) – селективных антагонистов рецепторов к АТ II произошло уже после укрепления иАПФ на позициях препаратов первой линии в терапии декомпенсации. Сегодня уже можно утверждать, что некоторые БРА II – кандесартан, валсартан и лозартан – могут применяться для лечения больных ХСН при непереносимости иАПФ . Титрование доз БРА II проводится таким же образом, что и титрование иАПФ (табл. 5).
Блокаторы рецепторов АТ II. Появление второго класса блокаторов ренин-ангиотензин-альдостероновой системы (РААС) – селективных антагонистов рецепторов к АТ II произошло уже после укрепления иАПФ на позициях препаратов первой линии в терапии декомпенсации. Сегодня уже можно утверждать, что некоторые БРА II – кандесартан, валсартан и лозартан – могут применяться для лечения больных ХСН при непереносимости иАПФ . Титрование доз БРА II проводится таким же образом, что и титрование иАПФ (табл. 5).
БРА II при ХСН показаны больным, у которых вследствие приема иАПФ развиваются такие негативные явления, как кашель или ангионевротический отек. БРА II назначают в комбинации с β-АБ и АМР. Комплексная терапия иАПФ , β-АБ и БРА II может рассматриваться при непереносимости АМР.
Диуретики. Задержка жидкости в организме и формирование отечного синдрома являются типичным и наиболее ярким проявлением ХСН. Поэтому дегидратационная терапия представляет собой одну из важнейших составляющих успешного лечения больных с ХСН.
Кому назначают диуретические препараты при ХСН?
Диуретические (мочегонные) препараты назначают пациентам с отечным синдромом независимо от ФВ ЛЖ сердца. Чаще всего больным назначают петлевые диуретики, комбинация которых с тиазидовыми может способствовать преодолению рефрактерности отечного синдрома.
Основные принципы диуретической терапии:
- Диуретики применяются с целью устранения отечного синдрома и улучшения клинического состояния и качества жизни больных ХСН.
- Большинство диуретиков (кроме торасемида) не замедляют прогрессирования ХСН и не улучшают прогноз.
- Лечение необходимо начинать с малых доз (особенно у больных, не получавших ранее мочегонных препаратов), в последующем подбирая дозу по принципу quantum satis (т. е. в требуемом количестве).
- Дегидратационная терапия при ХСН имеет две фазы – активную (в период декомпенсации) и поддерживающую (для поддержания эуволюмического состояния после достижения компенсации).
- В активной фазе объем выделившейся мочи может превышать таковой употребленной жидкости не более чем на 1 л в сутки при снижении веса ежедневно на 1 кг.
- Стремительная дегидратация приводит к чрезмерной гиперактивации нейрогормонов и «рикошетной» задержке жидкости в организме.
- Прерывистый прием диуретиков при ХСН усугубляет нейрогуморальный дисбаланс.
Сердечные гликозиды. Сердечные гликозиды вот уже более двух столетий остаются в числе приоритетных препаратов в лечении ХСН. Гликозиды имеют три основных механизма действия – положительный инотропный, отрицательный хронотропный и нейромодуляторный эффекты.
Кому и в каких дозах назначают дигоксин?
- Больным со стабильной гемодинамикой, персистирующей или постоянной формой фибрилляции предсердий (ФП), у которых с помощью β-АБ не удается контролировать частоту желудочковых сокращений (ЧЖС) (используют в сочетании с β-АБ).
- Больным со стабильной гемодинамикой, персистирующей или постоянной формой ФП, которые не переносят β-АБ, с целью контроля ЧЖС.
- В условиях острой декомпенсации возможно внутривенное введение дигоксина для контроля ЧЖС.
- Суточные дозы дигоксина при нормальном уровне креатинина крови составляют не более 0,125-0,25 мг, у пациентов пожилого возраста – 0,0625-0,125 мг.
Кому показан ивабрадин?
- Больным с синусовым ритмом и ФВ ЛЖ сердца ≤35%, у которых на фоне лечения иАПФ (или БРА II при непереносимости иАПФ ), β-АБ в максимально переносимых дозах и АМР показатель ЧСС равен ≥70 уд./мин.
- Больным с синусовым ритмом и ФП при ФВ ЛЖ сердца ≤35%, у которых на фоне лечения иАПФ (или БРА II при непереносимости иАПФ ) и АМР и непереносимости β-АБ показатель ЧСС равен ≥70 уд./мин.
Наиболее оправданным методом профилактики внезапной смерти у больных ХСН и жизнеугрожающими аритмиями является имплантация кардиовертера-дефибриллятора. Антитромбоцитарные препараты, пероральные антикоагулянты, препараты железа назначают по соответствующим показаниям. Для снижения риска внезапной смерти и госпитализаций по поводу сердечно-сосудистых событий пациентам с ХСН II-IV ФК со сниженной ФВ ЛЖ сердца, получающим иАПФ (или БРА II при непереносимости иАПФ), β-АБ и АМР, могут быть назначены омега-3 полиненасыщенные жирные кислоты. Одновременно проводится лечение сопутствующей патологии. Все пациенты с ХСН требуют диспансерного наблюдения в соответствии с требованиями существующих нормативных документов.
Ведение больного ХСН – непростая задача. Установление правильного диагноза и своевременное назначение комплексной терапии на первичном этапе оказания медицинской помощи позволяют замедлить прогрессирование синдрома, уменьшить число госпитализаций и улучшить прогноз пациентов в целом.
Список литературы находится в редакции.
Медична газета «Здоров’я України 21 сторіччя» № 15-16 (412-413), серпень 2017 р.
СТАТТІ ЗА ТЕМОЮ Кардіологія
Як відомо, кальцій бере участь у низці життєво важливих функцій. Хоча більшість досліджень добавок кальцію фокусувалися переважно на стані кісткової тканини та профілактиці остеопорозу, сприятливий вплив цього мінералу є значно ширшим і включає протидію артеріальній гіпертензії (передусім у осіб молодого віку, вагітних та потомства матерів, які приймали достатню кількість кальцію під час вагітності), профілактику колоректальних аденом, зниження вмісту холестерину тощо (Cormick G., Belizan J.M., 2019)....
Торакалгія – симптом, пов’язаний із захворюваннями хребта. Проте біль у грудній клітці може зустрічатися за багатьох інших захворювань, тому лікарям загальної практики важливо проводити ретельну диференційну діагностику цього патологічного стану та своєчасно визначати, в яких випадках торакалгії необхідна консультація невролога. В березні відбувся семінар «Академія сімейного лікаря. Біль у грудній клітці. Алгоритм дій сімейного лікаря та перенаправлення до профільного спеціаліста». Слово мала завідувачка кафедри неврології Харківського національного медичного університету, доктор медичних наук, професор Олена Леонідівна Товажнянська з доповіддю «Торакалгія. Коли потрібен невролог»....
Рівень ліпопротеїну (a) >50 мг/дл спостерігається в ≈20-25% населення і пов’язаний із підвищеним ризиком серцево-судинних захворювань (ССЗ) [1]. Ліпопротеїн (a) задіяний в атерогенезі та судинному запаленні, а також може відігравати певну роль у тромбозі через антифібринолітичну дію і взаємодію із тромбоцитами [2, 3]. Дієта та фізична активність не впливають на рівень ліпопротеїну (a); специфічної терапії для його зниження також не існує. Підвищений ризик ССЗ, пов’язаний з ліпопротеїном (а), залишається навіть у пацієнтів, які приймають статини [4]. Саме тому існує критична потреба в терапії для зниження цього ризику, особливо в первинній профілактиці. ...
Запалення відіграє важливу роль у розвитку багатьох хронічних захворювань, зокрема атеросклерозу. Нещодавно було встановлено, що гіперурикемія спричиняє запалення ендотеліальних клітин судин, ендотеліальну дисфункцію та, зрештою, атеросклероз. Експериментальна робота Mizuno та співавт. (2019), у якій було продемонстровано здатність фебуксостату пригнічувати запальні цитокіни, привернула увагу дослідників до протизапальних ефектів уратзнижувальних препаратів. Кількість лейкоцитів – надійний маркер запалення, пов’язаний із різними кардіоваскулярними захворюваннями, як-от ішемічна хвороба серця; у багатьох попередніх дослідженнях його використовували для оцінки протизапального ефекту терапевтичного втручання. Мета нового аналізу дослідження PRIZE – вивчити вплив фебуксостату на кількість лейкоцитів у пацієнтів із безсимптомною гіперурикемією....




