Перипартальная кардиомиопатия: имеем ли мы ответы на все вопросы?
Перипартальная кардиомиопатия (ПКМП), согласно определению Европейского общества кардиологов (ESC), представляет собой кардиомиопатию со сниженной фракцией выброса (ФВ) левого желудочка (ЛЖ) <45%, которая развивается у женщин без анамнеза заболевания сердца в конце беременности или на протяжении 5 мес после родов.
Впервые возникновение сердечной недостаточности (СН), связанной с перипартальным (от лат. peri – около, parturient – относящийся к беременности, родам) периодом, было описано в литературе еще в XIX веке Рудольфом Вирховым и другими исследователями, а первые клинические случаи опубликованы в г. Новый Орлеан (США) в 1937 году. Данный синдром оставался слабо изученным до 1971 года, когда Demakis и соавт. [9], представив данные 27 пациенток, у которых СН развилась в перипартальный период, впервые ввели термин peripartum cardiomyopathy – ПКМП. Развитие эхокардиографии (ЭхоКГ) позволило дать неинвазивную характеристику ПКМП, а критерий ФВ <45% был введен в 1999 году Национальным институтом сердца, легких и крови США [39].
Следует, однако, отметить, что сроки развития ПКМП на сегодняшний день не имеют жестких рамок. Те же Demakis и соавт. [9] оговаривали, что болезнь чаще всего манифестирует в первые недели после родов, хотя может себя проявлять и задолго до них.
Наличие достаточного количества «белых пятен» в понимании этиологии и патофизиологии, что связанно как с низкой заболеваемостью, так и с отсутствием больших рандомизированных исследований, определяет актуальность проблемы ПКМП [3].
В качестве клинического примера хотелось бы представить случай больной А., которая поступила в отделение ГУ «ННЦ «Институт кардиологии им. Н.Д. Стражеско» НАМН Украины» для диагностики и лечения ПКМП.
Пациентка А., 23 лет, на 10-й день после родов (первая беременность, первые роды) обратилась за медицинской помощью с жалобами на одышку в покое, которая усиливалась при разговоре, выраженные отеки конечностей, одутловатость лица, кашель, сердцебиение, выраженную общую слабость.
Anamnesis morbi: за неделю до родов (до этого, со слов, пациентка на протяжении всего периода беременности чувствовала себя хорошо) появились одышка, ощущение сердцебиения, усилилась отечность, общая слабость. На плановом визите у гинеколога состояние больной было расценено как удовлетворительное, а симптомы – как проявление вегетососудистой дистонии. Пациентка в плановом порядке госпитализирована в клинику за сутки до родоразрешения. Роды протекали физиологическим путем. На вторые сутки пребывания в стационаре пациентка почувствовала себя хуже, отмечая нарастание вышеуказанных симптомов, особенно одышки и тахикардии. В качестве вспомогательной терапии для купирования вышеуказанных симптомов на 5-й день после родов назначен амитриптилин в дозе 25 мг 3 раза в сутки, но в связи с плохой переносимостью и усилением симптомов на фоне лечения пациентка самостоятельно прекратила прием препарата. После выписки из стационара больная направлена на консультацию к эндокринологу по поводу выраженных отеков. Выставлен диагноз: послеродовый тиреоидит. Последующие обследования, которые включали УЗИ щитовидной железы и определение уровней тиреотропного гормона, Т3, Т4, антител к тиреоидной пероксидазе, не выявили отклонений.
В связи с отрицательной динамикой и прогрессирующим ухудшением общего состояния пациентке на 10-й день после родов проведены УЗИ органов брюшной полости (без клинически значимой патологии), мультиспиральная компьютерная томография органов грудной полости, где были выявлены признаки интерстициального поражения легких и двусторонний гидроторакс, а также выполнено ЭхоКГ, которая определила выраженную дилатацию камер сердца с тяжелым снижением систолической функции ЛЖ. С учетом данных исследований больная была направлена на консультацию к кардиологу.
Anamnesis vitae: в 4-летнем возрасте был впервые выставлен диагноз острого лимфобластного лейкоза. Пациентка получила полный курс химиотерапии. С 2003 года снята с диспансерного учета по поводу этого заболевания. С 1998 года страдает вирусным гепатитом В.
Данных о заболеваниях сердечно-сосудистой системы не было.
Status praesens objectivus: при поступлении в стационар состояние тяжелое. Ортопноэ. Усиление одышки при разговоре. Акроцианоз на фоне общей бледности кожи. Генерализированные отеки. Рост – 168 см, вес – 89 кг, индекс массы тела (ИМТ) – 31,53 кг/м2. Артериальное давление (АД) – 95/70 мм рт. ст. Укорочение перкуторного звука в нижних отделах легких, при аускультации (больше справа) мелкопузырчатые хрипы. Левая граница сердечной тупости по левой подмышечной линии. Тоны сердца глухие, деятельность ритмическая, тахикардия с частотой сердечных сокращений (ЧСС) 112 уд/мин. Систолический шум во всех точках аускультации, с максимумом выраженности на верхушке. Печень выступает на 3,5 см ниже края правого подреберья, нерезко выраженная болезненность при пальпации. Селезенка не пальпируется. Симптом поколачивания отрицательный с обеих сторон. Мочеиспускание свободное.
Общий анализ крови: эритроциты – 4,9×1012/л, гемоглобин – 138 г/л, лейкоциты – 7,6×109/л, гематокрит – 39,7%, эозинофилы – 0%, лимфоциты – 25,6%, моноциты – 1,9%, тромбоциты – 280×109/л, СОЭ – 6 мм/ч. В динамике – без отрицательных изменений.
Общий анализ мочи: без патологических изменений.
 Биохимический анализ крови: общий билирубин – 14 мкмоль/л, креатинин – 85 мкмоль/л, мочевина – 4 ммоль/л, мочевая кислота – 411 мкмоль/л, глюкоза – 4,7 ммоль/л, калий – 3,33 ммоль/л, натрий – 140 ммоль/л, общий белок – 63 г/л, общий холестерин – 6,4 ммоль/л, триглицериды – 2,0 ммоль/л, креатинкиназа – 66 Ед/л, АлАТ – 35 Ед/л, АсАТ – 27 Ед/л, скорость клубочковой фильтрации (СКФ) – 83 мл/мин/1,73 м2.
Биохимический анализ крови: общий билирубин – 14 мкмоль/л, креатинин – 85 мкмоль/л, мочевина – 4 ммоль/л, мочевая кислота – 411 мкмоль/л, глюкоза – 4,7 ммоль/л, калий – 3,33 ммоль/л, натрий – 140 ммоль/л, общий белок – 63 г/л, общий холестерин – 6,4 ммоль/л, триглицериды – 2,0 ммоль/л, креатинкиназа – 66 Ед/л, АлАТ – 35 Ед/л, АсАТ – 27 Ед/л, скорость клубочковой фильтрации (СКФ) – 83 мл/мин/1,73 м2.
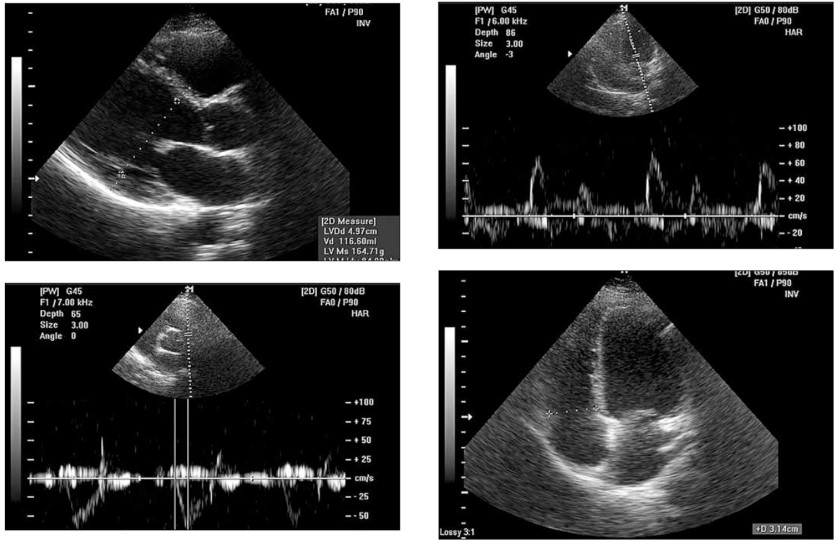
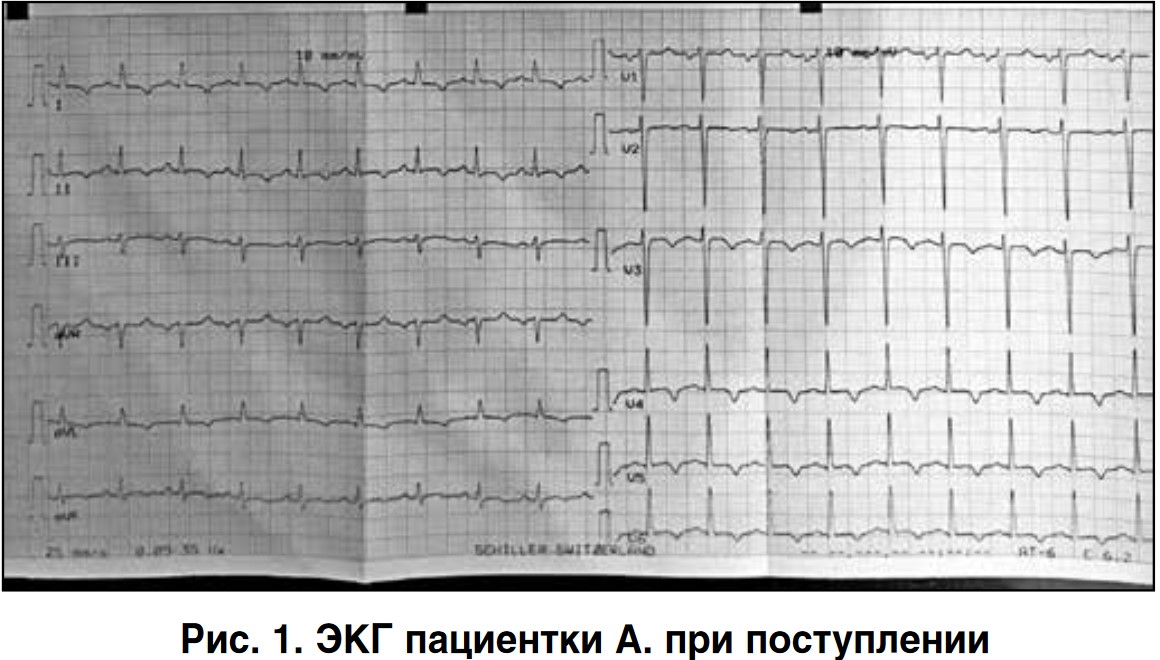
Коагулограмма: протромбиновый индекс – 82%, фибриноген – 4,0, международное нормализованное отношение – 1,24, свободный гепарин – 3. Электрокардиограмма (ЭКГ) при поступлении: синусовая тахикардия, ЧСС – 112 уд/мин, нормальное положение оси. Отрицательные зубцы Т I, II, AVL, V3-V6 (рис. 1).
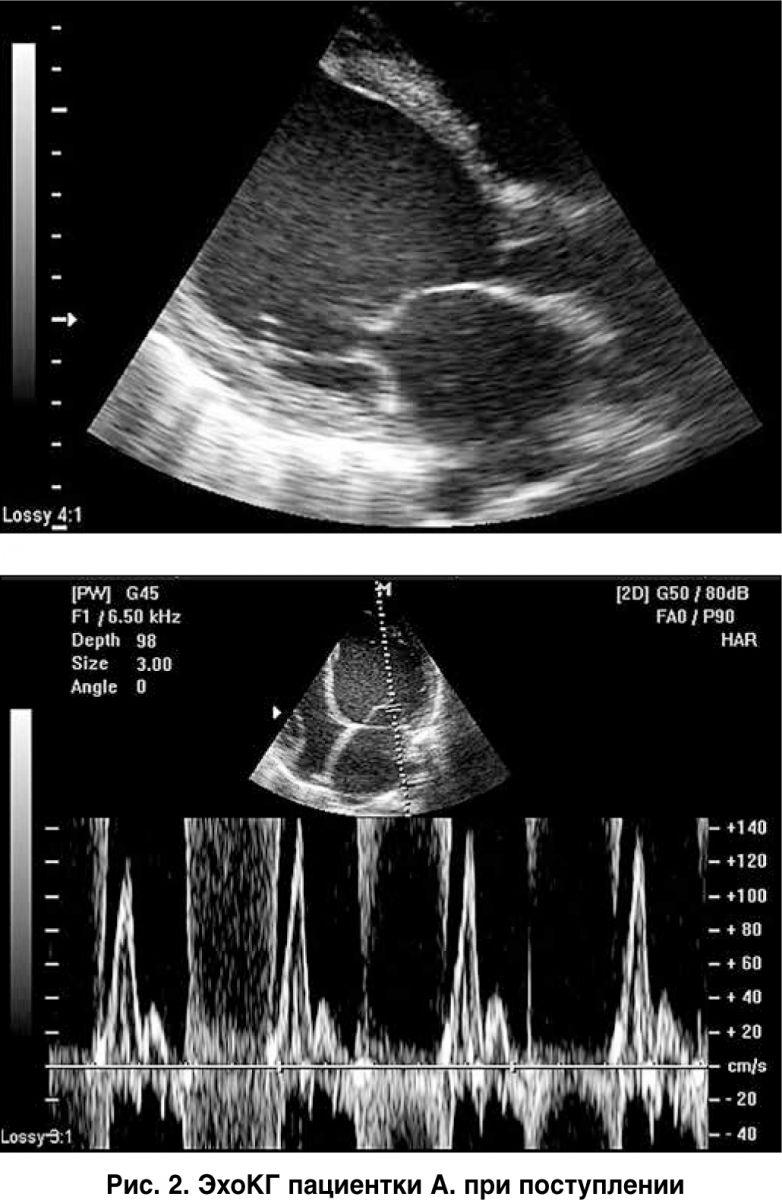 ЭхоКГ с допплерографией при поступлении (рис. 2): выносящий тракт ЛЖ (LVOT) – 2,0 см, корень аорты – 2,7 см, левое предсердие (ЛП) – 4,5 см (V – 132 мл), межжелудочковая перегородка (МЖП) – 1,05 см, задняя стенка ЛЖ – 0,8 см, ФВ – 32%, конечно-диастолический размер (КДР) – 6,5 см, конечно-систолический размер (КСР) – 5,5 см, конечно-диастолический объем (КДО) – 216 мл, конечно-систолический объем (КСО) – 148 мл, ударный объем (УО) – 68 мл, Е/А – 2,7, Е/е – 8,0, е’ – 5,4 см/с, DecTime – 150 мс, время изоволюмического расслабления ЛЖ (IVRT) – 70 мс, правый желудочек (ПЖ) – 4,9 см, стенка ПЖ – 0,3 см, правое предсердие (ПП) – 5,1 см.
ЭхоКГ с допплерографией при поступлении (рис. 2): выносящий тракт ЛЖ (LVOT) – 2,0 см, корень аорты – 2,7 см, левое предсердие (ЛП) – 4,5 см (V – 132 мл), межжелудочковая перегородка (МЖП) – 1,05 см, задняя стенка ЛЖ – 0,8 см, ФВ – 32%, конечно-диастолический размер (КДР) – 6,5 см, конечно-систолический размер (КСР) – 5,5 см, конечно-диастолический объем (КДО) – 216 мл, конечно-систолический объем (КСО) – 148 мл, ударный объем (УО) – 68 мл, Е/А – 2,7, Е/е – 8,0, е’ – 5,4 см/с, DecTime – 150 мс, время изоволюмического расслабления ЛЖ (IVRT) – 70 мс, правый желудочек (ПЖ) – 4,9 см, стенка ПЖ – 0,3 см, правое предсердие (ПП) – 5,1 см.
Систолическое давление в легочной артерии (СДЛА) – 55 мм рт. ст., масса миокарда (ММ) ЛЖ – 256 г, индекс ММ – 128 г/м2. Заключение: глобальная сократимость значительно снижена за счет диффузной гипокинезии стенок ЛЖ. Дилатация всех камер.
Умеренная легочная гипертензия. Умеренная митрально-трикуспидальная относительная недостаточность. Диастолическая дисфункция по рестриктивному типу.
Минимальный гидроперикард. Феномен спонтанного контрастирования (ФСК) в ЛЖ.
На контрольной ЭхоКГ через 5 дней: небольшая положительная динамика в виде уменьшения полостей правых отделов (ПЖ – 4,1 см, ПП – 4,2 см) и ЛП – 3,9 см (V – 112 мл). Сохраняется ФСК.
Заключение магнитно-резонансной томографии (МРТ) сердца с внутривенным болюсным контрастированием (гадопентетовая кислота – 20 мл): признаки дилатации полостей сердца, глобальный гипокинез.
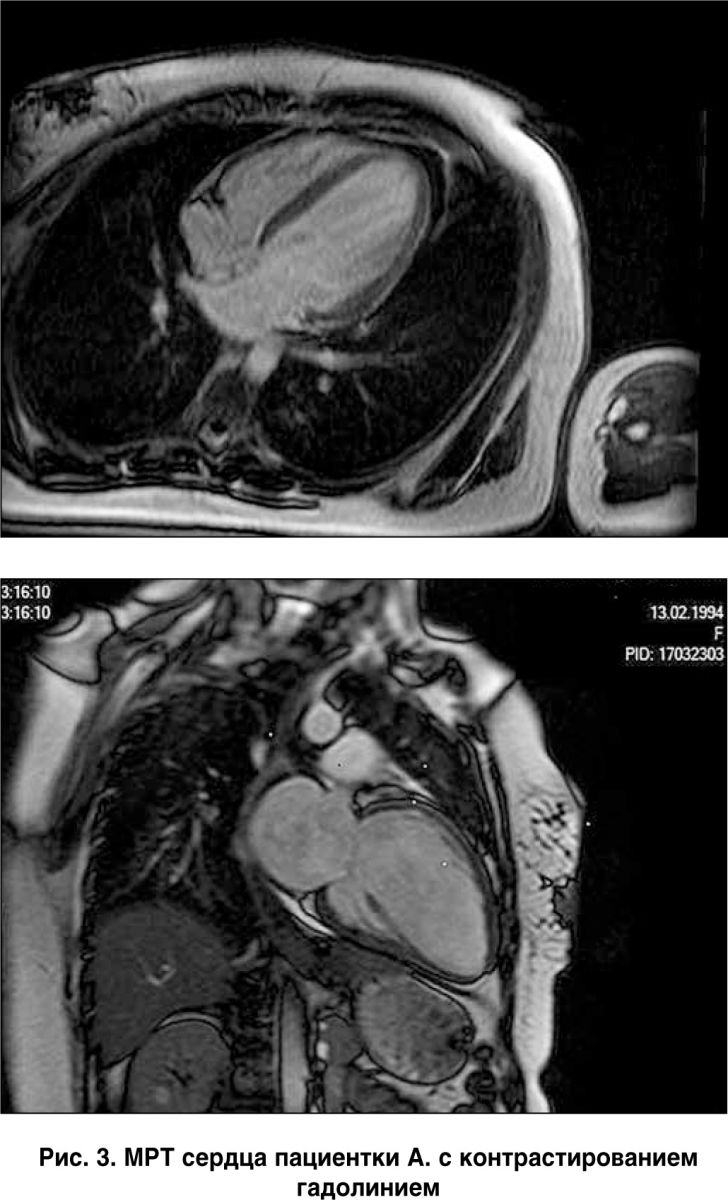 Отсутствие признаков ишемического поражения, фиброза, отека больше свидетельствуют в пользу дилатационной кардиомиопатии (ДКМП). Умеренная легочная гипертензия (рис. 3).
Отсутствие признаков ишемического поражения, фиброза, отека больше свидетельствуют в пользу дилатационной кардиомиопатии (ДКМП). Умеренная легочная гипертензия (рис. 3).
Учитывая анамнез, особенности течения болезни, объективный статус, данные лабораторно-инструментальных исследований, больной был выставлен диагноз: ПКМП с дилатацией всех камер. Относительная умеренная митрально-трикуспидальная недостаточность. Умеренная легочная гипертензия. СН II Б, IV функциональный класс по NYHA со сниженной ФВ. Сердечная астма. Двусторонний гидроторакс. Гидроперикард.
Лечение на стационарном этапе: фондапаринукс, торасемид, ацетилсалициловая кислота, эплеренон, эналаприл, карведилол, ивабрадин, ривароксабан.
Больная выписана из стационара на 11-й день с положительной динамикой. Вес – 79 кг, ИМТ – 27,99 кг/м2. АД – 105/75 мм рт. ст., ЧСС – 80 уд/мин. Значительно уменьшились симптомы СН: одышка, кашель. Сохранялась пастозность стоп и голеностопных суставов.
По данным ЭхоКГ: КДО – 208 мл, КСО – 145 мл, УО – 63 мл, оставалась сниженной систолическая функция ЛЖ (ФВ 30%), умеренная легочная гипертензия (СДЛА) – 45 мм рт. ст. Диастолическая дисфункция по рестриктивному типу. ФСК в ЛЖ.
Клинико-биохимические показатели в пределах нормы.
Рекомендации по поводу лечения на амбулаторном этапе: эналаприл, карведилол, эплеренон, торасемид, ривароксабан, ивабрадин.
Через 2 мес пациентке было проведено повторное ЭхоКГ-исследование, результаты которого свидетельствовали об улучшении систолической функции ЛЖ (ФВ возросла с 30 до 38%) с уменьшением полостей левых отделов, КДО – 146 мл, КСО – 91 мл, УО – 56 мл, ЛП – 3,2 см (V – 78 мл), соотношение ЛП/Ао – 1,27. Также произошло восстановление полостей правых отделов: ПЖ – 3,15 см, ПП – 3,4 см и СДЛА – 20 мм рт. ст.
Плановый осмотр через 6 мес: жалобы отсутствуют. При объективном обследовании: общее состояние удовлетворительное. ИМТ – 28,7 кг/м2. Кожные покровы бледно-розовые. Отеки отсутствуют. АД – 108/75 мм рт. ст. Пульс в положении сидя – 63 уд/мин, ритмический. Перкуторно над легкими определяется ясный легочной звук, аускультативно выслушивается везикулярное дыхание.
Границы сердца не расширены. Тоны ослаблены, деятельность ритмическая, ЧСС – 63 уд/мин. Живот мягкий, безболезненный. Печень под краем реберной дуги. Селезенка не пальпируется. Симптом поколачивания отрицательный с обеих сторон. Мочеиспускание свободное.
Общий анализ крови: эритроциты – 4,85×1012/л, гемоглобин – 135 г/л, лейкоциты – 5,63×109/л, гематокрит – 39,7%, эозинофилы – 1%, палочкоядерные – 2%, сегментоядерные – 59%, лимфоциты – 37%, моноциты – 1%, тромбоциты – 266×109/л, СОЭ – 6 мм/ч.
Общий анализ мочи: без патологических изменений.
 Биохимический анализ крови: общий билирубин – 10 мкмоль/л, креатинин – 70 мкмоль/л, мочевина – 3,8 ммоль/л, мочевая кислота – 230 мкмоль/л, глюкоза – 4,6 ммоль/л, калий – 4,37 ммоль/л, натрий – 144 ммоль/л, общий белок – 69 г/л, альбумин – 42 г/л, общий холестерин – 6,0 ммоль/л, триглицериды – 1,24 ммоль/л, креатинкиназа – 74 Ед/л, АлАТ – 16 Ед/л, АсАТ – 17 Ед/л, СКФ – 83 мл/мин/1,73 м2.
Биохимический анализ крови: общий билирубин – 10 мкмоль/л, креатинин – 70 мкмоль/л, мочевина – 3,8 ммоль/л, мочевая кислота – 230 мкмоль/л, глюкоза – 4,6 ммоль/л, калий – 4,37 ммоль/л, натрий – 144 ммоль/л, общий белок – 69 г/л, альбумин – 42 г/л, общий холестерин – 6,0 ммоль/л, триглицериды – 1,24 ммоль/л, креатинкиназа – 74 Ед/л, АлАТ – 16 Ед/л, АсАТ – 17 Ед/л, СКФ – 83 мл/мин/1,73 м2.
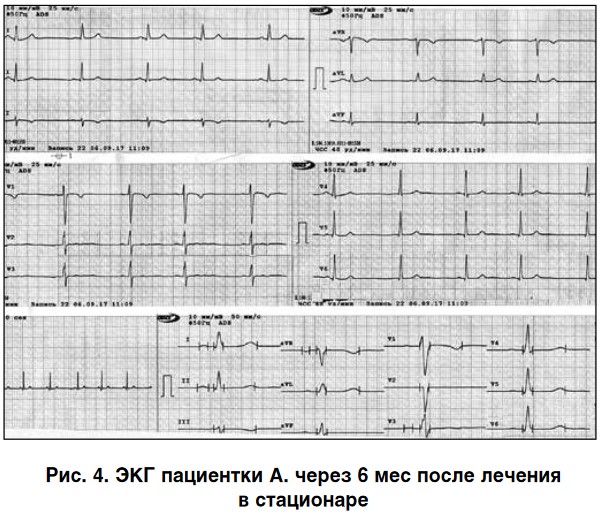
На ЭКГ: ритм синусовый, правильный, вольтаж сохранен. ЧСС – 60 уд/мин. В динамике – реверсия зубца Т в отведениях I, II, AVL, V3-V6 (рис. 4).
На ЭхоКГ (рис. 5): LVOT – 2,0 см, корень аорты – 2,7 см, ЛП – 2,8 см (V – 51 мл), МЖП – 1,05 см, задняя стенка ЛЖ – 0,8 см, ФВ – 45%, КДР – 4,95 см, КСР – 3,65 см, КДО – 103 мл, КСО – 57 мл, УО – 46 мл, Е/А – 1,41, Е/е – 8,0, DecTime – 150 мс, IVRT – 90 мс, е’ – 6,85 см/с, ПЖ – 3,1 см, ПП – 3,4 см. СДЛА – 20 мм рт. ст., ММ ЛЖ – 164,7 г, индекс ММ – 84,9 г/м2, нижняя полая вена – 1,65 см, коллабирует полностью. ФСК отсутствует. Заключение: положительная динамика от 05.05.2017 в виде нормализации полостей сердца, улучшения миокардиальной функции и глобальной сократимости ЛЖ. Минимальная трикуспидальная регургитация. ФСК отсутствует.
Рис. 5. ЭхоКГ через 6 мес после лечения в стационаре
Учитывая динамику, было принято решение об отмене ривароксабана, ивабрадина. Больная продолжает принимать эналаприл в дозе 7,5 мг/сут, карведилол 6,25 мг/сут, спиронолактон 25 мг/сут.
Столкнувшись на практике с трудностями диагностики ПКМП, считаем необходимым подчеркнуть особенности «клинического портрета» заболевания у нашей пациентки:
– возникновение симптомов СН у молодой женщины в поздние сроки первой одноплодной беременности при отсутствии соответствующего анамнеза патологии сердца;
– сниженная ФВ ЛЖ (<45%) с дилатацией всех камер сердца;
– достаточно быстрый темп уменьшения объемов камер сердца в динамике, с практически нормализацией их через 6 мес, синхронно с улучшением клинического состояния.
Естественно, при анализе этого клинического случая у нас возникло несколько вопросов. Во-первых, является ли типичным для ПКМП течение заболевания у нашей больной? Во-вторых, возможно, взгляды на патогенез и патофизиологию, принципы диагностики и лечения претерпели эволюцию? А может, существует возможность определить предикторы развития и прогноз у таких пациентов? Или все-таки ПКМП остается на сегодняшний день диагнозом исключения? Предлагаем обсудить эти вопросы.
Обсуждение
На сегодняшний день существуют яркие географические «горячие точки» ПКМП, причина которых остается неясной [3].
Например, на Гаити частота ПКМП составляет 1 случай на 300 [16], что, возможно, связанно с расовой принадлежностью, недостаточностью питания или высокой распространенностью преэклампсии (ПЭ), в Южной Африке – 1 случай на 1000 беременных.
Максимальный уровень заболеваемости отмечен в Северной Нигерии, где болезнь была обнаружена у 13% всех поступивших в клинику беременных женщин (1 случай на 100 живорождений) [25]. Среди возможных причин такого высокого процента заболевших первоначально были названы обычаи коренных жителей принимать горячие ванны, а также высокое потребление соли в перипартальном периоде, хотя недавние исследования по случаям заболевания ПКМП не подтвердили этот вывод [27-28]. Частота же ПКМП в США колеблется от ≈1 от 1000 до 4000 случаев живорождений, что, скорее всего, отражает, с одной стороны, демографическую неоднородность населения и отсутствие четкости самого определения данной патологии, а с другой – недооценку, вызванную недостаточной осведомленностью или неточным диагнозом.
Существует много публикаций касательно факторов, способствующих риску развития ПКМП. К ним относятся возраст матери, расовая принадлежность, многоплодная и/или многократная беременность, ПЭ, длительное использование токолитических препаратов, плохой социально-экономический статус [36].
Факторы риска
Возраст. Частота возникновения ПКМП сильно коррелирует с возрастом. Несмотря на то что заболевание может возникать у женщин любого возраста, более 50% случаев регистрируется у женщин старше 30 лет [6, 34].
Расовая принадлежность. Согласно эпидемиологическим данным ПКМП чаще встречается у чернокожих женщин, к тому же тяжесть заболевания у них выше. Так, в ходе обследования населения в штате Северная Каролина, США в 2003 году заболеваемость ПКМП у чернокожих женщин была в 4 раза выше, чем у женщин европеоидной расы (1:1087 против 1:4266). Уровень смертности в течение 5 лет наблюдения был также в 4 раза выше (24 против 6%). В ходе одноцентрового исследования случай-контроль в Джорджии и Теннесси, США было обнаружено 16-кратное увеличение заболеваемости ПКМП у негроидных женщин по сравнению с женщинами европеоидной расы [3].
ПЭ и артериальная гипертензия (АГ). Недавний метаанализ 22 исследований, охватывающих 979 случаев ПКМП, показал общую распространенность ПЭ у 22% пациенток, что более чем в 4 раза выше, нежели у женщин без ПКМП (от 3 до 5% соответственно) [4].
Однако не менее важным остается тот факт, что более чем у 90% женщин с ПЭ, даже если она тяжелая, не развивается ПКМП и, наоборот, как минимум 50% женщин с ПКМП не имеют ПЭ. Таким образом, два заболевания, являясь разными, но в то же время индуцируемыми и коррелируемыми друг с другом, предположительно могут иметь общие патофизиологические механизмы, а значит, клиницисту не следует отбрасывать подозрение на ПКМП при наличии ПЭ. Кроме того, поскольку данные о верификации ПКМП у больных с уже существующей АГ довольно противоречивы, было проведено исследование, в ходе которого сравнивались клинические особенности течения СН при ПКМП и у беременных с АГ [35]. Продемонстрированы существенные отличия начала развития СН, клинических особенностей, показателей ЭКГ и ЭхоКГ в исследуемых группах. В частности, у беременных с АГ и ПКМП наблюдались сокращения сроков госпитализации и более высокая ФВ ЛЖ в конце исследования по сравнению с пациентками с ПКМП без АГ.
Многократные беременности. Метаанализ 16 исследований продемонстрировал, что средняя частота беременностей двойней в случаях ПКМП составила 9%, что намного превышает среднюю 3% распространенность [42]. Сообщалось также о ряде случаев ПКМП у беременных тройней [13, 20].
Другие, но менее обоснованные факторы, способствующие развитию ПКМП, включали злоупотребление психоактивными веществами, анемию, бронхиальную астму, сахарный диабет, ожирение и недоедание.
Этиология и патофизиология
ПКМП часто приписывали патологическому гемодинамическому стрессу во время беременности. Увеличение объема крови и массы эритроцитов приводит к увеличению преднагрузки. Сердечный выброс увеличивается от 20 до 50%, что связано как с увеличением ЧСС на ≈15-30%, так и с увеличением УО на 15-25%. Сопротивление сосудов снижается на 30%, хотя постнагрузка снова увеличивается к концу беременности. Все эти изменения происходят между первым и вторым триместрами, а у пациенток с уже известной предшествующей органической СН клинические симптомы последней обычно проявляются именно в этот период беременности, поразительно контрастируя с терминами манифестации подавляющего большинства ПКМП.
Миокардит часто выдвигался как причина ПКМП, что в основном обусловлено частым, но вариабельным определением воспалительных инфильтратов в биоптатах эндомиокарда правых отделов. Однако подобные инфильтраты нередко встречаются при биопсии эндомиокарда и у контрольных групп. Например, в одном исследовании у 71% женщин с ПКМП и у 73% контрольных субъектов были обнаружены вирус Коксаки или эховирусная инфекция [12]. Аналогичным образом, в исследовании образцов биопсии эндомиокарда у 26 пациентов с ПКМП с применением полимеразной цепной реакции было продемонстрировано, что показатель распространенности вирусных геномов, часто вызывающих миокардит, составляет 30,7%, но распространенность их была идентична (30,3%) и в контрольной группе. Таким образом, из-за низкой специфичности этих результатов роль миокардита в развитии ПКМП остается неопределенной.
Биопсия правых отделов больше не показана в диагностике ПКМП и редко проводится. Кроме того, недавняя оценка 40 пациенток в исследовании IPAC (Investigations of Pregnancy-Associated Cardiomyopathy) представила данные, свидетельствующее о наличии миокардита только у одной пациентки (неопубликованные данные, Erik B. Schelbert, 2016) [3]. В настоящее время диагностическая ценность МРТ для верификации ПКМП является неопределенной.
Также был предложен ряд других потенциальных причин развития ПКМП. В частности, фетальный микрохимеризм может выступать триггером аутоиммунной реакции после родов.
Кроме того, существовало мнение относительно других особых отягчающих обстоятельств, уникальных для определенных географических районов, таких как различные формы недоедания, включая нехватку железа и селена. Например, недавнее исследование случаев заболевания у 39 пациенток в Нигерии, где частота перипартальной СН непропорционально высока, выявила вдвое более низкий средний уровень селена в сыроватке крови, чем у контрольной группы [28].
Таким образом, до недавнего времени причины ПКМП оставались неясными. Однако недавние работы значительно улучшили наше понимание болезни. Результаты этих исследований выяснили два новых аспекта ПКМП: токсическая роль критически высокого уровня гормонов поздних сроков гестации системы кровоснабжения матери и генетическая основа ПКМП. Эти последние данные обсуждаются ниже.
Сосудисто-гормональная гипотеза. В 2007 году впервые было введено понятие о ПКМП как о сосудистом заболевании, вызванном гормональными изменениями на поздних сроках беременности. Хотя идея предложена давно, экспериментальных данных, свидетельствующих в поддержку этой теории, было недостаточно. В связи с этим была разработана модель ПКМП на мышах, в которой из кардиомиоцитов был генетически удален транскрипционный фактор STAT3. В поддержку развития идеи этой модели говорит тот факт, что у пациенток с терминальной СН, вызванной ПКМП, была снижена экспрессия STAT3 в ЛЖ, по сравнению с контрольными субъектами без СН. Удаление STAT3 в кардиомиоцитах мышей приводит к уменьшению экспрессии генов, которые защищают сердце от реактивных видов оксидов, прежде всего марганцевой супероксиддисмутазы (MnSOD), которая нейтрализует супероксиды, генерируемые сохранной активностью митохондрий при повреждении кардиомиоцитов. Последовательное увеличение количества активных форм оксидов приводит к секреции через еще неясный механизм катепсина D. Эта внеклеточная пептидаза в последующем расщепляет пролактин – гормон, специфичный для поздней беременности, на фрагмент размером 16 кДа, который способствует апоптозу эндотелиальных клеток.
В результате STAT3-индуцированного «нокдауна» миокарда значительное количество клеток на поздних стадиях беременности «выбывает из игры», вызывая, как следствие, обусловленную беременностью ДКМП, то есть ПКМП. Наиболее убедительным аспектом этого исследования, доказывающего ключевую роль пролактина, является блокирование секреции пролактина из гипофиза бромокриптином.
Лечение бромокриптином мышей со STAT3-индуцированным «нокдауном» миокарда полностью меняло наблюдаемую ПКМП. Фрагмент пролактина 16 кДа вызывает повреждение эндотелия и кардиомиоцитов [21]. Исследования показали, что пролактин 16 кДа индуцирует эндотелиальные клетки для «упаковки» микроРНК‑146a (miRNA‑146a) в экзосомы – небольшие инкапсулированные липидные частицы, которые затем секретируются и в последствии поглощаются кардиомиоцитами. Затем miRNA‑146a, поглощенная кардиомиоцитами, подавляет путь нейрегулина/ErbB, тем самым способствуя апоптозу кардиомиоцитов. Поразительно, что циркулирующие уровни miRNA‑146a резко повышаются у женщин с ПКМП. Более того, его уровень значительно снижается при лечении бромокриптином, демонстрируя тем самым, что пролактин приводит к секреции miRNA‑146a. Следовательно, miRNA‑146a может быть полезной в качестве биомаркера ПКМП. Кроме того, miRNA‑146a может стать терапевтической мишенью, поскольку микроРНК можно эффективно и надежно ингибировать клинически. Таким образом, эти данные убедительно показали, что, по крайней мере на модели мышей, перипартальный гормон (пролактин) в сочетании с предрасположенностью (в данном случае отсутствие STAT3 в кардиомиоцитах) вызывают васкулопатию и, следовательно, ПКМП.
Растворимая Fms-подобная тирозинкиназа‑1 (sFlt1). На поздних сроках беременности у плацентарных млекопитающих плацента выделяет в кровообращение матери ингибиторы фактора роста эндотелия сосудов (VEGF), такие как sFlt1. Большинство свободных VEGF в материнском кровообращении нейтрализуются sFlt1 на поздних стадиях беременности. Введения sFlt1 первородящим животным было достаточно для того, чтобы вызвать кардиомиопатию даже при отсутствии беременности. Это доказывает, что sFlt1 является ключевым компонентом состояния тяжести, который вызывает ПКМП у этих животных. Таким образом, sFlt1 и пролактин являются двумя потенциально васкулотоксическими гормонами поздних сроков гестации, которые могут вызвать ПКМП у сенсибилизированных субъектов. Секреция плацентой sFlt1 заметно повышается при ПЭ [38] и беременности, тем самым подвергая сердце матери влиянию значительно более высоких уровней sFlt1, что, вероятно, объясняет сильную эпидемиологическую связь между ПЭ, многоплодной беременностью и ПКМП. Фактически женщины с ПЭ, но без ПКМП, все-таки имеют очевидную субклиническую сердечную дисфункцию на ЭхоКГ [5, 37], и в небольшом исследовании (n=20) показано, что степень дисфункции ЛЖ хорошо коррелирует с уровнями циркулирующей sFlt1 [36]. В исследовании IPAC было продемонстрировано корреляцию повышенного уровня sFlt1 с клиникой СН и неблагоприятным исходом [7]. Небольшое нерандомизированное открытое экспериментальное исследование (n=11), в котором проводилось экстракорпоральное удаление sFlt1 на ранних стадиях развития ПКМП, продемонстрировало многообещающие результаты [46], а одно исследование у женщин с агрессивным течением ПКМП показало лучший темп восстановления сердечной функции у тех, у кого применялся плазмаферез [3]. Вместе эти наблюдения демонстрируют, что sFlt1, секретируемая плацентой на поздних стадиях беременности, оказывает токсическое воздействие на сердце и может индуцировать развитие ПКМП, что вместе с моделью STAT3 подтверждают парадигму того, что ПКМП является сосудистым заболеванием, вызванным гормональным фоном перипартального периода. Понимание этого проливает свет на ряд фактов. Во-первых, это может объяснить, почему ПКМП типично развивается в перипартальный период, когда максимально выражены гормональные изменения, а не гораздо раньше, когда максимально выражены гемодинамические изменения. Во-вторых, роль sFlt1 может объяснить общепринятые эпидемиологические наблюдения о том, что ПКМП тесно ассоциируется с ПЭ и с многоплодными беременностями, обе из которых характеризируются высокой секрецией sFlt1. В-третьих, устранение токсичного влияния гормонального фона после родов может объяснить часто обнаруженное быстрое восстановление функции желудочков у больных с ПКМП, что обычно не наблюдается при других формах ДКМП. Гипотеза о влиянии гормонов также предоставляет клинические, диагностические, прогностические и терапевтические возможности. SFlt1, miRNA‑146a или еще не обнаруженные гормональные факторы могут стать полезными биомаркерами для прогнозирования риска возникновения или течения ПКМП.
Генетический фактор. Важный вопрос в патогенезе ПКМП касается факторов, предрасполагающих к болезни. Одним из них является генетический фон. Против этого свидетельствует то, что ПКМП обычно не является семейным заболеванием и родословные пациентов с ПКМП не пересекаются. Более того, ПКМП часто не повторяется во время повторной беременности, указывая на то, что любая генетическая «поломка», если она существует, не полностью пенетрирующая. Однако некоторые данные подтверждают мнение, что ПКМП может иметь наследственный или генетический компонент. Существуют данные об идентификации однонуклеотидного полиморфизма гена PTHLH как такого, что связан с ПКМП [24], а также о возможности PTHLH регулировать сосудистый гомеостаз [2]. В ходе оценки родословных пациенток с кардиомиопатиями, определенными как ПКМП и ДКМП, в генах, кодирующих миофибриллярные белки, идентифицировали ген, кодирующий саркомерный белок titin [32, 43]. Будут ли найдены схожие варианты относительно спорадической ПКМП, остается неопределенным.
Клиническая картина
Наиболее часто при ПКМП симптомы проявляются после родов, в основном на протяжении первой недели после них [9].
У большинства женщин СН проявляется ортопноэ и пароксизмальной ночной одышкой, что можно спутать с симптомами нормальной, особенно на поздних сроках гестации, беременности. Часто это способствует ошибочному или несвоевременному диагнозу и, соответственно, недооценке частоты ПКМП в популяции. При физикальном осмотре часто фиксируются тахикардия, повышенное яремное венозное давление, хрипы в легких и периферические отеки. Признаки дилатации ЛЖ, включая третий сердечный тон и смещенный верхушечный толчок, не характерны, поскольку ПКМП может возникать даже без увеличения ЛЖ. На ЭКГ обычно регистрируется синусовая тахикардия с неспецифическими изменениями, а при проведении рентгенографии грудной клетки – увеличение сердца и легочный венозный застой.
Дифференциальная диагностика предусматривает исключение легочных причин (например, тромбоэмболии ЛА как следствия состояния гиперкоагуляции в перипартальный период, отека легких при ПЭ) и непосредственно кардиальных причин, включая инфаркт миокарда или кардиомиопатию такоцубо. На ЭхоКГ, которая, как правило, позволяет провести дифференциальную диагностику этих состояний, выявляют дилатацию ЛЖ разной степени выраженности, систолическую дисфункцию ЛЖ, дилатацию ПЖ или обоих предсердий, митральную и трикуспидальную регургитацию и легочную гипертензию.
Лечение и осложнения
Имеются ограниченные данные о подходе к лечению ПКМП, поскольку мы располагаем результатами только двух рандомизированных контролируемых исследований, включивших в общей сложности 44 пациенток [10, 44]. Лечение ПКМП в общем основано на клиническом опыте и экстраполяции данных о лечении других форм систолической СН и сфокусировано на контроле состояния объема, нейтрализации неадаптивных нейрогормональных реакций и предотвращении тромбоэмболических и аритмических осложнений [40]. При использовании мочегонных препаратов необходимо соблюдать осторожность, назначая эти медикаменты перед самими родами во избежание гипотонии и нарушения перфузии матки. Ингибиторы ангиотензинпревращающего фермента (иАПФ) или блокаторы рецепторов ангиотензина ІІ могут использоваться после, но противопоказаны перед родами. Вместо этого в предродовой период может использоваться комбинация органических нитратов и гидралазина. Лечение β-блокаторами (предпочтительно селективными β1-адреноблокаторами), вероятно, безопасно во время беременности и может рассматриваться в качестве медикаментозной терапии. Хотя следует помнить о фетальной брадикардии, а также о возможном развитии синдрома задержки плода на фоне длительного приема препаратов этой группы. Данные исследований новых экспериментальных методов лечения (применение внутривенного иммуноглобулина, пентоксифиллина, левосимендана) до сих пор были противоречивы или отрицательны [3].
Бромокриптин и прекращение грудного вскармливания. В связи с предложенной идеей о возможном влиянии гормона пролактина на развитие ПКМП возникло предположение о целесообразности ингибирования секреции пролактина гипофиза путем прекращения лактации или с помощью бромокриптина. Небольшое рандомизированное одноцентровое исследование по применению бромокриптина у 20 африканских женщин с недавно диагностированной ПКМП показало восстановление ЛЖ через 6 мес (27 против 58%) и снижение частоты развития комбинированных конечных точек. В проспективном наблюдательном реестре в Германии бромокриптин использовался в два раза чаще у женщин с улучшением показателей при проведении ЭхоКГ, чем у тех, кто не принимал данный препарат [22].
Бромокриптин был признан в 1982 году безопасным для плода, но его одобрение на подавление лактации было снято в США в 1995 году в связи с озабоченностью по поводу неблагоприятных сосудистых событий у матерей [3]. Кроме того, нужно учитывать потенциальный вред для новорожденного вследствие подавления лактации, в особенности в развивающихся странах, где недоедание и небезопасное водоснабжение составляют основную часть среди причин детской смертности, что делает в целом необходимым использование грудного молока.
Тромбоэмболия и антикоагуляция. ПКМП ассоциируется с более высокой частой тромбоэмболии, чем другие формы кардиомиопатии [14]. Период беременности сам по себе является состоянием, сопряженным с гиперкоагуляцией [19], что, вероятно, связано с эволюционной адаптацией для минимизации послеродового кровоизлияния (исторически самой распространенной причиной материнской смерти).
Дилатация камер сердца, повреждение эндотелия и малоподвижность дополнительно способствуют коагуляции при ПКМП. В свете наличия высокого риска тромбоэмболии антикоагулянтная терапия рекомендована при ПКМП по крайней мере во время беременности и в первые 2 мес после родов. Применение гепаринов безопасно во время беременности, но использование нефракционированного гепарина предпочтительно из-за более короткого периода полувыведения.
Аритмии и антиаритмическая терапия. Данные о распространенности желудочковых аритмий при ПКМП весьма ограничены. Внезапная кардиальная смерть является наиболее частой причиной смертности, что свидетельствует о высокой распространенности аритмий.
Например, в ретроспективном обзоре 182 пациенток в Калифорнии, США 38% смертельных случаев были обусловлены внезапной кардиальной смертью [18]. В одном из докладов о наблюдении 19 пациенток в Республике Сенегал, которым проводилось 24-часовое холтеровское мониторирование ЭКГ, сообщалось о выявлении опасной желудочковой тахикардии (ЖТ) в 4 случаях [11]. ЖТ может сохраняться, требуя проведения абляции [47]. В ходе ретроспективного анализа случай-контроль у 19 женщин с ПКМП, которым был имплантирован постоянный кардиовертер-дефибриллятор (КВД) для первичной профилактики по сравнению с 60 женщинами контрольной группы с неишемической ДКМП, было сообщено о 37% случаев необходимости применения КВД-терапии в течение 3 лет наблюдения за женщинами с ПКМП и выраженной тенденции к более высокой заболеваемости, чем у женщин с неишемической ДКМП [8]. Однако из-за высокой скорости восстановления при ПКМП агрессивная тактика ранней имплантации постоянного КВД не оправдана. Кроме того, не существует четкой базы данных, основанной на рекомендациях относительно раннего использования временного кардиовертера/дефибриллятора.
Тем не менее целесообразно рассматривать возможность использования временных кардиовертеров/дефибрилляторов у пациентов с ФВ ЛЖ <30%, которые подвержены высокому риску осложнений, включая внезапную смерть, в качестве «моста для выздоровления» или имплантации постоянного КВД при отсутствии восстановления ритма в условиях оптимальной медикаментозной терапии.
Устройства для сердечной помощи. У пациенток с ПКМП может наблюдаться тяжелое снижение функции ЛЖ и, соответственно, быстро прогрессировать ухудшение состояния. В этих случаях следует учитывать возможность применения изотропных средств, внутриаортальных баллонных насосов, вспомогательных левожелудочковых или бивентрикулярных устройств и экстракорпоральной оксигенации [30, 45], что при отсутствии восстановления состояния может служить «мостом для трансплантации» [17].
Превентивная госпитализация. Доступных рекомендаций для принятия решения о сроках и способе госпитализаций не существует. В частности, не существует данных, указывающих на то, что ранняя или выборочная госпитализация по поводу кесарева сечения может улучшить течение ПКМП или улучшить состояние плода. Средний вес при рождении, размер и показатели по шкале Апгар ниже у новорожденных, рожденных женщинами с диагнозом ПКМП, что, вероятно, отражает более ранний гестационный возраст при родах.
Поэтому решения о тактике лечения, времени и способе госпитализации должны приниматься группой кардиологов и акушеров. Ранняя госпитализация должна сопоставляться с рисками для новорожденного и, как правило, предусматриваться в случаях предполагаемого развития опасных для матери или плода состояний.
Трансплантация. Несмотря на часто благоприятные исходы у пациенток с ПКМП, значительная часть больных в конечном итоге нуждаются в трансплантации, нередко с предшествующей механической поддержкой кровообращения (механический ЛЖ), при чем 5% сердечных трансплантаций у женщин в США проводятся по показаниям ПКМП [41]. Исследование, проведенное среди 99 пациенток с ПКМП, получивших механическую поддержку кровообращения в период с 2006 по 2012 год, показало в целом лучшие результаты, чем у 1159 женщин с ПКМП без проведения такой поддержки, но 48% пациенток все-таки была проведена кардиотрансплантация [30].
Прогноз
Прогноз у пациенток с ПКМП улучшился с момента его описания в 1971 году. В недавно завершенном перспективном исследовании IPAC было обследовано 100 женщин, которым проводилась клиническая оценка состояния в течение года, включая повторную ЭхоКГ. Это исследование показало, что 71% женщин выздоровели, ФВ ЛЖ увеличилась до >50%, тогда как только у 13% наблюдались серьезные события или персистирующая кардиомиопатия с ФВ <35% [31].
Смертность
По данным литературы, у женщин негроидной расы смертность выше. Согласно данным IPAC у чернокожих пациенток с более низкой ФВ ЛЖ (31 против 36%) были ниже как средняя ФВ в течение 1 года наблюдения (47 против 56%,), так и темп восстановления, определяемый как ФВ >50% (59 против 77%). В реестре одного из штатов США 7-летняя смертность составляла 24% у пациенток негроидной расы в сравнении с 6% у больных европеоидной расы [23]. Причины различий в результатах неопределенны и могут включать генетические различия (возможно, связанные с более высокой частотой ПКМП в этой популяции), различия в социально-экономических ресурсах, доступе к медицинскому обслуживанию, задержку верификации диагноза и другие факторы. В целом результатов для женщин определенных этнических групп и некоторых географических районов, особенно Африки, недостаточно.
Предикторы восстановления
В дополнение к расовому происхождению и частично независимо от него ФВ ЛЖ при манифестации заболевания лучше всего прогнозирует темпы восстановления. В исследовании IPAC только у одной трети из 27 женщин с ФВ ЛЖ <30% в течение 1 года ФВ ЛЖ была восстановлена до 50%. Сердечно-сосудистые события (смерть, применение искусственного ЛЖ или трансплантация сердца) наблюдались почти исключительно у женщин с ФВ ЛЖ <30% в начале исследования по сравнению с теми, у кого ФВ ЛЖ изначально была ≥30% (82 против 99% выживаемости без событий). Однако важно отметить, что сниженная ФВ не является абсолютным предиктором отсутствия восстановления и, следовательно, не должна быть показанием к преждевременной имплантации устройства для механической поддержки или к трансплантации сердца. Следует подчеркнуть, что более низкие уровни плазменного тропонина или мозгового натрийуретического пептида также были связаны с улучшенными результатами. Однако, как и ФВ ЛЖ, их прогнозирующая точность не достаточна для того, чтобы влиять на клинические решения.
Продолжаются дебаты относительно наличия АГ или ПЭ как предикторов лучшего клинического результата. В общенациональном японском исследовании, в которое были включены 102 женщины, 41% имели АГ во время беременности, наличие которой было независимо связано с более коротким сроком пребывания в стационаре и умеренным улучшением ФВ ЛЖ на протяжении 7 мес (59 против 51%; р<0,05) [26]. С другой стороны, ПЭ или АГ не влияли на улучшение результатов в исследовании IPAC [31]. Таким образом, является ли наличие ПЭ у беременных с ПКМП предиктором улучшения состояния, остается неопределенным.
Рецидив ПКМП и повторная беременность
Вопрос относительно риска рецидива во время второй беременности часто возникает у женщин, у которых была диагностирована ПКМП.
Недавний обширный обзор литературы по этой теме [3], охватывающий 191 повторную беременность, показал, что риск рецидива у пациенток с постоянной дисфункцией ЛЖ (первая группа) перед их повторной беременностью намного выше, чем у тех, у кого функция ЛЖ была восстановлена после первой беременности (вторая группа): 48% пациенток первой группы (n=93) имели значительное ухудшение функции ЛЖ, 16% – умерли, тогда как только у 27% пациенток второй группы наблюдалось ухудшение и не было сообщений о смерти. Таким образом, риск ухудшения, связанный с повторной беременностью при предшествующей ПКМП, является существенным. Лучшим предиктором для рецидива и ухудшения систолической функции является фактически качество восстановления ФВ ЛЖ, но нормализованная функция ЛЖ не гарантирует неосложненную последующую беременность. Поэтому при желании женщины повторно беременеть настоятельно рекомендуется тщательный мониторинг симптомов, функции ЛЖ и уровня мозгового натрийуретического пептида во время и после беременности [15].
Лечение после восстановления
Из-за отсутствия долгосрочных данных о наблюдении женщин с ПКМП остается неясным важный вопрос, касающийся решения о прекращении долгосрочного лечения молодых и здоровых женщин: можно ли считать выздоровление полным после перенесенной ПКМП? В одном из исследований с участием 15 пациенток с полным восстановлением ФВ ЛЖ, которые прекратили прием иАПФ или β-адреноблокаторов, не сообщалось об ухудшении функции ЛЖ на протяжении 2 лет наблюдения [1]. Ограниченные данные, полученные при анализе изображений МРТ, не обнаруживали стойкого повреждения миокарда у женщин с ПКМП [33]. С другой стороны, раннее ЭхоКГ-исследование женщин с восстановленной функцией ЛЖ продемонстрировало снижение сократительного резерва в ответ на применение добутамина [29], что указывает на наличие стойкой субклинической дисфункции. Кроме того, как обсуждалось выше, женщины с восстановленной ФВ ЛЖ остаются пациентками высокого риска рецидива, сопряженного с последующими беременностями.
Совокупно эти данные свидетельствуют о том, что восстановление клеток и молекул может значительно отставать от ЭхоКГ-восстановления. Разумный подход к прекращению приема препаратов у женщин при полном восстановлении функции ЛЖ предполагает наблюдение на протяжении нескольких месяцев после выздоровления функции ЛЖ с последующей отменой лекарств по одному, а также обеспечение тщательного клинического и ЭхоКГ-мониторинга во время процесса отмены медикаментозной терапии, за которым следует ежегодная оценка функции ЛЖ.
Выводы
Резюмируя данные литературы, хотелось бы отметить, что, невзирая на прогресс в понимании самой природы ПКМП, все-таки нет достаточно специфических диагностических и прогностических тестов для данной патологии. Однако большая база накопленных данных дает основания предполагать, что возможность внедрения их в клиническую практику модифицируется в ощутимую пользу для пациенток.
Литература
1. Amos A.M., Jaber W.A., Russell S.D. Improved outcomes in peripartum cardiomyopathy with contemporary. Am. Heart J. 2006; 152: 509-513.
2. Arany Z., Foo S.Y., Ma Y., Ruas J.L., Bommi-Reddy A., Girnun G., Cooper M., Laznik D., Chinsomboon J., Rangwala S.M., Baek K.H., Rosenzweig A., Spiegelman B.M. HIF-independent regulation of VEGF and angiogenesis by the transcriptional coactivator PGC‑1alpha. Nature, 2008; 451: 1008-1012.
3. Arany Z., Elkayam U. Peripartum Cardiomyopathy. Circulation, 2016; 133: 1397-1409.
4. Bello N., Rendon I.S., Arany Z. The relationship between pre-eclampsia and peripartum cardiomyopathy: a systematic review and meta-analysis. J. Am. Coll. Cardiol. 2013; 62: 1715-1723.
5. Hibbard J.U., Lindheimer M., Lang R.M. A modified definition for peripartum cardiomyopathy and prognosis based on echocardiography. Obstet. Gynecol. 1999; 94: 311-316.
6. Brar S.S., Khan S.S., Sandhu G.K., Jorgensen M.B., Parikh N., Hsu J.W., Shen A.Y. Incidence, mortality, and racial differences in peripartum cardiomyopathy. Am. J. Cardiol. 2007; 100: 302-304.
7. Damp J., Givertz M.M., Semigran M., Alharethi R., Ewald G., Felker G.M., Bozkurt B., Boehmer J., Haythe J., Skopicki H., Hanley-Yanez K., Pisarcik J., Halder I., Gorcsan J. 3rd, Rana S., Arany Z., Fett J.D., McNamara D.M.; IPAC Investigators. Relaxin‑2 and Soluble Flt1 Levels in Peripartum Cardiomyopathy: Results of the Multicenter IPAC Study. JACC Heart Fail. 2016 Feb 27.
8. DeBenedetti Zunino M.E., Schuger C., Lahiri M. High rate of ventricular arrhythmias in women with peripartum cardiomyopathy and implanted cardioverter defibrillators. J. Am. Coll. Cardiol. 2014; 63.
9. Demakis J.G., Rahimtoola S.H. Peripartum cardiomyopathy. Circulation, 1971; 44: 964-968.
10. Desplantie O., Tremblay-Gravel M., Avram R., Marquis-Gravel G., Ducharme A., Jolicoeur E.M.; BRO-HF Initiative Investigators. The medical treatment of new-onset peripartum cardiomyopathy: a systematic review of prospective studies. Can. J. Cardiol. 2015; 31: 1421-1426.
11. Diao M., Diop I.B., Kane A., Camara S., Kane A., Sarr M., Ba S.A., Diouf S.M. Electrocardiographic recording of long duration (Holter) of 24 hours during idiopathic cardiomyopathy of the peripartum [in French]. Arch. Mal. Coeur. Vaiss. 2004; 97: 25-30.
12. Cenac A., Gaultier Y., Devillechabrolle A., Moulias R. Enterovirus infection in peripartum cardiomyopathy. Lancet, 1988; 2: 968-969.
13. Chapa J.B., Heiberger H.B., Weinert L., Decara J., Lang R.M., Hibbard J.U. Prognostic value of echocardiography in peripartum cardiomyopathy. Obstet. Gynecol. 2005; 105: 1303-1308.
14. Elkayam U. Clinical characteristics of peripartum cardiomyopathy in the United States: diagnosis, prognosis, and management. J. Am. Coll. Cardiol. 2011; 58: 659-670.
15. Elkayam U. Risk of subsequent pregnancy in women with a history of peripartum cardiomyopathy. J. Am. Coll. Cardiol. 2014; 64: 1629-1636.
16. Fett J.D., Christie L.G., Carraway R.D., Murphy J.G. Five-year prospective study of the incidence and prognosis of peripartum cardiomyopathy at a single institution. Mayo Clin. Proc. 2005; 80: 1602-1606.
17. Gevaert S., Van Belleghem Y., Bouchez S., Herck I., De Somer F., De Block Y., Tromp F., Vandecasteele E., Martens F., De Pauw M. Acute and critically ill peripartum cardiomyopathy and “bridge to” therapeutic options: a single center experience with intra-aortic balloon pump, extra corporeal membrane oxygenation and continuous-flow left ventricular assist devices. Crit. Care, 2011; 15: R93.
18. Goland S., Modi K., Bitar F., Janmohamed M., Mirocha J.M., Czer L.S., Illum S., Hatamizadeh P., Elkayam U. Clinical profile and predictors of complications in peripartum cardiomyopathy. J. Card. Fail. 2009; 15: 645-650.
19. Greer I.A. Clinical practice: pregnancy complicated by venous thrombosis. N. Engl. J. Med. 2015; 373: 540-547.
20. Gunaydin Z.Y., Gurel Y.E., Erdogan G., Kaya A. Peripartum cardiomyopathy associated with triplet pregnancy. Anadolu Kardiyol Derg. 2014; 14: 661-662.
21. Halkein J., Tabruyn S.P., Ricke-Hoch M., Haghikia A., Nguyen N.Q., Scherr M., Castermans K., Malvaux L., Lambert V., Thiry M., Sliwa K., Noel A., Martial J.A., Hilfiker-Kleiner D., Struman I. MicroRNA‑146a is a therapeutic target and biomarker for peripartum cardiomyopathy. J. Clin. Invest. 2013; 123: 2143-2154.
22. Haghikia A., Podewski E., Libhaber E., Labidi S., Fischer D., Roentgen P., Tsikas D., Jordan J., Lichtinghagen R., von Kaisenberg C.S., Struman I., Bovy N., Sliwa K., Bauersachs J., Hilfiker-Kleiner D. Phenotyping and outcome on contemporary management in a German cohort of patients with peripartum cardiomyopathy. Basic Res. Cardiol. 2013; 108: 366.
23. Harper M.A., Meyer R.E., Berg C.J. Peripartum cardiomyopathy: population-based birth prevalence and 7-year mortality. Obstet. Gynecol. 2012; 120: 1013-1019.
24. Horne B.D., Rasmusson K.D., Alharethi R., Budge D., Brunisholz K.D., Metz T., Carlquist J.F., Connolly J.J., Porter T.F., Lappe D.L., Muhlestein J.B., Silver R., Stehlik J,. Park J.J., May H.T., Bair T.L., Anderson J.L., Renlund D.G., Kfoury A.G. Genome-wide significance and replication of the chromosome 12p11.22 locus near the PTHLH gene for peripartum cardiomyopathy. Circ. Cardiovasc. Genet. 2011; 4: 359-366.
25. Isezuo S.A., Abubakar S.A. Epidemiologic profile of peripartum cardiomyopathy in a tertiary care hospital. Ethn. Dis. 2007; 17: 228-233.
26. Kamiya C.A., Kitakaze M., Ishibashi-Ueda H., Nakatani S., Murohara T., Tomoike H., Ikeda T. Different characteristics of peripartum cardiomyopathy between patients complicated with and without hypertensive disorders: results from the Japanese nationwide survey of peripartum cardiomyopathy. Circ. J. 2011; 75: 1975-1981.
27. Kao D.P., Hsich E., Lindenfeld J. Characteristics, adverse events, and racial differences among delivering mothers with peripartum cardiomyopathy. JACC Heart Fail. 2013; 1: 409-416.
28. Karaye K.M., Yahaya I.A., Lindmark K., Henein M.Y. Serum selenium and ceruloplasmin in Nigerians with peripartum cardiomyopathy. Int. J. Mol. Sci. 2015; 16: 7644-7654.
29. Lampert M.B., Weinert L., Hibbard J., Korcarz C., Lindheimer M., Lang R.M. Contractile reserve in patients with peripartum cardiomyopathy and recovered left ventricular function. Am. J. Obstet. Gynecol. 1997; 176 (pt. 1): 189-195.
30. Loyaga-Rendon R.Y., Pamboukian S.V., Tallaj J.A., Acharya D., Cantor R., Starling R.C., Naftel D., Kirklin J. Outcomes of patients with peripartum cardiomyopathy who received mechanical circulatory support: data from the Interagency Registry for Mechanically Assisted Circulatory Support. Circ. Heart Fail. 2014; 7: 300-309.
31. McNamara D.M., Elkayam U., Alharethi R., Damp J., Hsich E., Ewald G., Modi K., Alexis J.D., Ramani G.V., Semigran M.J., Haythe J., Markham D.W., Marek J., Gorcsan J. 3rd, Wu W.C., Lin Y., Halder I., Pisarcik J., Cooper L.T., Fett J.D.; IPAC Investigators. Clinical outcomes for peripartum cardiomyopathy in north america: results of the IPAC Study (Investigations of Pregnancy Associated Cardiomyopathy). J. Am. Coll. Cardiol. 2015; 66: 905-914.
32. Morales A., Painter T., Li R., Siegfried J.D., Li D., Norton N., Hershberger R.E. Rare variant mutations in pregnancy-associated or peripartum cardiomyopathy. Circulation, 2010; 121: 2176-2182.
33. Mouquet F., Lions C., de Groote P., Bouabdallaoui N., Willoteaux S., Dagorn J., Deruelle P., Lamblin N., Bauters C., Beregi J.P. Characterisation of peripartum cardiomyopathy by cardiac magnetic resonance imaging. Eur. Radiol. 2008; 18: 2765-2769.
34. Mielniczuk L.M., Williams K., Davis D.R., Tang A.S., Lemery R., Green M.S., Gollob M.H., Haddad H., Birnie D.H. Frequency of peripartum cardiomyopathy. Am. J. Cardiol. 2006; 97: 1765-1768.
35. Ntobeko B.A., Ntusi N.B., Gumedze F., Sliwa K., Mayosi B.M. Pregnancy-Associated Heart Failure: A Comparison of Clinical Presentation and Outcome between Hypertensive Heart Failure of Pregnancy and Idiopathic Peripartum Cardiomyopathy. PLoS One. Aug 7, 2015; 10 (8): e0133466.
36. Ntusi N.B., Mayosi B.M. Aetiology and risk factors of peripartum cardiomyopathy: a systematic review. Int. J. Cardiol. 2009 Jan 9; 131 (2): 168-79.
37. Patten I.S., Rana S., Shahul S., Rowe G.C., Jang C., Liu L., Hacker M.R., Rhee J.S., Mitchell J., Mahmood F., Hess P., Farrell C., Koulisis N., Khankin E.V., Burke S.D., Tudorache I., Bauersachs J., del Monte F., Hilfiker-Kleiner D., Karumanchi S.A., Arany Z. Cardiac angiogenic imbalance leads to peripartum cardiomyopathy. Nature, 2012; 485: 333-338.
38. Powe C.E., Levine R.J., Karumanchi S.A. Preeclampsia, a disease of the maternal endothelium: the role of antiangiogenic factors and implications for later cardiovascular disease. Circulation, 2011; 123: 2856-2869.
39. Pearson G.D., Veille J.C., Rahimtoola S., Hsia J., Oakley C.M., Hosenpud J.D., Ansari A., Baughman K.L. Peripartum cardiomyopathy: National Heart, Lung, and Blood Institute and Office of Rare Diseases (National Institutes of Health) workshop recommendations and review. JAMA, 2000; 283: 1183-1188.
40. Ponikowski P., Voors A.A., Anker S.D., Bueno H., John G., et al. 2016 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. European Heart Journal, 2016; 37: 2129-2200.
41. Rasmusson K., Brunisholz K., Budge D., Horne B.D., Alharethi R., Folsom J., Connolly J.J., Stehlik J., Kfoury A. Peripartum cardiomyopathy: post-transplant outcomes from the United Network for Organ Sharing Database. J. Heart Lung Transplant. 2012; 31: 180-186.
42. Russell R.B., Petrini J.R., Damus K., Mattison D.R., Schwarz R.H. The changing epidemiology of multiple births in the United States. Obstet. Gynecol. 2003; 101: 129-135.
43. van Spaendonck-Zwarts K.Y., Posafalvi A., van den Berg M.P., Hilfiker-Kleiner D., Bollen I.A., Sliwa K., Alders M., Almomani R., van Langen I.M., van der Mer P., Sinke R.J., van der Velden J., van Veldhuisen D.J., van Tintelen J.P., Jongbloed J.D. Titin gene mutations are common in families with both peripartum cardiomyopathy and dilated cardiomyopathy. Eur. Heart J. 2014; 35: 2165-2173.
44. Sliwa K., Hilfiker-Kleiner D., Petrie M.C., Mebazaa A., Pieske B., Buchmann E., Regitz-Zagrosek V., Schaufelberger M., Tavazzi L., van Veldhuisen D.J., Watkins H., Shah A.J., Seferovic P.M., Elkayam U., Pankuweit S., Papp Z., Mouquet F., McMurray J.J.; Heart Failure Association of the European Society of Cardiology Working Group on Peripartum Cardiomyopathy. Current state of knowledge on aetiology, diagnosis, management, and therapy of peripartum cardiomyopathy: a position statement from the Heart Failure Association of the European Society of Cardiology Working Group on Peripartum Cardiomyopathy. Eur. J. Heart Fail. 2010; 12: 767-778.
45. Su T.W., Tseng Y.H., Wu T.I., Lin P.J., Wu M.Y. Extracorporeal life support in adults with hemodynamic collapse from fulminant cardiomyopathies: the chance of bridging to recovery. ASAIO J. 2014; 60: 664-669.
46. Thadhani R., Hagmann H., Schaarschmidt W., Roth B., Cingoez T., Karumanchi S.A., Wenger J., Lucchesi K.J., Tamez H., Lindner T., Fridman A., Thome U., Kribs A., Danner M., Hamacher S., Mallmann P., Stepan H., Benzing T. Removal of soluble Fms-like tyrosine kinase‑1 by dextran sulfate apheresis in preeclampsia. J. Am. Soc. Nephrol. 2016; 27: 903-913.
47. Tokuda M., Stevenson W.G., Nagashima K., Rubin D.A. Electrophysiological mapping and radiofrequency catheter ablation for ventricular tachycardia in a patient with peripartum cardiomyopathy. J. Cardiovasc. Electrophysiol. 2013; 24: 1299-1301.
Журнал "Серцева недостатність та коморбідні стани" № 3, грудень 2017 р.
СТАТТІ ЗА ТЕМОЮ Кардіологія
Як відомо, кальцій бере участь у низці життєво важливих функцій. Хоча більшість досліджень добавок кальцію фокусувалися переважно на стані кісткової тканини та профілактиці остеопорозу, сприятливий вплив цього мінералу є значно ширшим і включає протидію артеріальній гіпертензії (передусім у осіб молодого віку, вагітних та потомства матерів, які приймали достатню кількість кальцію під час вагітності), профілактику колоректальних аденом, зниження вмісту холестерину тощо (Cormick G., Belizan J.M., 2019)....
Торакалгія – симптом, пов’язаний із захворюваннями хребта. Проте біль у грудній клітці може зустрічатися за багатьох інших захворювань, тому лікарям загальної практики важливо проводити ретельну диференційну діагностику цього патологічного стану та своєчасно визначати, в яких випадках торакалгії необхідна консультація невролога. В березні відбувся семінар «Академія сімейного лікаря. Біль у грудній клітці. Алгоритм дій сімейного лікаря та перенаправлення до профільного спеціаліста». Слово мала завідувачка кафедри неврології Харківського національного медичного університету, доктор медичних наук, професор Олена Леонідівна Товажнянська з доповіддю «Торакалгія. Коли потрібен невролог»....
Рівень ліпопротеїну (a) >50 мг/дл спостерігається в ≈20-25% населення і пов’язаний із підвищеним ризиком серцево-судинних захворювань (ССЗ) [1]. Ліпопротеїн (a) задіяний в атерогенезі та судинному запаленні, а також може відігравати певну роль у тромбозі через антифібринолітичну дію і взаємодію із тромбоцитами [2, 3]. Дієта та фізична активність не впливають на рівень ліпопротеїну (a); специфічної терапії для його зниження також не існує. Підвищений ризик ССЗ, пов’язаний з ліпопротеїном (а), залишається навіть у пацієнтів, які приймають статини [4]. Саме тому існує критична потреба в терапії для зниження цього ризику, особливо в первинній профілактиці. ...
Запалення відіграє важливу роль у розвитку багатьох хронічних захворювань, зокрема атеросклерозу. Нещодавно було встановлено, що гіперурикемія спричиняє запалення ендотеліальних клітин судин, ендотеліальну дисфункцію та, зрештою, атеросклероз. Експериментальна робота Mizuno та співавт. (2019), у якій було продемонстровано здатність фебуксостату пригнічувати запальні цитокіни, привернула увагу дослідників до протизапальних ефектів уратзнижувальних препаратів. Кількість лейкоцитів – надійний маркер запалення, пов’язаний із різними кардіоваскулярними захворюваннями, як-от ішемічна хвороба серця; у багатьох попередніх дослідженнях його використовували для оцінки протизапального ефекту терапевтичного втручання. Мета нового аналізу дослідження PRIZE – вивчити вплив фебуксостату на кількість лейкоцитів у пацієнтів із безсимптомною гіперурикемією....