Мультимодальна аналгезія: альянс хірурга та анестезіолога
За матеріалами конференції
 Навесні цього року відбулася науково-практична конференція «Міждисциплінарний альянс: хірургія та анестезіологія», у рамках якої завідувач науково-дослідного відділення анестезіології та інтенсивної терапії ДНП «Національний інститут раку», доктор медичних наук, професор Іван Іванович Лісний представив доповідь «Мультимодальна аналгезія. Рекомендація з періопераційного знеболення для хірургів чи анестезіологів?», у якій висвітлив ключові моменти ефективного лікування гострого післяопераційного болю.
Навесні цього року відбулася науково-практична конференція «Міждисциплінарний альянс: хірургія та анестезіологія», у рамках якої завідувач науково-дослідного відділення анестезіології та інтенсивної терапії ДНП «Національний інститут раку», доктор медичних наук, професор Іван Іванович Лісний представив доповідь «Мультимодальна аналгезія. Рекомендація з періопераційного знеболення для хірургів чи анестезіологів?», у якій висвітлив ключові моменти ефективного лікування гострого післяопераційного болю.
Ключові слова: мультимодальна аналгезія, нестероїдні протизапальні препарати, декскетопрофен, періопераційне знеболення, гострий біль.
Тема ефективного періопераційного знеболення залишається актуальною до теперішнього часу, адже забезпечення задовільного лікування болю є проблемою для всіх закладів охорони здоров’я (Chang S.H., 2010). Понад 80% пацієнтів після перенесеного хірургічного втручання відчувають гострий післяопераційний біль, і близько 75% із них повідомляють про помірну, тяжку або екстремальну силу болю (Chou R., 2016). Крім того, післяопераційний біль часто недооцінюється лікарями, що спричиняє виникнення короткочасних і віддалених наслідків неефективного лікування (Beverly A., 2017). Тобто проблема ефективного знеболення залишається невирішеною вже понад 20 років із часу анонсування мультимодальної аналгезії (ММА).
Мультимодальна аналгезія: як знайти баланс?
Концепцію ММА запропонував і розпочав утілювати в клінічну практику данський професор хірургії H. Kehlet у 1993 році. На сьогодні численні світові настанови з менеджменту гострого болю базуються на принципах ММА (Sinatra R.S. et al., 2009; Ljungqvist O. et al., 2020; Macintyre P.E. et al., 2021). Чому ж проблема ефективного періопераційного знеболення залишається невирішеною? Як зазначив N. Rawal (2016): «Мультимодальна аналгезія – багато риторики, невтішні докази». На думку O. Mathiesen (2012), реалізація методів ММА у рутинній клінічній практиці виявилася складним завданням. Результати лікування у власній медичній клініці H. Kehlet також були дуже невтішними: 75% пацієнтів отримували опіоїди як терапію першої лінії протягом перших трьох післяопераційних днів, а дози застосовуваних неопіоїдних препаратів були недостатніми. Чітко оцінити якість знеболення було неможливо, оскільки в більшості пацієнтів не проводилася реєстрація оцінки болю.
Тобто для ефективної роботи того чи іншого механізму необхідне чітке дотримання правил його експлуатації. Механізм, або лікувальна схема, ММА включає в себе такі ключові компоненти, як парацетамол, нестероїдні протизапальні препарати (НПЗП), опіоїдні анальгетики, місцеві анестетики та допоміжні лікарські засоби.
У 2006 році група експертів США після огляду даних дійшла висновку, що існує недостатньо доказів щодо переваг будь-яких комбінацій ММА, крім комбінації парацетамолу та НП3П (Rathmell J.P. et al., 2006). J.B. Dahl (2014) не лише дійшов аналогічного висновку, а й зазначив, що у багатьох пацієнтів, які отримували комбінацію різних анальгетиків, значно збільшувався ризик появи побічних ефектів. Спікер зауважив, що хоча післяопераційні методики аналгезії з опіоїд-зберігаючим ефектом мають очевидні переваги у зменшенні побічних ефектів, деякі дослідження припускають, що опіоїдні препарати можуть бути кращими для лікування гострого болю порівняно з неопіоїдною терапією. Тобто доцільність безопіоїдної післяопераційної аналгезії залишається суперечливим питанням і потребує проведення додаткових досліджень.
З точки зору пацієнта, належна профілактика болю є більш привабливим варіантом, ніж його лікування, оскільки дає змогу запобігти розвитку інтенсивного больового синдрому, тоді як лікування останнього означає спочатку відчути дискомфорт від болю, а потім вже отримати полегшення від лікування. Біль під час операції та у післяопераційному періоді – одна з найчастіших подій, які згадують пацієнти, тому адекватна аналгезія є критично необхідною (Domino K.S.,1999). Краще попередити розвиток гострого післяопераційного болю та наслідки неадекватного знеболення.
Відчуття інтенсивності болю може значно різнитися у хворих: тому деякі пацієнти можуть отримувати забагато ліків, а деякі – недостатньо. Таким чином, ММА розпочинається ще до операції, коли важливо оцінити особливості запланованої хірургічної процедури, фактори ризику більш інтенсивного післяопераційного болю, ніж у середньому в конкретного пацієнта, та підібрати індивідуальну схему знеболення.
Парацетамол та НПЗП – оптимальна комбінація
Згідно з рекомендаціями «Acute pain management» (Macintyre P.E. et al., 2021), комбіноване використання парацетамолу та НПЗП забезпечує краще знеболення, ніж кожен препарат окремо. Парацетамол у правильно підібраному дозуванні є ефективним неопіоїдним анальгетиком для лікування гострого болю з мінімальним розвитком побічних ефектів впродовж тривалого часу використання.
Група експертів R. Chou et al. (2016) рекомендують для ефективного знеболення рутинне призначення по годинах неопіоїдних анальгетиків (НП3П, парацетамол) та нефармакологічних технік у режимі ММА. За такої тактики призначення опіоїдних анальгетиків можна взагалі уникнути.
Протокол прискореного відновлення після операції (Enhanced Recovery After Surgery – ERAS) також рекомендує регулярне застосування парацетамолу та НПЗП як частини ММА для періопераційного знеболення (Ljungqvist O. et al., 2020). Професор І.І. Лісний наголосив, що парацетамол вважається наріжним каменем базової превентивної аналгезії й має бути останнім препаратом, який слід відміняти у період відновлення після операції.
Інша велика група препаратів, які призначають як компонент ММА для лікування післяопераційного болю, – це НПЗП, які так само, як і парацетамол, рекомендовані протоколом ERAS (Ljungqvist O. et al., 2020).
Утім спікер зазначив, що НПЗП відрізняються між собою за анальгетичним ефектом, а також за показаннями та протипоказаннями до застосування. Наприклад, кеторолак не застосовують як засіб для премедикації, що підтримує анестезію та аналгезію перед і під час хірургічних вручань, через високий ризик появи кровотечі. Кетопрофен і диклофенак слід з обережністю застосовувати у пацієнтів, які одночасно приймають глюкокортикостероїди, антикоагулянти та антиагреганти у зв’язку з підвищеним ризиком розвитку шлунково-кишкових кровотеч. А застосування парекоксибу натрію протипоказане для лікування больового синдрому у післяопераційному періоді у пацієнтів, які раніше перенесли аортокоронарне шунтування.
Декскетопрофен – безпечний післяопераційний період
Препарат декскетопрофен (Дексалгін®) не збільшує крововтрату під час операції та у ранньому післяопераційному періоді після ортопедичних і великих порожнинних втручань (Cohen A.l. et al., 1997; Miralles F. et al., 2001; Hanna M.H. et al., 2003).
При огляді ефективності різних НПЗП було встановлено, що декскетопрофен викликає достатній рівень аналгезії, що еквівалентний дії інгібіторів ЦОГ‑2 (Hanna M. et al., 2018). Швидкість розвитку його анальгетичного ефекту порівняно з кетопрофеном у 3 рази більша, а порівняно із трамадолом – у 4 рази (Kuemmerle H.P. et al., 1998). У порівняльному аналізі анальгетичної ефективності кетопрофену та декскетопрофену вказано, що останній має сприятливіший профіль безпеки й ефективності (Nagraba L., 2018). До того ж у систематичному огляді A. Moore (2008), присвяченому застосуванню декскетопрофену для лікування як гострого, так і хронічного болю, зазначено, що він був щонайменше настільки ж ефективним, як й інші НПЗП, у тому числі селективні інгібітори ЦОГ-2, та комбінація парацетамолу з опіоїдом, але частота відміни декскетопрофену через розвиток несприятливих ефектів була найменшою порівняно з кетопрофеном і трамадолом.
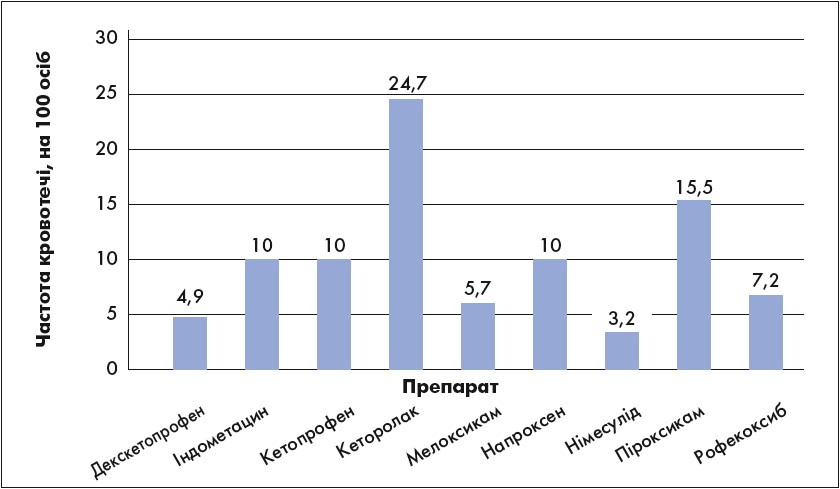
Результати дослідження J.R. Laporte et al. (2004) показали, що декскетопрофен викликає найменше побічних ефектів з боку шлунково-кишкового тракту (рисунок).
Рис. Профіль гастроінтестинальної безпеки деяких НПЗП (Laporte J.R. et al., 2004)
Думки хірургів та анестезіологів щодо передопераційного призначенні НПЗП розходяться з огляду на підвищені ризики посилення інтраопераційної кровотечі. Утім, як показали дослідження, використання декскетопрофену не збільшувало геморагічний ризик через хірургічне втручання, у тому числі при одночасному призначенні з антикоагулянтними препаратами, такими як низькомолекулярні гепарини (Miralles F., 2002).
Місцеві анестетики як безпечне доповнення ефективної аналгезії
Щодо місцевих анестетиків, на думку N. Rawal (2016), вони є одними з найбільш безпечних препаратів для анестезії, проте недостатньо використовуються як важливий компонент ММА.
Ропівакаїн – сучасний місцевий анестетик зі швидким початком дії, що зумовлено його низькою ліпофільністю та спорідненістю зв’язування з екстранейрональними ліпідами і тканинами. При цьому немає необхідності в додаванні адреналіну до розчину ропівакаїну з метою продовження тривалості ефекту при інфільтраційній анестезії. Крім того, ропівакаїн має найнижчий токсичний потенціал для хондроцитів людини, тому може використовуватися в ортопедії (Jacob B., 2019). Кардіо- і нейротоксичність ропівакаїну майже вдвічі менша, ніж бупівакаїну, а реанімація після зупинки серця внаслідок токсичної дії ропівакаїну була значно успішнішою, ніж після бупівакаїну та левобупівакаїну (Guinard J., 1991; Huang Y., 1998).
Отже, успіх сучасної мультимодальної аналгезії полягає в запобіганні больовому синдрому та забезпеченні таких підходів, як опіоїд-зберігаючий, процедуро-специфічний і пацієнт-специфічний (Wick E.C. et al., 2017). Важливо дотримуватися принципу рутинного погодинного призначення парацетамолу і НПЗП (Дексалгін®) з одночасним використанням нефармакологічних технік (Chou et al., 2016). Ефективне післяопераційне знеболення є результатом командної роботи хірургів та анестезіологів.
Підготувала Марія Пригода
Тематичний номер «Хірургія. Ортопедія. Травматологія. Інтенсивна терапія» № 2 (54), 2023 р.
СТАТТІ ЗА ТЕМОЮ Хірургія, ортопедія та анестезіологія
Дисфагія є поширеним явищем у пацієнтів відділення інтенсивної терапії (ВІТ), але вона часто залишається недостатньо розпізнаною та неконтрольованою, незважаючи на те що пов’язана з небезпечними для життя ускладненнями, тривалим перебуванням у ВІТ та госпіталізацією. Запропонований у статті експертний висновок щодо діагностики й лікування дисфагії розроблений на основі доказових клінічних рекомендацій та думок лікарів-практиків. Автори рекомендують прийняти ці клінічні алгоритми для надання стандартизованої та високоякісної допомоги, яка передбачає своєчасний систематичний скринінг, оцінку та лікування дисфагії в екстубованих пацієнтів і пацієнтів із трахеостомою у ВІТ. ...
Больовий синдром при хронічних ранах є рутинним явищем хірургічної практики. Рана вважається такою, що тривало не загоюється, якщо, незважаючи на відповідну терапію та достатній термін лікування (4-6 міс), відсутні або практично відсутні ознаки загоєння. Неопіоїдні та опіоїдні анальгетики є основними препаратами, що застосовуються для лікування больового синдрому при ранах. На науково-практичній конференції «Міждисциплінарний підхід у лікуванні коморбідних хірургічних пацієнтів», що відбулася наприкінці 2023 року, тему менеджменту хронічної ранової хвороби представив у доповіді «Контроль болю в хірургії ран та трофічних дефектів м’яких тканин різної етіології» завідувач кафедри хірургії та судинної хірургії Національного університету охорони здоров’я України ім. П.Л. Шупика (м. Київ), доктор медичних наук, професор Сергій Іванович Саволюк. Ключові слова: ранова хвороба, трофічна виразка, ВАК-терапія, больовий синдром, нестероїдні протизапальні препарати, Дексалгін®....
Актуальність проблеми переломів на сьогодні не залишає сумнівів, зокрема в контексті старіння населення та поширеності остеопорозу. Кальцій та вітамін D, виконуючи ключову роль у формуванні та підтриманні щільності кісткової тканини, є необхідними елементами для успішної профілактики переломів, особливо у вразливих груп населення. Також важливим є достатній рівень кальцію та вітаміну D в організмі для оптимального зрощення переломів і посттравматичної зміни кісток. У цьому контексті велике значення має вибір конкретного комплексу Са + D із позицій ефективності, безпеки та високого комплаєнсу. Ключові слова: остеопороз, крихкість кісток, кальцій, вітамін D, профілактика переломів. ...
З установленням центральних венозних катетерів (ЦВК) пов’язані різноманітні ускладнення, включаючи ті, що зумовлені безпосередньо введенням і/або доступом, через який уводиться катетер, а також віддалені (>1 тижня) ускладнення, такі як дисфункція катетера, стеноз або тромбоз центральної вени та розвиток інфекції. Кількість і тяжкість ускладнень зростають зі збільшенням розміру катетера, кількості використовуваних катетерів та часу їх перебування в організмі. У статті наведено огляд сучасних даних щодо ускладнень, пов’язаних із ЦВК, а також стратегії їх профілактики та лікування. Ключові слова: центральний венозний катетер, ускладнення, пункція артерії, пневмоторакс, тромбоз центральної вени, інфекції кровотоку, дисфункція катетера. ...