Неудачи первой линии таргетной терапии метастатического рака почки. Что дальше?
28 апреля в рамках научно-практической конференции «Достижения и перспективы в онкоурологии, пластической и реконструктивной хирургии мочевыводящих путей» старший научный сотрудник отделения пластической и реконструктивной онкоурологии Национального института рака, кандидат медицинских наук Олег Анатольевич Войленко рассказал о возможностях второй линии таргетной терапии пациентов с метастатическим раком почки. В докладе были представлены результаты основных исследований, современные рекомендации по второй линии терапии пациентов с метастатическим почечноклеточным раком (мПКР), а также перспективные направления лечения таких пациентов.
Он отметил, что, согласно данным Globocan за 2012 г., в мире насчитывалось около 337 тыс. больных ПКР, из них умерло 143 тыс., т.е. 40% от всех заболевших. При этом метастатическая форма заболевания диагностировалась в 30% случаев. По данным многих авторов, после проведенной нефрэктомии по поводу неметастатического рака почки в 30% случаев наблюдается прогрессирование заболевания. Из этого следует, что фактически половине пациентов с ПКР в дальнейшем потребуется проведение таргетной терапии. Выживаемость до года при мПКР составляет всего 36%, а 5-летняя выживаемость – 12%, в большинстве случаев прогрессирование заболевания возникает в течение 3 лет после операции. Лечение пациентов с мПКР требует мультидисциплинарного подхода, дальнейшая тактика, в том числе в отношении таргетной терапии, определяется совместно хирургом и химиотерапевтом.
Согласно рекомендациям NCCN 2016, акситиниб – единственный таргетный препарат второй линии терапии пациентов с мПКР, имеющий категорию I рекомендаций для применения как после прогрессирования на ингибиторах тирозинкиназы (ИТК), так и после цитокинов.
В Украине акситиниб зарегистрирован под торговым названием Инлита®. В случае его неэффективности в третьей и последующих линиях терапии применяются эверолимус, сунитиниб, сорафениб.
Акситиниб – пероральный высокоселективный ингибитор рецепторов VEGFR 1, 2 и 3 (D.D. Hu-Lowe et al., 2008). Было установлено, что акситиниб уменьшает кровоток в опухоли. На протяжении 24 ч после приема акситиниба быстро уменьшается проходимость сосудов, количество кровеносных сосудов и ангиогенез в опухоли (T. Inai et al., 2004). Кроме того, рост опухоли замедляется благодаря снижению проницаемости сосудов (L.J. Wilmes et al., 2007). На фоне терапии этим препаратом на протяжении 7 дней уменьшается количество кровеносных сосудов опухоли, в то же время его отмена приводит к возобновлению роста опухоли (M.R. Mancuso et al., 2006).
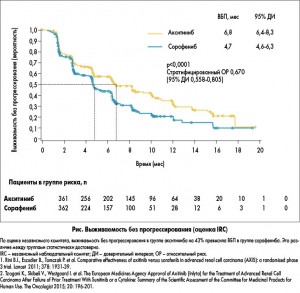
В рандомизированном исследовании AXIS сравнивалась эффективность акситиниба (5 мг 2 р/день) и сорафениба (400 мг 2 раза в день) у пациентов с гистологически подтвержденным мПКР (светлоклеточная форма) при прогрессировании заболевания на фоне первой линии терапии (сунитиниб, бевацизумаб + интерферон-α, темсиролимус, цитокины). Первичной конечной точкой исследования была выживаемость без прогрессирования (ВБП), в исследовании также оценивались общая выживаемость (ОВ), частота общего ответа (ЧОО), длительность ответа (ДО), безопасность и качество жизни. На фоне терапии акситинибом показатель ВБП был выше по сравнению с сорафенибом – 6,8 против 4,7 мес, при более детальном анализе, после стратификации пациентов, практически во всех подгруппах акситиниб также показал свое преимущество (рис.). Согласно данным исследования по критериям RESIST, частичная регрессия наблюдалась в 19 и 9%, стабилизация заболевания – в 49,9 и 54%, прогрессирование – в 21,6 и 21%, промежуточный ответ – в 6,1 и 11,1% случаев в группах акситиниба и сорафениба соответственно. Таким образом, в исследовании AXIS акситиниб показал преимущество над сорафенибом во второй линии терапии пациентов с мПКР в отношении медианы безрецидивной выживаемости (6,8 против 4,7 мес) и частоты объективного ответа (19 против 9%).
Было выявлено, что гипертензия, возникающая на фоне терапии акситинибом, является независимым предиктором увеличения ОВ. В группе пациентов с систолическим артериальным давлением (САД) ≥140 мм рт. ст. ОВ составила 20,7 мес, а с САД <140 мм рт. ст. – 15,7 мес на 8-й неделе после рандомизации и 20,8 против 14,8 мес на 12-й неделе, аналогично при диастолическом артериальном давлении (ДАД) ≥90 мм рт. ст. – 21,3 и 20,7 мес на 8-й и 12-й неделе после рандомизации, по сравнению с 13,9 и 12,9 мес при ДАД <90 мм рт. ст. в группе акситиниба и сорафениба соответственно.
По результатам исследований AXIS и RECORD-1 препараты акситиниб и эверолимус были включены во вторую линию терапии. Поскольку акситиниб продемонстрировал лучшую ВБП (6,8 против 4,9 мес), в дальнейшем все препараты сравнивались с эверолимусом.
В рандомизированном исследовании METEOR кабозантиниб сравнивали с эверолимусом во второй линии терапии у 658 пациентов со светлоклеточным ПКР при прогрессировании заболевания на фоне терапии ингибиторами рецепторов VEGFR. Были получены следующие результаты: ВБП была выше на фоне терапии кабозантинибом после как минимум одного цикла VEGFR-TKІ (9,1 против 3,7 мес), токсичность 3-4 степени наблюдалась как на фоне терапии кабозантинибом (68%), так и на фоне терапии эверолимусом (58%), по результатам исследований кабозантиниб был включен в терапию второй линии пациентов с мПКР (T.K. Choueiri et al., 2015).
Для того чтобы обеспечить максимальный клинический эффект, важно определить необходимую последовательность назначения таргетных препаратов при мПКР. По результатам исследования RECORD‑3, ВБП выше в группе пациентов, принимавших сунитиниб с дальнейшим переходом на эверолимус, по сравнению с пациентами, вначале принимавшими эверолимус (25,8 против 21,1 мес). Таким образом, сунитиниб остался стандартом первой линии терапии (R.J. Motzer et al., 2013).
Одним из перспективных направлений является комбинированная таргетная терапия, в настоящее время проводится ряд исследований по изучению эффективности различных комбинаций таргетных препаратов. Промежуточные результаты исследования JAVELIN 100 показали 100% частичный ответ у пациентов, получающих акситиниб в комбинации с авелумабом в первой линии (Larkin et al., 2016). В исследовании CHEKMATE‑016 комбинированная терапия также демонстрирует высокие показатели ВБП (A. Amin et al., 2014).
Активно изучаются возможности персонализированной терапии. Так, в исследовании IMmotion150 в первой группе пациенты получали атезолизумаб в комбинации с бевацизумабом после терапии атезолизумабом, во второй – после приема сунитиниба, а в третьей изначально пациенты принимали атезолизумаб в комбинации с бевацизумабом. Не было выявлено статистически значимого различия в ВБП между группами в целом, но среди пациентов с экспрессией PD-L1 >1% наблюдалось статистически значимое увеличение медианы ВБП в третьей группе – 5,5, 7,8 и 14,7 мес соответственно (D. McDermont et al., 2017).
Таким образом, эра таргетной терапии позволила достичь новых высот в борьбе с мПКР. В то же время хирургическое лечение продолжает занимать важное место в терапии этого заболевания. На сегодняшний день основной опцией терапии второй линии мПКР в Украине является акситиниб, который демонстрирует высокие показатели ВБП и ОВ.
Дальнейшие разработки, направленные на преодоление механизмов резистентности, позволят улучшить клинические результаты ОВ пациентов. Перспективными направлениями являются комбинированная таргетная терапия и персонализированная терапия. Изучение новых агентов, направленных на звено иммунного ответа, а также их комбинаций, персонализированный подбор препаратов на основании изучения антигенного статуса опухоли позволят улучшить показатели выживаемости пациентов с мПКР.
Подготовила Екатерина Марушко
Напечатано при поддержке Представительства «Пфайзер Эйч.Си.Пи. Корпорейшн» в Украине».
WUKINL0317005
СТАТТІ ЗА ТЕМОЮ Онкологія та гематологія
Гостра лімфобластна лейкемія (ГЛЛ) є найпоширенішим онкогематологічним захворюванням у дітей і складає значну частку серед лейкемій у дорослих. Незважаючи на значні успіхи в лікуванні ГЛЛ у дітей, де рівень виліковності сягає 90%, результати терапії у дорослих залишаються незадовільними. У рамках науково-практичної конференції з міжнародною участю «Діагностика та лікування гематологічних захворювань: підведення підсумків 2023 року» (15-16 грудня 2023 року) проведено секцію, присвячену ГЛЛ....
Хронічна лімфоцитарна лейкемія (ХЛЛ) залишається актуальною проблемою сучасної онкогематології. Незважаючи на певні досягнення в терапії, ХЛЛ є невиліковним захворюванням. Стандартна хіміотерапія не забезпечує стійкої відповіді, а трансплантація гемопоетичних стовбурових клітин можлива лише для окремої когорти пацієнтів. Тому пошук нових підходів до терапії ХЛЛ, зокрема таргетної, є нагальним завданням. ...
Гепатоцелюлярна карцинома (ГЦК) – злоякісне новоутворення в печінці, що розвивається з гепатоцитів. Рання діагностика і початок лікування пацієнтів із ГЦК запобігає виникненню тяжких ускладнень і покращує якість життя пацієнтів. Медична допомога пацієнтам із ГЦК потребує міждисциплінарної співпраці та інтегрованого ведення хворих мультидисциплінарною командою фахівців, яка займається або спеціалізується на злоякісних новоутвореннях печінки. Саме цьому сприятимуть положення Стандарту медичної допомоги «Гепатоцелюлярна карцинома»....
Традиційно січень є місяцем обізнаності про рак шийки матки (РШМ) – однієї з найпоширеніших патологій у структурі онкогінекологічних захворювань. Протягом цього місяця світ забарвлюється в палітру бірюзового та білого з метою привернення уваги громадськості до проблеми РШМ. ...