13 квітня, 2026
Ензимотерапія у профілактиці післяопераційних ускладнень при хірургічній корекції пролапсу тазових органів
 Післяопераційний запальний каскад із мікротромбозом, фібриновою депозицією та порушенням мікроциркуляції є ключовим механізмом розвитку ускладнень і рецидиву після хірургічної корекції пролапсу тазових органів (ПТО). Стандартна антибактеріальна терапія не усуває мікроциркуляторну блокаду і не запобігає надлишковому фіброзуванню та виникненню ерозій, інфільтратів й абсцесів. Комплекс дістрепт-ферментів Н46А стрептокінази та стрептодорнази діє безпосередньо на ці механізми: лізує мікротромби і фібринові депозити, відновлює тканинну перфузію, ліквідує матрикс мікробних біоплівок та інфільтрати, ексудати, гнійні скупчення. Клінічні дані підтверджують скорочення термінів больового синдрому, зменшення частоти ускладнень і зниження ризику спайкоутворення, ерозій та пролапсу алотрансплантатів, що обґрунтовує включення ензимотерапії до протоколу післяопераційного ведення пацієнтів, які підлягають хірургічному лікуванню ПТО.
Післяопераційний запальний каскад із мікротромбозом, фібриновою депозицією та порушенням мікроциркуляції є ключовим механізмом розвитку ускладнень і рецидиву після хірургічної корекції пролапсу тазових органів (ПТО). Стандартна антибактеріальна терапія не усуває мікроциркуляторну блокаду і не запобігає надлишковому фіброзуванню та виникненню ерозій, інфільтратів й абсцесів. Комплекс дістрепт-ферментів Н46А стрептокінази та стрептодорнази діє безпосередньо на ці механізми: лізує мікротромби і фібринові депозити, відновлює тканинну перфузію, ліквідує матрикс мікробних біоплівок та інфільтрати, ексудати, гнійні скупчення. Клінічні дані підтверджують скорочення термінів больового синдрому, зменшення частоти ускладнень і зниження ризику спайкоутворення, ерозій та пролапсу алотрансплантатів, що обґрунтовує включення ензимотерапії до протоколу післяопераційного ведення пацієнтів, які підлягають хірургічному лікуванню ПТО.
Ключові слова: пролапс тазових органів, післяопераційні ускладнення, спайкоутворення, фібринові депозити, мікротромбоз, ерозії, ензимотерапія, дістрепт-ферменти Н46А, стрептокіназа, стрептодорназа, Дістрептаза® Дістрепт.
ПТО – одна з найпоширеніших гінекологічних патологій, що суттєво знижує якість життя жінок репродуктивного і клімактеричного віку [1]. Хірургічне лікування ПТО спрямоване на відновлення дефектних тканин та анатомії й, відповідно, функції м’язів тазового дна [2]. Однак результат операції визначається не лише її технічною досконалістю, а й якістю післяопераційного ведення – насамперед ефективним контролем запальної реакції та профілактикою спайкоутворення.
Арсенал операційних технік при ПТО охоплює вагінальні, лапароскопічні й абдомінальні доступи, вибір між якими залежить від типу та ступеня пролапсу, супутньої патології, а також репродуктивних планів пацієнтки [2].
Систематичний огляд Maher et al. (Cochrane, 22 рандомізованих контрольованих дослідження, n=2368) дозволив систематизувати порівняльну ефективність різних хірургічних втручань [3]. Так, абдомінальна сакрокольпопексія має менший відсоток рецидивів порівняно з вагінальною сакроспінальною фіксацією – за показником рецидиву пролапсу склепіння піхви (відносний ризик [ВР] 0,23) і частотою диспареунії (ВР 0,39), – проте пов’язана з тривалішим часом втручання та вищою вартістю [3]. При дефектах передньої стінки піхви застосування поліпропіленової сітки знижує ризик анатомічного рецидиву (ВР 1,39-2,72). Незалежно від обраної техніки приблизно у 10% жінок після операції виникають дизуричні симптоми [3], що вказує на необхідність комплексного післяопераційного супроводу та мінімізації запальних ускладнень.
Для стандартизованого визначення ступеня пролапсу у сучасній практиці застосовується система POP-Q (Pelvic Organ Prolapse Quantification), що дозволяє об’єктивно оцінити вираженість опущення відносно гіменального кільця і є обов’язковою при плануванні хірургічного втручання. Важливу роль у виборі операційного доступу відіграє і передопераційний фенотип пролапсу: за даними Lowder et al. (2024), фенотипова характеристика анатомічного пролапсу корелює з хірургічним результатом при мінімально інвазивній сакрокольпопексії та може бути використана при плануванні операції й консультуванні пацієнтки [4].
Будь-яке хірургічне втручання на органах малого таза неминуче запускає локальну запальну реакцію [5]. Ушкодження тканин активує коагуляційний каскад, зумовлює ексудацію та формування мікротромбів у капілярному руслі операційної зони. Фібрин, що відкладається в тканинах і просвіті дрібних судин, обмежує місцевий кровотік і порушує доставку кисню, антибіотиків та імунокомпетентних клітин до рани [6, 7].
Персистування ішемії разом із накопиченням продуктів клітинного розпаду створює умови для хронізації запалення, гнійно-септичних інфільтратів та – у довгостроковій перспективі – спайкового процесу, що деформує підтримувальні структури й підвищує ризик рецидиву пролапсу [7]. Особливу роль у розвитку післяопераційних ускладнень відіграють мікротромби судин навколо операційної рани: вони не лише порушують мікроциркуляцію, а й унеможливлюють проникнення у вогнище запалення лімфоцитів, макрофагів, фагоцитів і лікарських засобів для боротьби з інфекцією [7]. Саме тому ліквідація мікротромбозу та відновлення адекватної тканинної перфузії є принципово важливим завданням ранньої післяопераційної терапії.
Ензимотерапія в гінекологічній хірургії: механізм дії та патогенетичне обґрунтування
Дістрептаза® Дістрепт – комбінований ферментний препарат у формі ректальних супозиторіїв, що містить дістрепт-ферменти Н46А – стрептокіназу 15 000 МО і стрептодорназу 1250 МО. Стрептокіназа активує плазміноген до плазміну – ключового ферменту фібринолізу, – забезпечуючи розчинення тромбів і фібринових депозитів у тканинах, зумовлюючи тим самим фібринолітичний ефект. Відновлення мікроциркуляції підвищує оксигенацію й покращує локальну концентрацію антибіотиків і фагоцитів [6]. Стрептодорназа чинить протеолітичну дію: деполімеризує позаклітинну ДНК загиблих клітин і руйнує нуклеопротеїни продуктів розпаду, мертвих клітин або гною, не ушкоджуючи при цьому інтактні тканини [6]. Синергічна дія обох компонентів забезпечує ефективну ліквідацію вогнища запалення, прискорює загоєння та запобігає надлишковому фіброзуванню [8].
Препарат офіційно показаний при хронічному запаленні придатків матки, післяопераційних та інфільтративних змінах, а саме при спайковій хворобі після операцій на органах малого таза, що безпосередньо відповідає клінічній ситуації після корекції ПТО [6]. Станом на 25 лютого 2026 року Дістрептаза® Дістрепт включена до переліку оригінальних (інноваційних) лікарських засобів, зареєстрованих в Україні (відповідно до Постанови Кабінету Міністрів України № 439 від 04.04.2025 р.), та є єдиним препаратом на фармацевтичному ринку України з доведеними показаннями до лікування гінекологічної патології у складі зі стрептокіназою 15 000 МО та стрептодорназою 1250 МО [9] (рис. 1).
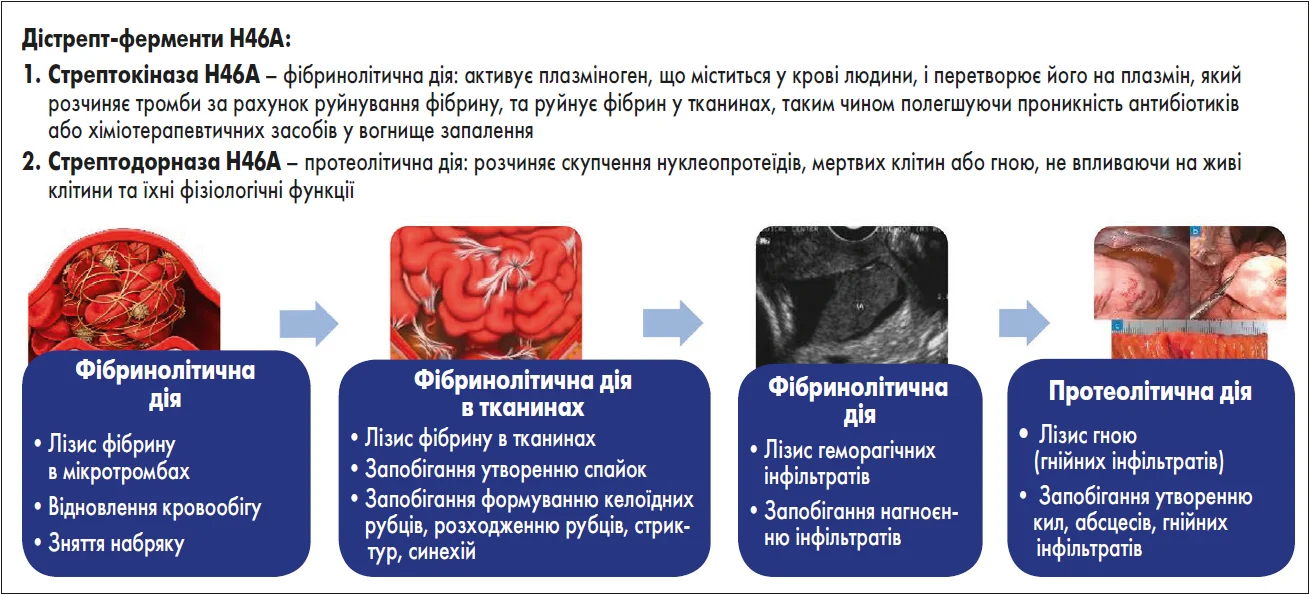 Рис. 1. Фармакологічна дія Дістрептаза® Дістрепт
Рис. 1. Фармакологічна дія Дістрептаза® Дістрепт
І.П. Коркан та співавт. (2012) провели порівняльне дослідження за участю 68 пацієнток, оперованих із приводу ПТО в умовах сімейних і міських медичних центрів [7]. Основна група (n=22) додатково до стандартної антибактеріальної терапії отримувала Дістрептаза® Дістрепт ректально за схемою: по 1 супозиторію 3 рази на добу протягом перших 3 днів; по 1 супозиторію 2 рази на добу протягом наступних 3 днів; по 1 супозиторію 1 раз на добу протягом ще 3 наступних днів. Контрольна група (n=18) отримувала лише антибіотики.
Результати основної групи виявилися достовірно кращими за всіма клінічними критеріями: біль після операції зник через 2,00±0,92 доби проти 5,00±0,33 доби в контрольній групі (рис. 2а), тривалість антибактеріальної терапії скоротилася до 2,44±0,11 доби проти 4,00±0,50 доби, лейкоцитарний індекс інтоксикації нормалізувався швидше (1,76±0,22 доби проти 2,32±0,76 доби), а ліжко-день становив 2,43±0,43 проти 5,11±0,43. Принципово важливо, що у групі Дістрептаза® Дістрепт не було зафіксовано жодного післяопераційного ускладнення, тоді як у групі контролю їх кількість склала один-два випадки (рис. 2б). Автори наголошують, що препарат сприяє прискоренню приживлення сітчастих протезів і знижує ризик їх інфікування, а відтак, кількість післяопераційних ускладнень і рецидивів (рис. 3).
![Рис. 2. Порівняння результатів лікування досліджуваних груп за часом зникнення болю (а) та частотою ускладнень (б) (за Коркан І.П., 2012) [7] Рис. 2. Порівняння результатів лікування досліджуваних груп за часом зникнення болю (а) та частотою ускладнень (б) (за Коркан І.П., 2012) [7]](/multimedia/userfiles/images/2026/Akush_1_2026/Akush_1_2026_st17_pic2.webp) Рис. 2. Порівняння результатів лікування досліджуваних груп за часом зникнення болю (а) та частотою ускладнень (б) (за Коркан І.П., 2012) [7]
Рис. 2. Порівняння результатів лікування досліджуваних груп за часом зникнення болю (а) та частотою ускладнень (б) (за Коркан І.П., 2012) [7]
Рис. 3. Ключові результати в післяопераційному періоді при лікуванні ПТО лікарським засобом Дістрептаза® Дістрепт [7]
Ефективність у суміжних гінекологічних ситуаціях
Доказова база для застосування Дістрептаза® Дістрепт у гінекологічній хірургії формується також у дослідженнях із суміжними клінічними сценаріями. Т.Ф. Татарчук та співавт. (2018) включили до дослідження 67 жінок постменопаузального віку після гістероскопічної поліпектомії (І група, n=35 – Дістрептаза® Дістрепт + стандартна терапія; ІІ група, n=32 – стандартна терапія) [6].
Больовий синдром вираженістю ≥3 бали за вербальною шкалою (0-10) виявлявся достовірно рідше у І групі: 2,85% проти 18,75% (р<0,05), а середній показник болю склав 1,63±0,42 бала проти 4,63±0,32 бала відповідно (рис. 4). Частота гематометри також була суттєво нижчою: 2,85% проти 12,5% [6].
![Рис. 4. Частота виявлення больового синдрому в досліджуваних групах (р<0,05) [6] Рис. 4. Частота виявлення больового синдрому в досліджуваних групах (р<0,05) [6]](/multimedia/userfiles/images/2026/Akush_1_2026/Akush_1_2026_st17_pic4.webp) Рис. 4. Частота виявлення больового синдрому в досліджуваних групах (р<0,05) [6]
Рис. 4. Частота виявлення больового синдрому в досліджуваних групах (р<0,05) [6]
У дослідженні Л.В. Калугіної та співавт. (2020) (І група, n=33 – Дістрептаза® Дістрепт + стандартна терапія; ІІ група, n=32 – стандартна терапія) у пацієнток з ускладненим хронічним сальпінгоофоритом і гідросальпінксом інтенсивність больового синдрому за візуально-аналоговою шкалою (ВАШ) до 10-ї доби лікування знизилася до 0,9±0,24 бала в І групі проти 2,9±0,29 бала у ІІ групі (рис. 5) [8].
![Рис. 5. Динаміка оцінки больового синдрому за ВАШ у досліджуваних групах на фоні лікування [8] Рис. 5. Динаміка оцінки больового синдрому за ВАШ у досліджуваних групах на фоні лікування [8]](/multimedia/userfiles/images/2026/Akush_1_2026/Akush_1_2026_st17_pic5.webp) Рис. 5. Динаміка оцінки больового синдрому за ВАШ у досліджуваних групах на фоні лікування [8]
Рис. 5. Динаміка оцінки больового синдрому за ВАШ у досліджуваних групах на фоні лікування [8]
Крім того, за даними ультразвукового дослідження через місяць після терапії в групі 1 достовірно рідше реєструвалися ехографічні маркери спайкового процесу: зміщення матки відносно середньої осі (27,27% проти 40,63%), атипове розміщення яєчників (15,15% проти 31,25%) і гіперехогенні включення у стромі яєчника (21,21% проти 31,25%) [8].
Дослідження S.B. Burxonova (2023) після ендохірургічних втручань на придатках матки зафіксувало зниження ймовірності спайкоутворення у 2,1 раза: частота виникнення спайок після операцій на маткових трубах склала 5% у групі Дістрептаза® Дістрепт проти 30% у групі контролю, після кістектомії – 7,5% проти 35% (рис. 6) [10].
Дослідження Sadlocha et al. (2024) продемонструвало достовірне зниження медіани болю при хронічному тазовому болю з 5 до 3 балів зі збереженням ефекту через місяць після завершення терапії; 24% пацієнток повністю відмовилися від знеболювальних, а 72% – оцінили результат як задовільний або відмінний [11].
![Рис. 6. Частота спайкоутворення у жінок, які перенесли ендохірургічні операції [10] Рис. 6. Частота спайкоутворення у жінок, які перенесли ендохірургічні операції [10]](/multimedia/userfiles/images/2026/Akush_1_2026/Akush_1_2026_st17_pic6.webp) Рис. 6. Частота спайкоутворення у жінок, які перенесли ендохірургічні операції [10]
Рис. 6. Частота спайкоутворення у жінок, які перенесли ендохірургічні операції [10]
Нові можливості: ензимотерапія та ендометріальна рецептивність
Показово, що терапевтичний потенціал дістрепт-ферментів стрептокінази та стрептодорнази виходить за межі профілактики спайок і поширюється на відновлення функції ендометрія, що є особливо актуальним у пацієнток репродуктивного віку після реконструктивних операцій на тазових органах.
У своєму дослідженні L. Phaladze (Інститут репродуктології ім. проф. Жорданії та проф. Хомасурідзе, Тбілісі) вивчала вплив ензимотерапії на стан ендометрія у 23 пацієнток 21-35 років із тонким ендометрієм і порушеннями репродуктивної функції, а також верифікованим хронічним ендометритом [12]. Група Б (n=11) отримувала дістрепт-ферменти Н46А стрептокіназу/ стрептодорназу з 6-го по 13-й день циклу в поєднанні з низькими дозами аспірину, вітаміном Е і дидрогестероном; група А (контрольна, n=12) – лише стандартну терапію. Після лікування товщина ендометрія у групі Б збільшилася з 5,86 до 7,28 мм проти 5,76-6,39 мм у групі контролю; різниця була статистично значущою на користь ензимотерапії [12].
Патогенетичне пояснення ефекту полягає в антибіоплівковій активності дістрепт-ферменту Н46А стрептодорнази, оскільки фібрин є структурним «каркасом» мікробних біоплівок, руйнування якого відновлює нормальне мікроциркуляторне забезпечення ендометрія, а також у здатності стрептокінази ліквідовувати фіброз і покращувати васкуляризацію [9]. Ці дані свідчать про те, що ензимотерапія може відігравати роль не лише у профілактиці запальних ускладнень, а й у структурно-функціональній реабілітації тазових органів після хірургічних втручань.
Практичний алгоритм застосування
На підставі наявних клінічних даних, оптимальний алгоритм застосування комплексу Дістрептаза® Дістрепт після хірургічної корекції ПТО передбачає початок терапії в ранньому післяопераційному періоді за схемою: по 1 супозиторію 3 рази на добу протягом перших 3 днів; по 1 супозиторію 2 рази на добу протягом наступних 3 днів; по 1 супозиторію 1 раз на добу протягом ще 3 наступних днів [7]. Ректальна форма є оптимальною для концентрації ферментів у параректальній і паравагінальній клітковині – основних зонах операційної травми при вагінальних і комбінованих доступах. Включення препарату до стандартного протоколу дозволяє прискорити ліквідацію запалення, скоротити курс антибактеріальної терапії, запобігти спайкоутворенню в ділянці фіксуючого апарата й навколо сітчастого матеріалу, а також мінімізувати ризик хронізації больового синдрому, виникнення ерозій, інфікування та рецидиву пролапсу. Відсутність значущих побічних ефектів, підтверджена в усіх розглянутих дослідженнях, робить Дістрептаза® Дістрепт безпечним вибором у пацієнток цієї категорії [7-10].
Отже, хірургічна корекція ПТО є ефективним, але патофізіологічно складним втручанням, результат якого суттєво залежить від якості післяопераційного ведення. Запальний каскад, мікроциркуляторні порушення та фібрино-утворення в зоні операції є ключовими детермінантами післяопераційних ускладнень і довгострокового рецидиву. Комбінований ферментний препарат Дістрептаза® Дістрепт завдяки подвійному – фібринолітичному та протеолітичному – механізму дії є патогенетично обґрунтованим для включення до протоколу ведення пацієнток після реконструктивних втручань на тазових органах.
Список літератури – у редакції.
Тематичний номер «Акушерство. Гінекологія. Репродуктологія» № 1 (67) 2026 р.



 Андрієць А.В.
Андрієць А.В.
![Рис. 3. Ключові результати в післяопераційному періоді при лікуванні ПТО лікарським засобом Дістрептаза® Дістрепт [7] Рис. 3. Ключові результати в післяопераційному періоді при лікуванні ПТО лікарським засобом Дістрептаза® Дістрепт [7]](/multimedia/userfiles/images/2026/Akush_1_2026/Akush_1_2026_st17_pic3.webp)
