18 липня, 2018
Выживаемость пациентов и прогностические факторы в первой линии таргетной терапии распространенной почечноклеточной карциномы в клинической практике
Анализ базы данных SEER-Medicare
Почечноклеточная карцинома (ПКК) составляет 80-85% первичных новообразований почек, метастатическая ПКК (мПКК) при первичном обследовании выявляется в 25-33% случаев. Цитокиновая терапия была стандартом лечения распространенной ПКК (рПКК) в 1990-х гг. Несмотря на то что полная ремиссия достигала 6-8%, применение этого метода лечения ограничивалось переносимостью цитокинов. За последние два десятилетия благодаря усовершенствованию терапевтических и диагностических возможностей удвоилась 5-летняя выживаемость пациентов с ПКК, что привело к снижению их смертности. В частности, таргетная терапия ингибиторами тирозинкиназы рецептора фактора роста эндотелия сосудов (ИТК VEGFR) и ингибиторами мишени рапамицина млекопитающих (mTOR) значительно увеличила общую выживаемость (ОВ) пациентов с рПКК.
Потребность в альтернативных методах лечения резистентной к цитокину ПКК привела к одобрению Управлением по контролю качества пищевых продуктов и лекарственных препаратов (FDA) США в 2005 г. первого препарата таргетной терапии – ИТК VEGFR сорафениба.
В 2006 г. был одобрен ИТК VEGFR сунитиниб, а в 2007 г. – ингибитор mTOR темсиролимус. Вторая волна инноваций в таргетной терапии началась в 2009 г. с одобрения ингибитора mTOR эверолимуса, гуманизированного анти-VEGF-моноклонального антитела бевацизумаба и ИТК VEGFR пазопаниба. Акситиниб, селективный ингибитор VEGFR, был одобрен в 2011 г. С момента появления таргетной терапии медиана ОВ пациентов с мПКК увеличилась с 10 до 20 мес, однако дальнейшая тенденция к увеличению ОВ, обусловленная внедрением новых целевых методов лечения, изучена недостаточно.
Прогностические факторы, связанные с более длительной ОВ, претерпели некоторые изменения с момента принятия парадигмы лечения, ориентированной на таргетную терапию. Некоторые основные прогностические модели, такие как шкала оценки симптомов MSKCC, которые были разработаны в эру цитокинотерапии, в настоящее время используются при принятии решений по лечению ПКК и могут быть полезны в эру таргетной терапии.
Ретроспективное исследование OВ среди пациентов с рПКК, в котором использовалась база данных эпиднадзора, эпидемиологии и конечных результатов (SEER) за 2013 г., показало значительное увеличение ОВ при применении таргетной терапии (2005-2008 гг.; 20 мес) по сравнению с цитокиновой (2000-2003 гг.; 15 мес), тогда как возраст >65 лет, негроидная раса и отсутствие нефрэктомии были определены как плохие прогностические факторы. Аналогичным образом исследование 2016 г. с использованием базы данных SEER за период с 2000 по 2010 г. показало, что у пациентов с ПКК, диагностированной в эру таргетной терапии (2006-2010 гг.), показатели 1- и 3-летней ОВ были лучше по сравнению с пациентами, у которых ПКК была обнаружена в эру цитокиновой терапии (2000-2005 гг.).
Однако это исследование не оценивало прогностических факторов ОВ. Таким образом, есть необходимость в определении факторов, связанных с пациентом, болезнью и проводимым лечением, которые могут повлиять на исходы в эру таргетной терапии, в частности ИТК VEGFR.
Чтобы оценить, существует ли тенденция к увеличению ОВ, и определить прогностические факторы, влияющие на ОВ у пациентов с ПКК в клинической практике, был проведен анализ базы данных SEER относительно первой линии лечения в раннюю и позднюю эру таргетной терапии. В этом исследовании оценивались результаты лечения пациентов с рПКК, начавших прием таргетных препаратов и получавших пособие по программе Medicare part D, связанной с базой данных SEER-Medicare, что позволило дополнить результаты предыдущих исследований. Улучшение выживаемости объясняется эволюцией стандартов лечения от иммунотерапии (например, интерлейкин‑2 и интерферон-альфа – ИФН-α) и высокотоксичных таргетных агентов до препаратов с большей эффективностью и более низкой токсичностью. Несмотря на то что в метаанализе исследований применения ИФН-α, проведенном в 2002 г., медиана ОВ составила около 13 мес, медиана ОВ на фоне таргетной терапии может быть увеличена в 2 раза, причем данные о 5-летней выживаемости уже не редкость.
В текущем анализе оценивалась ОВ на фоне таргетной терапии рПКК с большей степенью детализации путем деления периода на раннюю (2006-2009) и позднюю (2010-2012) эру таргетной терапии. В общей сложности 604 пациента и 641 пациент с рПКК начали лечение целевыми агентами в первой линии в период 2006-2009 и 2010-2012 гг. соответственно. Согласно полученным результатам медиана ОВ была значительно выше в позднюю эру таргетной терапии, что может быть связано с более широким арсеналом терапевтических возможностей у лечащих врачей.
Разработка прогностических моделей в эру таргетной терапии имеет большое значение, поскольку многие из существующих моделей (например, MSKCC и IMDC) были разработаны для оценки лечения рПКК цитокинами. Наиболее широко используемая модель стратификации риска по критериям MSKCC была разработана благодаря данным большой когорты пациентов с мПКК, участвовавших в клинических исследованиях и получавших ИФН-α. Факторы включают: интервал от постановки диагноза до начала лечения <1 года; статус по шкале Карновского <80%; высокий уровень лактатдегидрогеназы в сыворотке (в 1,5 раза больше верхней границы нормы); высокий уровень скорректированного кальция в сыворотке (>10 мг/дл); снижение уровня гемоглобина; предшествующую лучевую терапию и наличие >1 метастаза. Неблагоприятные прогностические факторы для ОВ в модели IMDC включают анемию, тромбоцитоз, нейтрофилию, статус по шкале Карновского <80% и время от постановки диагноза до начала таргетной терапии <1 года. Эффективность модели IMDC была подтверждена в популяции пациентов с мПКК, получавших последующую таргетную терапию после прогрессирования на фоне первой линии лечения. Сообщалось также, что у пациентов с проведенной циторедуктивной нефрэктомией ОВ была выше; проведение нефрэктомии улучшает ОВ у пациентов с наличием <4 прогностических факторов IMDC.
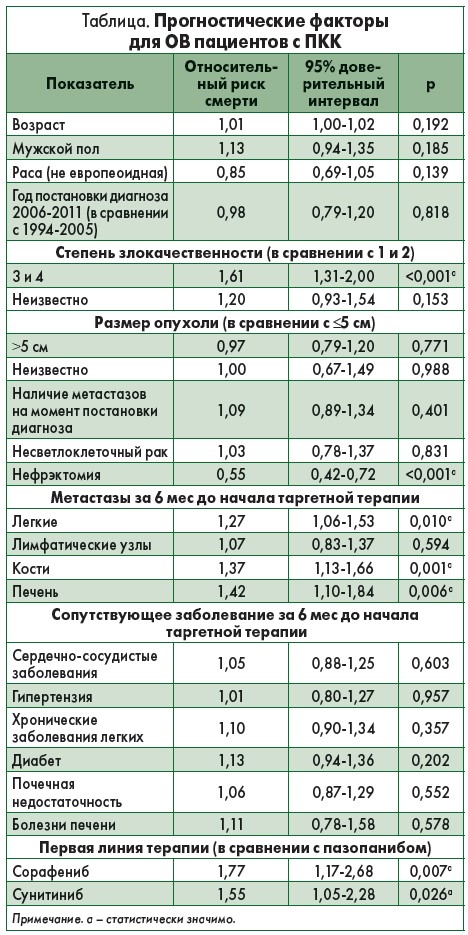 В текущем анализе прогностических факторов более низкая ОВ среди пациентов с рПКК, получавших таргетную терапию, была связана с более высокой злокачественностью опухоли и наличием метастазов в легких, костной ткани и печени (табл.). Эти данные согласуются с результатами нескольких других исследований, проведенных в эру цитокиновой терапии. Определение гистологической степени злокачественности играет важную роль среди прогностических факторов ПКК, наиболее широко используется классификация по Фурману. Также более длительная ОВ была связана с предшествующей нефрэктомией, что ранее подтверждалось в двух рандомизированных исследованиях у пациентов, получавших цитокины. В 2002 г. в системе подсчета MSKCC пункт «проведение нефрэктомии» был заменен на «время от постановки диагноза до начала терапии». Ввиду разработки новых терапевтических опций и режимов для рПКК заслуживает внимания пересмотр текущих прогностических факторов.
В текущем анализе прогностических факторов более низкая ОВ среди пациентов с рПКК, получавших таргетную терапию, была связана с более высокой злокачественностью опухоли и наличием метастазов в легких, костной ткани и печени (табл.). Эти данные согласуются с результатами нескольких других исследований, проведенных в эру цитокиновой терапии. Определение гистологической степени злокачественности играет важную роль среди прогностических факторов ПКК, наиболее широко используется классификация по Фурману. Также более длительная ОВ была связана с предшествующей нефрэктомией, что ранее подтверждалось в двух рандомизированных исследованиях у пациентов, получавших цитокины. В 2002 г. в системе подсчета MSKCC пункт «проведение нефрэктомии» был заменен на «время от постановки диагноза до начала терапии». Ввиду разработки новых терапевтических опций и режимов для рПКК заслуживает внимания пересмотр текущих прогностических факторов.
В рандомизированном клиническом исследовании III фазы COMPARZ сравнивались безопасность и эффективность пазопаниба и сунитиниба в первой линии таргетной терапии. В этом исследовании были отмечены сходные результаты ОВ и выживаемости без прогрессирования (ВБП) для двух терапевтических агентов. Пазопаниб ассоциировался с меньшим количеством побочных эффектов и улучшением качества жизни. Аналогичные результаты были получены в исследовании PISCES, в котором оценивали предпочтения среди пациентов с мПКК, получавших пазопаниб и сунитиниб, и в специальном анализе бессимптомного периода в исследовании COMPARZ. Также отмечалась более длительная ОВ и ВБП на фоне терапии пазопанибом по сравнению с сунитинибом среди пациентов с низким риском по критериям MSKCC. Ретроспективный медицинский обзор данных пациентов с мПКК и ≥3 прогностическими факторами MSKCC, проведенный в одном из медицинских центров, определил, что у пациентов, получавших пазопаниб, ОВ и ВБП были в 2 раза больше, чем у тех, кто получал сунитиниб. Несмотря на результаты ретроспективных исследований, предполагающие увеличение выживаемости на фоне пазопаниба, данные свидетельствуют о сохранении эквивалентности терапии пазопанибом и сунитинибом. Преимущество пазопаниба над сунитинибом, наблюдаемое в этом исследовании, может быть связано с тем, что врачи не участвовали в клинических исследованиях. Исходы пациентов могут отличаться в условиях реальной клинической практики и при проведении клинических исследований. В клинической практике пазопаниб действительно может обеспечить более длительную выживаемость из-за его более предсказуемого и управляемого профиля токсичности.
В дальнейших исследованиях оправданно использование альтернативных источников данных, таких как Национальная база данных о раке, проспективные мультиинституциональные реестры и другие базы данных (например, база данных Medicare), для дальнейшей оценки полученных результатов. Хотя в этом анализе основное внимание уделялось таргетным препаратам, одобренным в первой линии терапии, дополнительные исследования позволят расширить анализ благодаря изучению эффективности целевых агентов, которые могут использоваться в первой линии (темсиролимус и акситиниб), а также изучению последующих линий терапии. В это исследование не были включены пациенты с более агрессивной формой ПКК – саркоматоидной карциномой, хотя это позволило бы оценить ОВ у таких пациентов. В настоящее время продолжаются проспективные рандомизированные исследования CARMENA и SURTIME, призванные определить влияние циторедуктивной нефрэктомии на ОВ у пациентов с ПКК, получающих сунитиниб. Результаты этих исследований могут дать ценную информацию об этом терапевтическом подходе.
Согласно анализу базы данных SEER-Medicare ОВ на фоне таргетной терапии рПКК в клинической практике существенно увеличилась. Опухоли с более высокой степенью злокачественности, а также наличие метастазов в легких, костях и печени значительно сокращают продолжительность ОВ. И наоборот, предшествующая нефрэктомия и применение пазопаниба в первой линии терапии по сравнению с сунитинибом или сорафенибом связаны с более длительной ОВ. Эти данные свидетельствуют о прогрессе в лечении рПКК и позволяют выделить прогностические факторы при проведении первой линии терапии.
Адаптированный перевод
Pal S.K., Ghate S.R., Li Nanxin. Real-World Survival Outcomes
and Prognostic Factors Among Patients Receiving First Targeted Therapy for Advanced Renal Cell Carcinoma: A SEER-Medicare Database Analysis. Clinical Genitourinary Cancer, Vol. 15, № 4, 2017: e573-82.
Подготовила Екатерина Марушко
Тематичний номер «Урологія. Нефрологія. Андрологія» № 2 (13), червень 2018 р.




