31 березня, 2016
Актуальные аспекты фармакоэкономики таргетной терапии почечноклеточного рака
Почечноклеточный рак (ПКР) является наиболее распространенным онкологическим заболеванием, поражающим почки. Примерно 92% всех случаев злокачественных опухолей почки приходится на ПКР. В структуре общей онкологической заболеваемости он составлял 4% всех случаев онкологических заболеваний; согласно статистике, в 2014 году было выявлено 63 920 новых случаев этого заболевания и 13 680 связанных с ним летальных исходов.
Продвижение в понимании биологических и генетических особенностей ПКР привело к появлению новых подходов к лечению этого заболевания, основанных на таргетной терапии. Наличие нескольких возможных вариантов первой линии таргетной терапии ПКР обусловило необходимость анализа их экономической эффективности. Оценка расходов на здравоохранение особенно актуальна в связи со сложившейся экономической ситуацией и неуклонным ростом затрат, наблюдающимся в последние десятилетия.
Как известно, ПКР не реагирует на химиотерапию. Поэтому распространенные стадии заболевания традиционно считаются трудными для лечения, что обусловлено их устойчивостью к цитотоксической химиотерапии, облучению или гормональной терапии. До появления препаратов – ингибиторов ангиогенеза интерферон альфа (ИФН-α) и интерлейкин-2 (ИЛ-2) являлись основой терапии распространенного ПКР, несмотря на их значительную токсичность и ограниченную эффективность. Так, ИФН-α при недостаточной эффективности обладает одновременно значительным спектром побочных эффектов.
Прогресс в понимании молекулярной биологии опухоли позволил идентифицировать конкретные молекулярные мишени, на которые можно воздействовать при ПКР, в том числе фактор роста эндотелия сосудов (VEGF), тромбоцитарный фактор роста (PDGF) и мишень рапамицина млекопитающих (mTOR). Результатом этих открытий стало появление нескольких таргетных препаратов (сорафениб, сунитиниб, бевацизумаб (применяется в сочетании с ИФН-α), темсиролимус и эверолимус) и существенное улучшение результатов лечения пациентов с ПКР. Пазопаниб, инновационный ингибитор тирозинкиназ, который воздействует на VEGF, PDGF и рецептор стволовых клеток c-Kit, – последний из препаратов, получивших одобрение для применения в первой линии терапии распространенного ПКР. Сегодня метастатический ПКР относится к группе опухолей, для которых единственным стандартом лечения является таргетная терапия.
Пазопаниб, сунитиниб и бевацизумаб (в сочетании с ИФН-a) представлены в современных клинических руководствах и рекомендованы к применению в терапии первой линии распространенного ПКР у больных с благоприятным прогнозом и промежуточным риском.
В 2013 году было проведено исследование экономической эффективности разных режимов таргетной терапии при ПКР. Изучалась экономическая эффективность пазопаниба в сравнении с наилучшей поддерживающей терапией, ИФН-a и сунитинибом в терапии первой линии распространенного/метастатического ПКР. Исследование проводилось Национальным институтом здравоохранения и клинического совершенствования Великобритании (National Institute for Health and Care Excellence, NICE). Учитывались данные клинической эффективности, а также профиль безопасности и возможные последствия развития побочных эффектов лечения. Рентабельность терапии пазопанибом оценивалась у пациентов, ранее не получавших лечение. Дизайн исследования подразумевал сравнение пазопаниба с ИФН-α, сунитинибом и наилучшей поддерживающей терапией.
По информации производителя, модель исследования была описана как «разделенная выживаемость» (partitioned survival) и характеризовалась тремя взаимоисключающими состояниями: выживаемость до прогрессирования, выживаемость после прогрессирования и смерть. Разница между этой моделью и моделью Маркова состояла в том, что при ее использовании рассчитывалась доля пациентов в каждой группе в любое время от начала лечения с использованием параметрических кривых выживаемости, установленных на основе эмпирических данных, касающихся общей выживаемости (ОВ) и выживаемости без прогрессирования (ВБП). Отношение рисков (ОР) для ВБП и ОВ было получено из исследования VEG 105192 (National Institute for Health and Clinical Excellence. Renal cell carcinoma (first line metastatic): pazopanib. London: NICE; 2011).
Поскольку прямое сравнение пазопаниба с другими препаратами не проводилось на момент исследования NICE, необходимо было, как указано выше, оценить ОР для ВБП и ОВ для ИФН-a в сравнении с плацебо или наилучшей поддерживающей терапией у больных, ранее не получавших лечение, а затем и объединить их с оценкой ОР для ВБП и ОВ в группе пазопаниба в сравнении с плацебо или наилучшей поддерживающей терапией. Это позволило произвести косвенную оценку ВБП и ОВ для пазопаниба против ИФН-α. Производителем также проведено косвенное сравнение пазопаниба с сунитинибом и ИФН-α.
На основании представленной работы, в которой учитывалась скидка в стоимости на пазопаниб (в размере 12,5% в Великобритании), было сделано заключение, что расходы на терапию сунитинибом превысили таковые для пазопаниба и ИФН-α. С позиций фармакоэкономического анализа определялся показатель качества жизни, приведенный к адекватной продолжительности жизни QALY (quality-abjusted life-year). Дополнительные расходы по QALY для пазопаниба против ИФН-α составили 38 925. Показатели не сильно изменились по результатам одновариантного детерминированного анализа чувствительности, проведенного изготовителем, но парный вероятностный анализ чувствительности позволил предположить заданное пороговое значение в размере 30 000, 54%-ную вероятность того, что пазопаниб предпочли сунитинибу, 40%-ную вероятность для ИФН-α и 47%-ную вероятность для наилучшей базисной терапии.
В ходе окончательного анализа, выполненного аналитической группой NICE с использованием модели производителя и с учетом скидки 12,5% на стоимость пазопаниба в Великобритании, было установлено, что последний более экономически эффективен, чем сунитиниб, и имеет соотношение затрат и результатов от 1790 до 5330 по QALY. Учитывая пороговое значение эффективности затрат в размере 30 000, выявлена 54%-ная вероятность того, что пазопаниб предпочли сунитинибу. Тем не менее результаты сравнения NICE базировались на косвенном сравнении результатов лечения, полученных в исследованиях, где пазопаниб сравнивался с плацебо, ИФН-α с плацебо и сунитиниб – с ИФН-α.
Анализу фармакоэкономических показателей применения пазопаниба или сунитиниба у больных с распространенным ПКР было посвящено испанское исследование (G. Villa and L. Hernandez-Pastor, BMC Cancer 2013, 13:399). По мнению исследователей, нет опубликованных фармакоэкономических доказательств, свидетельствующих в пользу выбора одного из видов лечения в качестве первой линии терапии распространенного ПКР. Многие исследователи стремятся разработать популяционную модель, способную спрогнозировать количество новых случаев распространенного ПКР, которая может быть использована при принятии медицинских решений. Целью исследователей было использовать такую модель для анализа влияния на бюджет (т. е. финансовых последствий выбора той или иной интервенции) использования в клинической практике пазопаниба в сравнении с сунитинибом, который сегодня является стандартом первой линии терапии распространенного ПКР во всем мире.
По мнению авторов исследования, в Испании пока нет общепризнанных методов прогнозирования новых случаев распространенного ПКР. Поэтому была разработана зависящая от времени популяционная модель на основе модели Маркова для прогнозирования заболеваемости распространенными формами ПКР в будущем. Эта модель была использована для изучения бюджета, связанного с ведением в клиническую практику пазопаниба в сравнении с сунитинибом. Модель точно соответствует GLOBOCAN и содержит данные о распространенности ПКР в Испании. Подтверждено, что она является надежным инструментом прогнозирования распространенности метастатического ПКР в будущем на основе показателей заболеваемости ПКР. Выполненный анализ подтвердил чувствительность модели. Даже если эта модель включает в себя конкретные параметры, присущие Испании (например, показатели заболеваемости и популяционные показатели), параметры конкретных заболеваний, такие как процент пациентов с прогрессирующим заболеванием на момент постановки диагноза и вероятностью рецидива, были получены из наиболее достоверных доступных источников и не зависят от конкретной страны. Поэтому предложенная модель может быть легко перенесена на другие параметры посредством простой замены испанских демографических данных (общедоступных из национальной статистики) и показателей заболеваемости ПКР (доступных из GLOBOCAN) по конкретной стране.
Согласно этому исследованию, использование пазопаниба способствовало значительной экономии бюджета испанской системы здравоохранения вследствие снижения расходов на сам препарат и сокращения затрат, связанных с управлением побочными эффектами. По результатам исследования COMPARZ, некоторые побочные эффекты развиваются с большей частотой на фоне терапии сунитинибом (например, тромбоцитопения, анемия и нейтропения), в то время как другие чаще проявляются на фоне терапии пазопанибом (например, повышение активности печеночных ферментов). Для учета таких различий исследователи включили в анализ все затраты, связанные с управлением побочными эффектами от обоих препаратов.
Несмотря на развитие усталости и ладонно-подошвенный синдром, распространенные среди пациентов с ПКР, эти побочные эффекты не связаны со значительным увеличением использования ресурсов здравоохранения или дорогостоящих сопутствующих препаратов. Таким образом, в ходе текущего анализа было установлено, что эти побочные эффекты имели ограниченное влияние на расходы, связанные с терапией. В итоге было сделано заключение, что использование пазопаниба способствует экономии затрат на здравоохранение в Испании вследствие снижения цены и расходов, связанных с коррекцией побочных эффектов.
Следует отметить, что исследование NICE имеет определенные ограничения. В первую очередь это исследование, сравнивающее только пазопаниб и сунитиниб и не оценивающее экономическую эффективность других методов лечения, которые могут использоваться в качестве первой линии терапии распространенного или метастатического ПКР в США. При оценке фармакоэкономических показателей применения пазопаниба или сунитиниба в первой линии терапии больных с ПКР в США (T. Delea, J. Amdahl, J. Diaz et al., J Manag Care Pharm. 2015; 21(1): 46-54) использовались данные эффективности лечения (в том числе ОВ и ВБП) из исследования COMPARZ, данные экономической эффективности из исследования PISCES, а также опубликованные сметы расходов.
Экономическая эффективность по QALY составила $100 000, показатель чистой экономической выгоды (Net Monetary Benefit, NMB) пазопаниба в сравнении с сунитинибом был оценен в $15 857. Вероятностный анализ чувствительности показал, что пазопаниб с вероятностью ≥90% более рентабелен по сравнению с сунитинибом для пороговых значений рентабельности между $10 000 и 160 000 по QALY. Во всех сценариях, отработанных в ходе детерминированного анализа чувствительности, показатель NMB для пазопаниба при его сравнении с сунитинибом всегда был в пользу пазопаниба.
Сопоставление этих препаратов потребовало бы косвенного сравнения вариантов лечения, представляющего собой более низкий уровень доказательности, чем прямое сравнение пазопаниба с сунитинибом в исследовании COMPARZ, положенном в основу обсуждаемой оценки. Вероятные преимущества пазопаниба были получены из предполагаемых различий в эффективности затрат, понесенных пациентами из группы пазопаниба по сравнению с пациентами из группы сунитиниба (рис. 1).
Рис. 1. Чувствительный анализ фармакоэкономической эффективности пазопаниба vs сунитиниба
Поскольку исследование COMPARZ не включало оценку качества жизни, связанного со здоровьем (HRQoL), в аналитической модели были использованы результаты исследования PISCES. Данные, полученные в ходе исследования PISCES, представляют собой результаты оценки качества жизни (по шкале EQ-5D), достигаемого на фоне терапии пазопанибом и сунитинибом в клинических испытаниях. Из-за дизайна исследования, способа получения данных и различий в добавочной стоимости для пазопаниба и сунитиниба данные, используемые в этом анализе, не были основаны на рандомизированном сравнении.
Тем не менее оценка преимущества пазопаниба в отношении качества жизни в предлагаемой модели согласуется с другими результатами исследований PISCES и COMPARZ в отношении предпочтений пациента и HRQoL. Различия в побочных эффектах между группами лечения в исследовании PISCES согласовывались с данными исследования COMPARZ, подтверждая мнение, что показатели добавочной стоимости из исследования PISCES, вероятно, отражают те, которые были бы получены из исследования COMPARZ, если бы были собраны такие данные.
Рассчитанная в ходе этого анализа экономия затрат, полученная вследствие применения терапии пазопанибом, обусловлена в основном предполагаемой более низкой стоимостью пазопаниба по сравнению с сунитинибом, а также снижением ежемесячных расходов на другие услуги, связанные с лечением распространенного ПКР в исследовании COMPARZ. Фактические цены, устанавливаемые на каждый из препаратов, могут существенно отличаться у разных поставщиков и в разных системах здравоохранения (даже в пределах США) и не соответствовать тем, которые используются в представленном анализе. Поскольку исследование COMPARZ было многонациональным, его результаты не могут отражать экономические аспекты в любых условиях (J Manag Care Pharm. 2015; 21(1): 46-54).
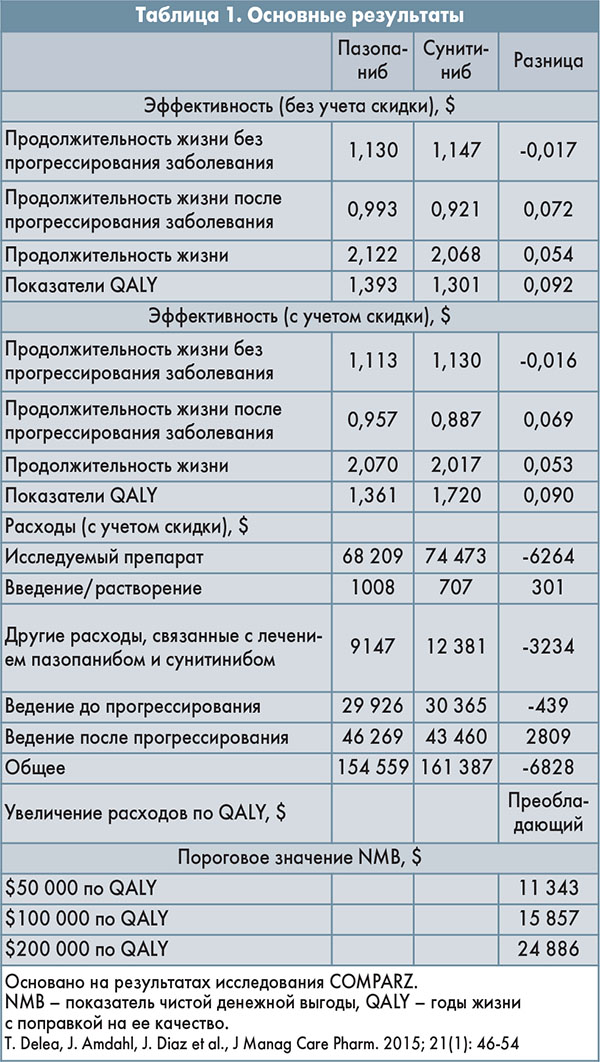
Результаты этого анализа эффективности затрат, в котором использовались данные двух рандомизированных клинических исследований III фазы, позволили предположить, что пазопаниб является экономически более эффективным вариантом лечения по сравнению с сунитинибом в качестве терапии первой линии у пациентов с метастатическим ПКР именно в США (табл. 1).
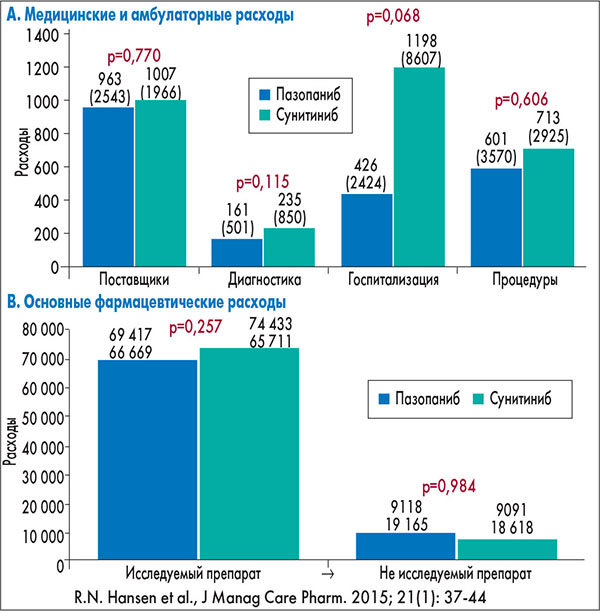
 Другое фармакоэкономическое исследование включало оценку эффективного расходования средств здравоохранения на лечение пациентов с ПКР с учетом терапии побочных эффектов (R.N. Hansen et al., J Manag Care Pharm. 2015; 21(1): 37-44). Основной целью исследования было сравнение общих затрат ресурсов здравоохранения, необходимых на лечение пациентов с распространенным ПКР, получавших в первой линии терапию пазопанибом или сунитинибом в ходе исследования COMPARZ. Вторая цель заключалась в сравнении суммарных затрат на коррекцию побочных эффектов в той же популяции пациентов. Общие затраты ресурсов здравоохранения включали составляющие контрактов поставщиков, затраты на диагностику, госпитализацию, процедуры, а также исследуемые и другие препараты.
Другое фармакоэкономическое исследование включало оценку эффективного расходования средств здравоохранения на лечение пациентов с ПКР с учетом терапии побочных эффектов (R.N. Hansen et al., J Manag Care Pharm. 2015; 21(1): 37-44). Основной целью исследования было сравнение общих затрат ресурсов здравоохранения, необходимых на лечение пациентов с распространенным ПКР, получавших в первой линии терапию пазопанибом или сунитинибом в ходе исследования COMPARZ. Вторая цель заключалась в сравнении суммарных затрат на коррекцию побочных эффектов в той же популяции пациентов. Общие затраты ресурсов здравоохранения включали составляющие контрактов поставщиков, затраты на диагностику, госпитализацию, процедуры, а также исследуемые и другие препараты.
Пациенты были разделены по критерию наличия или отсутствия побочных эффектов для оценки связанных с ними расходов. Расходы оценивались в долларах США (2013 год). По 1% пациентов, с которыми были связаны наибольшие расходы на лечение, были одинаково исключены из каждой группы. Для оценки результатов использовался одновариантный и многовариантный анализ.
В общей сложности затраты оценивались для 906 пациентов (пазопаниб, n=454; сунитиниб, n=452); более высокие показатели наблюдались на фоне терапии сунитинибом. Анализ нескорректированных затрат показал, что в среднем общие затраты у пациентов, получавших лечение пазопанибом, были на 8% ниже, чем у пациентов, использовавших сунитиниб ($80 464 против 86 886; р=0,20) (табл. 2).
Согласно результатам этого анализа, расходы на лечение небольшого количества пациентов (по 4 пациента в каждой группе) достигли экстремальных показателей в обеих группах исследования. В группе пазопаниба затраты на лечение 1% пациентов составили $320 871 при средней стоимости лечения в размере $4639. В группе сунитиниба затраты 1% пациентов составили $203 014 при средней стоимости лечения в размере $7281.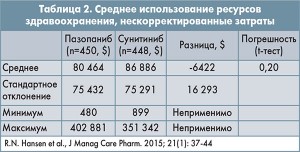
В итоге средние суммарные нескорректированные затраты (± стандартное отклонение) для пациентов, получавших лечение пазопанибом (n=450), составили $80 464±$75 432 по сравнению с $86 886±$75 291) для пациентов, получавших лечение сунитинибом (n=448). Разница в затратах составила $6422 (р=0,20), или 8%. Чтобы оценить отдельные компоненты затрат и выяснить происхождение разницы между затратами, была проведена серия из шести t-тестов. Различия в расходах на госпитализацию (на $772 выше на фоне терапии сунитинибом; р=0,068; 2А) и на сам препарат (на $5016 выше на фоне терапии сунитинибом; р=0,257; 2В) составили основную разницу между затратами в двух группах. За исключением затрат, не связанных с исследуемым препаратом, расходы на лечение были меньшими на фоне терапии пазопанибом по сравнению с сунитинибом. В целом расходы на терапию были на $12 543 ниже для группы пазопаниба ($143 585; 95% ДИ=$97 353-$148 005) по сравнению с группой сунитиниба ($156 128; 95% ДИ=$105 128-$157 231), и эта разница была статистически значимой (р=0,003) (рис. 2).
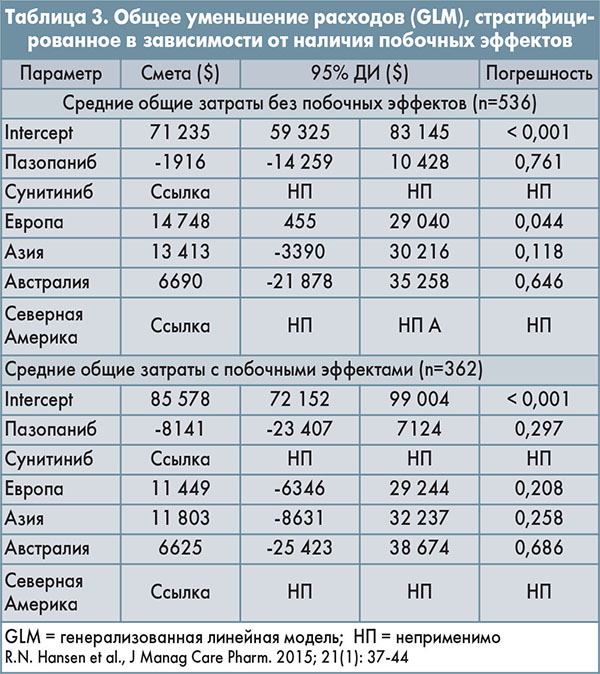
У пациентов, которые перенесли по крайней мере один побочный эффект 3-й или 4-й степени тяжести, расходы увеличились на $8118 на фоне терапии пазопанибом и на $14 343 – на фоне терапии сунитинибом. Речь идет о пациентах с поздними стадиями ПКР, получивших лечение первой линии в системе здравоохранения США. Частота посещений отделений лучевой терапии или скорой помощи была достоверно выше для пациентов, получавших сунитиниб, по сравнению с теми, кто лечился пазопанибом. Средний уровень общих нескорректированных затрат был на 8% выше для сунитиниба по сравнению с пазопанибом (р=0,20) по данным t-теста, и разница была признана достоверно большей для сунитиниба по сравнению с пазопанибом ($12 543). Кроме того, по данным многовариантных анализов, общие затраты ресурсов здравоохранения на пациентов, использовавших пазопаниб, были меньше, чем на пациентов, получавших терапию сунитинибом (табл. 3).
Финансовые затраты являются значимым фактором, влияющим на принятие решений о лечении. Было проведено несколько исследований, касающихся системы здравоохранения США и посвященных анализу затрат на онкологические процедуры. В целом были выявлены различия в затратах на лечение распространенного ПКР с использованием таргетных препаратов. Они обусловлены разной частотой развития сопутствующих побочных эффектов и использованием ресурсов здравоохранения для их коррекции.
Максимально детализированная информация, включающая стоимость медикаментозного лечения, расходы на коррекцию побочных эффектов и общий уровень затрат ресурсов здравоохранения, поможет принимать обоснованные решения при выборе терапии распространенного ПКР. Клиническое исследование COMPARZ дало возможность оценить, подсчитать и проанализировать общие затраты ресурсов здравоохранения и расходы на лечение побочных эффектов у больных с распространенным ПКР, получавших в первой линии пазопаниб или сунитиниб.
Результаты этого исследования показывают, что при одинаковой клинической эффективности сунитиниба и пазопаниба затраты ресурсов здравоохранения и расходы, связанные с коррекцией побочных эффектов, ниже среди пациентов, получавших терапию пазопанибом. Чтобы установить, транслируются ли эти результаты на клиническую практику, проявляясь в реальном уменьшении затрат при лечении пазопанибом, будущие исследования должны напрямую фиксировать и оценивать затраты на лечение пациентов при применении конкретных препаратов за пределами клинических испытаний.
Подготовила Катерина Котенко