12 червня, 2016
Гиперпролактинемия как междисциплинарная проблема: от причин к последствиям

В рамках Всеукраинской образовательной программы «Врач XXI столетия. Практическое применение достижений в медицине» состоялся межрегиональный научно-практический симпозиум, посвященный рассмотрению клинических аспектов такой сложной и интересной междисциплинарной проблемы, как гиперпролактинемия (ГПРЛ). Изучение вопроса повышенного уровня пролактина (ПРЛ), его причин и последствий началось еще в начале XIX в. и не прекращается по сей день, что свидетельствует о важнейшей клинической роли данного гормонального нарушения в течении целого ряда патологических состояний. Проведение симпозиума, в котором приняли участие специалисты из 5 городов Украины (Киев, Одесса, Харьков, Львов, Днепропетровск), стало возможным благодаря поддержке Министерства здравоохранения Украины, ГУ «Институт педиатрии, акушерства и гинекологии НАМН Украины», Ассоциации акушеров-гинекологов Украины, Украинской федерации гражданских организаций содействия здравоохранению гражданского общества, а также ведущей мировой фармацевтической компании Pfizer, выступившей в роли генерального спонсора. Программа симпозиума напрямую перекликалась с названием Всеукраинской образовательной программы, поскольку современные знания и практический опыт, полученные участниками данного мероприятия, несомненно, станут доказательством высокого профессионализма врачей XXI столетия.
 Работу симпозиума торжественно открыла заместитель директора по научной работе, заведующая отделением эндокринной гинекологии ГУ «Институт педиатрии, акушерства и гинекологии НАМН Украины», член-корреспондент НАМН Украины, доктор медицинских наук, профессор Татьяна Феофановна Татарчук. В своем докладе она подробно рассмотрела причины и последствия ГПРЛ, а также роль ПРЛ в процессах адаптации и дезадаптации.
Работу симпозиума торжественно открыла заместитель директора по научной работе, заведующая отделением эндокринной гинекологии ГУ «Институт педиатрии, акушерства и гинекологии НАМН Украины», член-корреспондент НАМН Украины, доктор медицинских наук, профессор Татьяна Феофановна Татарчук. В своем докладе она подробно рассмотрела причины и последствия ГПРЛ, а также роль ПРЛ в процессах адаптации и дезадаптации.
– ПРЛ представляет собой гормон, который секретируется лактотрофными клетками передней доли гипофиза и выполняет в организме более 80 биологических функций – больше, чем все гипофизарные гормоны в совокупности.
У женщин в период беременности ПРЛ совместно с другими гормонами стимулирует развитие секреторного аппарата молочной железы, а в послеродовом периоде – образование молока в молочных железах. Кроме того, ПРЛ наряду с гонадотропными гормонами синхронизирует созревание фолликула и овуляцию, а в дальнейшем поддерживает существование желтого тела и образование в нем «гормона материнства» – прогестерона (Г.А. Марова и соавт., 2007; M.M. Carvalho et al., 2011). В то же время ПРЛ у мужчин выступает в роли регулятора половой функции, а именно: увеличивает массу яичек и семенных канальцев; усиливает обменные процессы в яичках; потенцирует действие лютеинизирующего и фолликулостимулирующего гормонов, направленное на восстановление и поддержание сперматогенеза; участвует в процессе регуляции энергетического метаболизма в сперматозоидах, влияет на подвижность сперматозоидов и на углеводный обмен в сперматозоидах (Г.А. Мельниченко и соавт., 2007). Имеются данные, что ПРЛ участвует в регуляции активности ферментов и транспортных факторов в жировой ткани, тем самым выступая в роли модулятора строения и массы тела. Повышенный же уровень ПРЛ ассоциирован с прибавкой массы тела и развитием ожирения (Г.А. Мельниченко и соавт., 2007; С.Ю. Калинченко, 2010).
Таким образом, любые нарушения, связанные с увеличением или снижением уровня ПРЛ, отражаются на множестве функций не только женского, но и мужского организма.
При этом наиболее распространенным патологическим состоянием является ГПРЛ.
Патологическая ГПРЛ – устойчиво повышенное содержание ПРЛ в сыворотке крови, которое наблюдается не только у женщин вне беременности, но и у мужчин. Повышенный уровень лактотропных гормонов, как биохимический маркер гипоталамо-гипофизарной дисфункции, является наиболее распространенной нейроэндокринной патологией. Частота случаев ГПРЛ у мужчин составляет 20:100 000, у женщин – около 90:100000. Как правило, пик заболеваемости ГПРЛ у женщин наблюдается в возрасте 25-34 лет. Стоит также отметить, что уровень ежегодной заболеваемости продолжает расти, и, по последним данным, составляет 23,9 на 100 000 человеко-лет. При этом распространенность пролактином (гормонально активных опухолей передней доли гипофиза) колеблется от 6-10 до 50 случаев на 100 000 населения (P.G. Crosignani, 2012).
Наряду с метаболическими нарушениями (гиперхолестеринемия) ГПРЛ также является основной причиной остеопенического синдрома. Снижение плотности костной ткани происходит путем непосредственного и опосредованного подавления стероидогенеза в яичниках. Согласно данным, приведенным в клинических рекомендациях Международного эндокринологического общества «Диагностика и лечение ГПРЛ» (Diagnosis and Treatment of Hyperprolactinemia: Аn Endocrine Society Clinical Practice Guideline, 2011), плотность костной ткани позвоночника у женщин с ГПРЛ уменьшается примерно на 25% и не обязательно восстанавливается при нормализации уровня ПРЛ. Примерно у 80% молодых женщин с ГПРЛ, дебютировавшей в подростковом возрасте, наблюдается остеопения и/или остеопороз. У данной категории больных также наблюдается значительное снижение уровня сывороточного остеокальцина – стимулятора ремоделирования костной ткани, при этом указанные изменения положительно коррелировали с длительностью ГПРЛ.
При ГПРЛ очень часто обнаруживается нарушение менструальной функции (30-60% пациенток). Характер нарушений менструального цикла напрямую связан со степенью ГПРЛ: чем выше уровень ПРЛ, тем тяжелее нарушения менструального цикла (вплоть до олиго- и аменореи). При этом при аменорее по сравнению с олигоменореей и регулярным менструальным циклом диагностируется достоверно более высокий уровень ПРЛ.
Оценка функционального состояния яичников указывает на то, что у подавляющего большинства пациенток с ГПРЛ (84%) нарушение менструального цикла сопровождается хронической ановуляцией. У остальных 16% диагностируется недостаточность лютеиновой фазы, в основном это пациентки с олигоменореей или сохраненным ритмом менструаций. В практике врача-гинеколога встречается множество патологических состояний, которые связаны с ГПРЛ. Так, в случае аномального маточного кровотечения, гонадотропной аменореи, остеопенического, метаболического или диэнцефального пубертатного синдрома обязательно стоит учитывать возможное наличие ГПРЛ. Патологически повышенный уровень ПРЛ может наблюдаться и при доброкачественных заболеваниях молочных желез (ДЗМЖ), миомах матки, предменструальном синдроме и недостаточности лютеиновой фазы, а также являться одной из причин невынашивания беременности и бесплодия. Бесплодие у женщин, вызванное ГПРЛ, наблюдается в 20‑60% случаев, а у мужчин (бесплодие вследствие олигоспермии) – до 15% случаев. В связи с этим в рекомендациях ВОЗ указывается, что первым исследованием, проводимым женщине из бесплодной пары, должно быть определение концентрации ПРЛ (после исключения мужского фактора бесплодия).
При диагностике ГПРЛ следует обращать особое внимание на неврологическую симптоматику (головная боль, головокружение, нарушение сна, снижение памяти, зрительные нарушения), которая при наличии пролактиномы обусловлена непосредственно опухолевым ростом. Психоэмоциональные расстройства при ГПРЛ, в частности эмоционально-личностные (депрессия, нарушение сна), наблюдаются у 20-30% пациентов, жалобы неспецифического характера (повышенная утомляемость, слабость, снижение памяти, тянущие боли в области сердца без четкой локализации и иррадиации) – у 15-25% больных. Практически всегда у пациентов с ГПРЛ присутствуют раздражительность, тревога, эмоциональная лабильность, аутизация, а в некоторых случаях существует вероятность развития психоза.
Лабораторная диагностика ГПРЛ должна быть направлена на определение ПРЛ с учетом его изоформ:
- мономерная форма – основная, молекулярная масса – 23 кДа, 85% от общего ПРЛ;
- димерная форма – 48-56 кДа (big-пролактин), 10‑15% ПРЛ;
- полимерная форма – 150 кДа (big-big-пролактин, или макропролактин), присутствует в небольшом вариабельном количестве;
- изоформа ПРЛ с молекулярной массой 16 кДа (little- пролактин), которая образуется в результате воздействия кислых протеаз и освобождения одного дисульфидного мостика;
- гликозилированная форма ПРЛ – 25 кДа, до 15% ПРЛ, биологическая активность 20-24% по сравнению с негликозилированной формой.
Однако всегда следует учитывать возможность ложноотрицательного определения ПРЛ вследствие так называемого «хук-эффекта», являющегося основной причиной гиподиаг ностики ГПРЛ. В наборах реагентов, применяемых для проведения иммуноферментного анализа по «сэндвич-принципу», при высоких концентрациях определяемого вещества существует обратная зависимость величины оптической плотности от содержания вещества (так называемый «хук-эффект» высоких концентраций). При использовании большинства современных наборов для иммуноферментного анализа «хук-эффект» не обнаруживается вплоть до концентрации ПРЛ 100 000 мЕд/л.
О данном феномене необходимо помнить при наличии больших опухолей и выраженной клинической симптоматике ГПРЛ на фоне нормального содержания ПРЛ в крови. Для исключения «хук-эффекта» необходимо проводить разведения образца, в котором производится определение ПРЛ.
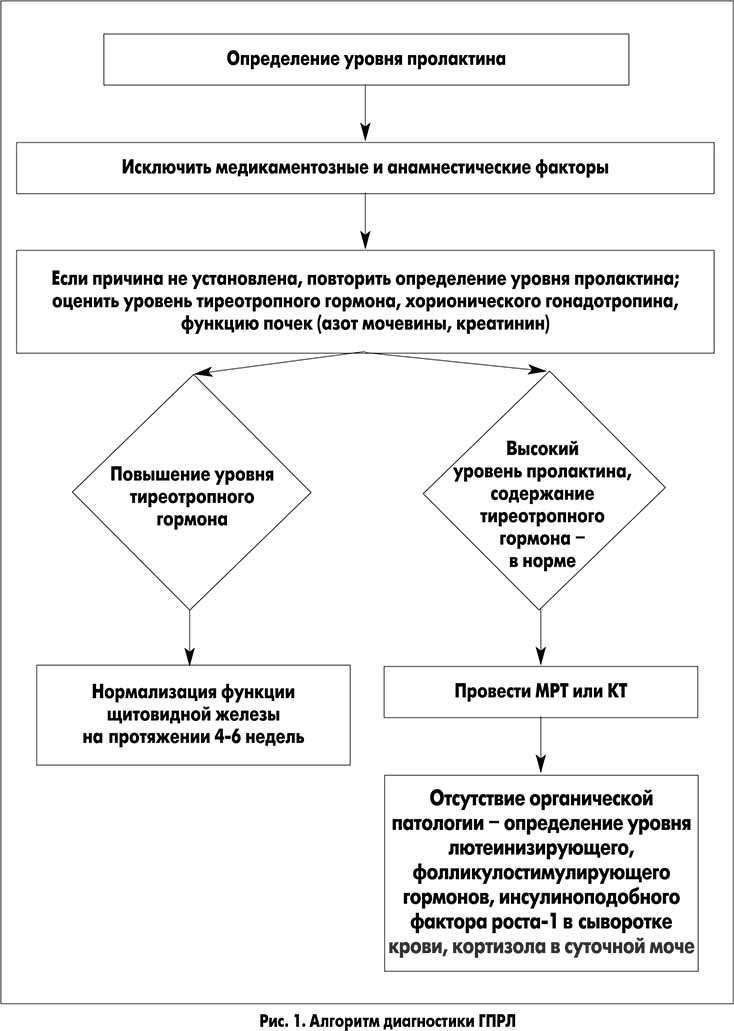
Наиболее оптимальный алгоритм диагностики ГПРЛ представлен на рисунке 1.
Переходя от успешной диагностики к тактике лечения, следует добиваться решения следующих основных задач: нормализация уровня ПРЛ, восстановление фертильности у женщин и половой функции у мужчин, устранение галактореи, нормализация менструального цикла. При наличии ПРЛ-секретирующей аденомы гипофиза основной целью лечения должно быть достижение регрессии или стабилизация ее роста.
В настоящее время ведущее место в лечении ГПРЛ принадлежит медикаментозному лечению с применением агонистов дофаминовых рецепторов. Агонисты дофаминовых рецепторов разделяются на три поколения (В.А. Олейник, Е.В. Эпштейн, 1996):
- первое поколение – эргот и его производные (бромокриптин, лизурид, перголид).
- второе поколение – неэрготсодержащие дофаминомиметики (квинаголид).
- третье поколение – дофаминергический дериват эрголина – каберголин (Достинекс®), представляющий собой высокоселективный пролонгированный ингибитор секреции ПРЛ.
Исходя из того, что клинические рекомендации по диагностике и лечению ГПРЛ не претерпели существенных изменений до настоящего времени (ноябрь 2015), основными положениями, которыми должен руководствоваться врач-гинеколог в своей клинической практике, являются клинические рекомендации Международного эндокринологического общества «Диагностика и лечение ГПРЛ» (Diagnosis and Treatment of Hyperprolactinemia: Аn Endocrine Society Clinical Practice Guideline, 2011):
- ГПРЛ – наиболее частая причина нарушения фертильности;
- диагностика ГПРЛ – обязательная составляющая обследования пациенток:
– с нарушениями менструального цикла (олигоменорея, аномальные маточные кровотечения);
– бесплодием и невынашиванием беременности;
– миомой матки, дисгормональными заболеваниями молочных желез;
- хронический стресс, аденомы гипофиза (пролактиномы), а также ятрогенные факторы – самые распространенные причины развития ГПРЛ;
- первая линия терапии при наличии пролактином – медикаментозное лечение (агонисты дофаминовых рецепторов);
- медикаментозная терапия высокоэффективна в отношении восстановления фертильности;
- после отмены каберголина (Достинекс®) в результате эффективного лечения целесообразен длительный (не менее года) мониторинг уровня ПРЛ;
- пролактиномы редко растут на фоне беременности; контроль состояния аденом на фоне беременности – только клинический, исследование ПРЛ при беременности не показательно;
- риск рецидивов ГПРЛ после беременности и лактации не увеличивается.
Как известно, одной из наиболее частых причин увеличения уровня ПРЛ и, как следствие, развития ГПРЛ, является наличие пролактином. О ключевой роли пролактином в развитии ГПРЛ участникам симпозиума рассказал сотрудник отделения транссфеноидальной нейрохирургии ГУ «Институт нейрохирургии им. акад. А.П. Ромоданова НАМН Украины», кандидат медицинских наук Николай Александрович Гук.
– История изучения пролактином начинается с открытия в 1928 г. ПРЛ как лактогенной субстанции. В 1954 г. учеными Форбсом и Олбрайтом (A. Forbes, F. Albright) была доказана взаимосвязь синдрома аменореи-галактореи с аденомой гипофиза. Фактически применение термина «пролактинома» является корректным только после иммуногистохимической верификации ткани аденомы гипофиза (4-й уровень классификации; И.З. Ковач и соавт., 1993). В наше время гормонально активная форма аденомы гипофиза встречается в 40% случаев диагностированных аденом гипофиза. А наиболее частая форма гормонально-активной аденомы гипофиза – это пролактинома.
В диагностике пролактином ключевая роль принадлежит лабораторным методам, в частности определению уровня ПРЛ. Как правило, при содержании ПРЛ в крови пациента >150-200 нг/мл проведение МРТ головного мозга подтверждает диагноз аденомы в 99% случаев, а при уровне ПРЛ <70 нг/мл в 99% случаев отмечается ее отсутствие.
В случае подтверждения диагноза важным шагом с точки зрения реализации мультидисциплинарного подхода является определение формы пролактиномы (микропролактинома, макропролактинома). Микропролактинома характеризуется отсутствием дальнейшего роста опухоли (в 95% случаев) и лучше поддается медикаментозному лечению.
Пациентам с микропролактиномами рекомендовано наблюдение у эндокринолога. Макропролактинома – более агрессивная форма пролактином, при наличии которой может потребоваться хирургическое вмешательство. Исходя из этого, лечение пациентов с данной патологией должно осуществляться нейрохирургами. Усовершенствование подходов к медикаментозной терапии пролактином, в частности применение агонистов дофамина, в корне изменило роль нейрохирургии в лечении этих опухолей. Частота хирургических вмешательств по поводу пролактином в хирургии аденом гипофиза за последние 10 лет снизилась с 16,5% (2004) до 5,8% (2014).
Исключение составляют кистозные макропролактиномы или симптоматические случаи гипофизарной апоплексии на любых этапах лечения. Согласно рекомендациям, представленным в различных международных руководствах, основная роль в медикаментозной терапии пролактином сегодня принадлежит агонисту дофамина каберголину. Если нормализации уровня ПРЛ не удается достичь, но размеры опухоли уменьшились, следует повышать дозу каберголина. При непереносимости или резистентности к бромокриптину также рекомендуется назначать терапию каберголином. Пациентам с симптоматическим течением пролактиномы, которые не переносят высокие дозы каберголина или нечувствительны к лечению агонистами дофамина, должно быть предложено транссфеноидальное нейрохирургическое вмешательство (S. Melmed et al., 2011).
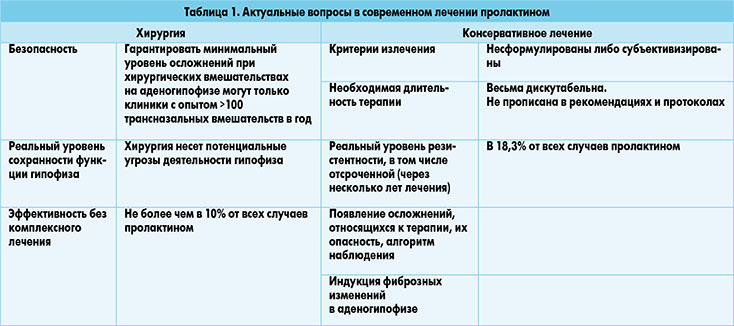
Несмотря на очевидный прогресс в современных подходах к лечению пролактином, несколько вопросов все еще остаются дискутабельними (табл. 1).
Таким образом, гормонально активные опухоли передней доли гипофиза являются серьезной междисциплинарной проблемой современной клинической практики.
Дальнейший поиск необходимых решений должен основываться на уже известных фактах:
- пролактинома не является первичной хирургической патологией, но требует мультидисциплинарного подхода к диагностике и лечению;
- первичное хирургическое лечение может применяться только в случаях тяжелой гипофизарной апоплексии (нарушений кровообращения в аденогипофизе) и полностью кистозных макропролактином (не более 2-5% от всех пролактином);
- пациентам с диагнозом макропролактинома или гигантская пролактинома следует также проводить терапию агонистами дофамина (каберголин), но с обязательным наблюдением нейрохирурга.
Также стоит помнить о том, что в 11-13% случаях пациентам с пролактиномами во время медикаментозного лечения из-за непереносимости препаратов, их побочных эффектов, при длительном приеме, резистентности опухоли или ее агрессивном течении может потребоваться оперативное вмешательство.
 Обсуждение современных подходов к медикаментозной терапии ГПРЛ продолжила профессор кафедры акушерства и гинекологии № 1 Одесского национального медицинского университета, доктор медицинских наук Светлана Родионовна Галич. Особенностью ее доклада стало подробное рассмотрение современных рекомендаций по лечению ГПРЛ, а также особенностей применения агонистов дофаминовых рецепторов у женщин с ГПРЛ при планировании беременности.
Обсуждение современных подходов к медикаментозной терапии ГПРЛ продолжила профессор кафедры акушерства и гинекологии № 1 Одесского национального медицинского университета, доктор медицинских наук Светлана Родионовна Галич. Особенностью ее доклада стало подробное рассмотрение современных рекомендаций по лечению ГПРЛ, а также особенностей применения агонистов дофаминовых рецепторов у женщин с ГПРЛ при планировании беременности.
– Среди существующих литературных источников и исследовательских баз по диагностике и лечению ГПРЛ наиболее содержательными на сегодняшний день являются клинические рекомендации Международного эндокринологического общества (International Society of Endocrinology – ISE, 2011). В данных рекомендациях подробно описаны доказательные подходы к оценке этиологии ГПРЛ, лечению лекарственно-индуцированной ГПРЛ и пролактином у беременных и небеременных женщин.
Кроме того, в данных рекомендациях рассмотрен выбор лекарственных средств для лечения пролактином, показания к их использованию, а также побочные эффекты (S. Melmed et al., 2011).
Согласно рекомендациям ISE особое внимание следует уделять прегравидарному периоду (подготовке к беременности).
Именно в этот период особенно важно нормализовать уровень ПРЛ, менструальный цикл, восстановить фертильность у женщин и мужчин, половую функцию у мужчин, а в случае наличия пролактин-секретирующей аденомы гипофиза – уменьшить массу опухоли.
Известно, что при всех формах ГПРЛ основным методом лечения является медикаментозная терапия с применением агонистов дофаминовых рецепторов. Однако применение агонистов дофамина не рекомендовано у пациентов с микропролактиномами, не проявляющимися клинической симптоматикой. Тем не менее пациентам с симптоматическими пролактин-секретирующими микроаденомами или макроаденомами показана медикаментозная терапия агонистами дофамина с целью снижения уровня ПРЛ, уменьшения размеров опухоли и восстановления гонадной функции (S. Melmed et al., 2011). Согласно классификации Г.А. Мельниченко и соавт. (2007), лекарственные средства, используемые для лечения ГПРЛ, разделяются на производные трициклических бензогуанолинов – хинаголид (квинаголид) – и производные алкалоидов спорыньи (эрголиновые): бромокриптин и каберголин (Достинекс®). Каждое из вышеперечисленных лекарственных средств относится к определенному поколению, а их эффективность определяется тремя параметрами: дозировкой, частотой приема и продолжительностью эффекта (табл. 2).
Возвращаясь к клиническим рекомендациям ISE, следует подчеркнуть, что при выборе агониста дофамина для медикаментозной терапии ГПРЛ или пролактиномы предпочтение отдается каберголину (Достинекс®), учитывая его высокую эффективность в отношении нормализации уровня ПРЛ, а также более частых случаев уменьшения размера опухоли (S. Melmed et al., 2011). Эффективность каберголина (Достинекс®) была доказана в исследовании L. Vilar и соавт. (2008), в котором приняли участие 1234 пациента с ГПРЛ различной этиологии, из которых у 388 была диагностирована пролактинома. Все пациенты были разделены на 2 группы: получавшие каберголин (Достинекс®; в дозе 1,0-3,5 мг/нед, средняя продолжительность курса – 12,5±8,9 мес) и бромокриптин (5- 15 мг/сут, средняя продолжительность – 13,3±9,6 мес). Значительное уменьшение размера опухоли наблюдалось у 80% принимавших каберголин (Достинекс®), и у 58,7% принимавших бромокриптин (p=0,048), полное исчезновение опухоли было отмечено у 57,5% и 34,7% пациентов соответственно (p=0,034).
Достоверно известно, что каберголин (Достинекс®) имеет лучший профиль безопасности в сравнении с другими агонистами дофамина. В исследовании J. Webster и соавт. (1994) с участием 459 пациенток с ГПРЛ частота побочных реакций от приема препарата (тошнота и рвота) была значительно ниже в группе, принимавшей каберголин (Достинекс®, 31% и 4%), нежели бромокриптин (50% и 10%). Кроме того, вследствие побочных реакций от лечения отказались 3% пациентов из группы каберголина (Достинекс®) и 12% пациентов из группы бромокриптина. При подтверждении наступления беременности у пациенток с ГПРЛ терапию агонистами дофамина отменяют.
Возобновляют терапию только при наличии показаний в виде признаков прогрессивного роста опухоли.
 Вопросам профилактики канцерогенеза у женщин с мастопатией на фоне ГПРЛ посвятил свое выступление заведующий кафедрой акушерства и гинекологии ГУ «Днепропетровская медицинская академия» МЗ Украины, доктор медицинских наук, профессор Валентин Александрович Потапов.
Вопросам профилактики канцерогенеза у женщин с мастопатией на фоне ГПРЛ посвятил свое выступление заведующий кафедрой акушерства и гинекологии ГУ «Днепропетровская медицинская академия» МЗ Украины, доктор медицинских наук, профессор Валентин Александрович Потапов.
– Процесс канцерогенеза в молочной железе можно условно разделить на 4 основных этапа: инициация, промоция, накопление стволовой линии мутированных клеток, опухолевая прогрессия с прорастанием в соседние ткани и метастазированием. Этап инициации характеризуется повреждением генетического аппарата клетки, приводящим к их неконтролируемому делению под воздействием внешних и внутренних канцерогенных факторов. Вполне рациональным решением было бы сфокусировать все мероприятия по профилактике канцерогенеза именно на этом этапе. Однако методы диагностики и профилактики злокачественного процесса на этапе инициации до настоящего времени не разработаны. Поэтому основные меры для предупреждения развития злокачественного процесса должны предприниматься в период промоции – активизации митозов как нормальных, так и мутированных клеток с экспрессией факторов неоангиогенеза. Наиболее важными в данный период являются диагностика и лечение мастопатий, направленное на замедление митоза и повышение дифференцировки клеток.
Согласно современной трактовке ВОЗ, термин «мастопатия» представляет собой объединенное название группы дисгормональных доброкачественных заболеваний молочных желез, характеризующихся гиперплазией ее ткани. ГПРЛ наряду с остальными дисгормональными патологиями (тиреоидная, яичниковая, гипоталамо-гипофизарная дисфункции и т.п.) является одной из основных причин мастопатии, которая вследствие активации процессов, способствующих преобладанию пролиферации клеток над их апоптозом.
Мастопатия встречается у 60% женщин до 40 лет и у 85,7% в возрасте 41-50 лет при риске малигнизации у каждой третьей. Поэтому эти пациентки должны находиться под постоянным наблюдением врача (диспансеризация) с обязательным проведением адекватной терапии в соответствии с генезом заболевания.
Как известно, ГПРЛ характеризуется повышенным уровнем ПРЛ – основного индуктора гиперпролиферации ткани молочной железы.
Повышенный уровень ПРЛ оказывает прямое стимулирующее воздействие на процессы пролиферации в молочных железах и способствует ускорению роста эпителиальных клеток молочной железы. Кроме того, ГПРЛ также характеризуется увеличением содержания рецепторов к эстрадиолу и повышением чувствительности клеток к его воздействию. При этом развитие гиперпластических процессов в молочных железах отмечается у 52% больных с ГПРЛ (Е. Андреева, М. Хамошина, 2010). В сравнительных исследованиях по оценке уровня ПРЛ у больных с узловыми доброкачественными и малигнизированными образованиями молочной железы распространенность ГПРЛ до хирургического лечения примерно одинакова и составляет 5-7% (R. Jaffe, C. Yen, 2009).
Основным критерием диагностики ГПРЛ является определение уровня ПРЛ, который в норме у женщин составляет 12 нг/мл (240 мЕд/л), а его максимальный уровень не превышает 20-27 нг/мл (400-540 мЕд/л). Поэтому диагноз ГПРЛ устанавливается только при повышенных концентрациях ПРЛ (>27 нг/мл, >540 мЕд/л) в сыворотке крови в нескольких образцах (Г.А. Мельниченко и соавт., 2007).
Основным методом лечения при всех формах ГПРЛ является медикаментозная терапия (фармакотерапия агонистами дофаминовых рецепторов). При этом предпочтение отдается представителю третьего поколения агонистов дофаминовых рецепторов – каберголину (Достинекс®). Исходя из нашего клинического опыта, мы рекомендуем следующую схему лечения мастопатии на фоне ГПРЛ каберголином (Достинекс®). Основной курс лечения подразумевает назначение 0,5-1 таблетки (0,25-0,5 мг) 1-2 раза в неделю. В случае необходимости дозу можно постепенно повышать в зависимости от переносимости и реакции на терапию. Режим повышения дозы не должен превышать 0,5 мг в мес. Средняя терапевтическая доза препарата Достинекс® составялет 1 мг в неделю, максимальная – 4,5 мг в неделю. Как только будет подобран оптимальный режим дозирования, необходимо 1 раз в месяц осуществлять определение содержания ПРЛ в крови. В среднем нормализация уровня ПРЛ наблюдается через 0,5-1 мес лечения.
Доклад «Роль гиперпролактинемии в нарушении женской фертильности», представленный заведующей кафедрой перинатологии, акушерства и гинекологии Харьковской медицинской академии последипломного образования, доктором медицинских наук, профессором Ольгой Валентиновной Грищенко, был посвящен проблеме гиперпролактинемии в практике репродуктолога.
Сочетание повышения концентрации пролактина с бесплодием, нарушениями менструального цикла и галактореей у женщин, снижением либидо и потенции, а также бесплодием у женщин и мужчин называется синдромом гиперпролактинемии. У пациентов обоих полов он также обозначен термином «синдром гиперпролактинемического гипогонадизма», а у женщин – «синдром персистирующей галактореиаменореи».
Гиперпролактинемия разделяется на физиологическую и патологическую. Первая наблюдается:
– у новорожденных девочек;
– у женщин в период беременности и лактации;
– во время глубокого сна;
– при приеме белковой пищи;
– при проведении некоторых медицинских манипуляций;
– при гипогликемических состояниях;
– при физических и эмоциональных перегрузках;
– при коитусе у женщин.
Патологическая гиперпролактинемия возникает на фоне:
– эндокринных заболеваний (синдромы Нельсона, Цондека, ВанВика, Иценко–Кушинга, инсулинозависимый сахарный диабет с частыми гипогликемиями);
– опухолевых процессов (внегипофизарные опухоли головного мозга, пролактинсекретирующие гипернефромы, бронхогенный рак);
– опоясывающего лишая (Herpes zoster);
– цирроза печени.
Эта форма может иметь также ятрогенную природу (на фоне приема резерпина, амитриптилина, церукала, мотилиума, эстрогенов, антибиотиков группы макролидов, эглонила, ранитидина, противосудорожных препаратов и др.).
Физиологические эффекты пролактина при беременности:
- поддерживает существование желтого тела и образование им прогестерона;
- подготавливает молочные железы (МЖ) к лактации;
- контролирует транспорт воды и ионов через амнион и таким образом регулирует объем и состав амниотической жидкости.
В послеродовом периоде пролактин стимулирует образование молока в МЖ.
Следует отметить, что при беременности нормальный уровень пролактина достигает 4500-6500 мМЕ/л. При более значительном повышении показателей в каждом случае индивидуально решается вопрос о целесообразности пролонгирования беременности.
В результате совершенствования препаратов для лечения гиперпролактинемии возросла их селективность, улучшились удобство применения и переносимость. Профессор О. В. Грищенко отметила, что в терапии беременных целесообразно применение представителя ІІІ поколения агонистов дофамина – каберголина.
Показаниями к назначению Достинекса в акушерской практике являются:
- патологическая гиперпролактинемия;
- контроль развития беременности;
- предотвращение или подавление лактации после прерывания беременности.
Докладчик представила результаты длительного международного исследования (1996), целью которого было определение безопасности каберголина в отношении репродуктивной функции. Результаты исследования показали, что Достинекс не повышает риск многоплодной либо внематочной беременности и преждевременных родов; не оказывает негативного влияния на здоровье матери и ребенка; беременность, индуцированная каберголином, не требует прерывания.
В клинических рекомендациях Эндокринного общества по диагностике и лечению ГПРЛ (2014) на основании результатов недавних исследований отмечена безопасность зачатия на фоне приема каберголина и его безопасность на ранних сроках беременности.
Важным аспектом в работе репродуктолога является борьба за снижение частоты развития синдрома гиперстимуляции яичников (СГЯ).
Установлено, что у женщин, принимавших каберголин по поводу гиперпролактинемии, ниже вероятность возникновения этой патологии. Применение каберголина не оказывает влияния ни на процессы имплантации, ни на исходы беременности, ни на развитие побочных эффектов.
Профилактический эффект каберголина в отношении риска развития и прогрессирования СГЯ объясняется его способностью блокировать взаимодействие сосудистого эндотелиального фактора роста со специфическими рецепторами 2-го типа, за счет чего уменьшается сосудистая проницаемость, то еть устраняется ключевой фактор патогенеза.
В международных рекомендациях указывается, что при применении Достинекса в программах вспомогательных репродуктивных технологий у женщин с гиперпролактинемией его назначают в минимальных дозах: 0,5 мг/сут на протяжении 3 недель, начиная с первого дня после извлечения яйцеклетки. Существует альтернативная схема применения каберголина – 0,5 мг/сут в течение 8 дней. Короткий курс терапии обеспечивает профилактический эффект в отношении проявлений раннего СГЯ.
Максимальная суточная доза каберголина для профилактики и лечения СГЯ составляет 0,5 мг.
В заключение О. В. Грищенко отметила, что по сравнению с другими препаратами агонистами дофамина Достинекс более безопасен для пациентов, поскольку реже вызывает побочные эффекты, их проявления менее выражены, что улучшает комплаенс.
Подготовил Антон Вовчек
Тематичний номер «Гінекологія, Акушерство, Репродуктологія» № 4 (20) грудень 2015 р.