23 жовтня, 2020
Практичні рекомендації щодо ведення пацієнтів з артеріальною гіпертензією
Артеріальна гіпертензія (АГ) лишається провідною причиною смерті в усьому світі. Поширеність АГ та її вплив на серцево-судинну (СС) захворюваність і смертність продовжує зростати. Для зменшення глобального тягаря підвищення артеріального тиску (АТ) Міжнародне товариство з артеріальної гіпертензії (ISH) 2020 року розробило практичну настанову щодо лікування АГ у дорослих хворих віком від 18 років. Автори представили рекомендації відповідно до основних (мінімальних) та оптимальних (науково обґрунтованих та підкріплених доказами, відображеними у сучасних настановах) стандартів надання медичної допомоги особам з АГ. Сформульовані положення слугують інструментом для поліпшення ведення пацієнтів з метою зменшення СС-захворюваності та смертності, пов’язаних з АГ. Пропонуємо до вашої уваги короткий огляд документа з акцентом на аспектах модифікації способу життя, фармакотерапії, лікуванні АГ та коморбідних станів тощо.
Лікування пацієнтів з АГ
Модифікація способу життя
Модифікація способу життя може запобігти підвищенню АТ або відстрочити його початок, а також знизити СС-ризик у хворих (Piepoli et al., 2016). Зміни способу життя, що включені до антигіпертензивного лікування першої лінії, можуть посилити ефект терапії.
Корекція способу життя у пацієнтів з АГ передбачають зменшення вживання солі, перегляд режиму харчування, помірне споживання алкоголю, зниження ваги, відмову від куріння, регулярну фізичну активність, уникання стресових ситуацій, застосування додаткових, альтернативних чи традиційних ліків. Також важливим є зменшення впливу негативних чинників довкілля та низьких температур (Cicero et al., 2019; Costa et al., 2018; Solano Lopez, 2018; Roerecke et al., 2017).
Фармакотерапія
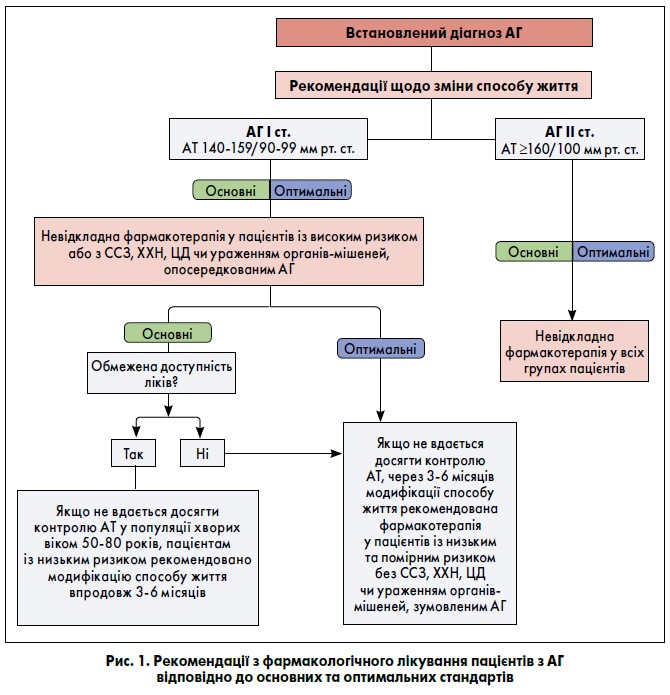
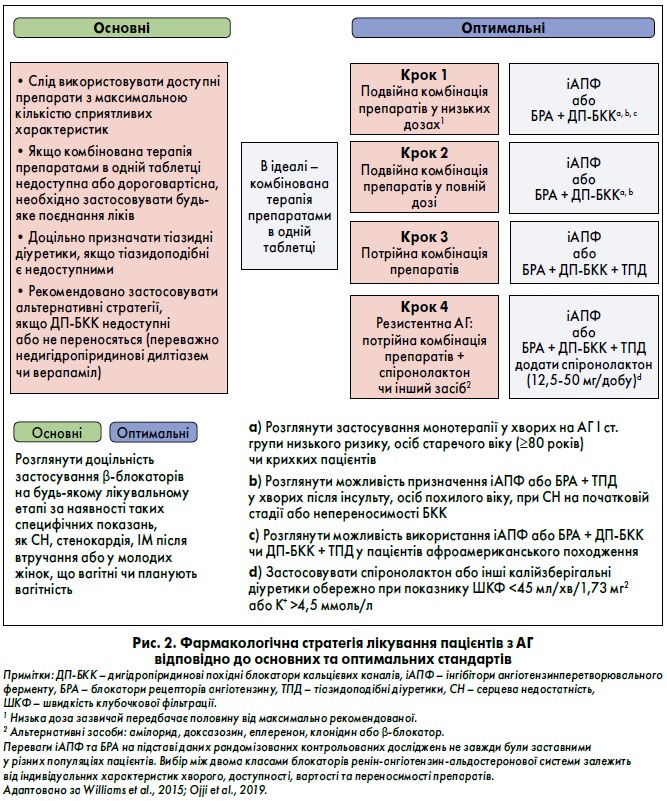
За актуальними даними, у світі в середньому менш ніж 50% дорослих пацієнтів з АГ отримують ліки для зниження АТ (Geldsetzer et al., 2019). Рекомендації щодо медикаментозного лікування, які відповідають сучасним міжнародним настановам, відображені на рисунках 1 та 2 (Williams et al., 2018; Whelton et al., 2018; NICE, 2019).
Оптимальні характеристики лікування препаратами наступні:
1. Лікування має бути науково обґрунтованим щодо попереджання захворюваності та смертності.
2. Слід використовувати схему приймання препарату один раз на день, яка забезпечуватиме цілодобовий контроль АТ.
3. Лікування має бути доступним та/або економічно ефективним.
4. Терапія повинна добре переноситися.
5. Застосування лікарських засобів у популяціях пацієнтів, в яких їх призначатимуть, має бути підкріплене доказами клінічної користі.
Основні стандарти лікування АГ передбачають досягнення цільового зниження АТ принаймні на 20/10 мм рт. ст. Оптимальні стандарти терапії у пацієнтів віком <65 років включають досягнення цільового значення АТ <130/80 мм рт. ст. (але >120/70 мм рт. ст.) у разі переносимості препаратів, ≥65 років – менш ніж 140/90 мм рт. ст., проте показники можуть варіювати залежно від індивідуальних характеристик та комплаєнсу хворого. Ключова мета передбачає досягнення контролю АТ упродовж трьох місяців.
Прихильність до антигіпертензивного лікування
Неналежне дотримання режиму антигіпертензивного лікування впливає на 10‑80% пацієнтів з АГ та є одним із основних факторів неоптимального контролю АТ (Tomaszewski et al., 2014; Mazzaglia et al., 2009; Corrao et al., 2011). Незадовільний комплаєнс корелює зі зростанням рівня АТ і є показником поганого прогнозу в осіб з АГ (Gupta et al., 2016, 2017; Wei et al., 2018; Abegaz et al., 2017).
Рекомендації щодо поліпшення прихильності до антигіпертензивної терапії відповідно до основних та оптимальних стандартів
- Необхідно оцінювати дотримання режиму антигіпертензивного лікування при кожному візиті пацієнта до ескалації доз препаратів.
- Слід розглянути наступні лікувальні стратегії для покращання комплаєнсу (Conn et al., 2015, 2017; Verma et al., 2018; Gupta et al., 2017; Ruppar et al., 2017; Costa et al., 2015):
- зменшення поліпрагмазії – використання фіксованих комбінацій препаратів в одній таблетці;
- застосування лікарського засобу один раз на добу;
- прихильність до терапії має корелювати з щоденними звичками хворого;
- забезпечення зворотного зв’язку з пацієнтами;
- домашній моніторинг АТ;
- консультування хворих для забезпечення можливості самостійного контролю стану;
- електронні засоби для підвищення комплаєнсу (органайзери, таймери, застосунки у мобільних телефонах, короткі повідомлення-нагадування тощо);
- мультидисциплінарний підхід для поліпшення контролю дотримання режиму терапії.
Рекомендації щодо поліпшення прихильності до антигіпертензивної терапії відповідно до оптимальних стандартів
1. Об’єктивні посередні (перевірка аптечного формуляру хворого, підрахунок таблеток, електронні пристрої для моніторингу) та безпосередні (приймання препаратів за присутності іншої людини, біохімічне виявлення ліків у сечі чи крові) методи контролю недотримання антигіпертензивного лікування зазвичай є кращими за суб’єктивні (Gupta et al., 2016, 2017).
2. Найефективніші методи контролю комплаєнсу потребують комплексного підходу, що включає консультування, самоконтроль, нагляд тощо.
Коморбідні захворювання та ускладнення АГ
У пацієнтів з АГ можуть спостерігатися супутні патології, які чинять вплив на СС-ризик та стратегії лікування. З віком кількість коморбідностей, зокрема АГ та інших захворювань, зростає.
Поширені супутні стани включають ішемічну хворобу серця (ІХС), інсульт, хронічну хворобу нирок (ХХН), серцеву недостатність (СН), хронічне обструктивне захворювання легень (ХОЗЛ). Рідше зустрічаються ревматичні та психічні патології, які значною мірою недооцінюються у рекомендаціях та часто лікуються пацієнтами самостійно, що може перешкоджати контролю АТ. Часті й нечасті коморбідні стани слід виявляти та лікувати відповідно до наявних доказових даних.
АГ та ІХС
За епідеміологічними даними, існує потужний зв’язок між ІХС та АГ, що включає 25‑30% випадків гострого інфаркту міокарда (ІМ) (Yusuf et al., 2004). Для контролю цієї коморбідності рекомендовано модифікацію способу життя, як-то відмова від куріння, належні режим харчування та фізична активність. АТ слід знижувати, якщо показник ≥140/90 мм рт. ст., до цільового <130/80 мм рт. ст. (<140/80 у літніх пацієнтів).
Незалежно від рівня АТ блокатори ренін-ангіотензин-альдостеронової системи (РААС), β-блокатори з/без блокаторів кальцієвих каналів (БКК) є препаратами першого вибору в осіб з АГ. Гіполіпідемічну терапію застосовують для досягнення рівня холестерину (ХС) ліпопротеїнів низької щільності (ЛПНЩ) <55 мг/дл (1,4 ммоль/л) (Mach et al., 2020). Також зазвичай рекомендоване регулярне антитромбоцитарне лікування ацетилсаліциловою кислотою (Williams et al., 2018).
АГ та інсульт
АГ є найважливішим фактором ризику ішемічного або геморагічного інсульту (O’Donnell et al., 2010). Завдяки контролю АТ можна запобігти розвитку інсульту. АТ слід знижувати, якщо ≥140/90 мм рт. ст., і прагнути досягти цільового значення <130/80 мм рт. ст. (<140/80 у пацієнтів похилого віку) (Williams et al., 2018).
Блокатори РААС, БКК та діуретики є лікуванням першої лінії. При перенесеному ішемічному інсульті застосування ліпідознижувальних препаратів обов’язкове для досягнення цільового показника ХС ЛПНЩ <70 мг/дл (1,8 ммоль/л). На додаток, при ішемічному, але не геморагічному інсульті рекомендовано призначати антитромбоцитарну терапію. В осіб після геморагічного інсульту можна розглянути використання антиагрегантів лише за наявності переконливих показань (Williams et al., 2018).
АГ та СН
АГ являє собою фактор ризику розвитку СН зі зниженою (СНзнФВ) та збереженою фракцією викиду (СНзбФВ). У хворих на АГ та СН клінічні наслідки є гіршими, а смертність збільшується (Whelton et al., 2017). Тому в таких пацієнтів рекомендовані зміни способу життя, як-от корекція режиму харчування та збільшення фізичної активності. Лікування АГ зумовлює зниження ризику розвитку СН та пов’язаних із нею госпіталізацій. АТ слід знижувати за наявності показника ≥140/90 мм рт. ст. і прагнути досягти цільового рівня <130/80 мм рт. ст., але >120/70 мм рт. ст.
Блокатори РААС, β-блокатори та антагоністи мінералокортикоїдних рецепторів ефективні у пацієнтів зі встановленою СНзнФВ, тоді як для діуретиків докази обмежуються симптоматичним поліпшенням (Williams et al., 2018). БКК призначають у разі поганого контролю АТ. Інгібітор рецептора ангіотензину/неприлізину показаний для лікування СНзнФВ як альтернатива іАПФ чи БРА у пацієнтів з АГ. Таку ж стратегію терапії можна застосувати в осіб із СНзбФВ, навіть якщо оптимальну тактику не визначено (Bohm et al., 2017).
АГ та ХХН
АГ є основним фактором ризику розвитку/прогресування альбумінурії та будь-якої форми ХХН. Зниження розрахункової швидкості клубочкової фільтрації (рШКФ) асоційоване з резистентною, маскованою АГ та підвищенням рівня АТ у нічний час (Drawz et al., 2016). АТ слід знижувати, якщо показник становить ≥140/90 мм рт. ст., до досягнення цільового <130/80 мм рт. ст. (<140/80 у літніх пацієнтів) (Williams et al., 2018).
Інгібітори РААС є препаратами першого вибору, оскільки вони зменшують альбумінурію на додачу до контролю АТ. Також можуть бути додані БКК та діуретики (петльові, якщо рШКФ <30 мл/хв/1,73 м2). Під час лікування важливо контролювати рШКФ, мікроальбумінурію та електроліти у крові (Williams et al., 2018).
АГ та ХОЗЛ
АГ являє собою найчастішу коморбідність у пацієнтів із ХОЗЛ. АТ слід знижувати, якщо його рівень ≥140/90 мм рт. ст. і прагнути досягти цільового <130/80 мм рт. ст. (<140/80 мм рт. ст. у пацієнтів похилого віку). Модифікація способу життя (припинення куріння) є обов’язковою. Слід за можливості уникати впливу негативних чинників навколишнього середовища, як-то забруднене повітря (Drawz et al., 2016).
Стратегія лікування має включати блокатор AT1-рецепторів ангіотензину (БРА) і БКК та/або діуретик. В окремій групі хворих (з ІХС, СН) можна застосовувати β-блокатори (β1-селективні). Необхідно контролювати додаткові фактори вірогідності розвитку СС-подій відповідно до профілю СС-ризику.
АГ та ЦД
У пацієнтів із коморбідними АГ і ЦД слід знижувати АТ, якщо він ≥140/90 мм рт. ст., до цільового рівня <130/80 мм рт. ст. (<140/80 мм рт. ст. у літніх хворих) (ADA, 2017). Лікування передбачає призначення інгібітора РААС і БКК та/або тіазидоподібного діуретика. Статини потрібно застосовувати в межах первинної профілактики, якщо ХС ЛПНЩ >70 мг/дл, або 1,8 ммоль/л (ЦД з ураженням органів-мішеней) чи >100 мг/дл, або 2,6 ммоль/л (неускладнений ЦД). Окрім того, терапія має включати зниження рівня глюкози та ліпідів у крові згідно з чинними рекомендаціями.
АГ, порушення ліпідного обміну й метаболічний синдром
Терапевтичні заходи стосовно зниження АТ мають бути такими, як у загальній популяції хворих, переважно з використанням інгібіторів РААС (БРА, іАПФ) та БКК (Sever et al., 2003). Статини є ліпідознижувальними препаратами вибору з/без застосування езетимібу та/або інгібітора PCSK9 (за оптимальних умов) (Nordestgaard, 2016). Слід зазначити, що потрібне зниження вмісту тригліцеридів у сироватці крові, якщо показник становить >200 мг/дл (2,3 ммоль/л), особливо в осіб з АГ та ЦД. Можливі додаткові переваги у разі призначення фенофібрату в пацієнтів із низьким рівнем ЛПВЩ / високим рівнем тригліцеридів.
Хворі, які мають супутні АГ та метаболічний синдром, входять до групи високого ризику. Лікування базується на модифікації способу життя, як-то правильне харчування, належна фізична активність, та повинно включати контроль АТ як у загальній популяції пацієнтів, а також додаткових факторів ризику на основі рівня СС-ризику (відповідно до шкали SCORE та/або ASCVD).
АГ та інші супутні стани
Запальні ревматичні захворювання (ревматоїдний, псоріатичний артрит тощо) пов’язані з підвищенням поширеності діагностованої АГ, що погано контролюється. Такі патології призводять до зростання вірогідності розвитку СС-ускладнень, що лише частково корелює з факторами СС-ризику.
Лікувальні заходи щодо зниження АТ мають бути такими, як у загальній популяції хворих, переважно із застосуванням інгібіторів РААС та БКК. Під час терапії слід прагнути зменшити запалення, викликане коморбідними ревматичними хворобами, уникаючи високих доз нестероїдних протизапальних препаратів. Гіполіпідемічну терапію варто призначати відповідно до профілю СС-ризику (за шкалою SCORE/ASCVD), враховуючи ефекти біологічних засобів (Agca et al., 2017; Ikdahl et al., 2019).
Лікування осіб з АГ та коморбідними станами відповідно до основних та оптимальних стандартів
1. Окрім контролю АТ, терапевтична стратегія має включати зміни способу життя, контроль маси тіла та ефективне лікування інших факторів ризику для зниження резидуального СС-ризику (Williams et al., 2018).
2. Рівень ХС ЛПНЩ слід знижувати відповідно до профілю ризику (Williams et al., 2018; Mach et al., 2020):
- >50%, та <70 мг/дл (1,8 ммоль/л) при АГ і ССЗ, ХХН, ЦД або без ССЗ та високого ризику;
- >50%, та <100 мг/дл (2,6 ммоль/л) у пацієнтів із високим ризиком;
- <115 мг/дл (3 ммоль/л) у хворих із помірним ризиком.
3. Слід знизити вміст глюкози в сироватці натще <126 мг/дл (7 ммоль/л) або глікованого гемоглобіну <7% (53 ммоль/моль) (Williams et al., 2018).
4. Слід підтримувати рівень сечової кислоти <6,5 мг/дл (0,387 ммоль/л), у пацієнтів із подагрою – нижчий за 6 мг/дл (0,357 ммоль/л) (Borghi et al., 2015).
5. У хворих на ССЗ доцільно розглянути антитромбоцитарну терапію (лише як вторинну профілактику) (Arnett et al., 2019).
На додаток, поширеність АГ зростає серед пацієнтів із психічними розладами та, зокрема, депресією (Musselman et al., 1998; Patten et al., 2009). Відповідно до рекомендацій, психосоціальний стрес та основні психічні захворювання підвищують СС-ризик. Депресія пов’язана зі збільшенням СС-захворюваності та смертності, що свідчить про важливість контролю АТ.
Стратегія зниження АТ повинна бути такою, як у загальній популяції хворих, переважно з використанням інгібіторів РААС та діуретиків із меншою частотою фармакологічної взаємодії з антидепресантами. БКК та α-блокатори слід застосовувати обережно у пацієнтів з ортостатичною гіпотензією. Загалом важливо враховувати ризик взаємодій лікарських засобів, порушення на електрокардіограмі та зміни постурального АТ. Бета-блокатори (не метопролол) варто призначати за наявності тахікардії, пов’язаної з лікуванням (антидепресантами, антипсихотиками) (Siwek et al., 2020). На додачу, необхідно контролювати додаткові фактори ризику відповідно до профілю СС-ризику (за шкалою SCORE/ASCVD).
Ведення пацієнтів із резистентною АГ
Резистентна АГ визначається як офісний АТ >140/90 мм рт. ст. у положенні сидячи в пацієнта, який отримував три або більше антигіпертензивні препарати в оптимальних (або максимально переносимих) дозах, включно з діуретиком. При цьому потрібно виключити псевдорезистентність, що може асоціюватися з поганою методикою вимірювання АТ, ефектом білого халату, низьким комплаєнсом. Також вона нерідко корелює з некоректним вибором антигіпертензивної терапії. Крім того, слід виключити АГ, викликану ліками / психоактивними речовинами (ПАР), і вторинну АГ (Wei et al., 2018).
Резистентна форма становить близько 10% захворюваності на АГ, підвищуючи ризик розвитку ІХС, хронічної СН, інсульту, ниркової недостатності на термінальній стадії та смертності за будь-яких причин (Vongpatanasin, 2014; Ayala et al., 2013). Приблизно 50% пацієнтів із діагнозом резистентної АГ насправді мають псевдорезистентність (Bhatt et al., 2016; de Jager et al., 2018; Nazarzadeh et al., 2019).
Рекомендації відповідно до основних стандартів лікування
1. Якщо пацієнти, які отримували три або більше антигіпертензивні препарати в оптимальних (або максимально переносимих) дозах, включно з діуретиком, мають офісний АТ >140/90 мм рт. ст. у положенні сидячи, спочатку слід виключити причини псевдорезистентності та підвищення АТ, зумовленого ліками/ПАР.
2. За потреби доцільно обстежити хворих на наявність вторинних причин розвитку резистентної АГ.
3. Варто оптимізувати поточну схему лікування, включно з модифікацією способу життя та діуретичної терапії: розглянути можливість застосування максимально переносимих доз препаратів, тіазидоподібних, а не тіазидних діуретиків, та початок приймання петльових діуретиків при рШКФ <30 мл/хв/1,73 м2 або перевантаженні об’ємом (Rossignol et al., 2015).
4. Необхідно додати спіронолактон у низькій дозі як лікування четвертої лінії пацієнтам із рівнем сироваткового калію <4,5 ммоль/л та рШКФ >45 мл/хв/1,73 м2 для досягнення цільових показників АТ (Williams et al., 2015, 2018; NICE, 2019). Якщо спіронолактон протипоказаний або не переноситься, альтернативним варіантом можуть бути амілорид, доксазозин, еплеренон, клонідин, β-блокатори або будь-який інший доступний клас антигіпертензивних засобів, який ще не використовувався (Sinnott et al., 2017; Krieger et al., 2018; Brown et al., 2016; Manolis et al., 2019).
Рекомендації відповідно до оптимальних стандартів лікування
Лікування резистентної АГ повинні проводити клініцисти із достатнім досвідом у спеціалізованих медичних центрах. При цьому мають бути доступні відповідні ресурси, необхідні для діагностики та терапії цього стану (Denker et al., 2013).
Терапія осіб із вторинною АГ
Специфічне захворювання чи стан можуть стати причиною розвитку вторинної (симптоматичної) АГ у 5‑10% хворих на АГ. Рання діагностика вторинної АГ та ініціювання відповідної терапії дозволяють вилікувати АГ, покращити контроль АТ чи зменшити кількість призначених антигіпертензивних препаратів. Найпоширенішими типами вторинної АГ у дорослих є ниркова паренхіматозна, реноваскулярна АГ, первинний альдостеронізм, хронічне апное уві сні, а також АГ, індукована ліками/ПАР, тощо (Funder et al., 2016; Gornik et al., 2019; Rimoldi et al., 2014; Borgel et al., 2010).
Рекомендації відповідно до основних стандартів лікування
1. Необхідно провести обстеження пацієнтів щодо наявності вторинної АГ у таких групах:
- у пацієнтів із ранньою АГ (віком <30 років), зокрема, за відсутності факторів ризику АГ, як-от ожиріння, метаболічний синдром, сімейний анамнез тощо;
- у хворих на резистентну АГ;
- в осіб із раптовим погіршенням контролю АТ;
- за екстрених/невідкладних станів (гіпертонічний криз);
- у пацієнтів із високою імовірністю розвитку вторинної АГ на основі переконливих клінічних доказів.
2. У пацієнтів із резистентною формою перед обстеженням із приводу вторинної АГ зазвичай слід виключити наявність псевдорезистентної та індукованої ліками/ПАР АГ.
3. Базовий скринінг на вторинну АГ повинен включати ретельну оцінку анамнезу, фізикальне обстеження, основний біохімічний аналіз крові (зокрема рівня натрію, калію, рШКФ, тиреотропного гормону) та аналіз сечі за допомогою тесту-смужки.
Рекомендації відповідно до оптимальних стандартів лікування
1. Подальші методи оцінки пацієнтів із приводу вторинної АГ (додаткові біохімічні аналізи / візуалізація тощо) слід ретельно вибирати на основі анамнезу хворих, даних фізикального обстеження та основних клінічних досліджень.
2. У разі підозри на наявність вторинної АГ, необхідно розглянути направлення пацієнта на подальше обстеження та лікування до спеціалізованого центру з відповідними фахівцями та медичними ресурсами.
АГ у вагітних
Ризики для матері під час вагітності включають відшарування плаценти, інсульт, поліорганну недостатність (печінки, нирок), дисеміноване внутрішньосудинне згортання крові. До ризиків для плода відносять затримку внутрішньоутробного розвитку, передчасні пологи, внутрішньоутробну смерть. АГ при вагітності включає такі стани, як раніше наявна АГ, гестаційна АГ, раніше наявна + гестаційна АГ із протеїнурією, прееклампсія, еклампсія, HELLP-синдром (гемоліз, підвищення печінкових ферментів, низький рівень тромбоцитів) (Regitz-Zagrosek et al., 2018; Lowe et al., 2015; Rolnik et al., 2017; Abalos et al., 2014).
Обстеження у вагітних із приводу АГ відповідно до основних стандартів надання медичної допомоги передбачає проведення аналізу сечі, загального аналізу крові, визначення гематокриту, рівня сироваткового креатиніну, сечової кислоти та тесту на ферменти печінки. Також необхідний аналіз на протеїнурію на ранніх строках та у другій половині вагітності. Терапевтична оцінка щодо наявності АГ у вагітних відповідно до оптимальних стандартів надання медичної допомоги включає ультразвукове дослідження нирок і наднирників, аналіз на вільну форму метанефринів плазми (якщо є клінічні ознаки феохромоцитоми), доплерографію маткових артерій.
Фармакотерапія
Медикаментозне лікування за легкої форми АГ у вагітних призначають при стійкому АТ >150/95 мм рт. ст., у разі гестаційної АГ, раніше наявної та супутньої гестаційної АГ – при стійкому АТ >140/90 мм рт. ст., а також за ураження органів-мішеней, опосередкованого АГ (HMOD), на будь-якому етапі вагітності. Терапія першої лінії включає метилдопу, β-блокатори (лабеталол) та дигідропіридинові похідні блокатори кальцієвих каналів (ДП-БКК) (некапсульний ніфедипін, нікардипін).
Протипоказані блокатори РААС (іАПФ, БРА, прямі інгібітори реніну) через несприятливі наслідки для плода та новонародженого. У вагітних із тяжкою формою АГ, у разі систолічного та/або діастолічного АТ >170 і >110 мм рт. ст. показано негайну госпіталізацію, лабеталол внутрішньовенно (альтернатива – нікардипін, есмолол, гідралазин, урапідил), метилдопу перорально або некапсульний ніфедипін, нікардипін. При гіпертонічному кризі для запобігання еклампсії слід додати магній, за набряку легенів потрібна внутрішньовенна інфузія нітрогліцерину. Варто уникати застосування нітропрусиду натрію через небезпеку отруєння плода ціанідом при тривалому лікуванні.
Якщо після пологів АГ зберігається, доцільно призначити будь-який із зазначених препаратів, крім метилдопи (для уникнення післяпологової депресії). Рекомендації відповідно до основних та оптимальних стандартів надання допомоги включають модифікацію способу життя та щорічне контрольне обстеження (АТ, метаболічні фактори).
Лікування пацієнтів із гіпертонічним кризом
Гіпертонічний криз – це суттєве підвищення рівня АТ, що супроводжується гострим HMOD. До можливих органів-мішеней належать сітківка, мозок, серце, великі артерії та нирки (van den Born et al., 2019). Клінічні прояви гіпертонічного кризу включають злоякісну АГ, гіпертензивну енцефалопатію, тромботичну мікроангіопатію. Також можуть спостерігатися виразне підвищення АТ, пов’язане з крововиливом у мозок, гострий інсульт, гострий коронарний синдром, кардіогенний набряк легенів, аневризма / розшарування аорти та тяжка прееклампсія, еклампсія. Пацієнти зі значно підвищеним АТ без гострого HMOD не вважаються такими, що мають гіпертонічний криз, і зазвичай можуть отримувати пероральну антигіпертензивну терапію (van den Born et al., 2006).
Гіпертонічний криз потребує швидкого діагностичного обстеження та негайного зниження АТ, щоб уникнути прогресивної органної недостатності. Зазвичай необхідна внутрішньовенна терапія. Вибір антигіпертензивного лікування переважно визначається типом ураження органів.
Невідкладна терапія та особливі клінічні ситуації
Основна мета у пацієнтів із гіпертонічним кризом полягає у контрольованому зниженні АТ до безпечніших рівнів для запобігання або обмеження подальшого гіпертонічного ураження, уникаючи гіпотензії та супутніх ускладнень. На жаль, бракує даних рандомізованих контрольованих випробувань для надання чітких рекомендацій щодо цільових показників АТ та періоду, протягом якого вони мають бути досягнуті. Часові межі та величина зниження АТ значною мірою залежать від клінічного контексту. Наприклад, гострий набряк легенів та розшарування аорти потребують швидкого зниження АТ, тоді як значення, що не перевищують 220/120 мм рт. ст., зазвичай коригуються при гострому ішемічному інсульті протягом певного часу.
Доступність лікарських засобів та досвід застосування окремих препаратів, імовірно, впливатимуть на вибір лікування. Лабеталол і нікардипін переважно безпечні при усіх типах гіпертонічного кризу. Нітрогліцерин та нітропрусид особливо ефективні при гіпертонічному кризі із ураженням серця та аорти.
Якщо є підозра, що інтоксикація симпатоміметиками або ПАР являє собою причину появи гіпертонічного кризу (симпатична гіперреактивність), слід розглянути застосування бензодіазепінів до початку специфічного антигіпертензивного лікування. Фентоламін і клонідин можуть виявитися корисними, якщо потрібна додаткова терапія для зниження АТ. Нікардипін і нітропрусид є альтернативними засобами. У разі розвитку феохромоцитоми варто призначити фентоламін. Бета-блокатори застосовують лише після α-блокаторів, щоб уникнути посилення АГ. Урапідил і нітропрусид – додаткові прийнятні варіанти.
Подальше спостереження
Пацієнти, які перенесли гіпертонічний криз, мають підвищений ризик розвитку кардіоваскулярної та ниркової патології (Amraoui et al., 2014; Gonzalez et al., 2010). Обов’язковими є ретельне обстеження щодо можливих причин та оцінка HMOD для запобігання повторним проявам гіпертонічного кризу. Крім того, коригування та спрощення антигіпертензивної терапії в поєднанні з порадами щодо зміни способу життя допоможе покращити комплаєнс та довготривалий контроль АТ. Також рекомендоване регулярне й часте спостереження (щомісяця) до досягнення цільового АТ та, в ідеалі, регресу HMOD.
Підготувала Олена Коробка
Оригінальний текст документа читайте на сайті www.ahajournals.org
Тематичний номер «Кардіологія, Ревматологія, Кардіохірургія» № 4 (71) 2020 р.