25 квітня, 2021
Неконтрольована артеріальна гіпертензія: додаткові можливості покращення контролю артеріального тиску та якості життя пацієнтів
 Головним завданням терапії артеріальної гіпертензії (АГ) є досягнення цільового рівня артеріального тиску (АТ) та його утримання в межах цільового діапазону. Результати масштабного спостережного дослідження, до якого було залучено 13 947 пацієнтів (середній період спостереження становив 19,1 року), довели, що хворі з нелікованою чи лікованою, але неконтрольованою АГ (порівняно з нормотензивними особами) мають вищий ризик серцево-судинної смерті та смерті від усіх причин. Водночас достовірних відмінностей між нормотензивними особами та пацієнтами з ефективно контрольованою АГ виявлено не було. Встановлені зв’язки не залежали від раси, віку чи статі [1], при цьому ризик серцево-судинної смерті є вищим за умови недосягнення як окремо систолічного АТ (САТ) або діастолічного АТ (ДАТ), так і обох показників [2].
Головним завданням терапії артеріальної гіпертензії (АГ) є досягнення цільового рівня артеріального тиску (АТ) та його утримання в межах цільового діапазону. Результати масштабного спостережного дослідження, до якого було залучено 13 947 пацієнтів (середній період спостереження становив 19,1 року), довели, що хворі з нелікованою чи лікованою, але неконтрольованою АГ (порівняно з нормотензивними особами) мають вищий ризик серцево-судинної смерті та смерті від усіх причин. Водночас достовірних відмінностей між нормотензивними особами та пацієнтами з ефективно контрольованою АГ виявлено не було. Встановлені зв’язки не залежали від раси, віку чи статі [1], при цьому ризик серцево-судинної смерті є вищим за умови недосягнення як окремо систолічного АТ (САТ) або діастолічного АТ (ДАТ), так і обох показників [2].
Досягнення й утримання цільового АТ є ключовою умовою зниження ризику серцево-судинних ускладнень. Одним із потужних чинників незадовільного контролю АТ є недостатня прихильність пацієнтів до лікування. Низька прихильність до антигіпертензивної терапії асоціюється не тільки з недостатньою ефективністю лікування, а й із високою міжвізитною варіабельністю АТ [3], збільшенням кількості первинних і повторних госпіталізацій, а також тривалості перебування в стаціонарі [4, 5].
Незважаючи на вдосконалення діагностичних і терапевтичних втручань із доведеною перевагою в зменшенні серцево-судинної захворюваності та смертності, показники контролю АГ залишаються незадовільними. Результати систематичного аналізу популяційних досліджень із 90 країн продемонстрували високу розповсюдженість АГ в усьому світі та низький рівень її контролю [6]. Зокрема, за даними китайського дослідження, серед 364 тис. учасників АГ була наявна в 24,7%; лише 25,4% із них контролювали рівень АТ [7].
Причинами неконтрольованої АГ, окрім резистентної та вторинної, можуть бути «гіпертензія білого халата», відсутність прихильності пацієнта до терапії, лікарська інерція, котра часто зумовлює призначення неадекватної антигіпертензивної терапії, а також зміни психоемоційного стану (особливо тривожні розлади).
Одним із частих ускладнень неконтрольованої АГ є гіпертензивний криз. Згідно з класифікацією Українського товариства кардіологів, гіпертензивні кризи (залежно від наявності ускладнень із боку органів-мішеней) розподіляють на ускладнені та неускладнені [8]. Найчастіше гіпертензивні кризи ускладнюються ішемічним інсультом (24,5% випадків), гострим набряком легень (22,5% випадків), гіпертензивною енцефалопатією (16,3% випадків), гострою серцевою недостатністю (14,3% випадків), інфарктом міокарда чи нестабільною стенокардією (12% випадків), інтрацеребральним і субарахноїдальним крововиливом (4,5% випадків), еклампсією (4,5% випадків), гострою нирковою недостатністю (<10 випадків), розшаруванням аорти (2% випадків); інші ускладнення трапляються менш ніж у 1% випадків [9]. Неускладнені гіпертензивні кризи характеризуються також швидким і значним підвищенням АТ із клінічними проявами, але без розвитку гострого ураження органів-мішеней. Найчутливішим до раптового та значного підвищення АТ є головний мозок. За гострого підвищення АТ спостерігається зрив механізмів авторегуляції мозкового кровообігу, що спричиняє вазогенний набряк мозку.
Для профілактики та лікування набряково-больового синдрому, пов’язаного з різними станами, зокрема з лікворно-венозними порушеннями при хронічній ішемії мозку, черепно-мозкових травмах, мозковими інсультами, використовується L‑лізину есцинат®. Ефективність і безпечність L‑лізину есцинату вивчалась у 12 дослідженнях у 1727 пацієнтів (727 із них отримували цей препарат додатково до стандартної терапії) [10]. Дія зазначеного лікарського засобу забезпечується речовинами, котрі входять до його складу, – сапоніну есцину з плодів кінського каштана та незамінної амінокислоти L‑лізину. L‑лізину есцинат® нормалізує судинно-тканинну проникність, має виражений протинабряковий, венотонізуючий та ендотеліопротекторний ефекти [10, 11].
Метою зазначеного дослідження було вивчення впливу препарату L‑лізину есцинат® (виробництва ПАТ «Галичфарм») на швидкість досягнення цільового АТ, стану церебральної гемодинаміки та функції ендотелію з оцінкою показників якості життя госпіталізованих пацієнтів із неконтрольованою АГ.
Матеріали та методи
До випробування було залучено 60 пацієнтів із неконтрольованою АГ (середній вік – 59,9±1,5 року; чоловіки – 22,4%, жінки – 77,6%), які перебували на лікуванні у відділі гіпертонічної хвороби ДУ «ННЦ «Інститут кардіології ім. М. Д. Стражеска» НАМН України». Більшість пацієнтів були госпіталізовані через гіпертензивний криз (53 особи), 7 хворих потребували госпіталізації з інших причин. Усі залучені пацієнти надали інформовану згоду на участь у дослідженні. До випробування не залучали пацієнтів за таких умов: відома підвищена чутливість до препарату L‑лізину есцинат® або його компонентів; наявність вторинної АГ, міокардиту, вад серця, котрі потребують хірургічного лікування, декомпенсованої серцевої недостатності, цукрового діабету в стадії декомпенсації та/або з епізодами гіпоглікемії в анамнезі, інфекційних захворювань; вагітність і грудне вигодовування; печінкова й ниркова недостатність; злоякісні новоутворення; супутня терапія з використанням лікарських засобів зі схожими на досліджуваний препарат фармакологічними ефектами чи механізмом дії.
На етапі скринінгу всім пацієнтам були проведені реєстрація скарг, збір анамнезу, загальноклінічне обстеження, що включало вимірювання частоти серцевих скорочень (ЧСС), офісного АТ медичним працівником і вимірювання АТ пацієнтом за відсутності медичного персоналу, фізикальне та неврологічне обстеження, електрокардіографія, добове моніторування АТ (ДМАТ), біохімічне дослідження крові.
Вимірювання офісного АТ здійснювалося відповідно до Настанови Міжнародного товариства з гіпертензії (2020) [12] в один і той самий час щодня лікарем, а також на перший, третій, п’ятий, сьомий, дев’ятий і десятий дні дослідження; вимірювання АТ проводилося за відсутності медичного персоналу. Використовували прилад для автоматичного вимірювання АТ OMRON M10-IT з можливістю програмування, що дає змогу вимірювати АТ пацієнтом без участі медичного персоналу (аналогічний метод вимірювання АТ застосовувався в дослідженні SPRINT). ДМАТ проводили за стандартною методикою на етапі скринінгу та після завершення дослідження з використанням приладу Meditech 04.
Стан церебрального кровотоку оцінювали за допомогою дуплексного сканування екстра- й інтракраніальних артерій, яке проводили на апараті Sonoline Omnia (Siemens, Німеччина) за стандартною методикою на початку та наприкінці дослідження [13].
Визначали діаметри загальної (ЗСА), внутрішньої (ВСА), зовнішньої (ЗоСА) сонних артерій і товщину комплексу інтима-медіа (ТКІМ) у ділянці бляшки, а також показники кровотоку за ЗСА, ВСА, ЗоСА, середньої (СМА), передньої, задньої (ЗМА) мозкових і основної (ОА) артерій, які включали максимальну систолічну (ЛСШК), мінімальну діастолічну швидкість кровотоку (ЛДШК), а також розраховували їхній індекс резистивності (ІР), швидкість кровотоку базальними венами та великою веною мозку.
Для оцінки стану цереброваскулярної реактивності проводили тест із затримкою дихання; використовували усереднену за часом максимальну швидкість кровотоку в СМА з двох боків і обчислювали середній із двох боків показник до та після проведення проби (з подальшим розрахунком індексу реактивності).
Для оцінки ендотеліального механізму регуляції судинного тонусу використовували пробу з компресією плечової артерії, котру проводили відповідно до загальноприйнятої методики, дотримуючись усіх необхідних умов [14].
Для визначення рівня тривоги та депресії використовували опитувальник «Госпітальна шкала тривоги та депресії» HADS (Hospital Anxiety and Depression Scale), що містить 14 запитань і складається з двох підшкал по 7 запитань у кожній: HADS-D (depression) – на виявлення депресії, HADS-А (anxiety) – на виявлення тривожності. Кожен пункт пацієнти оцінювали від 0 до 3 балів за вираженістю симптомів протягом останнього тижня. Загальний бал вираховували шляхом додавання балів за всіма відповідями окремо для підшкал HADS-D і HADS-А. Якщо сума балів, набрана за підшкалою тривоги/депресії, перебувала в діапазоні 0-7, – депресія відсутня, якщо становила 8-10 балів, – депресія є субклінічно вираженою, якщо дорівнювала >11 балів, – клінічно вираженою [15].
Оцінку якості життя проводили за візуальною аналоговою шкалою (ВАШ) оцінки стану пацієнта в балах від 1 до 10, де 1 бал – найгірші стан і самопочуття, зумовлені симптомами захворювання, котрі пацієнт може собі уявити, 10 балів – найкращий настрій і самопочуття хворого. Водночас використовували опитувальник САН, за допомогою якого оцінювали самопочуття, активність і настрій. Результати опитувальника САН оцінювали за балами та розраховували середнє арифметичне як загалом, так і окремо для активності, самопочуття та настрою. Критерієм хорошого стану були оцінки >4 балів. Під час проведення опитувань використовувалася стандартна процедура відповідей на запитання без участі сторонніх осіб і медичного персоналу. Дані про хворого документував лікар.
Інтенсивність головного болю визначали за допомогою ВАШ. Зміни інтенсивності болю вважали об’єктивними й істотними, якщо значення ВАШ відрізнялося від попереднього більш ніж на 1,3 бала (13 мм).
Усі пацієнти, залучені до випробування, отримували лікування відповідно до протоколу надання допомоги пацієнтам з АГ, затвердженого наказом Міністерства охорони здоров’я України № 384 від 24.05.2012, яке включало комбіновану антигіпертензивну терапію, статини, антитромбоцитарні та цукрознижувальні препарати (за наявності показань).
Пацієнти були розподілені на дві групи: основну – 30 хворих (із них 80,0% становили жінки) та контрольну – 30 пацієнтів (83,3% – жінки). Додатково до стандартної терапії АГ хворим основної групи був призначений препарат L‑лізину есцинат® (розчин для інфузій) виробництва ПАТ «Галичфарм» по 10 мл 0,1% розчину для ін’єкцій, розведеного в 100 мл фізіологічного розчину NaCl, внутрішньовенно крапельно впродовж 20 хв 1 р/добу протягом 10 днів.
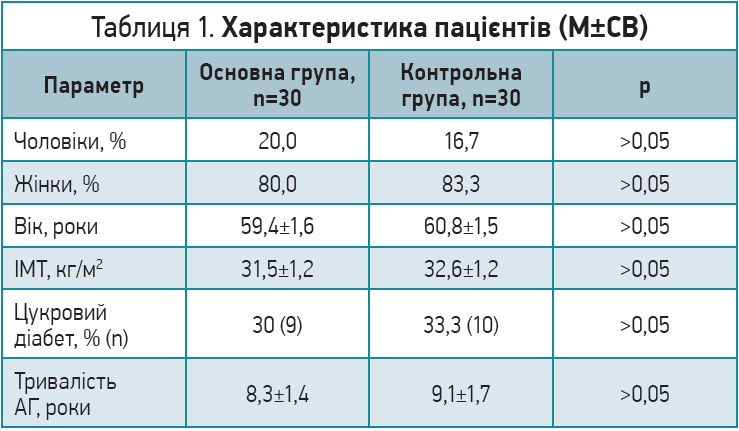
Пацієнти основної групи та групи контролю були співставними за віком, статтю, рівнем АТ, тривалістю АГ, індексом маси тіла (ІМТ), частотою цукрового діабету та рівнем глікемії (табл. 1).
Усі пацієнти приймали антигіпертензивну терапію, що включала 4 препарати (37% хворих), 3 препарати (47% пацієнтів) і 2 препарати (16% хворих). В основній і контрольній групах розподіл частоти кількості застосованих препаратів був співставним. В основній і контрольній групах більшість пацієнтів приймали статини (в основній групі – 76,1% хворих, у контрольній – 74,5% пацієнтів).
Отримані дані обробляли за допомогою методів варіаційної статистики з використанням програми SPSS 10.0. Для кількісних змінних висновки про наявність неоднорідності зроблені на основі порівняння за допомогою критерію Стьюдента (з правкою Уелча) для нормально розподілених даних або критерію Манна-Уїтні, якщо дані хоча би в одній групі не підлягали нормальному розподілу. Кількісні показники наведено у вигляді середньої величини (М) із відповідним стандартним відхиленням від середньої величини (СВ).
Результати й обговорення
На момент залучення до випробування пацієнти обох груп скаржилися на головні болі (переважно в ділянці потилиці), що були зазвичай пов’язані з підвищенням АТ, мали розпираючий характер; середній бал за ВАШ становив 8,7±0,3 бала – в основній групі та 8,9±0,3 бала – в контрольній. Наприкінці періоду спостереження всі пацієнти відзначали зменшення частоти й інтенсивності головного болю, що було продемонстровано в динаміці балів ВАШ: 2,3±0,4 бала – в основній групі та 5,2±0,4 бала – в контрольній (р<0,001 в обох випадках). Слід зазначити, що в основній групі головний біль регресував у перші дні (до 3-го дня) від початку захворювання.
Зменшення головного болю супроводжувалося покращенням загального самопочуття, про що свідчать також зміни показників ВАШ оцінки стану пацієнта й опитувальника САН.
На початку дослідження в пацієнтів обох груп інтегральний показник якості життя, котрий оцінювали за результатами ВАШ оцінки стану пацієнта, був співставним: в основній групі 3,7±0,5 бала, в контрольній – 3,9±0,3 бала. До завершення випробування цей показник зріс в основній групі у 2,1 раза, в групі контролю – в 1,6 раза та становив відповідно 7,8±0,3 та 6,2±0,3 бала, при цьому різниця показників між двома групами наприкінці дослідження була достовірною (р=0,03).
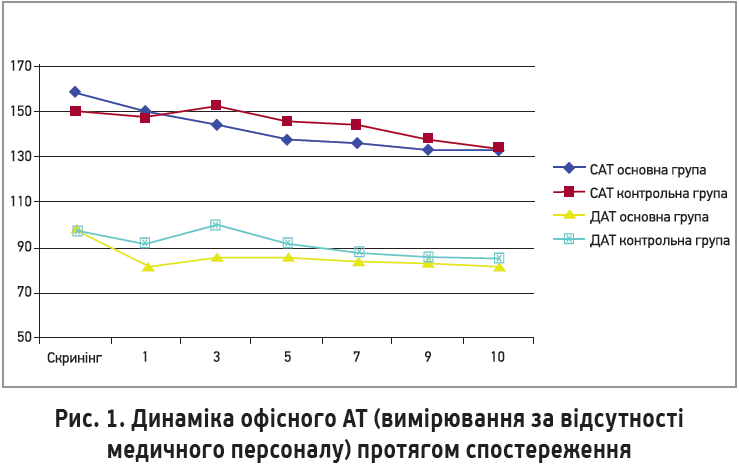
Про покращення стану пацієнтів на тлі додавання до антигіпертензивної терапії L‑лізину есцинату також свідчать результати тестування за опитувальником САН, що підтверджується достовірним збільшенням загального бала з 4,2±0,2 до 5,3±0,4 (р=0,02) в пацієнтів основної групи й опосередковано відображає покращення якості життя хворих. При ретельному аналізі результатів проведеного опитування виявлено, що збільшення загального бала за шкалою САН відбулося здебільшого за рахунок покращення самопочуття (збільшення бала самопочуття з 3,6±0,3 до 5,1±0,3; р=0,01); також збільшилися активність (збільшення бала активності з 4,2±0,2 до 5,3±0,2; р=0,03) та настрій (збільшення бала настрою з 4,8±0,3 до 5,7±0,3; р=0,03). У контрольній групі ми також відзначили зміни показників у бік покращення, проте ці зміни були достовірно меншими порівняно з основною групою (рис. 1).
Тривога й депресія є значними чинниками розвитку та погіршення перебігу АГ. Неадекватні психологічні й емоційні реакції – тригери підвищення АТ, що зумовлюють втрату чи погіршення контролю АТ [16, 17]. У нашому дослідженні покращення самопочуття супроводжувалося зменшенням тривожних проявів у обстежених пацієнтів обох груп. Так, на початку обстеження в основній і контрольній групах за допомогою госпітальної шкали тривоги й депресії була виявлена субклінічна тривога в 17 пацієнтів основної групи та 16 хворих групи контролю. Після завершення випробування в основній групі субклінічна тривога була виявлена в 4 пацієнтів, а в основній – у 10 хворих.
Отже, додавання до стандартної антигіпертензивної терапії L‑лізину есцинату госпіталізованим пацієнтам із неконтрольованою АГ сприяє покращенню якості життя, загального самопочуття, зменшенню головного болю та проявів тривоги.
Пацієнти обох груп мали співставний вихідний рівень офісного АТ. Аналіз динаміки показників офісних САТ і ДАТ продемонстрував достовірне зниження АТ наприкінці періоду спостереження в обох групах, що свідчить про ефективність підібраної антигіпертензивної терапії. Водночас величина зниження АТ була дещо більшою в основній групі порівняно з контрольною, але різниця не сягала межі достовірності: зниження офісного САТ становило 14,8% в основній групі та 13,7% – у контрольній (р=0,10), ДАТ – 14,7% в основній групі та 12,7% – у контрольній (р=0,13). Такі самі тенденції спостерігалися й для показників ДМАТ, зокрема середньодобовий САТ знизився на 12,7% в основній групі та на 12,3% – у контрольній (р=0,15), середньодобовий ДАТ – на 10,2 та 9,6% відповідно (р=0,09). Аналогічні тенденції відзначалися й для ступеня зниження САТ і ДАТ у денний і нічний періоди доби. Достовірних змін ЧСС за період спостереження не відбулося. Частота досягнення цільового рівня АТ була співставною в обох групах і становила в основній групі – 93%, у групі контролю – 91%.
Показники АТ, отримані під час вимірювання за відсутності медичного персоналу, були дещо нижчими за показники, отримані під час вимірювання медичним працівником, що узгоджується з даними літератури та пов’язане з відсутністю ефекту «білого халата». Аналіз динаміки отриманих показників продемонстрував, що пацієнти основної групи досягли цільового рівня АТ у середньому на четверту добу, а пацієнти контрольної групи – на сьому (з подальшим утриманням АТ на досягнутому рівні).
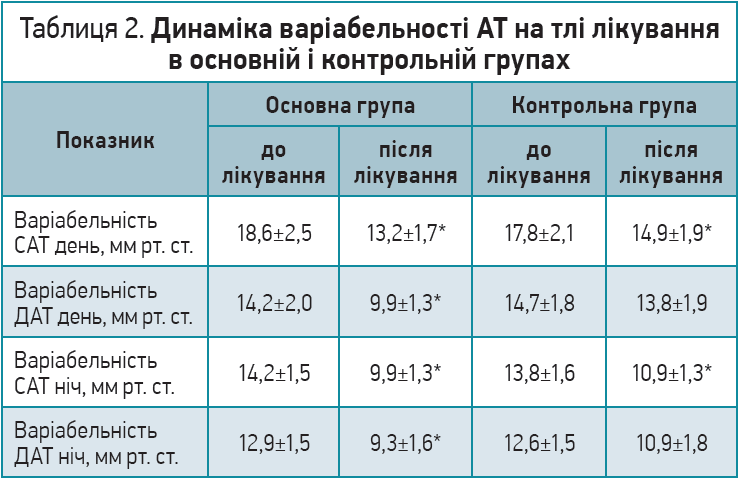
Відомо, що зростання варіабельності АТ пов’язане з підвищеним ризиком розвитку серцево-судинних ускладнень. У нашому дослідженні на тлі додавання препарату L‑лізину есцинат® до стандартної антигіпертензивної терапії встановлено достовірне зменшення варіабельності АТ за добу, день і ніч: наприкінці періоду спостереження ми виявили її зниження в денний період із 18,6±2,0 до 13,2±1,7 мм рт. ст. (р=0,003), у нічний період – із 14,2±2,0 до 9,9±1,3 мм рт. ст. (р=0,01). У групі контролю на тлі антигіпертензивної терапії варіабельність САТ зменшилася меншою мірою, ДАТ – достовірно не змінилася (табл. 2).
Оцінка динаміки величини нічного зниження АТ, який значимо пов’язаний зі ступенем ураження органів-мішеней, дала змогу встановити, що величина добового індексу САТ і ДАТ за період лікування достовірно не змінилися. В основній групі довірчий інтервал САТ до лікування становив 11,5±1,8%, після – 12,8±1,7% (р=0,45), а в групі контролю він дорівнював 11,3±1,8% та 10,9±1,8% (р=0, 63) відповідно.
Отже, в обох групах у результаті застосованої антигіпертензивної терапії спостерігалося достовірне співставне зниження показників АТ як офісних, так і середніх за добу, денний і нічний періоди, а також показників АТ, отриманих при вимірюванні за відсутності медичного персоналу, а додавання препарату L-лізину есцинат® до стандартної антигіпертензивної терапії сприяло швидшому досягненню цільового рівня АТ і зменшенню його варіабельності.
Відомо, що підвищення АТ зумовлює структурні зміни великих і мілких судин. На макросудинному рівні це проявляється потовщенням комплексу інтима-медіа, збільшенням просвіту судин і жорсткості судинної стінки, на мікрорівні – вазоконстрикцією, порушенням здатності до розтягнення, зниженням вазодилататорного резерву [18]. Головними механізмами регуляції судинного тонусу та забезпечення сталого органного кровотоку є ендотеліальний, метаболічний і міогенний [19].
Із метою вивчення впливу препарату L-лізину есцинат® на функцію ендотелію пацієнтам обох груп до та після лікування було проведено пробу ендотелійзалежної вазодилатації (ЕЗВД). На початку періоду спостереження індекс ЕЗВД в основній групі становив 6,6±0,73%, що не відрізнялося від показника групи контролю (6,50±0,9%) і засвідчувало порушення ендотеліальної функції (в нормі цей показник має бути >10%) в обстежених. Наприкінці періоду спостереження показник ЕЗВД достовірно зріс у пацієнтів обох груп. У хворих, яким додавали L-лізину есцинат®, спостерігали нормалізацію показника ЕЗВД у середньому по групі: він зріс до 10,6±0,6% (р=0,004 порівняно з вихідним значенням), тоді як у групі контролю його зростання було менш вираженим, але достовірним – до 9,5±0,9% (р=0,03). Достовірної різниці досягнутих значень між групами порівняння встановлено не було (р=0,23). Покращення індексу ЕЗВД в обох групах наприкінці дослідження найімовірніше пов’язане з досягненням цільового рівня АТ у більшості хворих обох груп і зменшенням ушкоджувальної дії високого АТ на ендотелій судин.
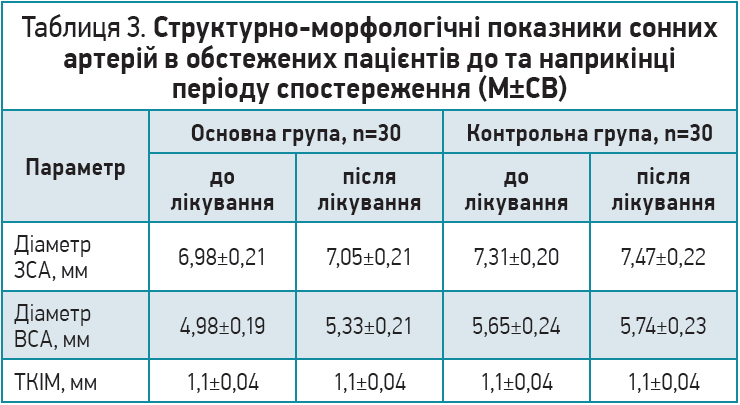
Із метою оцінки структурних параметрів і показників кровотоку пацієнтам з АГ було проведено дуплексне сканування магістральних екстра- й інтракраніальних артерій. За його результатами виявлено, що 47,5% пацієнтів основної групи та 44,9% хворих контрольної групи мали гемодинамічно незначимі атеросклеротичні бляшки. За період спостереження достовірних змін структурно-морфологічних показників сонних артерій виявлено не було (табл. 3).
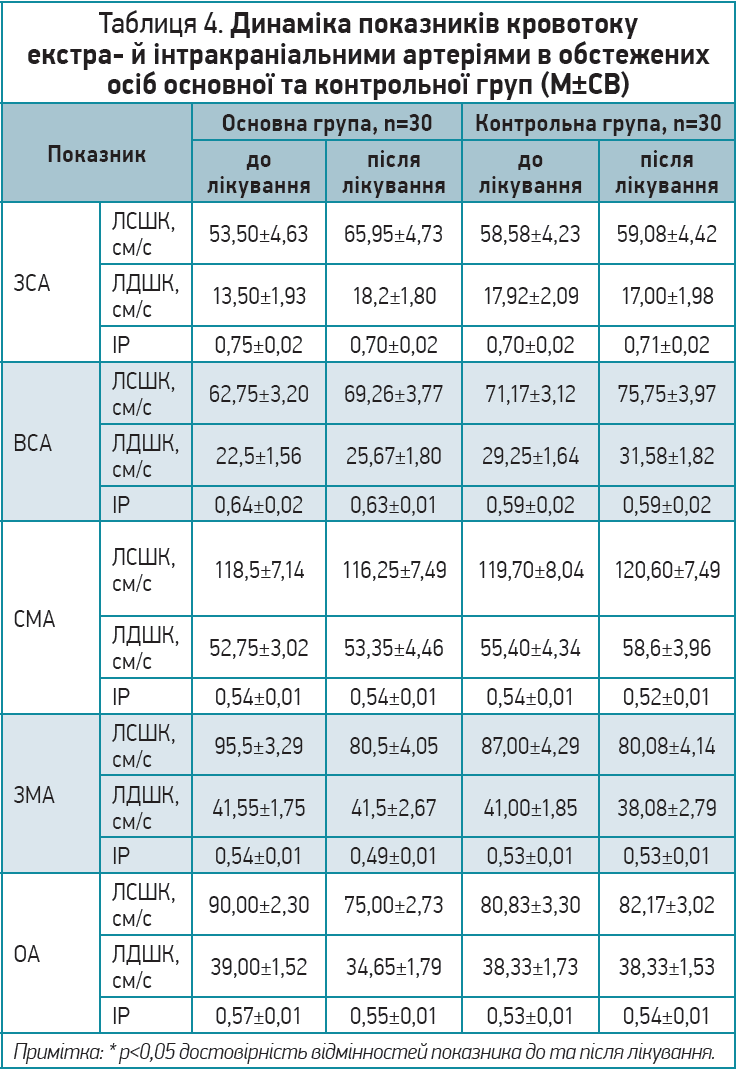
Аналогічна ситуація спостерігалася й для показників швидкості кровотоку екстра- й інтракраніальними артеріями в обох групах. Результати аналізу не виявили їхніх достовірних змін наприкінці періоду спостереження порівняно з такими на початку дослідження в пацієнтів обох груп (табл. 4).
Аналіз показника кровотоку базальними венами виявив, що пацієнти обох груп мали порушення інтракраніального венозного кровообігу, що проявлялося збільшенням швидкостей кровотоку ними; швидкість кровотоку базальними венами мозку становила 27,2±3,6 см/с – в основній групі, в контрольній – 25,7±3,5 см/с, а великими венами мозку дорівнювала 34±4,2 см/с – в основній групі та 33±4,2 см/с – у контрольній. Виявлені зміни можуть бути проявом синдрому доброякісної інтракраніальної гіпертензії, котра розвивається внаслідок швидкого підвищення АТ, що спричиняє зрив реакції авторегуляції мозкового кровообігу та вазогенний набряк головного мозку й має зворотний характер. Наприкінці дослідження в пацієнтів основної групи, котрим до стандартної терапії додавали L-лізину есцинат®, спостерігали достовірне зниження швидкостей кровотоку інтракраніальними венами: для базальних вен – на 25,4% (до 20,3±3,5 см/с; р=0,03), для великої вени мозку – на 25,6% (до 25,3±3,9 см/с; р=0,002) (рис. 2). У пацієнтів групи контролю, котрі отримували стандартну антигіпертензивну терапію, швидкості щодо досліджуваних вен наприкінці періоду спостереження не змінилися: базальними венами становили 25,4±3,5 см/с, великою веною мозку – 28,8±4,9 см/с (р>0,05). Отже, додавання препарату L-лізину есцинат® до стандартної терапії АГ сприяло нормалізації венозного інтракраніального кровотоку.
Наші дані узгоджуються з даними літератури, де було продемонстровано позитивний вплив на венозний кровоток у результаті додавання препарату L-лізину есцинат® до стандартної терапії. Проте в раніше проведені дослідження були залучені пацієнти з черепно-мозковою травмою, гострими порушеннями мозкового кровообігу, гіпертензивною енцефалопатією, а також хронічною ішемією мозку [10, 11, 20, 21]. Нами продемонстровано позитивний вплив L‑лізину есцинату в комплексній терапії госпіталізованих пацієнтів із неконтрольованою АГ.
У нашому дослідженні ми не виявили додаткового впливу на рівень АТ у результаті додавання препарату L-лізину есцинат® до стандартної терапії неконтрольованої АГ, що може бути пов’язано з оптимальною антигіпертензивною терапією та зниженням АТ до цільових рівнів. У деяких випробуваннях був виявлений додатковий вплив засобу L-лізину есцинат® на АТ. Так, Візир і співавт. установили, що додавання препарату L-лізину есцинат® до традиційного антигіпертензивного лікування сприяло підвищенню ефективності терапії гіпертензивних кризів, при цьому достовірна різниця у величинах САТ між групами хворих була відзначена вже через 60 хв, 72 та 96 год від початку лікування. ДАТ також був нижчим у групі, що отримувала L-лізину есцинат®; він досягав достовірної різниці на третю добу, при цьому динаміка АТ мала стійку тенденцію до зниження (без повторних кризів) [22].
Більшість проведених досліджень присвячені вивченню дії препарату L-лізину есцинат®, пов’язаної з умістом есцину, котрий забезпечує саме протинабрякову та венотонічну дії. Водночас відсутні роботи щодо вивчення дії, пов’язаної з L‑лізином, – незамінною амінокислотою, що проявляє анксіолітичний ефект завдяки впливу на серотонінові рецептори. Нами було виявлено зменшення кількості пацієнтів із субклінічною тривогою на тлі додавання до стандартної антигіпертензивної терапії препарату L-лізину есцинат®, що в поєднанні з нормалізацією венозного інтракраніального кровотоку, ймовірно, сприяло покращенню контролю АТ у коротший термін і зменшенню його коливань протягом доби.
Висновки
- Порушення інтракраніального венозного кровообігу у вигляді збільшення швидкостей кровотоку базальними венами та великою веною мозку було виявлено в госпіталізованих пацієнтів із неконтрольованою АГ. Їхній добовий профіль АТ характеризувався високою варіабельністю АТ у денний і нічний періоди часу, що асоціювалося з наявністю в них субклінічної тривоги.
- Додавання до комбінованої антигіпертензивної терапії препарату L-лізину есцинат® в госпіталізованих пацієнтів із неконтрольованою АГ сприяло покращенню мозкового венозного кровообігу, що проявлялося зниженням на 25% швидкостей кровотоку базальними венами та великою веною мозку.
- Покращення мозкового венозного кровообігу на тлі додавання препарату L-лізину есцинат® асоціювалося зі швидшим досягненням цільового АТ – в середньому на четверту добу, тоді як у контрольній – на сьому добу лікування.
- Призначення пацієнтам з АГ препарату L-лізину есцинат® паралельно з адекватною антигіпертензивною терапією зумовило покращення психосоматичного стану пацієнтів і зменшення проявів тривожного синдрому, що, ймовірно, сприяло суттєвішому зниженню короткострокової (середньоденної та середньонічної) варіабельності АТ.
Список літератури знаходиться в редакції.
Медична газета «Здоров’я України 21 сторіччя» № 6 (499), 2021 р.