22 жовтня, 2021
Ефективність агомелатину в лікуванні симптомів тривоги та функціональних порушень у пацієнтів із генералізованим тривожним розладом
Генералізований тривожний розлад (ГТР) – хронічне захворювання, що характеризується надмірним занепокоєнням, психічними та соматичними проявами тривоги у пацієнтів. ГТР є найпоширенішим тривожним розладом у практиці надання первинної медичної допомоги і часто асоційований із супутніми патологіями, як-то велика депресія та інші тривожні розлади, а також значущими психосоціальними порушеннями та економічними витратами. При веденні осіб із ГТР продемонстровано переваги низки ліків різних класів, а також когнітивно-поведінкової терапії (КПТ) як важливого варіанту лікування. Проте багато хворих не відповідають на лікування чи не переносять рекомендовані нині методи фармакотерапії або ж мають суттєві побічні явища. D.J. Stein et al. проаналізували дані сучасних досліджень про вплив агомелатину як альтернативного препарату на симптоми тривоги та функціональні порушення у пацієнтів із ГТР. Матеріал опубліковано у виданні Advances in Therapy (2021; 38: 1567‑1583).
Агомелатин – препарат групи антидепресантів, що діє як антагоніст рецепторів 5-HT2C та агоніст рецепторів мелатоніну (MT1 та MT2) (de Bodinat et al., 2010; Millan et al., 2003). Таким чином, агомелатин має відмітний механізм дії порівняно з антидепресантами, які інгібують захоплення моноамінів, із бензодіазепінами, що діють на ГАМКергічну систему, та з буспіроном як частковим агоністом 5-HT1A-рецепторів (Craske et al., 2017). Імовірно, що зазначений подвійний механізм дії лежить в основі клінічної ефективності та сприятливої переносимості агомелатину в осіб, що страждають на велику депресію (Guardiola-Lemaitre et al., 2014). Також препарат чинить виразний анксіолітичний ефект, поліпшує сон і циркадні ритми (Millan et al., 2005).
Вплив агомелатину при лікуванні ГТР вивчали у межах двох короткострокових подвійних сліпих випробувань та одного дослідження щодо запобігання розвитку рецидивів (Levitan et al., 2015; Stein et al., 2014). Було продемонстровано ефективність і хорошу переносимість агомелатину в дозуванні 25‑50 мг порівняно з есциталопрамом та плацебо. У додатковому дослідженні III фази агомелатин у дозі 25 мг показав переваги у коротко- та довгочасній терапії ГТР, а вторинний аналіз даних підтвердив його користь у пацієнтів із тяжкими проявами ГТР (Stein et al., 2018). Однак відповідно до нещодавнього систематичного огляду літератури, масштабних рандомізованих плацебо-контрольованих випробувань, присвячених ефективності агомелатину при ГТР, бракує (Slee et al., 2019).
D.J. Stein et al. (2021) розглянули результати трьох короткочасних рандомізованих подвійних сліпих плацебо-контрольованих клінічних досліджень за участю дорослих пацієнтів із ГТР, які отримували терапію агомелатином. Автори мали на меті визначити частоту досягнення ремісії та відповіді на лікування, а також переваги препарату в пацієнтів із виразними симптомами тривоги.
Матеріали й методи дослідження
Критерії відбору пацієнтів та розподіл за групами
Для включення у дослідження пацієнти повинні були мати відповідний бал за шкалою Гамільтона для оцінки тривоги (HAM-A), госпітальною шкалою тривоги та депресії (HADS) та шкалою оцінки депресії Монтгомері – Асберг. У всіх випробуваннях первинні наслідки терапії тривалістю не менш ніж 12 тижнів оцінювали за HAM-A на вихідному рівні та 2, 4, 8 і 12-му тижнях. Анксіолітичну клінічну ефективність визначали за загальним балом HAM-A порівняно з показником на початку спостереження. Відповідь на лікування, тобто зменшення проявів ГТР щонайменше на 50% від вихідного рівня за HAM-A, та ремісія симптомів (загальна оцінка HAM-A) вважалися вторинними результатами. Функціональні порушення визначали за допомогою шкали оцінки непрацездатності Шихана (SDS).
Загалом було проаналізовано дані 669 пацієнтів: 340 на лікуванні агомелатином у дозуванні 25‑50 мг і 329 – у групі плацебо; середній вік учасників становив 43,7±13,5 та 42,9±12,7 року відповідно. Клінічно значущих відмінностей між групами за демографічними чи клінічними характеристиками не спостерігалося.
У процесі двох досліджень використовували гнучке дозування агомелатину 25‑50 мг, у третьому – фіксоване (25 мг; дані хворих, які приймали по 10 мг, не були включені в аналіз). Дозу препарату підвищували у разі недостатнього поліпшення стану на 2-му (дослідження 1) та 4-му тижні (дослідження 2) у 12,9% пацієнтів. Усі хворі відповідали критеріям первинного діагнозу ГТР згідно з Діагностичним і статистичним посібником із психічних розладів, 4-го переглянутого видання (DSM‑IV-TR). Додаткове медикаментозне лікування та психотерапію не застосовували. Аналіз безпеки включав повідомлення про несприятливі події під час кожного візиту, життєво важливі показники, результати стандартних лабораторних тестів, зокрема для оцінки функції печінки.
Загалом дослідження завершили 84% пацієнтів. Причинами вибування переважно були брак ефективності (18 учасників у групі агомелатину, 45 – плацебо) та немедичні причини (12 та 14 пацієнтів відповідно).
Статистичний аналіз
За допомогою повного набору аналізів (FAS) реєстрували базові характеристики учасників та проводили оцінку ефективності в усіх рандомізованих пацієнтів, які приймали щонайменше одну дозу ліків на вихідному рівні та під час одного візиту впродовж лікування. Різницю між агомелатином і плацебо відповідно до загального бала за HAM-A та SDS у кінцевій точці визначали шляхом виконання дисперсійного аналізу. Метааналіз із застосуванням моделі випадкових ефектів слугував для оцінки загального ефекту терапії, відповіді пацієнтів на лікування та частоти досягнення ремісії у кінцевій точці. Для визначення гомогенності між ефектами лікування використовували кокранівський критерій однорідності, ступінь невідповідності I2 та форест-діаграми. Статистичний аналіз проводили за допомогою програмного забезпечення SAS, версії 9.2 (Кері, Північна Кароліна, США).
Результати дослідження
Оцінка симптомів тривоги
У всій досліджуваній популяції лікування агомелатином асоціювалося зі статистично більш значущим зниженням показника за HAM-A, ніж приймання плацебо: різниця при останньому вимірюванні порівняно з вихідним становила 6,30±2,51 бала. Відповідь на терапію мала місце у 67,1% пацієнтів групи агомелатину та у 32,5% – плацебо. Кількість хворих, яких необхідно пролікувати (NNT), становила 3,1. Ремісії симптомів за HAM-A було досягнуто у 38,8% пацієнтів, які отримували агомелатин, та у 17,3% осіб групи плацебо (NNT=4,6). Слід відзначити, що на 4-му тижні 30,21% учасників на тлі застосування агомелатину відповіли на лікування порівняно з 14,95% групи плацебо.
У пацієнтів із виразнішими проявами тривоги (87,7% загальної популяції) агомелатин показав переваги над плацебо із загальним показником 6,49±2,71 бала. Частота відповіді на лікування становила 67,6% у групі агомелатину та 31,6% – плацебо (NNT=3,0), частота ремісії – 38,2 і 17,5% відповідно (NNT=4,9).
Оцінка функціональних порушень
За загальним показником SDS у кінцевій точці було виявлено суттєвіші переваги агомелатину порівняно з плацебо в усіх дослідженнях: різниця при останньому вимірюванні порівняно з вихідним становила 5,11±1,81 бала. Спостерігалися статистично значущі відмінності на користь агомелатину порівняно із плацебо за трьома підшкалами SDS: при оцінюванні функціонування на роботі – 1,73±0,59 бала, соціальних функцій – 1,74±0,64 бала, поводження у родині – 1,70±0,63 бала. Функціональну відповідь було отримано у 79,1% пацієнтів групи агомелатину та у 43,2% – групи плацебо (NNT=3,0), функціональної ремісії досягли 55,2 і 25,4% відповідно (NNT=3,4).
Для пацієнтів із загальним балом 25 за HAM-A на вихідному рівні показник за SDS під час останнього вимірювання був значно нижчим у групі агомелатину, ніж плацебо, з різницею у 5,24±1,97 бала. Значущі відмінності на користь агомелатину порівняно із плацебо були виявлені за всіма підшкалами. Функціональна відповідь на лікування мала місце у 77,6% пацієнтів групи агомелатину та у 41,2% – плацебо (NNT=3,0), а функціональної ремісії досягли 54,4 та 23,7% відповідно (NNT=3,3).
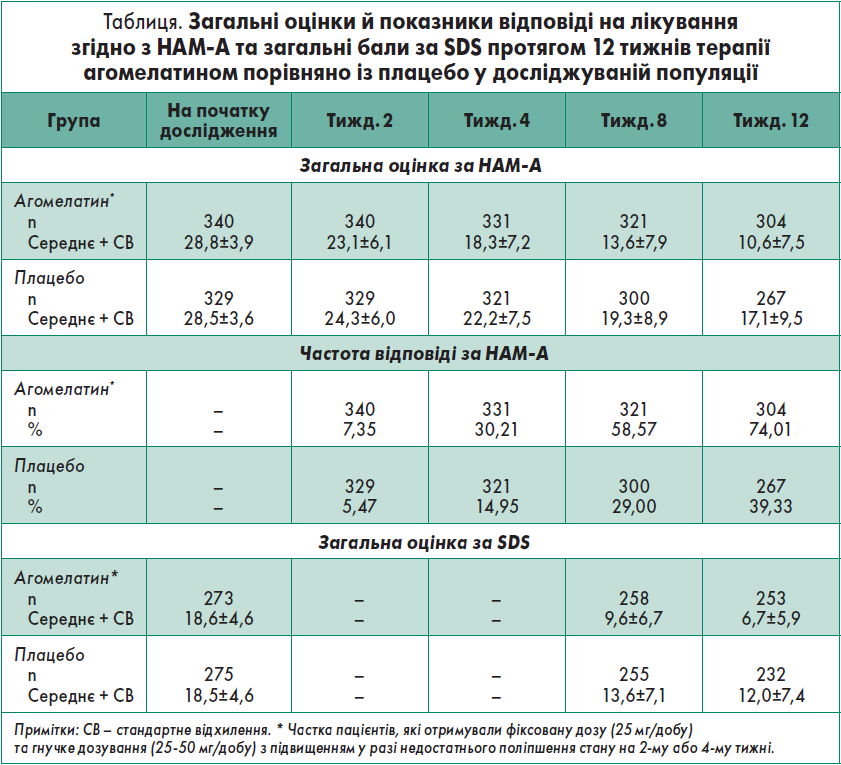
Загальні оцінки й показники відповіді на лікування згідно із HAM-А та загальні бали за SDS протягом 12 тижнів терапії агомелатином порівняно із прийманням плацебо у досліджуваній популяції наведені у таблиці.
Аналіз безпеки
Частки пацієнтів, які повідомили про щонайменше одне несприятливе явище протягом 12-тижневого періоду лікування у групах агомелатину та плацебо, були зіставними (44,3 та 41,3% відповідно). Найпоширенішими побічними ефектами при лікуванні агомелатином були головний біль, назофарингіт та нудота. Через небажані реакції припинили терапію по 2,1% учасників у групах агомелатину та плацебо відповідно. Серйозні побічні ефекти були зафіксовані в однакової кількості пацієнтів обох груп (по 1,2%); найчастішими у групі агомелатину були підвищення рівнів активності аспартат- та аланінамінотрансферази.
Обговорення
Аналіз первинних результатів показав клінічно значущу різницю на користь агомелатину порівняно із плацебо у 6,3 бала згідно з показниками за шкалою HAM-A. Про це свідчать високі частки тих, хто відповів на лікування вже з 2-го тижня (67,1%) та досяг ремісії (38,8%). Отримані висновки узгоджуються з даними сукупного аналізу інших рандомізованих клінічних випробувань селективних інгібіторів зворотного захоплення серотоніну та інгібіторів зворотного захоплення серотоніну й норадреналіну в лікуванні ГТР (Goodman et al., 2005; Pae et al., 2015). Також схожі докази були виявлені внаслідок проведення систематичного огляду та мережевого метааналізу, відповідно до яких серед великої групи фармакологічних препаратів агомелатин продемонстрував високу ефективність та переносимість, якщо тільки не спричиняв реакції з боку печінки (Slee et al., 2019).
Автори зауважують, що у пацієнтів із виразними проявами ГТР часто мають місце значні соціальні та професійні проблеми, підвищений ризик суїцидів та нижчий рівень відповіді на лікування (Wittchen et al., 2011; Stein et al., 2008). Результати цього аналізу узгоджуються з даними нещодавнього дослідження ефективності агомелатину та підтверджують його користь щодо зменшення симптомів тривоги і функціональних порушень у вибірці хворих на тяжку форму ГТР (Stein et al., 2018).
Ступінь відновлення пацієнтів із ГТР після отриманої терапії можна визначити як за зменшенням проявів симптомів, так і показниками загального функціонування (Stein et al., 2009). Оцінка працездатності та функціональних показників все частіше визнається важливою в рутинній практиці та клінічних дослідженнях. Відповідно до загального аналізу балів шкали за SDS D.J. Stein et al. (2021) виявили, що агомелатин сприяв статистично значущому поліпшенню функціонування пацієнтів порівняно із плацебо після 12 тижнів лікування за всіма доменами. Після короткочасної терапії функціональну відповідь було встановлено у 79,1% хворих, а функціональну ремісію – у 55,2%.
При цьому клінічно значуще поліпшення стану пацієнтів відповідало отриманому в попередніх роботах із вивчення впливу агомелатину (Kennedy et al., 2016; Udristoiu et al., 2016).
В осіб із ГТР часто спостерігається суттєве зниження якості життя. Швидке та ефективне лікування симптомів тривоги агомелатином може сприяти значному поліпшенню глобального функціонування хворих (Hoffman et al., 2008; Wilson et al., 2015). Наведені переваги препарату разом зі сприятливим профілем безпеки можуть свідчити про хорошу прихильність до лікування.
Висновки
За отриманими результатами, доведено швидку та значну ефективність і переносимість агомелатину в дозуванні 25‑50 мг при короткочасному лікуванні функціональних порушень і симптомів ГТР, зокрема його тяжчих проявів. Загальна частота побічних явищ при застосуванні агомелатину та плацебо була зіставною. Таким чином, з огляду на встановлені ефективність, безпеку та переносимість, агомелатин можна вважати терапевтичним варіантом вибору для пацієнтів із ГТР. Необхідні додаткові клінічні дослідження щодо зменшення симптомів та поліпшення якості життя хворих на ГТР, оскільки функціональна ремісія є важливим критерієм видужання. Також корисним буде подальше вивчення переваг агомелатину при інших тривожних розладах.
Підготувала Олена Коробка
Тематичний номер «Неврологія, Психіатрія, Психотерапія» № 3 (58) 2021 р.