23 жовтня, 2021
Практичні рекомендації щодо вторинної профілактики ішемічного інсульту та транзиторної ішемічної атаки
У 2021 р. Американська асоціація серця й Американська асоціація з вивчення інсульту (АНА/ASA) спільно розробили оновлену практичну настанову з профілактики ішемічного інсульту або транзиторної ішемічної атаки (ТІА). Документ містить вичерпні рекомендації щодо діагностичної оцінки, контролю факторів судинного ризику, лікування відповідно до етіологічних аспектів тощо. Основна мета – допомогти лікарям у прийнятті зважених рішень при веденні цих хворих залежно від індивідуальних потреб, уподобань та клінічного стану як у США, так і в усьому світі. Клас рекомендацій вказує на їх силу, що охоплює передбачувану величину та визначення користі пропорційно ризику, а рівень доказовості – на якість даних клінічних випробувань та інших джерел, на яких ґрунтуються клінічні стратегії, втручання, методи лікування або діагностичні тестування. Рекомендації перевірено на предмет відповідності науково-доказовим принципам і схвалено Американською асоціацією неврологічних хірургів (AANS), Конгресом неврологічних хірургів (CNS), Товариством судинної та інтервенційної неврології (SVIN). Окрім того, Американська академія неврології (AAN) підтвердила їх цінність як навчального посібника для неврологів. Пропонуємо до вашої уваги ключові положення даної настанови.
Щороку в США у 795 тис. осіб трапляється інсульт, зокрема у 87% (690 тис.) – ішемічний; 185 тис. переносять інсульт повторно (Virani et al., 2020). Приблизно 240 тис. пацієнтів щороку зазнають TIA (Kleindorfer et al., 2005). Високу ймовірність повторного інсульту або ТІА можна зменшити шляхом проведення відповідної вторинної профілактики. У когортних дослідженнях було продемонстроване зниження частоти повторних інсультів і ТІА впродовж останніх років завдяки поліпшенню стратегій вторинної профілактики (Johnston et al., 2000; Amarenco, 2016).
Виникненню переважної більшості інсультів можна запобігти за допомогою контролю артеріального тиску (АТ), здорового харчування, регулярної фізичної активності та відмови від куріння. За наявними даними, 90,5% глобального тягаря інсульту пов’язано з факторами ризику, що піддаються модифікації (Feigin et al., 2016). Було показано, що цілеспрямований вплив на множинні чинники ризику зумовлює додаткові переваги у межах вторинної профілактики; зокрема, використання ацетилсаліцилової кислоти (АСК), статинів та антигіпертензивних препаратів у поєднанні з корегуванням режиму харчування та фізичними вправами дозволяє знизити ризик повторних судинних подій на 80% (Hackam et al., 2007).
Ключовими компонентами вторинної профілактики інсульту є оцінка й усунення перешкод у дотриманні режиму терапії та здорового способу життя. Якщо під час застосування препаратів для вторинної профілактики інсульту в пацієнта розвинувся повторний епізод, важливо з’ясувати, чи приймав він призначені ліки та за можливості визначити й усунути фактори, що зумовили брак прихильності до терапії, перш ніж скасувати її через потенційну неефективність.
Застосування класу рекомендацій та рівня доказовості при оцінюванні клінічних стратегій, терапевтичних втручань і методів або діагностичних інструментів під час лікування пацієнтів
Клас (сила) рекомендації
- клас 1 (сильна): переваги >>> ризики
- клас 2а (помірна): переваги >> ризики
- клас 2а (слабка): переваги ≥ ризики
- клас 3: переваг немає (помірна): переваги = ризики
- клас 3: шкода (сильна): ризики > переваги
Рівень (якість) доказів
Рівень А
- докази високої якості з ≥1 РКД
- метааналіз даних високоякісних РКД
- ≥1 РКД, підкріплене даними якісних реєстрових досліджень
Рівень B-R (рандомізовані)
- докази помірної якості з ≥1 РКД
- метааналіз даних РКД помірної якості
Рівень B-NR (нерандомізовані)
- докази помірної якості з ≥1 добре спланованих, якісно виконаних нерандомізованих обсерваційних або реєстрових досліджень
- метааналіз даних таких досліджень
Рівень C‑LD (обмежені дані)
- результати рандомізованих/нерандомізованих обсерваційних/реєстрових досліджень з обмеженнями у дизайні або при проведенні
- метааналіз даних таких досліджень
- дані фізіологічних або механістичних досліджень за участю людей
Рівень C-EO (експертна думка)
- консенсусні експертні висновки на основі клінічного досвіду
Примітка: РКД – рандомізовані контрольовані дослідження.
Діагностична оцінка в межах профілактики вторинного інсульту
Пацієнтам із підозрою на інсульт або ТІА рекомендовано проводити електрокардіографію (ЕКГ) для виявлення фібриляції (ФП) і тріпотіння передсердь та контролю інших супутніх серцево-судинних захворювань (ССЗ) (1, B-R) (Sposato et al., 2015; Micheli et al., 2012). Також діагностична оцінка даної когорти хворих важлива для розуміння етіології та планування оптимальних стратегій запобігання розвитку повторного інсульту, при цьому обстеження має бути розпочате та завершене протягом 48 год із моменту появи симптомів інсульту (1, B-NR) (Arsava et al., 2016; Petty et al., 2000). В осіб із симптоматичним інфарктом головного мозку або ТІА, які є кандидатами на реваскуляризацію, слід проводити неінвазивну візуалізацію шийного відділу каротидної артерії за допомогою ультразвукового дослідження, комп’ютерно-томографічної (КТА) або магнітно-резонансної ангіографії (МРА) для виявлення стенозу (1, B-NR) (Kim et al., 2018; Debrey et al., 2008).
Окрім того, пацієнтам із підозрою на інсульт або ТІА рекомендовано виконати комп’ютерну (КТ) чи магнітно-резонансну томографію (МРТ) головного мозку для підтвердження діагнозу симптоматичної ішемії головного мозку (1, B-NR) (Kvistad et al., 2019; Madsen et al., 2016). Особам із підтвердженим діагнозом необхідно зробити аналіз крові, зокрема загальний, для визначення протромбінового, часткового тромбопластинового часу, рівня глюкози, глікованого гемоглобіну (HbA1С), креатиніну та ліпідного профілю натще / не натще, щоб отримати уявлення про наявні фактори ризику інсульту та встановити терапевтичні цілі (1, B-NR) (Roquer et al., 2014; Agarwal et al., 2019).
У пацієнтів із криптогенним інсультом доцільно провести ехокардіографію (ЕхоКГ) із/без контрасту для оцінки можливих джерел церебральної емболії (2а, B-R) (Holmes et al., 2014; Katsanos et al., 2016). У цій популяції хворих за відсутності протипоказань для антикоагулянтної терапії з метою виявлення інтермітивної ФП обґрунтованим є тривалий моніторинг ритму за допомогою мобільної кардіологічної амбулаторної телеметрії, імплантації петлевого реєстратора або іншого підходу (2а, B-R) (Gladstone et al., 2014; Wachter et al., 2016).
Якщо в осіб із підозрою на ішемічний інсульт на КТ або МРТ не виявлено симптоматичного інфаркту мозку, для підтвердження діагнозу доцільне виконання контрольної КТ чи МРТ головного мозку (2а, B-R) (Hammoud et al., 2016; Nadeau et al., 2016). Якщо у пацієнтів із підозрою на ТІА первинна візуалізація за допомогою КТ або МРТ головного мозку не показала симптоматичного інфаркту мозку, слід виконати повторну МРТ для прогнозування ризику раннього інсульту та підтвердження діагнозу (2а, B-R) (Kelly et al., 2016; Wardlaw et al., 2014).
Для виявлення факторів ризику інсульту або чинників, що провокують його розвиток, у пацієнтів із криптогенним інсультом за клінічних показань доцільно застосовувати тести для виявлення: спадкового або набутого стану гіперкоагуляції; інфекцій крові або спинномозкової рідини; інфекцій, що можуть викликати васкуліт центральної нервової системи, як-от ВІЛ та сифіліс; вживання психоактивних речовин (ПАР); маркерів системного запалення; генетичних та спадкових захворювань (2а, C‑LD) (Hobohm et al., 2016; Bersano et al., 2016).
У пацієнтів з ішемічним інсультом або ТІА неінвазивна візуалізація інтракраніального відділу великих артерій та візуалізація екстракраніальної вертебробазилярної артеріальної системи за допомогою МРА або КТА можуть бути ефективними для виявлення атеросклерозу, розшарування, хвороби моямоя або інших етіологічно значущих васкулопатій (2а, C‑LD) (Liebeskind et al., 2014; Gulli et al., 2013).
У пацієнтів з ішемічним інсультом і планом лікування, що включає антикоагулянти, можна розглянути доцільність проведення КТ або МРТ головного мозку до початку терапії для оцінки геморагічної трансформації та остаточного розміру інфаркту (2b, B-NR) (Paciaroni et al., 2018).
У хворих, які перенесли емболічний інсульт із невизначеною причиною (ESUS), виконання трансезофагеальної ЕхоКГ, КТ чи МРТ серця може бути доцільним для виявлення можливих кардіоаортальних джерел або транскардіальних шляхів церебральної емболії (2а, C‑LD) (Khariton et al., 2014; Liberman et al., 2017).
В осіб з ішемічним інсультом або ТІА, у яких передбачається закриття відкритого овального вікна (ВОВ), слід провести скринінг на наявність серцевого шунта справа наліво за допомогою транскраніальної доплерографії з емболодетекцією (Mazzucco et al., 2018).
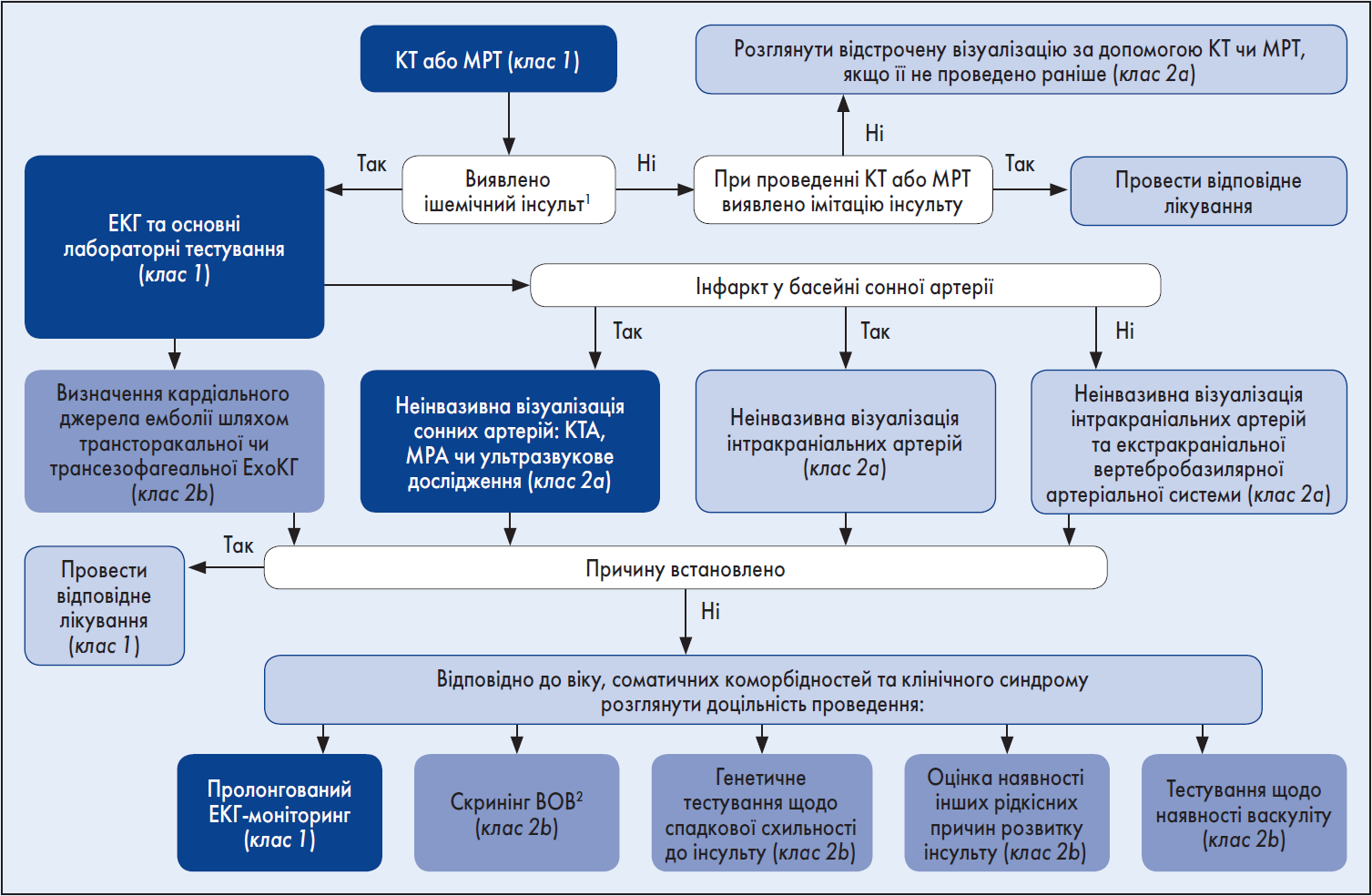
Алгоритм оцінки пацієнтів із діагнозом інсульту з метою оптимізації профілактики повторного ішемічного інсульту представлений на рисунку 1.
Рис. 1. Алгоритм оцінки пацієнтів із діагнозом інсульту з метою оптимізації профілактики повторного ішемічного інсульту
Примітки: 1 Якщо у хворих наявний минущий неврологічний дефіцит, клінічно характерний для ТІА, його слід обстежувати так само, як і пацієнтів, що перенесли ішемічний інсульт із підтвердженим візуалізацією інфарктом мозку. 2 Трансторакальна, трансезофагеальна ЕхоКГ, транскраніальна доплерографія, МРТ або КТ серця.
Адаптовано за D.O. Kleindorfer et al., 2021
Контроль судинних факторів ризику
Модифікація способу життя
Харчування. Пацієнтам з інсультом та ТІА слід радити дотримуватися середземноморської дієти та вживати продукти з низьким вмістом жирів, щоб знизити ризик повторного інсульту (2а, B-R) (Estruch et al., 2018; Rees et al., 2019). Особам з артеріальною гіпертензією (АГ), які перенесли інсульт чи ТІА, варто рекомендувати обмежити споживання солі щонайменше до 2,5 г/добу, щоб зменшити ймовірність серцево-судинних подій, включно з інсультом (2а, B-R) (He et al., 2020; Sacks et al., 2001).
Фізична активність. Пацієнтам з інсультом або ТІА, які здатні виконувати фізичні навантаження, рекомендовані аеробні вправи помірної інтенсивності принаймні по 10 хв чотири рази на тиждень або високої – щонайменше 20 хв двічі на тиждень для зниження ризику повторного інсульту та комбінованої кінцевої точки, що включає рецидив інсульту, інфаркт міокарда (ІМ) або смерть через ССЗ (1, C‑LD) (Turan et al., 2017). Особам після інсульту чи ТІА, які здатні та хочуть збільшити фізичні навантаження, заняття разом із консультуванням щодо зміни фізичної активності можуть бути корисними для зменшення кардіометаболічних факторів ризику (2а, B-R) (Deijle et al., 2017; Wang et al., 2019).
Якщо у пацієнтів, що перенесли інсульт, спостерігається знижена здатність до фізичних навантажень, для вторинної профілактики інсульту на додаток до звичайної реабілітації може бути корисним контроль програми фізичних вправ фізіотерапевтом або фахівцем із кардіологічної реабілітації (2а, С-ЕО). Особам з інсультом або ТІА, які ведуть малорухомий спосіб життя, зокрема сидять тривалий час без перерв, доцільно рекомендувати робити інтервали по 3 хв стоячи або легкі фізичні вправи кожні 30 хв для зміцнення серцево-судинної системи (2b, B-NR) (English et al., 2018).
Відмова від куріння. Із хворими після інсульту або ТІА, які курять, слід провести консультування з/без медикаментозного лікування (як-то нікотинова замісна терапія, бупропіон або варениклін) (1, А) та переконати їх відмовитися від цієї згубної звички (або хоча б зменшити кількість викурених сигарет щодня), щоб знизити ризик повторного інсульту (1, B-NR) (Chen et al., 2019; Huang et al., 2019). Пацієнтам з інсультом або ТІА для зменшення ймовірності рецидиву інсульту рекомендовано уникати пасивного куріння (1, B-NR) (Pan et al., 2019; Lee et al., 2017).
Вживання психоактивних речовин. Особам з ішемічним інсультом або ТІА, які вживають >2 і >1 алкогольних напоїв на день для чоловіків та жінок відповідно, слід радити відмовитися від алкоголю або зменшити споживання для зниження ризику інсульту (1, B-NR) (Ricci et al., 2018; Patra et al., 2010). Пацієнтів після інсульту чи ТІА, які приймають стимулятори, а також хворих на інфекційний ендокардит при вживанні ПАР внутрішньовенно важливо переконати, що це являє серйозну загрозу для здоров’я, та їм слід зупинитися (1, С-ЕО). Пацієнтам з інсультом або ТІА, які страждають на розлад, пов’язаний зі зловживанням ПАР, варто рекомендувати звернутися до спеціалізованих служб, що допоможуть впоратися із залежністю (1, С-ЕО).
Ведення пацієнтів з артеріальною гіпертензією
У пацієнтів з АГ, які перенесли інсульт або ТІА, лікування тіазидним діуретиком, інгібітором ангіотензинперетворювального ферменту (іАПФ) або блокаторами рецепторів ангіотензину II (БРА) є корисним для зниження АТ та ризику повторного інсульту (1, А) (Zonneveld et al., 2018; Liu et al., 2009). Для більшості хворих рекомендований рівень АТ становить <130/80 мм рт. ст. з метою зменшення ймовірності повторного інсульту та судинних подій (1, B-R) (Kitagawa et al., 2019; Katsanos et al., 2017).
Окрім того, пацієнтам цієї когорти для максимальної ефективності терапії необхідно призначати індивідуальні схеми приймання препаратів з огляду на супутні захворювання та їхні уподобання, а також фармакологічний клас ліків (1, B-NR) (Lakhan et al., 2009; Wang et al., 2016). В осіб без АГ в анамнезі, які перенесли інсульт чи ТІА і мають середній АТ ≥130/80 мм рт. ст., лікування антигіпертензивними засобами може мати переваги для зниження ризику повторного інсульту, ішемічної хвороби серця та інших судинних подій (2, B-R) (Mant et al., 2016; Bath et al., 2017).
Лікування гіперліпідемії в межах вторинної профілактики інсульту
Терапія та моніторинг ліпідів крові. Ефект гіполіпідемічної терапії у пацієнтів після ішемічного інсульту вивчали у рандомізованих контрольованих дослідженнях (РКД) SPARCL та TST (Amarenco et al., 2006, 2020). В обох було виявлено значну користь від лікування, що знижує рівень холестерину (ХС), у запобіганні судинним подіям, включно з інсультом. Зокрема, результати SPARCL показали, що аторвастатин у дозі 80 мг/добу дієвіше порівняно із плацебо зменшував кількість рецидивів інсульту в пацієнтів з ішемічним інсультом без підтвердженої ішемічної хвороби серця, значущих кардіальних джерел емболії та з рівнем ХС ліпопротеїнів низької щільності (ЛПНЩ) >2,6 ммоль/л (>100 мг/дл) (1, А). Так, протягом середнього періоду спостереження 4,9 року первинна кінцева точка інсульту сталася у 11,2% хворих, які використовували аторвастатин, та у 13,1% у групі плацебо.
Дані, отримані у цих двох випробуваннях, надалі були підтримані доказами численних РКД ліпідних гіполіпідемічних препаратів, відповідно до яких хворі з високим ризиком атеросклеротичних ССЗ мають отримувати високоінтенсивну статинотерапію (80 мг/добу аторвастатину чи 20 мг/добу розувастатину) (AHA/ACC, 2018).
Для зменшення ймовірності розвитку серйозних серцево-судинних подій особам з ішемічним інсультом або ТІА та атеросклерозом (внутрішньочерепних, каротидних, коронарних артерій чи аорти) за потреби рекомендовано гіполіпідемічну терапію статинами, а також езетимібом, метою якої є досягнення концентрації ХС ЛПНЩ <1,8 ммоль/л (<70 мг/дл) (1, А) (Amarenco et al., 2020). Хворим, що перенесли ішемічний інсульт, із дуже високим ризиком (визначається як інсульт + інше серйозне атеросклеротичне захворювання або інсульт + декілька клінічних станів високого ризику), які приймають статини та езетиміб у максимально переносимих дозах і все ще мають рівень ХС ЛПНЩ >1,8 ммоль/л, доцільно призначити інгібітор пропротеїн конвертази субтилізин/кексин типу 9 (PCSK9) для запобігання атеросклеротичним подіям (2а, B-NR) (Sabatine et al., 2017; Schwartz et al., 2018).
У пацієнтів з інсультом або ТІА й гіперліпідемією слід оцінювати прихильність до зміни способу життя та ефективність препаратів, що зменшують уміст ЛПНЩ, шляхом вимірювання рівня ліпідів натще та відповідних показників безпеки через 4‑12 тижнів після початку приймання статинів або корегувати дозу кожні 3‑12 місяців залежно від необхідності аналізу дотримання режиму лікування чи безпеки (1, А) (Chiavaroli et al., 2018; Benner et al., 2004).
Лікування гіпертригліцеридемії. У хворих після ішемічного інсульту або ТІА із рівнем тригліцеридів (ТГ) натще 1,5-5,6 ммоль/л (135‑499 мг/дл), ХС ЛПНЩ 1-2,6 ммоль/л (41‑100 мг/дл), HbA1С <10% та без панкреатиту, ФП чи тяжкої серцевої недостатності (СН) в анамнезі, що перебувають на статинотерапії помірної або високої інтенсивності, лікування ікозапентетилом у дозі 2 г двічі на добу є доцільним для зниження ризику повторного інсульту (2а, B-R) (Bhatt et al., 2019; Tanaka et al., 2008). У пацієнтів із виразною гіпертригліцеридемією (вміст ТГ натще ≥5,7 ммоль/л, або ≥500 мг/дл) слід виявити та усунути причини розвитку гіпертригліцеридемії. Якщо концентрація ТГ постійно зростає, необхідне подальше її зниження, щоб зменшити ймовірність виникнення атеросклеротичного ССЗ, шляхом дотримання режиму харчування із дуже низьким вмістом жирів і значною кількістю жирних кислот омега‑3, відмови від вживання рафінованих вуглеводів / алкоголю та, якщо це потрібно для запобігання гострому панкреатиту, призначення терапії фібратами (2а, B-NR) (Christian et al., 2012; Rhodes et al., 2015).
Контроль рівня глюкози. В осіб з ішемічним інсультом або ТІА, які також мають цукровий діабет (ЦД), мета контролю глікемії повинна бути індивідуалізована, залежно від ризику виникнення побічних явищ, індивідуальних характеристик та уподобань хворих. До того ж для більшості пацієнтів, особливо віком <65 років та без супутніх захворювань, які обмежують якість життя, рекомендоване досягнення цільової концентрації HbA1С ≤7% для зменшення ймовірності розвитку мікросудинних ускладнень (1, А) (UKPDS Group, 1998). Лікування ЦД має включати глюкозознижувальні препарати із доведеною користю для серцево-судинної системи з метою зниження ризику серйозних небажаних кардіоваскулярних подій у майбутньому, як-то інсульт, ІМ та серцево-судинна смерть (1, B-R) (Gerstein et al., 2019; Neal et al., 2017). Також у даній когорті хворих для досягнення цільових показників глікемії та зменшення факторів ризику інсульту показана комплексна медична допомога, зокрема консультування щодо способу життя, лікувальне харчування, навчання самоконтролю ЦД, підтримка та терапія (1, С-ЕО).
У пацієнтів із предіабетом та ішемічним інсультом або ТІА оптимізація способу життя, тобто дотримання здорового харчування, регулярні фізичні навантаження та відмова від куріння, може бути корисною для запобігання прогресуванню ЦД (2а, B-R) (Tuomilehto et al., 2001; Knowler et al., 2002). В осіб, які перенесли ТІА або ішемічний інсульт, доцільно проводити скринінг на предіабет/ЦД із вимірюванням HbA1С (2а, С-ЕО). Метформін може бути корисний для пацієнтів із предіабетом та ішемічним інсультом або ТІА, особливо особам з індексом маси тіла ≥35 кг/м2, віком до 60 років чи жінкам із гестаційним ЦД в анамнезі для контролю рівня цукру в крові та запобігання розвитку ЦД (2b, B-R) (DeFronzo et al., 2011; le Roux et al., 2017).
Для хворих на ЦД після ішемічного інсульту чи ТІА переваги інтенсивного контролю глюкози (досягнення HbA1С ≤7%) внаслідок гострої фази ішемічної події для профілактики повторного інсульту невідомі (2b, B-R) (Kelly et al., 2009; Ray et al., 2009). Якщо у пацієнтів мають місце інсулінорезистентність, HbA1С <7,0% і відсутні СН або рак сечового міхура, а після ТІА або ішемічного інсульту минуло ≤6 місяців, може бути розглянуте лікування піоглітазоном для запобігання повторному інсульту (2b, B-R) (Kernan et al., 2016).
Ожиріння. Пацієнтам з ішемічним інсультом чи ТІА, які мають надмірну вагу або ожиріння, рекомендовано схуднути для поліпшення профілю факторів ризику атеросклеротичних ССЗ (1, B-R) (Ikramuddin et al., 2013; Schauer et al., 2012). Хворим після ішемічного інсульту або ТІА, які страждають на ожиріння, слід пройти інтенсивну багатокомпонентну програму модифікації способу життя для досягнення стійкої втрати ваги (1, B-R) (LeBlanc et al., 2018; Kurth et al., 2002). В осіб з ішемічним інсультом або атеросклеротичними ССЗ під час епізоду необхідно розрахувати індекс маси тіла і потім робити це щорічно для виявлення та класифікації ожиріння (1, С-ЕО).
Обструктивне апное уві сні. У пацієнтів з ішемічним інсультом або TIA та обструктивним апное уві сні може бути корисним лікування за допомогою постійного позитивного тиску в дихальних шляхах (Jonas et al., 2017; Bravata et al., 2018). Окрім того, у таких хворих слід розглянути доцільність оцінки обструктивного апное сну для діагностики апное уві сні (Saletu et al., 2018; McEvoy et al., 2016).
Лікування відповідно до етіологічних аспектів
Атеросклероз великих артерій
Атеросклероз інтракраніального відділу великих артерій. Пацієнтам з інсультом або ТІА, спричиненими 50‑99% стенозом інтракраніального сегмента магістральної артерії (ІСМА), в межах антитромботичної терапії рекомендовано приймати АСК у дозі 325 мг/добу замість варфарину, щоб зменшити ймовірність повторного ішемічного інсульту та судинної смерті (1, B-R) (Chimowitz et al., 2005, 2011). В осіб із нещодавно (≤30 днів тому) перенесеним інсультом чи ТІА внаслідок тяжкого стенозу (70‑99%) ІСМА додавання 75 мг/добу клопідогрелю до АСК протягом 90 днів є доцільним для подальшого зниження ризику повторного інсульту (2а, B-NR) (Liu et al., 2015; Wong et al., 2010).
У хворих, які нещодавно (≤24 год тому) перенесли малий інсульт або ТІА високого ризику, із супутнім іпсилатеральним стенозом ІСМА >30% можна розглянути додавання 90 мг тикагрелору двічі на день до АСК протягом 30 днів для зменшення ймовірності повторного інсульту (2b, B-NR) (Amarenco et al., 2020). У пацієнтів з інсультом чи ТІА внаслідок 50‑99% стенозу ІСМА для зниження ризику повторного інсульту доцільно розглянути застосування 200 мг/добу цилостазолу в поєднанні з АСК або клопідогрелем (2b, C‑LD) (Uchiyama et al., 2015; Toyoda et al., 2019). Слід зазначити, що у цій когорті хворих користь клопідогрелю, комбінації АСК та дипіридамолу, лише тикагрелору або цилостазолу для вторинної профілактики інсульту вивчено недостатньо (2b, C-EO).
У пацієнтів з інсультом чи ТІА, спричинених 50‑99% стенозом ІСМА, рекомендовано підтримувати рівень систолічного АТ <140 мм рт. ст. (1, B-NR) (Amin-Hanjani et al., 2017).
У пацієнтів із тяжким стенозом ІСМА (70‑99%), симптомами, що активно прогресують, чи повторним ТІА/інсультом та систолічним АТ <140 мм рт. ст., які розпочали лікування АСК і клопідогрелем та отримують високоінтенсивну статинотерапію, переваги ангіопластики або встановлення стенту для запобігання розвитку ішемічного інсульту в ділянці стенозованої артерії невідомі (2b, C‑LD) (Alexander et al., 2019; Aghaebrahim et al., 2019). В осіб після інсульту або ТІА через виразний стеноз ІСМА не слід проводити ангіопластику та стентування як ініціальне лікування, навіть у хворих, які приймали антитромботичні засоби під час епізоду (3: завдає шкоди, А) (Lutsep et al., 2015; Wabnitz et al., 2018). У хворих після інсульту або ТІА внаслідок помірного стенозу ІСМА (50‑69%) ангіопластика чи стентування асоційовані з підвищеними захворюваністю та смертністю порівняно з медикаментозною терапією (3: завдає шкоди, B-NR) (Miao et al., 2012; Zaidat et al., 2015).
Пацієнтам з інсультом або ТІА, спричиненими 50‑99% стенозом або оклюзією ІСМА, екстракраніально-інтракраніальне шунтування не рекомендоване (3: переваг немає, B-R) (EC/IC Bypass Study Group, 1985).
Атеросклероз екстракраніального відділу великих артерій. Пацієнтам, які ≤6 місяців тому перенесли ТІА або ішемічний інсульт, що не призвів до інвалідності, та тяжким іпсилатеральним стенозом сонної артерії (70‑99%) необхідно провести каротидну ендартеректомію (КЕА) для зменшення ймовірності інсульту в майбутньому за умови, що ризик періопераційної захворюваності та смертності становить <6% (1, А) (Rothwell et al., 2003). В осіб після ішемічного інсульту чи ТІА із симптоматичним стенозом екстракраніального сегмента сонної артерії, яким заплановане стентування сонної артерії (ССА) або КEA, процедури слід виконувати за встановленого ризику перипроцедурного інсульту та летальних наслідків <6% для зменшення ймовірності побічних ефектів, пов’язаних із хірургічним втручанням (1, А) (Barnett et al., 1991). Хворим зі стенозом сонної артерії та ТІА або інсультом для зниження ризику повторного епізоду рекомендовано інтенсивну фармакотерапію антитромбоцитарними, гіполіпідемічними й антигіпертензивними засобами (1, А).
В осіб із нещодавно перенесеною ТІА або ішемічним інсультом та іпсилатеральним помірним стенозом сонної артерії (50‑69%), підтвердженим за допомогою катетерної або неінвазивної візуалізації, доцільно провести КЕА для зменшення ймовірності рецидиву інсульту, залежно від специфічних для хворого факторів, як-то вік, стать та супутні захворювання. При цьому ризик періопераційної захворюваності та смертності має оцінюватися як <6% (1, B-R) (Rothwell et al., 2003).
У пацієнтів віком ≥70 років з інсультом або ТІА, щодо яких розглядається питання про проведення реваскуляризації сонної артерії, доцільно вибрати КEA замість ССА, щоб знизити частоту перипроцедурних інсультів (2а, B-R) (Howard et al., 2016). У хворих із запланованою реваскуляризацією протягом одного тижня після індексного інсульту варто віддати перевагу КEA замість ССА для зменшення частоти перипроцедурних інсультів (2а, B-R) (Rantner et al., 2017).
У пацієнтів із неінвалідизувальною ТІА або інсультом, яким показано реваскуляризацію, слід проводити процедуру протягом двох тижнів після основного епізоду, щоб збільшити ймовірність сприятливого результату без інсультів (2a, C‑LD) (Rothwell et al., 2004). Якщо в осіб із симптоматичним тяжким стенозом (≥70%) є анатомічні або клінічні умови, які підвищують ризик проведення хірургічного втручання (наприклад, радіаційно-індукований стеноз або рестеноз після КЕА), доцільним є ССА для зниження частоти перипроцедурних ускладнень (2a, C‑LD) (Yadav et al., 2004).
У симптомних пацієнтів із помірним або низьким ризиком ускладнень, пов’язаних з ендоваскулярним втручанням, коли виявлений за допомогою неінвазивної візуалізації стеноз внутрішньої сонної артерії становить ≥70% або катетерної – більш ніж 50%, а очікувана частота перипроцедурного інсульту або смерті є <6%, ССА можна розглядати як альтернативу КEA для профілактики інсульту, особливо в осіб зі значними коморбідними ССЗ, що схильні до розвитку серцево-судинних подій після ендартеректомії (2b, A) (Brott et al., 2010). У хворих із нещодавно (протягом останніх шести місяців) перенесеним інсультом або ТІА користь реваскуляризації транскаротидної артерії для запобігання повторному інсульту та ТІА лишається невизначеною (2b, B-NR) (Schermerhorn et al., 2019).
Пацієнтам із нещодавно перенесеною ТІА або ішемічним інсультом при ступені стенозу <50% не слід проводити реваскуляризацію за допомогою КEA або CСА для зниження ризику інсульту в майбутньому (3: переваг немає, А) (Rothwell et al., 2003). Особам із нещодавньою (протягом останніх 120 днів) ТІА / ішемічним інсультом, іпсилатеральним атеросклеротичним стенозом або оклюзією середньої мозкової чи сонної артерії екстракраніально-інтракраніальне шунтування не рекомендоване (3: переваг немає, А) (Powers et al., 2011).
Хворим із нещодавнім симптоматичним стенозом екстракраніального відділу хребетної артерії для зниження ризику інсульту рекомендоване інтенсивне медикаментозне лікування, що включає антитромбоцитарну терапію, зменшення вмісту ліпідів та контроль АТ (1, А). У симптомних пацієнтів з ішемічним інсультом або ТІА та стенозом позачерепного сегмента хребетної артерії користь стентування недостатньо вивчено незалежно від оптимального фармакологічного лікування (2b, B-R) (Markus et al., 2019). Окрім того, у даної категорії хворих не встановлено переваги відкритих хірургічних процедур, зокрема ендартеректомії та транспозиції хребетної артерії, незважаючи на належну фармакотерапію (2b, C-EO).
Атеросклеротичні бляшки в дузі аорти. Пацієнтам з інсультом або ТІА та ознаками атероми дуги аорти рекомендовано призначити інтенсивне регулювання рівня ліпідів до цільового ХС ЛПНЩ <1,8 ммоль/л (<70 мг/дл) для запобігання повторному інсульту (1, B-R) (Amarenco et al., 2020). На додаток, у таких хворих для попереджання рецидиву інсульту слід проводити терапію антиагрегантами (1, С‑LD) (Johnston et al., 2018; Antithrombotic Trialists Collaboration, 2002).
Хвороба моямоя та патологія дрібних судин
В осіб із хворобою моямоя та ішемічним інсультом або ТІА в анамнезі може бути корисною хірургічна реваскуляризація із прямим/непрямим екстракраніально-інтракраніальним шунтуванням для профілактики ішемічного інсульту чи ТІА (2а, С‑LD) (Jeon et al., 2018; Li et al., 2019). Також у цій когорті пацієнтів імовірні переваги застосування антитромбоцитарного лікування, зазвичай монотерапії АСК, для профілактики ішемічного інсульту або ТІА (2а, С‑LD) (Jang et al., 2017; Zhao et al., 2017).
У пацієнтів після ішемічного інсульту, пов’язаного із захворюванням дрібних судин, користь цилостазолу для вторинної профілактики інсульту невідома (2b, B-R) (Pan et al., 2019; Wang et al., 2013).
Кардіоемболія
Фібриляція передсердь. Пацієнтам із неклапанною ФП та інсультом або ТІА рекомендовано призначати пероральні антикоагулянти, наприклад апіксабан, дабігатран, едоксабан, ривароксабан або варфарин, для зменшення ймовірності повторного інсульту (1, А) (Granger et al., 2011; Giugliano et al., 2013). Особам із ФП та інсультом чи ТІА для зниження ризику рецидиву інсульту показана пероральна антикоагулянтна терапія, незалежно від того, чи є ФП пароксизмальною, персистентною чи стійкою (1, B-R) (Healey et al., 2012). Окрім того, таким хворим без мітрального стенозу (від помірного до тяжкого) або механічного клапана серця для зменшення ймовірності повторного інсульту рекомендовані апіксабан, дабігатран, едоксабан або ривароксабан, але не варфарин (1, B-R) (Mason et al., 2012; Olesen et al., 2012). Це було підтверджено в межах чотирьох масштабних рандомізованих досліджень та отримано послідовні докази неменшої ефективності для зниження тромбоемболічного ризику і зменшення ймовірності кровотеч при застосуванні зазначених препаратів порівняно з антагоністами вітаміну К (Patel et al., 2011; Giugliano et al., 2013).
Пацієнтам із тріпотінням передсердь та інсультом або ТІА для зниження ризику рецидиву інсульту показано антикоагулянтну терапію, аналогічну такій при ФП (1, B-NR) (Healey et al., 2012). В осіб із перенесеним інсультом, що мають високий ризик геморагічної конверсії на тлі ФП, доцільно відкласти застосування пероральних антикоагулянтів більш ніж на 14 днів для зменшення імовірності внутрішньочерепних крововиливів (2a, B-NR) (Seiffge et al., 2019; Ahmed et al., 2017).
У хворих, що перенесли ТІА на тлі неклапанної ФП, доцільно розпочати антикоагулянтне лікування одразу після індексної події, щоб знизити ризик повторного інсульту (2a, C-EO). У пацієнтів з інсультом або ТІА внаслідок неклапанної ФП, які мають протипоказання для проведення антикоагулянтної терапії впродовж життя, але здатні переносити її щонайменше 45 днів, можна розглянути питання про черезшкірне закриття вушка лівого передсердя за допомогою пристрою Watchman, щоб зменшити ймовірність рецидиву інсульту та кровотеч (2b, B-R) (Holmes et al., 2014; Reddy et al., 2017).
В осіб з інсультом та низьким ризиком геморагічної конверсії на тлі ФП може бути доцільним розпочати приймання антикоагулянтів через 2‑14 днів після індексної події, щоб зменшити ймовірність повторного інсульту (2b, B-NR) (Abdul-Rahim et al., 2015) У пацієнтів із ФП та інсультом чи ТІА, які мають термінальну стадію ниркової недостатності або перебувають на діалізі, доцільно розглянути застосування апіксабану або варфарину (якщо показано, із корегуванням дози), щоб знизити ризик рецидиву інсульту (2b, B-NR).
У великому ретроспективному дослідженні в осіб із ФП на діалізі, які приймали апіксабан та варфарин, було виявлено на 28% нижчу частоту кровотеч у тих, хто лікувався апіксабаном (Siontis et al., 2018). Ці дані підтверджують ефективність використання апіксабану як альтернативного методу антикоагулянтної терапії у пацієнтів із ФП, які перебувають на діалізі.
Захворювання клапанів серця. Пацієнтам з ішемічним інсультом чи ТІА та клапанною ФП (із мітральним стенозом від помірного до тяжкого ступеня або механічним клапаном серця) рекомендовано призначати варфарин для зниження ризику повторного інсульту чи ТІА (1, B-R) (Pan et al., 2017; Avezum et al., 2015). В осіб із захворюванням клапанів серця (за винятком помірного/тяжкого мітрального стенозу або наявності механічного клапана серця), ішемічним інсультом або ТІА та ФП необхідно використовувати пероральні антикоагулянти подвійної дії, як-то апіксабан, дабігатран, ривароксабан та едоксабан замість варфарину (Ezekowitz et al., 2016; Eikelboom et al., 2013). У пацієнтів із механічним мітральним клапаном та ішемічним інсультом або ТІА в анамнезі до заміни клапана слід застосовувати АСК в дозі 75‑100 мг/добу на додаток до варфарину за цільового міжнародного нормалізованого відношення (МНВ) у діапазоні 2,5‑3,5 для зменшення ймовірності розвитку тромбозу та рецидиву інсульту чи TIA (1, C‑LD) (Hering et al., 2005; Massel et al., 2013).
Хворим, що перенесли ішемічний інсульт або ТІА, страждають на захворювання нативного аортального клапана або неревматичне ураження мітрального клапана, наприклад кальциноз мітрального кільця чи пролапс мітрального клапана, та не мають ФП або інших показань для антикоагулянтної терапії, рекомендовано призначити антитромбоцитарне лікування для зниження ризику повторного інсульту/ТІА (1, C-ЕО). У пацієнтів із біопротезом аортального або мітрального клапана, ішемічним інсультом чи ТІА в анамнезі до заміни клапана та за відсутності інших показань для використання антикоагулянтів через 3‑6 місяців після встановлення клапана доцільною є тривала терапія АСК, на відміну від антикоагулянтів, для зменшення ймовірності рецидиву інсульту або ТІА (1, C-ЕО).
У пацієнтів з ішемічним інсультом чи ТІА та інфекційним ендокардитом, у яких, незважаючи на відповідну антибіотикотерапію, спостерігаються рецидивна емболія та персистивні вегетації, доцільним є раннє хірургічне втручання (під час першої госпіталізації до завершення повного терапевтичного курсу антибіотиків) для зменшення ймовірності рецидиву емболії, якщо немає ознак внутрішньочерепного крововиливу або значних неврологічних пошкоджень (2a, B-NR) (Garcнa-Cabrera et al., 2013; Kang et al., 2012).
В осіб з ішемічним інсультом або ТІА в анамнезі та механічним аортальним клапаном проведення антикоагулянтної терапії варфарином вищої інтенсивності для досягнення МНВ у діапазоні 2,5‑3,5 або додавання АСК по 75‑100 мг/добу може бути корисним для зниження ризику тромбоемболічних подій (2а, C-ЕО). У пацієнтів з ішемічним інсультом або ТІА та ендокардитом нативного лівобічного клапана, які мають рухливі вегетації довжиною більш ніж 10 мм, доцільно розглянути раннє хірургічне втручання (під час першої госпіталізації до завершення повного терапевтичного курсу антибіотиків) для зменшення ймовірності повторної емболії, якщо немає ознак внутрішньочерепної кровотечі або значних неврологічних пошкоджень (2b, B-NR) (Thuny et al., 2005; Durante Mangoni et al., 2003).
У пацієнтів з ішемічним інсультом або ТІА та інфекційним ендокардитом рання операція на клапані (під час першої госпіталізації до завершення повного курсу антибіотикотерапії) можлива за наявності показань до хірургічного втручання та за відсутності ознак внутрішньочерепної кровотечі або суттєвих неврологічних порушень (2b, B-NR) (Barsic et al., 2013). В осіб з інфекційним ендокардитом та великим ішемічним інсультом у разі внутрішньочерепної кровотечі доцільно розглянути відстрочення операції на клапані щонайменше на чотири тижні, якщо гемодинамічні показники хворого стабільні (2b, B-NR).
У пацієнтів з ішемічним інсультом або ТІА та механічними клапанами серця лікування дабігатраном заподіює шкоду (3: завдає шкоди, B-R) (Eikelboom et al., 2013).
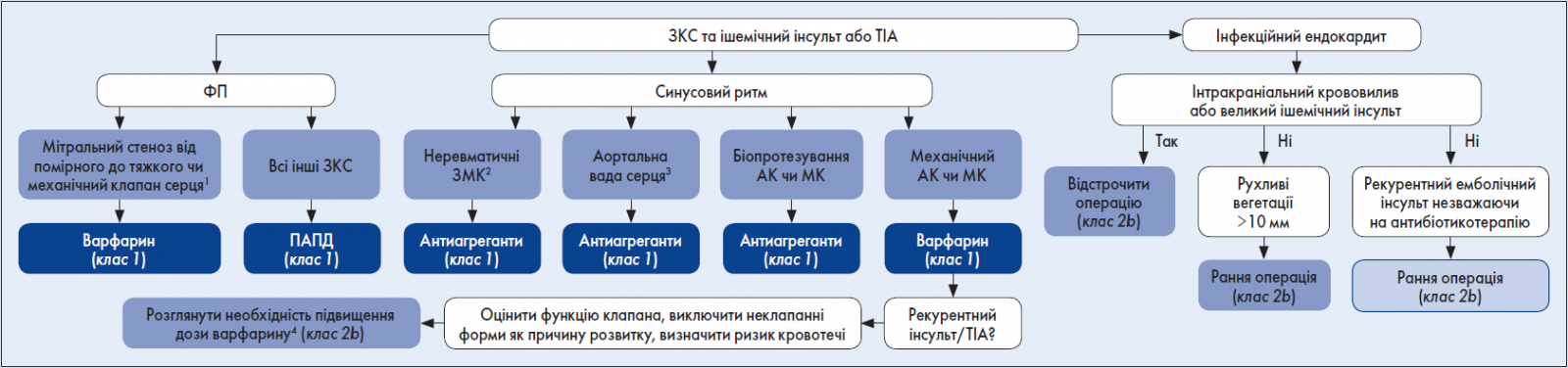
На рисунку 2 узагальнено рекомендований режим лікування антитромботичними препаратами у пацієнтів з ішемічним інсультом або ТІА в анамнезі та різними захворюваннями клапанів серця.
Рис. 2. Рекомендований режим лікування антитромботичними засобами у пацієнтів з ішемічним інсультом або ТІА в анамнезі та різними захворюваннями клапанів серця
Примітки: ЗКС – захворювання клапанів серця, ПАПД – пероральні антикоагулянти прямої дії, ЗМК – захворювання мітрального клапана, АК – аортальний клапан, МК – мітральний клапан. 1 Визначення клапанної ФП;
2 включно із кальцинозом мітрального кільця або пролапсом мітрального клапана; 3 ревматична та неревматична; 4 збільшити цільовий показник МНВ на 0,5 залежно від ризику кровотечі.
Адаптовано за D.O. Kleindorfer et al., 2021
Тромбоз лівого шлуночка. Пацієнтам з інсультом або ТІА та тромбозом лівого шлуночка (ЛШ) рекомендовано призначати антикоагулянтне лікування варфарином у терапевтичній дозі протягом щонайменше трьох місяців для зменшення ймовірності повторного інсульту (1, B-NR) (Phan et al., 2019; Merkler et al., 2019). У хворих після інсульту чи ТІА на тлі гострого ІМ доцільно провести детальну візуалізацію серця (наприклад, контрастну ЕхоКГ або МРТ серця) для оцінки наявності тромбу в ЛШ (2а, C-ЕО).
В осіб з інсультом або ТІА та новим тромбозом ЛШ (<3 місяців) безпека застосування пероральних антикоагулянтів прямої дії для зниження ризику рецидиву інсульту є невизначеною (2b, C‑LD) (Fleddermann et al., 2019). У пацієнтів з інсультом чи ТІА на тлі гострого переднього ІМ зі зниженою фракцією викиду (<50%), але без ознак тромбу в ЛШ можна розглянути емпіричну антикоагулянтну терапію протягом щонайменше трьох місяців для зменшення ймовірності повторного кардіоемболічного інсульту (2b, C-EO).
Кардіоміопатія. Пацієнтам з ішемічним інсультом або ТІА і тромбозом лівого передсердя чи його вушка в умовах ішемічної, неішемічної або рестриктивної кардіоміопатії та дисфункції ЛШ рекомендовано антикоагулянтну терапію варфарином принаймні впродовж трьох місяців для зниження ризику повторного інсульту або ТІА (1, C-ЕО). У хворих, які перенесли ішемічний інсульт або ТІА, лікування варфарином та АСК може бути корисним при встановленні допоміжного механічного пристрою для зменшення ймовірності рецидиву (2а, C‑LD) (Frontera et al., 2017; Cho et al., 2017).
В осіб з ішемічним інсультом або ТІА на тлі відсутності компресії ЛШ можливі переваги застосування варфарину для зниження ризику повторного епізоду (2а, C-ЕО). У пацієнтів з ішемічним інсультом або ТІА в умовах синусового ритму, що мають ішемічну/неішемічну кардіоміопатію та зниження фракції викиду без ознак тромбозу лівого передсердя або ЛШ, ефективність антикоагулянтної терапії порівняно з антитромбоцитарною є невизначеною, і вибір повинен залежати від індивідуальних особливостей хворих (2b, B-R) (Homma et al., 2012; Zannad et al., 2018). У пацієнтів з інсультом чи ТІА та шлуночковими допоміжними пристроями лікування дабігатраном замість варфарину в межах первинної чи вторинної профілактики повторного епізоду є шкідливим (3: завдає шкоди, B-R) (Andreas et al., 2018).
Відкрите овальне вікно. У пацієнтів із нелакунарним ішемічним інсультом невизначеної причини та ВОВ рішення щодо закриття ВОВ та медикаментозного лікування має бути прийняте сумісно хворим, кардіологом та невропатологом, беручи до уваги ймовірність причинно-наслідкової ролі ВОВ (2а, C-ЕО). У пацієнтів цієї когорти віком від 18 до 60 років, що перенесли нелакунарний ішемічний інсульт невизначеної етіології, незважаючи на ретельну оцінку стану, та мають анатомічні особливості ВОВ, пов’язані з високим ризиком, для профілактики повторного інсульту доцільними є його закриття за допомогою транскатетерного пристрою та тривала антитромбоцитарна терапія, а не саме лише використання антитромбоцитарних засобів (2а, B-R) (Kent et al., 2016; Lee et al., 2018).
У хворих цієї групи без анатомічних особливостей ВОВ, пов’язаних із високим ризиком, користь його закриття шляхом застосування транскатетерного пристрою та тривале антитромбоцитарне лікування замість самої лише антитромбоцитарної терапії для запобігання рецидиву інсульту вивчено недостатньо (2b, C‑LD) (Saver et al., 2017; Turc et al., 2020). У пацієнтів даної вікової категорії з нелакунарним ішемічним інсультом невизначеного ґенезу, незважаючи на анатомічні особливості ВОВ та ретельну оцінку стану, переваги його закриття за допомогою транскатетерного пристрою порівняно з варфарином невідомі (2b, C‑LD) (Mas et al., 2017).
Вроджена вада серця та пухлини серця
Пацієнтам з ішемічним інсультом або ТІА та вродженою вадою серця, які отримують паліативну терапію за Фонтеном, рекомендовано застосовувати варфарин для зменшення ймовірності рецидиву (1, C‑LD) (Seipelt et al., 2002; Monagle et al., 2011). Для осіб із ціанотичною вродженою вадою серця та іншими складними ураженнями, ішемічним інсультом чи ТІА можливого кардіоемболічного походження доцільним є лікування варфарином для зниження ризику повторного епізоду (2a, C-EO).
У пацієнтів з інсультом або ТІА, в яких виявлено лівобічну пухлину серця, її резекція може бути корисною для зменшення ймовірності повторного інсульту (2а, C‑LD) (Elbardissi et al., 2009).
Дисекція артерій
Пацієнтам з ішемічним інсультом або ТІА після дисекції екстракраніального відділу сонної або хребетної артерії показано антитромботичну терапію протягом щонайменше трьох місяців для запобігання повторному інсульту чи ТІА (1, C-EO). У хворих даної популяції, які перенесли дисекцію екстракраніального сегмента сонної або хребетної артерії <3 місяців тому, розумно використовувати АСК або варфарин для запобігання рецидиву інсульту чи ТІА (2а, B-R) (Markus et al., 2019).
В осіб з інсультом або ТІА та дисекцією екстракраніального відділу сонної або хребетної артерії, які мають рецидиви незважаючи на антитромботичне лікування, можна розглянути ендоваскулярну терапію для запобігання розвитку повторного інсульту чи ТІА (2b, C‑LD) (Moon et al., 2017; Spanos et al., 2016).
Стани гіперкоагуляції
У пацієнтів з ішемічним інсультом або ТІА невідомого ґенезу (незважаючи на ретельну діагностичну оцінку та відсутність в анамнезі інших тромбів), у яких виявлено мутацію протромбіну 20210А, стійкість до активованого білка С, підвищений рівень фактора VIII або дефіцит білка С, S або антитромбіну III, доцільною є антитромбоцитарна терапія для зменшення ймовірності повторного інсульту чи ТІА (2а, C‑LD) (Schellekens et al., 2018; Chiasakul et al., 2019).
В осіб з ішемічним інсультом або ТІА, які мають ізольовані антифосфоліпідні антитіла, але не відповідають критеріям антифосфоліпідного синдрому, для зниження ризику рецидиву інсульту рекомендована лише антитромбоцитарна терапія (1, B-NR) (Levine et al., 2004). У хворих цієї когорти із підтвердженим антифосфоліпідним синдромом, які отримують лікування варфарином, доцільне досягнення цільового показника МНВ 2‑3 на відміну від >3, щоб ефективно збалансувати ризик надмірної кровотечі та тромбозу (2а, B-R) (Finazzi et al., 2005).
У пацієнтів з ішемічним інсультом або ТІА, які відповідають критеріям антифосфоліпідного синдрому, доцільно використовувати варфарин для зменшення ймовірності повторного інсульту чи ТІА (2а, C‑LD) (Okuma et al., 2009). Особам з ішемічним інсультом або ТІА, антифосфоліпідним синдромом, тромбозом в анамнезі та позитивними антифосфоліпідними антитілами, як-то вовчаковий антикоагулянт, антикардіоліпін та анти-β2-глікопротеїн-I, не рекомендовано призначати ривароксабан, оскільки його приймання пов’язане із високою частотою тромботичних подій (3: завдає шкоди, B-R) (Pengo et al., 2018; Dufrost et al., 2018).
Гіпергомоцистеїнемія, рак, серповидноклітинна анемія
У пацієнтів з ішемічним інсультом або ТІА та гіпергомоцистеїнемією добавки з фолієвою кислотою, вітамінами В6 та В12 неефективні для запобігання повторному інсульту (3: переваги відсутні, B-R) (VITATOPS Trial Study Group, 2010; Toole et al., 2004). В осіб з ішемічним інсультом або ТІА на тлі ФП та раку доцільно розглянути застосування пероральних антикоагулянтів прямої дії, а не варфарину для профілактики інсульту (2a, B-NR) (Chen et al., 2019; Yang et al., 2020).
Хворим на серпоподібноклітинну анемію, які перенесли ішемічний інсульт або ТІА, рекомендоване постійне переливання крові для зниження рівня гемоглобіну S до <30% від загального гемоглобіну для профілактики повторного ішемічного інсульту (1, B-NR) (Adams et al., 1998). Також у цій популяції пацієнтів лікування гідроксисечовиною може бути розумним вибором для запобігання рецидиву інсульту, якщо трансфузійна терапія недоступна або недоцільна (2a, B-R) (Ware et al., 2016; Lucarelli et al., 2012).
Васкуліти
Пацієнтам з ішемічним інсультом або ТІА та симптомами, пов’язаними з гігантоклітинним артеріїтом, для зниження ризику рецидиву інсульту рекомендовано негайно розпочати пероральне застосування глюкокортикоїдів у високих дозах (1, B-NR) (Brekke et al., 2017; van der Geest et al., 2020). В осіб з ішемічним інсультом чи ТІА та підтвердженим діагнозом гігантоклітинного артеріїту терапія метотрексатом або тоцилізумабом на додаток до стероїдів є доцільною для зменшення ймовірності повторного інсульту (2а, B-NR) (Stone et al., 2017; Onen et al., 2017).
У пацієнтів з ішемічним інсультом чи ТІА та первинним ангіїтом центральної нервової системи індукційна терапія глюкокортикоїдами та/або імуносупресантами з подальшим тривалим підтримувальним лікуванням стероїдзберігальними імуносупресантами є розумним варіантом для зниження ризику рецидиву інсульту (2а, B-NR) (de Boysson et al., 2018). У хворих, що перенесли ішемічний інсульт чи ТІА та мають підтверджений діагноз гігантоклітинного артеріїту, терапія інфліксимабом асоційована з періодичними очними симптомами та маркерами активності захворювання, тому його не слід призначати (3: завдає шкоди, B-R) (Fasano et al., 2017; Shapiro et al., 2018).
В осіб з ішемічним інсультом або ТІА та інфекційним васкулітом, таким як церебральний васкуліт, нейросифіліс чи бактеріальний менінгіт як наслідок вірусу вітряної віспи, показане лікування основної інфекції для зниження ризику інсульту (1, B-NR) (Nagel et al., 2007; Callegari et al., 2014). У пацієнтів з ішемічним інсультом чи ТІА в контексті ВІЛ-васкулопатії щоденне приймання АСК + контроль вірусу ВІЛ у поєднанні з антиретровірусною терапією є доцільними для зменшення ймовірності повторного інсульту (2a, C‑LD) (Gunthard et al., 2014; Benjamin et al., 2017).
Використання антитромботичних препаратів у вторинній профілактиці інсульту
У пацієнтів із некардіоемболічним ішемічним інсультом або ТІА антитромбоцитарна терапія має переваги перед пероральними антикоагулянтами для зменшення ймовірності повторного ішемічного інсульту та інших серцево-судинних подій при мінімальному ризику кровотечі (1, А) (De Schryver et al., 2012; Mohr et al., 2001). Для вторинної профілактики ішемічного інсульту в цій групі хворих показано призначення АСК у дозуванні 50‑325 мг/добу, клопідогрелю по 75 мг або комбінація 25 мг АСК та 200 мг дипіридамолу пролонгованого вивільнення двічі на день (1, А) (Kwok et al., 2015; Sacco et al., 2008).
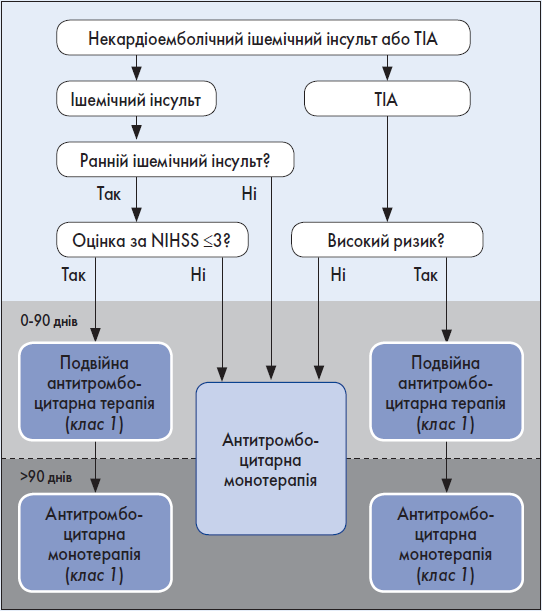
В осіб із нещодавно перенесеним легким (за шкалою NIHSS ≤3) некардіоемболічним ішемічним інсультом або ТІА високого ризику (за шкалою ABCD2 ≥4) призначення пероральних антикоагулянтів прямої дії (АСК + клопідогрель) має бути раннім (в ідеалі протягом 12‑24 год від появи симптомів і принаймні впродовж семи днів від моменту початку епізоду) і продовжуватися 21‑90 днів із подальшою антитромбоцитарною монотерапією для зниження ризику повторного ішемічного інсульту (1, А) (рис. 3) (Albay et al., 2020; Naqvi et al., 2020). Для пацієнтів із нещодавнім (<24 год) інсультом легкого або помірного ступеня тяжкості (оцінка за NIHSS ≤5), ТІА високого ризику (оцінка за ABCD2 ≥6) або симптоматичним стенозом інтра-/екстракраніального відділу ≥30% коронарної артерії використання пероральних антикоагулянтів прямої дії з тикагрелором + АСК протягом 30 днів можна розглядати для зменшення ймовірності рецидиву інсульту впродовж 30 днів; однак слід враховувати, що воно також асоційоване зі зростанням ризику серйозних кровотеч, включно із внутрішньомозковими (2b, B-R) (Johnston et al., 2020).
Рис. 3. Антитромбоцитарна терапія при некардіоемболічному інсульті та ТІА
Примітки: Алгоритм не поширюється на пацієнтів, які отримували інтенсивну тромболітичну терапію. Ранній ішемічний інсульт означає, що минуло <24 год від його початку. У разі ТІА високого ризику оцінка за ABCD2 ≥4, низького ризику – ABCD2 <4. Подвійна антитромбоцитарна терапія включає АСК + клопідогрель.
Адаптовано за Brown et al., 2021; Pan et al., 2019; Wang et al., 2013
Для пацієнтів, які вже приймали АСК під час некардіоемболічного ішемічного інсульту або ТІА, ефективність збільшення дози АСК чи переходу на інший антитромбоцитарний препарат вивчено недостатньо (2b, B-NR) (Lee et al., 2017). Для осіб із некардіоемболічним ішемічним інсультом чи ТІА безперервне застосування пероральних антикоагулянтів прямої дії протягом >90 днів або потрійної антитромбоцитарної терапії корелює з підвищеним ризиком крововиливів (3: завдає шкоди, А) (Bath et al., 2018).
Підготувала Олена Коробка
Оригінальний текст документа читайте на сайті
www.ahajournals.org
Тематичний номер «Неврологія, Психіатрія, Психотерапія» № 3 (58) 2021 р.