26 квітня, 2023
Діагностика й лікування неалкогольної жирової хвороби печінки в закладах первинної медичної допомоги та ендокринологічних клінічних установах
Повна версія статті у форматі PDF
Клінічні рекомендації Американської асоціації клінічної ендокринології (ААСЕ) спільно з Американською асоціацією з вивчення захворювань печінки (AASLD). Частина 1
 Неалкогольна жирова хвороба печінки (НАЖХП) є найпоширенішою причиною хронічної хвороби печінки, яка вражає 25% населення світу. Попри її значну та зростаючу поширеність, обізнаність про хворобу залишається обмеженою: поінформовані про свою хворобу <5% пацієнтів із НАЖХП проти 38% осіб із вірусним гепатитом. 12-14% пацієнтів із НАЖХП має агресивний перебіг неалкогольного стеатогепатиту (НАСГ), що може прогресувати до вираженого фіброзу, цирозу або раку печінки. Ризик розвитку НАСГ у 2-3 рази вищий в осіб з ожирінням і/або цукровим діабетом (ЦД) 2 типу. НАСГ у США є однією з найпоширеніших причин раку печінки та другим за поширеністю після гепатиту С показанням до трансплантації печінки. На сьогодні немає ліків, схвалених Управлінням із санітарного нагляду за якістю харчових продуктів і медикаментів США (FDA) для лікування НАЖХП, однак деякі ліки від діабету та ожиріння можуть бути ефективними.
Неалкогольна жирова хвороба печінки (НАЖХП) є найпоширенішою причиною хронічної хвороби печінки, яка вражає 25% населення світу. Попри її значну та зростаючу поширеність, обізнаність про хворобу залишається обмеженою: поінформовані про свою хворобу <5% пацієнтів із НАЖХП проти 38% осіб із вірусним гепатитом. 12-14% пацієнтів із НАЖХП має агресивний перебіг неалкогольного стеатогепатиту (НАСГ), що може прогресувати до вираженого фіброзу, цирозу або раку печінки. Ризик розвитку НАСГ у 2-3 рази вищий в осіб з ожирінням і/або цукровим діабетом (ЦД) 2 типу. НАСГ у США є однією з найпоширеніших причин раку печінки та другим за поширеністю після гепатиту С показанням до трансплантації печінки. На сьогодні немає ліків, схвалених Управлінням із санітарного нагляду за якістю харчових продуктів і медикаментів США (FDA) для лікування НАЖХП, однак деякі ліки від діабету та ожиріння можуть бути ефективними.
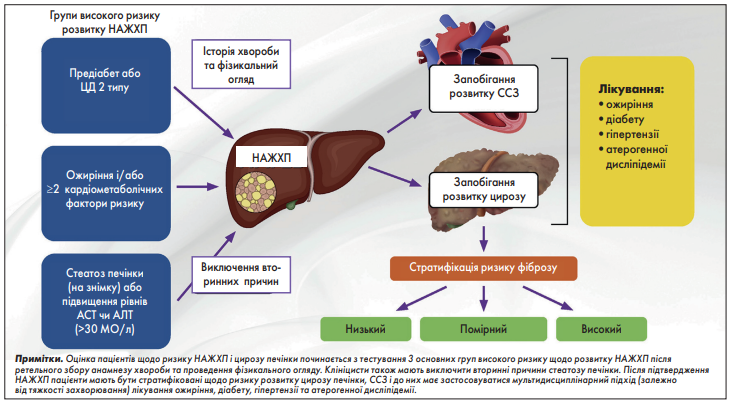
НАЖХП не пов’язана з надмірним уживанням алкоголю чи іншими причинами захворювання печінки, її діагностують за результатами аномальних печінкових тестів (хоча результати можуть бути нормальними) та даними візуалізаційних досліджень. Діагноз НАСГ підтверджують за допомогою біопсії печінки, проте спеціалізовані аналізи крові та візуалізація можуть допомогти визначити ризик значного фіброзу. З НАЖХП пов’язана низка кардіометаболічних розладів: ожиріння, резистентність до інсуліну, ЦД 2 типу, високий артеріальний тиск і атерогенна дисліпідемія – ці чинники підвищують ризик виникнення серцевого нападу або інсульту, що є найпоширенішою причиною смерті.
Основним принципом лікування НАЖХП є зниження ваги за допомогою низькокалорійної дієти; обмеження споживання насичених жирів, крохмалю та цукру; поліпшення режиму харчування (наприклад, середземноморська дієта та цільні продукти з мінімальною обробкою); фізична активність. У разі втрати ваги >5% можна спостерігати кардіометаболічний ефект і зменшення кількості жиру в печінці. Більша втрата ваги має більше переваг і може сприяти регресу стеатогепатиту або фіброзу печінки (у разі втрати ваги на 10%).
Епідеміологія
Який масштаб проблеми/захворювання в ендокринній системі та клініці первинної медичної допомоги?
НАЖХП є мультисистемним захворюванням і тісно пов’язана з ожирінням, інсулінорезистентністю (ІР), ЦД 2 типу, гіпертензією та атерогенною дисліпідемією [1, 2]. Визначення НАЖХП передбачає наявність стеатозу печінки в >5% гепатоцитів за відсутності значного поточного або нещодавнього вживання алкоголю та інших відомих причин захворювання печінки [1, 2]. НАСГ, який частіше прогресує до виражених стадій фіброзу, окрім стеатозу характеризується ще й активним ураженням гепатоцитів (балонування) і запаленням.
В усьому світі загальна поширеність НАЖХП становить 25%, тоді як її потенційно прогресуючої форми або НАСГ – від 12% до 14% [5]. Найвищі показники поширеності НАЖХП і НАСГ зафіксовані в країнах Близького Сходу [1]. Крім того, показники поширеності значно вищі в осіб із ЦД 2 типу та вісцеральним ожирінням. Насправді серед людей з ожирінням поширеність НАСГ становить від 25% до 30%, тоді як приблизно 30-40% хворих на діабет страждають на НАСГ [1, 6-8]. Нещодавно проведене дослідження продемонструвало, що відповідно до останніх популяційних досліджень у США в амбулаторних стаціонарах сімейної медицини, внутрішньої медицини та ендокринологічних клініках приблизно 70% пацієнтів із ЦД 2 типу страждають на НАЖХП (стеатоз) і приблизно 15% – мають клінічно значущий фіброз печінки (стадії F2) [9-11].
Є привід думати, що поширеність НАЖХП продовжуватиме зростати, імовірно, з непропорційним збільшенням поширеності хвороби [12, 13]. Поточні дані демонструють, що в приблизно 20% осіб із НАСГ є ймовірність розвитку серйозних захворювань печінки, насамперед цирозу та його ускладнень [14]. Сьогодні НАСГ є однією з головних причин виникнення гепатоцелюлярної карциноми (ГЦК) та другою за поширеністю причиною ГЦК у пацієнтів, які очікують на трансплантацію печінки в США після гепатиту С [1, 15, 16].
Незважаючи на значне зростання поширеності НАЖХП, обізнаність про хворобу залишається досить обмеженою: лише <5% людей із НАЖХП знають про своє захворювання проти 38% осіб із вірусним гепатитом [19]. Крім того, нещодавно проведене глобальне опитування понад 2200 лікарів показало прогалину в знаннях щодо НАЖХП серед постачальників послуг, передусім у лікарів первинної медичної допомоги (ПМД) та ендокринологів [20]. Інше нещодавно проведене опитування 751 клініциста в США, у тому числі лікарів ПМД, ендокринологів, гастроентерологів і гепатологів, виявило, що зазначені спеціалісти недооцінюють поширеність НАЖХП у групах високого ризику (наприклад, у пацієнтів із тяжким ожирінням або ЦД 2 типу) і що в разі НАСГ мало місце недостатнє використання лікарських засобів із доведеною ефективністю [21]. Урешті-решт, діагностика та направлення до спеціалістів для лікування залишаються серед ендокринологів на низькому рівні [21, 22]. На відміну від інших широко поширених неінфекційних хронічних станів, таких як ожиріння, ЦД і серцево-судинні захворювання (ССЗ), до НАЖХП прикуто менше уваги з боку громадської охорони здоров’я [23]. Ця головоломка зростаючого тягаря захворювань, обмеженої обізнаності та клінічної інерції загострює проблему громадської охорони здоров’я, що особливо важливо, беручи до уваги той факт, що переважна більшість людей із ЦД 2 типу, які можуть мати супутню НАЖХП, зазвичай спостерігаються у клініцистів первинної ланки та ендокринологів, проте залишаються недіагностованими та нелікованими. Таким чином, метою розробки цієї науково-обґрунтованої настанови є підвищення обізнаності щодо НАЖХП і НАСГ та наведення простих і практичних рекомендацій, що допоможуть клініцистам в оцінці НАЖХП у своїй практиці.
Що відомо про природний перебіг НАЖХП?
ЦД 2 типу – основний фактор прогресування НАЖХП. Дослідження, проведене в 20 країнах, виявило тривожну поширеність НАЖХП серед осіб із ЦД 2 типу, що свідчить про недооцінку реальної поширеності стеатозу, оскільки скринінг у майже 90% досліджень проводився за допомогою ультразвукового дослідження (УЗД) печінки [60]. Цей метод вважається менш чутливим для виявлення стеатозу печінки, ніж еластографія, тобто контрольований параметр ослаблення хвилі (CAP), або магнітно-резонансна томографія (МРТ) [24]. На основі 8 досліджень, проведених у 2020 та 2021 роках в Європі, Південно-Східній Азії та США з використанням для скринінгу НАЖХП, НАСГ та фіброзу транзиторної еластографії (ТЕ) і/або МРТ, були представлені вищі показники поширеності НАЖХП і фіброзу печінки в пацієнтів із ЦД 2 типу [25]. Вік (>50 років), ІР та особливості метаболічного синдрому (МС) підвищують імовірність виникнення НАСГ із тяжчою стадією фіброзу і цирозом печінки [5, 26-28]. Попри те що стеатогепатит і ЦД 2 типу тісно пов’язані, це не допомагає встановити причинно-наслідковий зв’язок, але демонструє вплив діабету на печінку через більшу поширеність ожиріння серед латиноамериканців, якщо порівняти з європейцями [29].
Тоді як швидкість прогресування захворювання в більшості людей є відносно повільною, воно може бути швидшим у деяких осіб із факторами ризику (наприклад, ожирінням і ЦД 2 типу), і в приблизно однієї третини людей хвороба зрештою прогресує до НАСГ, з них у приблизно 20% розвивається фіброз із високим ризиком позапечінкових ускладнень, цирозу та печінкової недостатності [40, 41]. Розвиток фіброзу є ключовим предиктором наслідків, пов’язаних із печінкою. Наявні суттєві докази, що підтверджують дозозалежний вплив фіброзу на смертність, пов’язану з печінкою, та смертність від усіх причин (підвищення відносного ризику від 5 до 12 разів) з більшим ризиком декомпенсації печінки, ГЦК, трансплантації печінки та смерті [42, 43]. Причиною високої смертності, пов’язаної з НАЖХП, здебільшого є позапечінковий рак, цироз, ССЗ та ГЦК. Усі гістологічні стадії НАЖХП (Панель1), у тому числі ізольований стеатоз без фіброзу, пов’язані зі значним підвищенням загальної смертності, що прогресує з тяжкістю захворювання печінки [44].
У зв’язку з почастішанням випадків ожиріння та ЦД поширеність НАЖХП-ГЦК зростає. Тому НАЖХП, імовірно, замінить віруси гепатиту B і C як головну причину ГЦК в усьому світі. Деякі варіанти генів, такі як PNPLA3 або TM6SF2, пов’язані з набагато вищим ризиком виникнення не лише цирозу, але й ГЦК, причому обидва ризики посилюються за наявності ожиріння чи діабету [38]. Збільшується кількість доказів зв’язку НАЖХП і раку, що дає можливість пояснити патофізіологію, що лежить в основі тривалого спостереження, згідно з яким діабет пов’язаний із удвічі вищим ризиком розвитку ГЦК та позапечінкових ракових захворювань [17, 45, 46]. У ході декількох попередніх довгострокових когортних досліджень було виявлено, що позапечінковий рак є другою основною причиною смерті після ССЗ, особливо в пацієнтів із вираженішим (мостовим) фіброзом [41, 47]. Таким чином, зростаюча частота НАЖХП-ГЦК потребує ефективніших стратегій скринінгу раку в цій популяції.
Які позапечінкові ускладнення стосуються роботи ендокринологів і лікарів-практиків, які спостерігають пацієнтів з ендокринними і кардіометаболічними захворюваннями?
ЦД 2 типу і ССЗ є двома найважливішими позапечінковими захворюваннями, що тісно пов’язані з НАЖХП, вісцеральним ожирінням та ІР. Зв’язок між НАЖХП і ЦД 2 типу є двонаправленим, причому вісцеральне ожиріння й ІР є посередниками [48, 49]. Відомо, що вісцеральна жирова тканина посилює глюконеогенез de novo, а жир у печінці пов’язаний із печінковою ІР [48]. НАЖХП, особливо НАСГ, посилює ІР печінки та жирової тканини, що може сприяти розвитку ЦД 2 типу [50].
Оскільки приблизно одна третина хворих на ЦД 1 типу мають ожиріння, більше уваги приділяється ризику розвитку НАЖХП [55].
Зв’язок між НАЖХП й діабетичними ускладненнями залишається недостатньо вивченим. Є дані, що ті, хто страждає на стеатоз і ЦД 1 типу, мають більший ризик розвитку ССЗ, аритмій та інших серцевих ускладнень [58-60]. Наявність НАЖХП також асоціюється з мікросудинними діабетичними ускладненнями, особливо з хронічною хворобою нирок (ХХН) [61, 62].
Жінки із синдромом полікістозних яєчників (СПКЯ) мають підвищений ризик розвитку ЦД 2 типу і НАЖХП.
Механізми, що лежать в основі розвитку НАЖХП у разі СПКЯ, є багатофакторними, однак ІР є ключовим [68]. Потрібно зазначити, що жінки із СПКЯ та гіперандрогенією мають утричі більшу поширеність НАЖХП, яка тісно пов’язана з тяжким перебігом ІР [69, 70]. Ожиріння, ІР та розвиток ЦД 2 типу є основними чинниками НАЖХП за низки ендокринних захворювань; найбільш вивченими є гіпотиреоз, дефіцит гормону росту (ГР) і гіпогонадизм. Дефіцит ГР асоціюється з НАЖХП, з урахуванням широкого впливу ГР на метаболізм глюкози [77]. Пангіпопітуїтаризм також пов’язаний із НАЖХП [78]. Замісна терапія ГР продемонструвала певну користь у разі завчасної рекомендації пацієнтам з ендокринопатіями регулярно обстежуватися на НАЖХП, поза межами ризику, пов’язаного з наявністю ожиріння або ЦД 2 типу [79].
З огляду на високу поширеність НАЖХП і ССЗ та їхній зв’язок із МС, не є несподіванкою коморбідність цих двох станів. Незважаючи на те що термінальна стадія захворювання печінки і ГЦК є найпоширенішими причинами смерті людей із цирозом печінки, ССЗ та позапечінкові злоякісні новоутворення є основними причинами захворюваності і смертності в більшості осіб із менш розвиненим захворюванням [60, 81, 82].
Із НАЖХП, окрім атеросклеротичного ССЗ, можуть бути пов’язані інші ускладнення.
Під час проведення метааналізу в 2020 р. було виявлено, що інші серцеві ускладнення, такі як кардіоміопатія, кальцифікація серцевого клапана та серцеві аритмії, також були поширеними серед пацієнтів із НАЖХП [84].
Нарешті, є декілька інших ускладнень, зокрема хвороба жовчного міхура, обструктивне апное уві сні, колоректальні новоутворення та інші види раку, а також саркопенія, які частіше спостерігаються в пацієнтів із НАЖХП [87, 90-94]. Цікавим є той факт, що особи з НАЖХП і саркопенією мають вищий ризик розвитку ССЗ (OR1,83; р=0,014), ніж особи без НАЖХП та саркопенії [95]. Крім того, нещодавно отримані дані свідчать про те, що саркопенія в разі НАЖХП пов’язана з підвищеною смертністю [96].
Мета
З огляду на високу поширеність НАЖХП у клінічній ендокринології та практиці ПМД, а також обмеженість рекомендацій щодо метаболічних і ендокринологічних аспектів, наявна мала кількість рекомендацій для лікарів первинної ланки, що ведуть хворих із НАЖХП, більшість із яких недіагностовані. Метою цієї настанови є надання ендокринологам і клініцистам первинної медичної ланки практичних рекомендацій із діагностики й лікування НАЖХП, заснованих на доказах (Див. Резюме рекомендацій із діагностики та лікування НАЖХП).
Область застосування
Настанова розглядає ключові питання лікування і зосереджена на метаболічних та ендокринологічних аспектах профілактики, діагностики, лікування та довгострокового прогнозу для всієї популяції людей із НАЖХП. Поза межами рекомендації лишається огляд епідеміології в загальній популяції або розгляд спірних аспектів НАЖХП, призначених для спеціалістів із захворювань печінки. Огляд має на меті надання практичних рекомендацій, орієнтованих на пацієнта, для ендокринологів і терапевтів, які часто мають справу з пацієнтами з групи високого ризику розвитку НАСГ (тобто тих, хто має ожиріння, МС і/або ЦД 2 типу). Також огляд не стосується втручань суто дослідницького характеру, а лише втручань, доступних клініцисту-практику: зміни способу життя, баріатрична хірургія, препарати для зниження ваги та лікування ЦД й будь-які інші засоби з переконливими доказами, отриманими в рандомізованих контрольованих дослідженнях (РКД), що вважаються безпечними і ефективними.
Рекомендації з доказовою базою
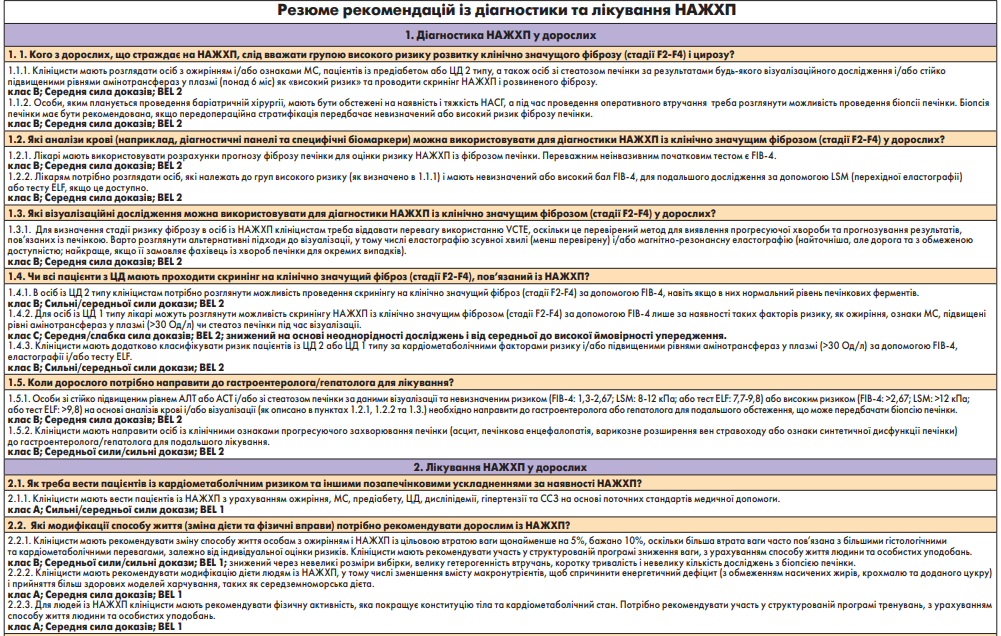
1. Діагностика НАЖХП у дорослих
1.1. Кого з дорослих, які страждають на НАЖХП, слід віднести до групи високого ризику клінічно значущого фіброзу (стадії F2-F4) і ризику цирозу?
Доказова база щодо пункту 1.1.1. Діагноз НАЖХП ґрунтується на: наявності стеатозу печінки на додачу до відсутності значного вживання алкоголю (визначається як постійне або нещодавнє вживання алкоголю >21 стандартної дози алкоголю (Standard drink) [1 drink = 14 г чистого алкоголю]/тиж для чоловіків і >14 drinks/тиж для жінок) та виключення інших захворювань печінки [101]. Початкове обстеження осіб із підозрою або випадковим виявленням стеатозу печінки за допомогою візуалізації має охоплювати дослідження для виключення конкуруючих причин стеатозу та захворювання печінки (наприклад, серологічні дослідження на гепатит В і C, визначення антимітохондріальних антитіл, антинуклеарних антитіл, антитіл до гладеньких м’язів, сироваткового рівня феритину, альфа‑1-антитрипсину та оцінка МС (див. панель 1).
За останні 20 років стало очевидним, що в пацієнтів із ЦД 2 типу дуже висока поширеність НАЖХП та пов’язаного з ним фіброзу [5, 6, 9-11, 52, 102-104].
Крім того, особи зі стало відхиленими рівнями амінотрансфераз за відсутності інших причин захворювання печінки (наприклад, вірусного гепатиту та надмірного вживання алкоголю) також мають високий ризик НАЖХП і розвитку фіброзу печінки (панель 2) [105, 106].
Насправді особи з декількома компонентами МС або IР, ожирінням чи предіабетом також мають ризик розвитку значного фіброзу та підвищеної смертності [5, 6, 9-11, 52, 102-104]. Групи високого ризику НАЖХП із фіброзом печінки – це особи віком ≥50 років і/або мають ожиріння від середнього до тяжкого ступеня (ІМТ >35 кг/м2), у тому числі ті, хто звертається за консультацією з приводу баріатричної хірургії, або ЦД 2 типу і/або МС [6, 30, 103, 111, 113-115]. Варто також зазначити, що метою скринінгу на НАЖХП є виявлення осіб, в яких є ризик прогресування захворювання та розвитку фіброзу печінки. Скринінг є важливим, оскільки раннє втручання може зупинити або сприяти регресу захворювання. У нещодавно проведеному дослідженні за участю осіб із ЦД 2 типу скринінг на НАЖХП з подальшим інтенсивним втручанням у спосіб життя або застосуванням піоглітазону був ефективним, і забезпечив підтримання рекомендацій щодо скринінгу [113, 115].
Доказова база щодо пункту 1.1.2. Баріатрична хірургія може забезпечити стійку втрату ваги, покращити перебіг ЦД і знизити ризик розвитку ССЗ і раку, які є поширеними супутніми захворюваннями при НАЖХП [116-121].
Тоді як переважна більшість людей, яким показана баріатрична хірургія, страждають на НАЖХП, лише приблизно 8,5% мають F3 і F4 (цироз) під час інтраопераційної біопсії печінки, а у 2% до 4% під час операції виявляють неочікуваний цироз [125, 126]. Певною мірою це пов’язано з доопераційним скринінгом та ймовірним небажанням продовжувати хірургічне втручання в пацієнтів із діагностованим стабільним раннім або прогресуючим цирозом печінки. Баріатричну хірургію не можна застосовувати особам із декомпенсованим цирозом через підвищену післяопераційну смертність.
1.2. Які аналізи крові (наприклад, діагностичні панелі та специфічні біомаркери) можна використовувати для діагностики НАЖХП з клінічно значущим фіброзом (стадії F2-F4) у дорослих?
Доказова база щодо пункту 1.2.1. Рівні печінкової амінотрансферази в плазмі крові можуть бути ненадійними та не виходити за межі референтних значень у багатьох випадках НАЖХП, тому їх не можна використовувати окремо для діагностики НАЖХП [128]. У дослідженні за участю осіб із ЦД 2 типу до 50% пацієнтів мали НАЖХП, незважаючи на нормальні рівні АЛТ (у цьому дослідженні рівні визначені як <40 Од/л) [30]. Проведені згодом дослідження підтвердили, що переважна більшість пацієнтів із НАЖХП із клінічно значущим фіброзом (F2) у клініках ПМД або в ендокринологічних клініках мають рівень амінотрансферази в плазмі <40 Од/л [9, 10, 102, 114]. Діагноз «стеатоз печінки» можна підтвердити за допомогою візуалізації, у тому числі УЗД печінки, CAP, комп’ютерної томографії або 2 найбільш точних і чутливих методів, 1H-MRS і МРТ з визначенням протонної густини жирової фракції (MRI-PDFF).
УЗД печінки сильно залежить від оператора та не дає інформації про ступінь тяжкості фіброзу печінки (за відсутності цирозу). Методи на основі МРТ (1H-MRS і MRI-PDFF) для діагностики стеатозу сьогодні здебільшого зарезервовані для клінічних досліджень. Магнітно-резонансна еластографія (МРЕ) має призначатися певними особами, насамперед фахівцями з хвороб печінки для діагностики фіброзу печінки, але тест є дорогим і не замінює біопсію печінки як золотий стандарт для діагностики НАСГ [2, 130-133, 134].
Найважливішим для ендокринологів і клініцистів первинної медичної ланки є визначення показників фіброзу печінки для діагностики клінічно значущого фіброзу, зокрема за допомогою FIB‑4. FIB‑4 добре себе зарекомендував завдяки своїй здатності передбачати розвиток фіброзу печінки з часом і дає можливість проводити стратифікацію ризику в людей із погляду майбутньої захворюваності та смертності, пов’язаної з печінкою [135].
Ендокринологи та клініцисти первинної медичної ланки мають бути обізнаними щодо обмеженої інформативності біохімічних панелей в порівнянні з біопсією печінки (золотим стандартом). Їм бракує адекватної чутливості та позитивної прогностичної цінності (PPV) для встановлення поширеного фіброзу; тому деякі особи потраплять у групу «невизначеного ризику».
Доказова база щодо пункту 1.2.2. У клініках ендокринологічної та первинної медичної допомоги першим кроком у веденні осіб із високим ризиком НАЖХП (предіабет, ЦД 2 типу, ожиріння і/або МС або підвищений рівень амінотрансферази в плазмі крові) є оцінка ризику НАЖХП. Стеатоз печінки оцінюють за допомогою простих неінвазивних показників стеатозу печінки (індекс ожиріння печінки, індекс жирової дистрофії печінки та індекс стеатозу печінки), хоча ці методи діагностики мають характерні обмеження [11, 115, 152]. УЗД печінки не рекомендується для рутинної клінічної діагностики [115]. Натомість TE є кращим варіантом у порівнянні з УЗД печінки, оскільки дає змогу визначити кількість печінкового жиру (CAP) і фіброз (перехідна еластографія з контрольованим вібрацією [VCTE]) для стратифікації ризику під час того самого тестування. Для осіб із високою претестовою ймовірністю НАЖХП, таких як 3 групи ризику, визначені в діагностичному алгоритмі (рис. 1), доцільно проводити стратифікацію ризику (FIB‑4) без УЗД для діагностики стеатозу печінки (тобто в 3 групах ризику ймовірність стеатозу печінки дуже висока і становить 70%) [5, 9-11, 52, 102-104].
Рис. 1. Огляд діагностичного алгоритму ведення НАЖХП
Важливо зібрати повну історію хвороби та провести звичайні клінічні лабораторні дослідження, які дадуть клініцистам можливість виключити вторинні причини стеатозу печінки (див. панель 1) та підвищення рівня амінотрансферази в плазмі крові (див. панель 2). Необхідно провести ретельне обстеження, щоб виключити конкуруючі причини стеатозу та значне зловживання алкоголем.
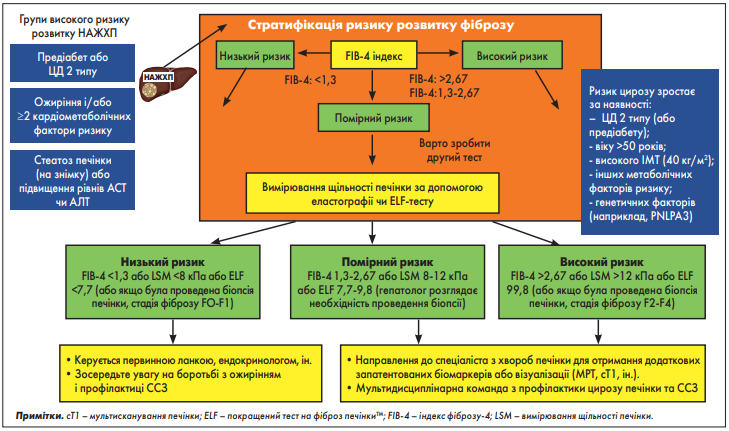
Має значення додаткова оцінка ризику клінічно значущого фіброзу (стадії F2-F4), який надає прогностичну інформацію щодо майбутнього ризику цирозу печінки та може допомогти в розробці стратегії лікування, а також визначає потребу в направленні до гепатолога/гастроентеролога. Комбінація FIB‑4 із подальшою VCTE є найкращим підходом. Якщо показник FIB‑4 >1,3, потрібно виконати тест другого рівня, наприклад VCTE або ELF (рис. 2). Використання FIB‑4 як тесту першої лінії, а VCTE – другої може допомогти стратифікувати осіб у «невизначеній зоні» та значно зменшити кількість направлень до спеціалістів [130, 134, 137, 147, 148, 153]. Варто підкреслити, що для визначення прогресуючого фіброзу в осіб літнього віку (65 років) були запропоновані вищі межі FIB‑4 у діапазоні від 1,9 до 2,0 (а не >1,3) [154, 155].
Така комбінація або послідовне використання тестів дає вищий PPV у разі виявлення осіб групи ризику з активним НАСГ і фіброзом. У дослідженні за участю 968 осіб із підтвердженою за допомогою біопсії НАЖХП послідовне тестування за допомогою FIB‑4 або NFS з подальшою ТЕ у пацієнтів із невизначеним балом було точнішим, ніж виконання будь-якого тесту окремо [156]. В іншому перехресному дослідженні за участю 3202 осіб із мостоподібним фіброзом і компенсованим цирозом печінки застосування неінвазивних тестів окремо або в поєднанні з візуалізацією (VCTE) зменшувало потребу в біопсії печінки під час спроби розрізнити розвинений фіброз, спричинений НАСГ [150]. Особи з високим або середнім ризиком розвитку фіброзу мають бути направлені до гепатолога для подальшого обстеження та розгляду питання про біопсію печінки. Вона залишається золотим стандартом діагностики НАСГ, однак її не варто використовувати як метод скринінгу для діагностики НАЖХП, з огляду на численні застереження: вона є інвазивною, є схильність до помилок під час інтерпретації, і її важко застосовувати у великих популяціях [157]. Саме тому було запропоновано алгоритм скринінгу НАЖХП та виявлення осіб із ризиком клінічно значущого фіброзу (рис. 2).
Рис. 2. Профілактика цирозу при НАЖХП
1.3. Які візуалізаційні методи дослідження можна використати для діагностики НАЖХП із клінічно значущим фіброзом (стадії F2-F4) у дорослих?
Доказова база щодо пункту 1.3.1. Сучасним золотим стандартом діагностики стеатогепатиту є біопсія печінки. Незважаючи на те що метод є безпечним, це все-таки інвазивна процедура, пов’язана з потенційними побічними ефектами, такими як біль, кровотеча та інфекція. Крім того, біопсія має інші обмеження, такі як недостатня прийнятність пацієнтами, варіабельність всередині та між спостерігачами, мінливість вибірки та вартість [157]. Як зазначалося раніше, VCTE (рис. 2) є найширше використовуваним неінвазивним методом визначення щільності печінки (LSM) для встановлення ризику розвитку фіброзу печінки та остаточного виключення цирозу [158-160].
Також доступні інші методи виявлення фіброзу печінки. Треба ще раз наголосити, що MРТ є найбільш точною, проте дороговартісною та обмежено доступною; за певних обставин, коли необхідне додаткове обстеження, вона має призначатися гепатологом [130-133]. Гепатологи мають значний досвід щодо еластографії зі зсувом хвилі (SWE), двовимірною (2DSWE) або точковою (pSWE) [165-167]. Точність 2DSWE і pSWE подібна до TE, але менша, ніж у МРТ.
1.4. Чи всі пацієнти з ЦД мають проходити скринінг на наявність клінічно значущого фіброзу (стадії F2-F4), пов’язаного з НАЖХП?
Доказова база щодо пунктів 1.4.1, 1.4.2, 1.4.3. Між НАЖХП і ЦД 2 типу існує двонаправлений зв’язок, за якого наявність одного захворювання підвищує ризик і тяжкість іншого [174]. Обґрунтування універсального скринінгу базується на нових доказах того, що ЦД 2 типу є основним чинником, що підвищує ризик тяжкості захворювання та його прогресування до цирозу печінки в осіб із НАЖХП. Дослідження переконливо доводять взаємозв’язок між НАЖХП, ІР, МС і ЦД 2 типу [29, 53].
Наявність НАЖХП пов’язана з використанням вищих доз інсуліну для порівнянного глікемічного контролю в популяціях як із ЦД 1 типу, так і з ЦД 2 типу [57, 177, 178]. Ожиріння та ІР є рушійними факторами, зі значною гетерогенністю серед досліджень, що ускладнює повну оцінку впливу ЦД 1 типу на розвиток НАЖХП. Загалом, скринінг є виправданим лише в осіб з ожирінням, МС, підвищеним рівнем амінотрансферази в плазмі крові (>30 Од/л) або стеатозом печінки за результатами візуалізаційних досліджень [152, 179-183].
Є ймовірність, що втручання, які покращують перебіг НАЖХП та ІР печінки, можуть зменшити ризик розвитку ЦД 2 типу, як це запропоновано щодо піоглітазону, який зменшує прогресування предіабету до ЦД 2 типу на 70-80% в осіб із ризиком розвитку ЦД 2 типу [2, 52, 53, 184-187]. Особи з ЦД 2 типу та НАЖХП також мають підвищений ризик розвитку НАСГ із прогресуючим фіброзом, особливо особи старше 50 років із ЦД 2 типу або ожирінням [81]. Очевидно, що це прискорює прогресування захворювання печінки до НАЖХП та сприяє її розвитку в молодшому віці [6].
1.5. Коли дорослого треба направити до гастроентеролога/гепатолога для лікування?
Доказова база щодо пунктів 1.5.1, 1.5.2. Початкові кроки у веденні осіб із НАЖХП передбачають оцінку та лікування кардіометаболічних ризиків, таких як вісцеральне ожиріння, ЦД 2 типу, гіпертензія та дисліпідемія, пов’язаних із НАЖХП [192]. Особи з ожирінням і ЦД 2 типу мають підвищений ризик розвитку НАЖХП, ускладнений НАСГ та прогресуючим фіброзом [9, 10, 102, 110, 114, 188-190]. Незважаючи на те що лише в незначної кількості осіб НАЖХП прогресує до тяжкого захворювання печінки та потребує спеціальної допомоги, її виявлення часто може бути ускладнене. Ще одна проблема полягає в тому, що більшість хворих із прогресуючим захворюванням печінки в контексті НАЖХП можуть не мати симптомів. Таким чином, стратифікація високого ризику в осіб або тих, хто має діагностовану НАЖХП, за допомогою простих клінічно доступних методів дослідження має вирішальне значення для виявлення пацієнтів із вищим ризиком пов’язаних із печінкою наслідків, у тому числі смертності, які потрібно мати на увазі в спеціальних практиках, а також тих, кого можна лікувати в закладах ПМД або в ендокринологічній клініці.
Додаткове лікування осіб із НАЖХП залежить від стадії та тяжкості захворювання печінки. Стадія фіброзу є важливим предиктором віддалених наслідків [43, 148, 195]. Знову ж таки, початкові кроки стратифікації ризику з використанням алгоритмів, наведених на рисунках 1 і 2, мають виконуватися ендокринологами та в установах ПМД [194, 196-198]. Особи, які мають докази прогресуючого захворювання печінки (наприклад, асцит, печінкова енцефалопатія, варикозне розширення вен стравоходу, гіперспленізм / низька кількість тромбоцитів або ознаки синтетичної дисфункції печінки, що характеризується низьким рівнем альбуміну і/або ознаками подовженого протромбінового часу / міжнародного нормалізованого співвідношення), можуть потребувати консультації та лікування в гастроентеролога чи гепатолога. У цьому контексті може знадобитися оцінка ризику з використанням додаткових тестів, у тому числі біопсії печінки. Насправді біопсія печінки важлива не лише для виключення супутніх причин захворювання печінки (наприклад, автоімунного гепатиту та перевантаження залізом), але й для точного встановлення стадії захворювання, оскільки аналізи крові та візуалізація дають суперечливі результати. Крім того, біопсія печінки необхідна для участі в більшості клінічних випробувань нового фармакологічного лікування НАСГ. На додачу до біопсії печінки гастроентерологи або гепатологи вестимуть пацієнтів із прогресуючими захворюваннями печінки, що передбачає періодичний скринінг на ГЦК, великі варикозні розширення вени стравоходу, прогресування захворювання печінки та своєчасне направлення на трансплантацію печінки.
Продовження – у наступних номерах.
Список літератури – у редакції.
Реферативний огляд статті Cusi K. et al. American Association of Clinical Endocrinology Clinical Practice Guideline for the Diagnosis and Management of Nonalcoholic Fatty Liver Disease in Primary Care and Endocrinology Clinical Settings. Co-Sponsored by the American Association for the Study of Liver Diseases (AASLD). Endocrine Practice. 28 (2022). 528-562.
Підготувала Дарина Павленко
Повну версію дивіться: https://www.endocrinepractice.org/article/S1530-891X(22)00090-8/fulltext
Тематичний номер «Діабетологія. Тиреоїдологія. Метаболічні розлади» № 1 (61) 2023 р.