17 грудня, 2021
Езетиміб і покращення кардіоваскулярних наслідків: сучасні докази та перспективи
Призначення статинів з метою первинної та вторинної профілактики доведено зменшує ризики несприятливих серцево-судинних подій шляхом зниження холестерину ліпопротеїнів низької щільності (ХС ЛПНЩ). Однак у деяких випадках, незважаючи на високодозову терапію статинами, в пацієнтів зберігаються залишкові серцево-судинні ризики через недостатню ефективніть терапії. Альтернативою для таких пацієнтів може бути езетиміб, який при додаванні до тепапії статином значно підвищує ефективніть гіполіпідемічної терапії.
У великому дослідженні IMPROVE-IT продемонстровано виражене зниження частоти серйозних кардіоваскулярних подій серед учасників, які отримували езетиміб у комбінації зі статинами. Позитивний ефект езетимібу спостерігався серед пацієнтів чоловічої та жіночої статі, в т. ч. у людей похилого віку, хворих на хронічну ниркову недостатність (ХНН), цукровий діабет (ЦД), а також у пацієнтів, котрим раніше було проведене шунтування коронарної артерії. Езетиміб (як і статини) відіграє роль у зниженні біомаркерів запалення та сприяє регресуванню холестеринових бляшок. Завдяки вищезазначеним позитивним ефектам, а також сприятливому профілю безпеки езетиміб широко використовується в комбінації зі статинами у випадках, коли монотерапія не дозволяє досягти цільових рівнів ХС ЛПНЩ, а також у разі індивідуальної непереносимості статинів. Призначення езетимібу регламентоване в новітніх клінічних рекомендаціях Американської колегії кардіологів та Американської асоціації серця (ACC/AHA), а також Європейського товариства кардіологів (ESC).
Боротьба з гіперліпідемією: статинів може бути недостатньо
Як відомо, відкладення ЛПНЩ, які містять аполіпопротеїн В (Apo-B), у стінках артерій спричиняє атеросклероз. Атеросклеротичні кардіоваскулярні хвороби (АСКВХ), до яких належать гострий коронарний синдром (ГКС), інфаркт міокарда (ІМ), ішемічна хвороба серця (ІХС), інсульт і транзиторна ішемічна атака, атеросклероз периферичних судин, – найчастіші причини смерті в усьому світі. Саме тому вкрай важливою є первинна та вторинна профілактика АСКВХ шляхом контролю факторів ризику, як-от гіперхолестеринемія, діабет та артеріальна гіпертензія. В багатьох клінічних та епідеміологічних дослідженнях продемонстрований взаємозв’язок між рівнем ХС ЛПНЩ плазми та ризиком АСКВХ: так, високий рівень ХС ЛПНЩ має позитивну кореляцію із серцево-судинним ризиком, тоді як тривале підтримання низьких рівнів ХС ЛПНЩ знижує ризик кардіоваскулярних ускладнень (Chen, Peto, Collins et al., 1991; Stamler, Vaccaro, Neaton, Wentworth, 1993).
Статини є найрозповсюдженішими гіполіпідемічними препаратами. Фармакологічна мішень статинів – фермент 3-гідрокси‑3-метилглутарил-коензим А‑редуктази (ГМГ-КоА‑редуктази), що каталізує біосинтез холестерину в гепатоцитах. Метааналіз 27 рандомізованих досліджень (загальна кількість учасників склала 174 000) продемонстрував, що при кожному зниженні ХС ЛПНЩ на 1 ммоль/л за допомогою статинів ризик загрозливих кардіоваскулярних подій зменшується на 20-25%, а загальна смертність – на 10% (Mihaylova, Emberson, Blackwell et al., 2012).
Статини дозволяють знизити плазмові рівні ХС ЛПНЩ на 30-50%, проте їхній прийом асоційований з компенсаторним збільшенням продукції печінкових рецепторів ЛПНЩ, отже, й з підсиленням захоплення сироваткових ЛПНЩ у печінці. Водночас спостерігається активніша абсорбція ЛПНЩ у тонкому кишечнику (Huff, Burnett, 1997).
У метааналізі основних клінічних випробувань терапевтичної дії статинів доведено, що навіть після інтенсивного лікування статинами в пацієнтів зберігається певний залишковий ризик серцево-судинних ускладнень. П’ятирічна частота серйозних кардіоваскулярних подій становила 22% серед учасників із серцево-судинними захворюваннями в анамнезі; для пацієнтів, котрі не мали раніше описаних хвороб серцево-судинної системи, такий ризик сягнув 10% (Baigent, Keech, Kearney, 2005). Цей залишковий ризик може бути спричинений ліпідозалежними (високий рівень тригліцеридів і низький рівень ліпопротеїнів високої щільності), а також ліпідонезалежними факторами, як-от рівень запалення. Пошук альтернативних варіантів гіполіпідемічної терапії протягом минулого десятиріччя дозволив езетимібу вийти на передній план як дієвому засобу, що знижує рівні ХС ЛПНЩ плазми та допомагає зменшити кардіоваскулярні ризики.
Езетиміб знижує абсорбцію ліпідів ентероцитами тонкого кишечнику, інгібуючи холестеринові транспортні білки, в т. ч. схожий на протеїн Німанна – Піка С1-рецептор 1 (NPC1L1P). Комбіноване лікування статинами (тобто інгібіторами холестериногенезу в печінці) й інгібіторами кишкової абсорбції ЛПНЩ демонструє кумулятивний гіполіпідемічний ефект, що є важливим для пацієнтів, які не можуть досягти цільових рівнів ХС ЛПНЩ під час монотерапії статинами та мають високі залишкові ризики серцево-судинних ускладнень (Guyton, 2010).
Дослідження IMPROVE-IT
У масштабному міжнародному клінічному дослідженні IMPROVE-IT порівнювалися ефекти комбінації симвастатину й езетимібу та монотерапії симвастатином у пацієнтів, які перенесли ГКС упродовж останніх 10 діб (Cannon, Blazing, Giugliano et al., 2015). Усі учасники на момент проведення випробування знаходилися в стабільному стані та мали рівні ліпідів крові в межах, регламентованих клінічними рекомендаціями. До дослідження залучили пацієнтів віком >50 років (із ГКС протягом останніх 10 днів).
Критерії виключення: кліренс креатиніну <30 мл/хв, захворювання печінки в активній стадії, заплановане коронарне шунтування. Первинна контрольна точка дослідження: сумарна частота таких подій, як смерть унаслідок серцево-судинного захворювання, інсульт, ІМ, ГКС, потреба в екстреній коронарній реваскуляризації (за умови, що такі події сталися протягом 30 днів від рандомізації та не зумовили смерті пацієнта). Вторинні контрольні точки: загальна смертність, серйозні кардіоваскулярні наслідки, інсульт, або сумарна частота смертельних випадків від ІХС, ІМ, що не спричинив смерті пацієнта, а також ургентна коронарна реваскуляризація через >30 днів після рандомізації, або загальна частота смертей унаслідок серцево-судинних захворювань, ІМ, що не зумовив смерті пацієнта, госпіталізацій щодо ГКС, а також частота ургентних і планових операцій з коронарної реваскуляризації, проведених через >30 днів після рандомізації.
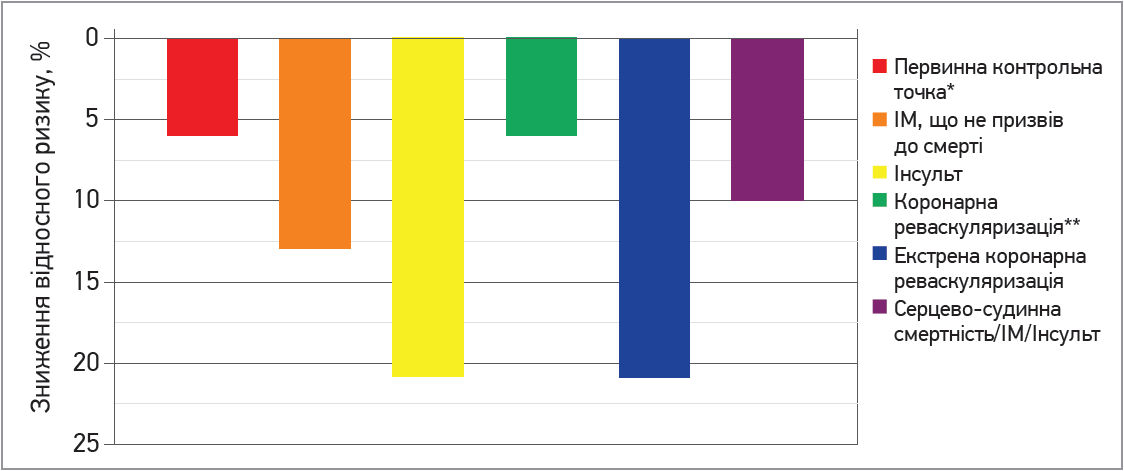
Середній вік учасників дослідження складав 64 роки; частка жінок становила 24%, чоловіків – 76%, а також 27% мали ЦД. У 88% досліджуваних в анамнезі була коронарна ангіографія; для 70% учасників проведено підшкірне коронарне втручання під час госпіталізації, що передувало початку клінічного дослідження. Лише 34% учасників отримували терапію статинами перед тим, як бути госпіталізованими; після вищезазначеної госпіталізації частка пацієнтів, котрим були призначені статини, зросла до 77%. Після 1-го року терапії середній рівень ХС ЛПНЩ у групі симвастатину складав 1,74 ммоль/л, а в групі симвастатину й езетимібу – 1,33 ммоль/л. На 7-му році частота досягнення первинної контрольної точки, а також всіх трьох вторинних точок була значно нижчою в групі симвастатин + езетиміб (рис.). Позитивні наслідки прийому езетимібу відзначалися в усіх підгрупах, найбільше – серед хворих віком >75 років і пацієнтів із ЦД.
Рис. Клінічні переваги комбінації езетимібу та симвастатину, досягнуті в рамках дослідження IMPROVE-IT
Примітки: * первинною контрольною точкою була сумарна частота кардіоваскулярної смертності, серйозних серцево-судинних наслідків та інсультів, що не спричинили смерті;
** незначні переваги. У рамках дослідження не виявлено значимої різниці в частоті серцево-судинної смертності та ГКС.
Схожі результати отримано у випробуванні I-ROSETTE (Hong et al., 2018). У пацієнтів із гіперхолестеринемією комбінація езетимібу й розувастатину значно покращувала ліпідний профіль (ХС ЛПНЩ знизився на 50%) без будь-яких додаткових побічних ефектів. Комбінована терапія переносилася навіть краще, ніж еквівалентна доза розувастатину, завдяки різним метаболічним шляхам дії двох препаратів.
Додаткові переваги езетимібу для пацієнтів похилого віку
Похилий вік є фактором підвищеного ризику розвитку серйозних ускладнень ГКС. Хоча люди віком >75 років складають лише <6% загального пулу пацієнтів із ГКС, у цій підгрупі стається до 65% усіх смертей, пов’язаних із ГКС (Vezum, Makdisse, Spencer et al., 2005; Mozaffarian, Benjamin, Go et al., 2016). Високі дози статинів часто призводять до побічних ефектів у людей похилого віку; вважається, що застосування комбінації езетимібу та статинів дозволяє досягнути цільових рівнів ХС ЛПНЩ без суттєвого підвищення частоти небажаних реакцій. Саме такі результати були отримані в дослідженні IMPROVE-IT: поєднання езетимібу та статинів допомогло значно знизити рівні ХС ЛПНЩ плазми і, відповідно, кардіоваскулярні ризики в учасників віком понад 75 років. Цікаво, що абсолютне зменшення ризику досягнення первинних контрольних точок у літніх пацієнтів було значно вираженішим, ніж у молодших учасників (Bach, Cannon, Giugliano et al., 2019).
Езетиміб у лікуванні пацієнтів із ЦД
ЦД в анамнезі збільшує ризик захворювань коронарних артерій і підвищує летальність під час та після епізоду ГКС (Donahoe, Stewart, McCabe et al., 2007). Пацієнти із ЦД демонструють вираженіші позитивні ефекти лікування езетимібом.
Підгрупа ЦД у складі дослідження IMPROVE-IT налічувала 4933 учасники (27%) (Giugliano, Cannon, Blazing et al., 2018). Серед цих пацієнтів із більшою ймовірністю зустрічалися жінки, люди похилого віку та хворі з ІМ або коронарним шунтуванням в анамнезі. Пацієнти із ЦД, які отримували комбіновану терапію, протягом 7 років продемонстрували абсолютне зниження ризику на 5,5% (співвідношення ризиків (СР) 0,85; 95% довірчий інтервал (ДІ) 0,78-0,94), натомість учасники групи монотерапії статинами за той же період показали абсолютне зниження ризику лише на 0,7% (СР 0,98; 95% ДІ 0,91-1,04; р=0,02). Найсильніше відносний ризик знизився для таких ускладнень, як ІМ (24%) та ішемічний інсульт (39%).
Застосування езетимібу в пацієнтів із ХНН
Хворі на ХНН мають підвищений ризик серцево-судинної смерті, предиктором якого слугує зниження швидкості клубочкової фільтрації (ШКФ) (Go, Chertow, Fan et al., 2004]. У метааналізі 14 публікацій, що досліджували дію статинів, була продемонстрована закономірність щодо зниження частоти первинних серцево-судинних ускладнень зі зменшенням сироваткових рівнів ХС ЛПНЩ; проте цей позитивний ефект нівелюється подальшим погіршенням ниркової функції і зниженням ШКФ (Baigent, Keech, Kearney, 2005).
Завдяки схвальним результатам клінічного дослідження SHARP, згідно з якими комбінація симвастатину та езетимібу дозволяє знизити ризики несприятливих кардіоваскулярних подій у пацієнтів із різними ступенями ХНН, у клінічних рекомендаціях ACC/AHA 2013 року було регламентоване використання езетимібу в пацієнтів із ШКФ <60 мл/хв (Stone, Robinson, Lichtenstein et al., 2013). Подібні результати були отримані й у дослідженні IMPROVE-IT, де 3791 учасник мав ШКФ <60 мл/хв. Додавання езетимібу до лікування статинами покращувало параметри ліпідів крові в усіх пацієнтів із ХНН. Також відмічалося зниження кардіоваскулярного ризику на 12% у підгрупі із середньою ШКФ <60 мл/хв і на 13% у підгрупі із середньою ШКФ <45 мл/хв (Stanifer, Charytan, White et al., 2017).
Езетиміб зменшує розміри холестеринових бляшок
Ще одним фактором, який дає змогу оцінити перебіг кардіоваскулярних захворювань і можливість виникнення ускладнень, є розмір холестеринових бляшок. Доведено, що прийом статинів модифікує перебіг атеросклерозу коронарних судин шляхом уповільнення росту бляшок та їх регресії. Дослідження PRECISE-IVUS мало на меті виявити, наскільки ефективніше комбінована гіполіпідемічна терапія буде зменшувати розмір атеросклеротичних уражень порівняно зі стандартним лікуванням статинами (Tsujita, Sugiyama, Sumida et al., 2015). За даними внутрішньосудинного УЗД у результаті комбінованої терапії об’єм бляшок знизився на 78% порівняно з 58% регресії бляшок унаслідок монотерапії.
Езетиміб у клінічних рекомендаціях
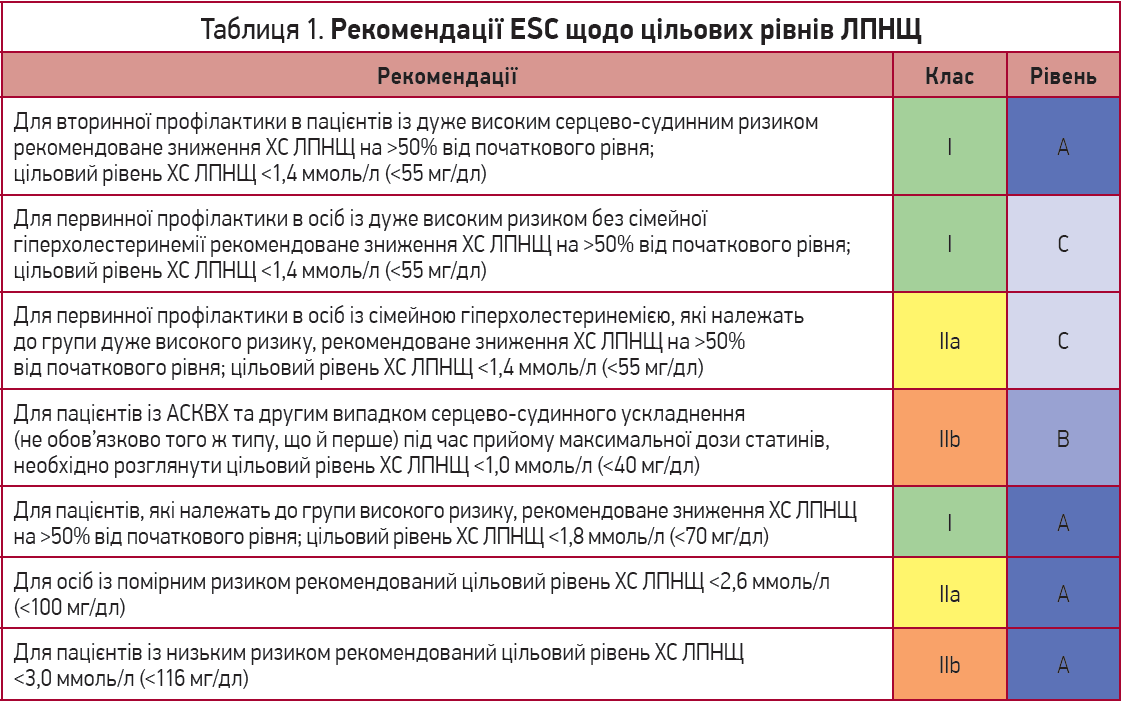
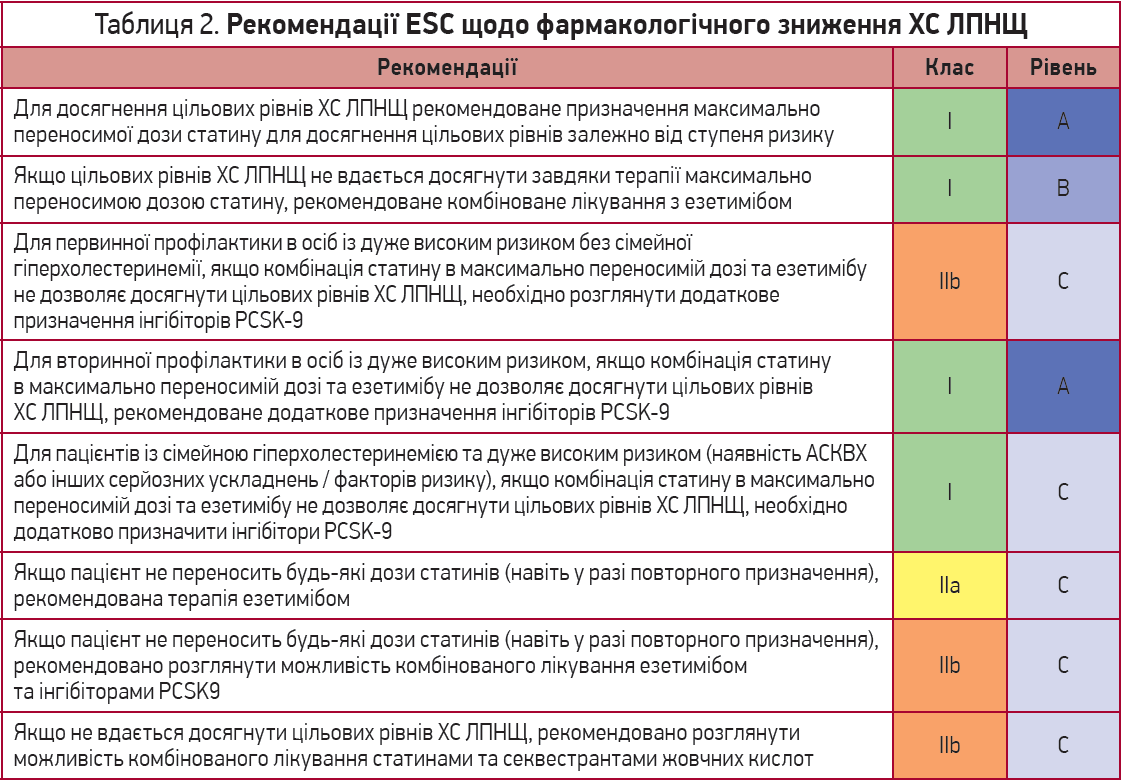
Згідно з рекомендаціями ACC/AHA 2018 року, пацієнтам із клінічними проявами АСКВХ, які належать до групи високого ризику, показано досягнути цільових значень ХС ЛПНЩ <70 мг/дл або знизити концентрацію ХС ЛПНЩ у плазмі на >50% від початкового рівня (Grundy, Stone, Bailey et al., 2018). Однак у новітніх рекомендаціях Європейської кардіологічної спілки (ESC) з менеджменту дисліпідемій зазначається, що для вторинної профілактики серцево-судинних ускладнень оптимальними рівнями ХС ЛПНЩ будуть <55 мг/дл або зниження на >50% від початкового рівня (Mach, Baigent, Catapano et al., 2019). Рекомендації ESC щодо цільових рівнів ХС ЛПНЩ подано в таблиці 1. Якщо максимально переносимі дози статинів не дозволяють досягнути таких показників, то обидва документи рекомендують додати до гіполіпідемічної терапії езетиміб (рекомендації класу ІІа в настановах ACC/AHA 2018, рекомендації класу І в настановах ESC 2019). Рекомендації ESC щодо фармакологічного зниження ХС ЛПНЩ наведено в таблиці 2.
Висновки
Підвищення вмісту ХС ЛПНЩ у плазмі має ключову роль у розвитку атеросклерозу та пов’язаних з ним серцево-судинних захворювань. Статини є основною групою препаратів, що знижують рівні ХС ЛПНЩ, отже, й ризики кардіоваскулярних ускладнень. Однак значний відсоток пацієнтів демонструє недостатній контроль ліпідемії навіть за прийому максимальних доз статинів. Для підвищення ефективності гіполіпідемічної терапії та зниження кардіоваскулярного ризику доцільно використовувати альтернативні гіполіпідемічні препарати. Одним з таких варіантів, що ефективно знижує рівні ХС ЛПНЩ як у монотерапії, так і в комбінації зі статинами, є езетиміб. Цей лікарський засіб належить до інгібіторів абсорбції ліпідів у тонкому кишечнику, він доповнює дію статинів, які блокують синтез холестерину в гепатоцитах. Використання езетимібу в поєднанні зі статином дозволяє знизити рівні ХС ЛПНЩ на 65%, в той час як монотерапія статином – лише на 30-50%. Позитивні ефекти комбінації статинів та езетимібу (як-от виражене зменшення ризиків первинних і повторних серцево-судинних ускладнень, регресія атеросклеротичних бляшок, зниження рівнів біомаркерів запалення) продемонстровані в багатьох клінічних дослідженнях, наймасштабнішим з яких є міжнародне дослідження IMPROVE-IT, опубліковане в 2015 році. Езетиміб не лише добре переноситься пацієнтами похилого віку та особами, котрі мають ХНН або ЦД, а й доводить свою перевагу в зниженні ХС ЛПНЩ і серцево-судинних ризиків саме серед цих підгруп. Езетиміб демонструє високу ефективність, безпечність та сприятливий профіль лікарських взаємодій, що є украй важливим для пацієнтів із серцево-судинними захворюваннями, які часто мають значні рівні коморбідності та лікарського навантаження. Завдяки цим перевагам езетиміб внесено до сучасних клінічних рекомендацій з ведення гіперліпідемії.
Стаття друкується у скороченні.
Список літератури знаходиться в редакції.
Pradhan A., Bhandari M., Sethi R. Ezetimibe and Improving Cardiovascular Outcomes:
Current Evidence and Perspectives. Cardiol Res Pract. 2020 Jun 28;2020:9815016.
Переклала з англ. Ганна Гаврюшенко