22 серпня, 2023
Вплив прихильності до терапії на реальну ефективність аналогів простагландинів при глаукомі
Глаукома – один із найбільших глобальних медичних викликів, що ставить під загрозу зір мільйонів людей по всьому світу. Незважаючи на значний прогрес у розробці топічних препаратів, реальна ефективність лікування глаукоми залишається недостатньо вивченою. Традиційні дослідження ефективності цих ліків зазвичай проводять у контрольованих умовах, де реальні фактори, як-от перевантаження інформацією, мультизадачність, стрес, відволікаючі фактори та кратність застосування препарату на добу, практично не враховуються. Однак вони можуть впливати – і впливають на прихильність пацієнтів до терапії, що, своєю чергою, змінює реальну ефективність лікування. Отже, дані та спостереження, які беруть до уваги ці фактори та здійснюють оцінку ефективності в умовах, максимально наближених до реального життя пацієнта з глаукомою, становлять великий інтерес.
Основним чинником ризику прогресування глаукоми вважається підвищений внутрішньоочний тиск (ВОТ), який визначають як стійке перевищення показника у 21 мм рт. ст. (Kniestedt С. et al., 2008). Відповідно, стандартом медичної допомоги при глаукомі є зниження ВОТ та стійка підтримка його у межах норми. Оскільки рівень ВОТ є наслідком балансу між виробленням водянистої вологи війчастим тілом та її відтоком через трабекулярну мережу й увеосклеральний тракт, досягти зниження ВОТ можна шляхом пригнічення утворення водянистої вологи або сприяння її відтоку. Однак слід зауважити, що оскільки водяниста волога є основним джерелом живлення та оксигенації аваскулярної рогівки і кришталика, перевагу варто надавати тактиці сприяння відтоку. Найчастіше застосовуваними препаратами першої лінії лікування глаукоми є аналоги простагландинів (АПГ), які покращують відтік водянистої вологи обидвома шляхами. АПГ є найдієвішими і найпотужнішими препаратами, які можна застосовувати один раз на день (Klimko P. G., Sharif N. A., 2018). Впровадження в клінічну практику АПГ, яке розпочалося у середині 1990-х рр., революціонізувало лікування глаукоми. Порівняно з іншими препаратами для зниження ВОТ (приміром, β-адреноблокатором тимололом та агоністом α-адренорецепторів бримонідином) АПГ демонструють значно вищу гіпотензивну активність та більшу тривалість дії (Cheema A. et al., 2016). Показано, що після припинення застосування АПГ зниження ВОТ зберігається протягом 84 год (Dubiner H. B. et al., 2004). За даними R. Rashmiel та співавт. (2006), впровадження лікування АПГ в Онтаріо (Канада) асоціювалося зі зниженням потреби у хірургічних втручаннях з приводу глаукоми з 1996 до 2004 року на 20%.
Зниження варіабельності ВОТ для запобігання прогресуванню хвороби
Окрім зниження ВОТ, ключовим фактором успіху в довготривалій терапії глаукоми має значення мінімізація варіабельності ВОТ протягом доби, оскільки значні перепади ВОТ сприяють прогресуванню хвороби (Parrish R. K. et al., 2003).
Загалом ВОТ притаманна тенденція коливатися протягом доби, досягаючи піку рано вранці або у горизонтальному положенні. Велике дослідження за участю осіб з рефрактерною відкритокутовою глаукомою під назвою Advanced Glaucoma Intervention Study (AGIS) виявило, що на кожен 1 мм рт. ст. підвищення коливань ВОТ ризик зменшення поля зору зростає на 30%, а потреба в інвазивному втручанні – на 74% (Nouri-Mahdavi K. et al., 2004).
Дослідження J. H. Kim та J. Caprioli (2018), присвячене впливу коливань ВОТ на прогноз пацієнтів з глаукомою, дійшло висновку, що у лікуванні глаукоми слід акцентувати увагу саме на модуляції ВОТ, а не на простому його зниженні. Для контролю перебігу ПВКГ у клінічній практиці необхідний не лише низький, а й постійний (стабільний) ВОТ. Підтримка сталого ВОТ з мінімізацією його піків запобігає прогресуванню хвороби, особливо в пацієнтів, стан зорової функції яких погіршується, незважаючи на досягнене зниження ВОТ.
Таким чином, у лікуванні глаукоми підтримка стабільного профілю ВОТ протягом доби та триваліших періодів часу має більше значення, ніж простий гіпотензивний ефект. Крім того, останнього можна досягти за допомогою будь-якого класу протиглаукомних препаратів або комбінації препаратів кількох класів, натомість для оптимального зниження коливань ВОТ доцільно призначення АПГ.
Прихильність до терапії глаукоми як ключовий фактор ефективності лікування
Як і у випадку будь-якого лікування, яке пацієнт приймає (вводить, закрапує) самостійно, головним критерієм, який обмежує ефективність ліків, є недостатня прихильність до лікування (Tsai J. C., 2009). Покращити цей показник допомагають низька частота застосування та мінімальна кількість побічних ефектів; у лікуванні глаукоми обидві ці властивості притаманні АПГ (Klimko P. G., Sharif N. A., 2018).
Саме висока і довготривала прихильність (персистенція) до лікування ПВКГ дозволяє досягти успіху терапії та уникнути зайвих витрат на лікування. Важливість прихильності при глаукомі співставна з показниками при інших хронічних безсимптомних чи малосимптомних хворобах, як-от цукровий діабет чи артеріальна гіпертензія, але через відсутність яскравої симптоматики пацієнти часто не розуміють доцільності щоденного постійного лікування (Alany R. G., 2013). Наприклад, до лікування артеріальної гіпертензії неприхильні 50-80% хворих (Brown M. T., Bussell J. K., 2011). Недостатня прихильність асоціюється з поганою ефективністю лікування, прогресуванням хвороби, розвитком ускладнень та потребою в госпіталізації (Monnette A. et al., 2018), а також підвищує сумарні витрати на лікування (McGuire M., 2014). Що стосується конкретно глаукоми, недостатню прихильність нерідко помилково вважають невдачею лікування, що призводить до непотрібних змін схем гіпотензивного лікування, зайвих хірургічних втручань та, знов-таки, збільшення витрат на медичну допомогу (Quaranta L. et al., 2023). Натомість висока прихильність до антиглаукомних препаратів покращує якість життя та зменшує витрати (Newmann-Casey Р.А. et al., 2015).
Причинами недостатньої прихильності до лікування глаукоми є звичайна забудькуватість, велика кількість призначених засобів, недостатня обізнаність щодо патофізіології глаукоми та часта відсутність негайного сприятливого ефекту (прогресуюча природа ПВКГ не дає пацієнту можливості одразу помітити виразне зменшення симптоматики). Крім того, прихильність до топічних офтальмологічних препаратів нерідко погіршується внаслідок розладів рухової функції, які перешкоджають точному закрапуванню препарату, незадовільної координації та низької гостроти зору (Robin A., Grover D., 2011). A. G. Konstas та співавт. (2004) поділяють причини неприхильності до топічного лікування глаукоми на дві групи: мимовільні (забування, труднощі з інстиляцією) та добровільні (відмова від препаратів внаслідок побічних ефектів).
Літературні дані свідчать, що серед пацієнтів з глаукомою, які дожили до 90 років, поширеність моно- або білатеральної втрати зору становить 42,6% для неприхильних до лікування осіб і лише 19% для прихильних. Серед стратегій покращення прихильності пропонується особисте консультування і навчання пацієнтів, перегляд навчальних відеоматеріалів, інтерактивні тренінги під керівництвом медсестер та роз’яснення важливості дотримання призначеного режиму лікування для отримання належного ефекту. Важливе значення має також спрощення режиму лікування, бажано застосування монотерапії (Quaranta L. et al., 2023).
Прихильність пацієнтів залежить і від класу препаратів: у кількох дослідженнях найкращі показники прихильності та персистенції продемонстровані для АПГ (Dasgupta S. et al., 2002; Diestelhorst M. et al., 2003; Nordstrom B. L. et al., 2005). Так, лише 33-39% пацієнтів, які отримували тимолол, продовжили приймати його через рік, натомість стійка прихильність до АПГ склала близько 70% (Schwartz G. F. et al., 2008; 2004).
Тафлупрост: АПГ з широким спектром переваг
Тафлупрост є новим АПГ, афінність якого до простагландинових рецепторів FP класу у 12 разів перевищує аналогічний показник латанопросту. Тафлупрост практично не має потенціалу зв’язування з іншими рецепторами, що свідчить про його високу селективність. Остання забезпечує кращу переносимість, низьку частоту локальних побічних ефектів та можливість застосування засобу в нижчій концентрації. Крім того, розчини тафлупросту містять у 20 разів меншу концентрацію бензалконію хлориду (БАХ), ніж краплі латанопросту, а саме 0,001%, а безконсерватна форма тафлупросту повністю позбавлена БАХ. Зменшення вмісту і відсутність БАХ у складі дозволяє мінімізувати несприятливий вплив топічного препарату на поверхню ока (ПО) (Takagi Y. et al., 2004). БАХ є найпоширенішим консервантом для мультидозових офтальмологічних препаратів, однак цей консервант може ушкоджувати ПО, порушуючи її ліпідний шар. Несприятливі цитотоксичні ефекти БАХ та здатність цього консерванту провокувати симптоми хвороби сухого ока є дозозалежними, що неодноразово було підтверджено клінічними дослідженнями (Pellinen P. et al., 2012; Hommer A., 2010). Показано, що перехід з латанопросту або травопросту на тафлупрост забезпечує зниження вираженості поверхневої точкової кератопатії у 75% пацієнтів з глаукомою (Kumagami T. et al., 2014).
Оскільки топічні офтальмопрепарати не забезпечують повного одужання пацієнтів з ПВКГ чи офтальмогіпертензією, а лише підтримують ВОТ на належному рівні, щоб запобігти прогресуванню хвороби, пацієнтам необхідне постійне тривале лікування. У зв’язку з цим однією з головних задач лікування глаукоми полягає у адекватному контролі ВОТ водночас із мінімізацією шкідливого впливу БАХ на ПО (Wong T. T. et al., 2018).
Клінічні дослідження безконсервантного та низькоконсервантного тафлупросту
J.-K. Lin та співавт. (2022) перевели учасників свого дослідження з 0,005% розчину латанопросту на 0,0015% розчин тафлупросту зі зниженим вмістом БАХ. Основним критерієм покращення стану ПО виступало забарвлення флуоресцеїном. Вихідна оцінка забарвлення за шкалою National Eye Institute (NEI) становила 7,1±3,2 бала, а через 12 тиж лікування – 5,3±1,8 бала. Покращення оцінки за шкалою NEI мало місце у 64,7% учасників. Стан ПО покращився і за вторинними кінцевими точками. Так, частка осіб без ознак гіперемії кон’юнктиви очного яблука зросла з 58,8% (вихідний показник) до 82,4% через 4 тиж та 94,1% через 12 тиж. Аналогічно, частка пацієнтів без ознак гіперемії кон’юнктиви повік зросла з 64,7% до 82,4% та 94,1% відповідно. Було також зафіксовано збільшення часу розриву слізної плівки на 40,8% (0,8±1,5 с; p<0,05) через 4 тиж та на 70,6% (1,2±1,7 с; p<0,05) через 12 тиж. Більшість учасників дослідження відзначили також зменшення таких дискомфортних відчуттів, як подразнення, печіння, свербіж, відчуття стороннього тіла в оці, сльозотеча. Слід зауважити, що покращення стану ПО мало місце на тлі утримання належного контролю над ВОТ. Низький ризик побічних ефектів для ПО при застосуванні 0,0015% тафлупросту із зниженим вмістом БАХ потенційно здатний покращити прихильність до лікування, що має вагоме значення для лікування таких хронічних патологічних станів, як глаукома. Наприкінці дослідження 88,2% пацієнтів повідомили про 100% прихильність до лікування, тобто про повну відсутність пропущених доз призначеного препарату.
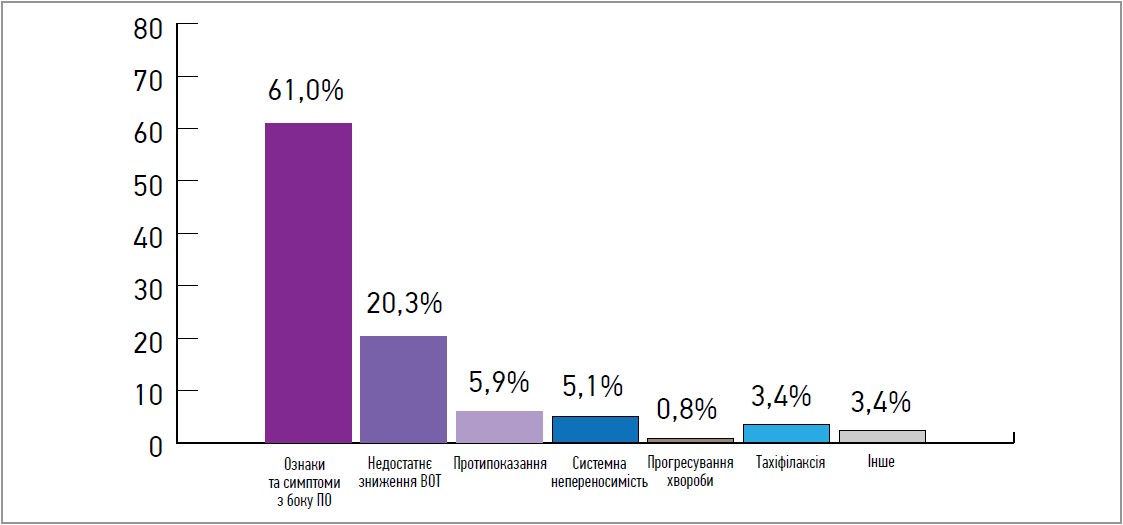
У подібному за дизайном проспективному багатоцентровому обсерваційному відкритому дослідженні A. Hommer та F. Kimmich (2011) пацієнтів з глаукомою, які отримували монотерапію різними консервантними АПГ (латанопростом, травопростом або біматопростом), перевели на безконсервантний тафлупрост. Найчастішою причиною зміни препарату були симптоми з боку ПО (рис. 1).
Рис. 1. Причини переходу з інших АПГ на тафлупрост
Через 12 тиж лікування ВОТ учасників достовірно знизився: з 16,2±4,3 мм рт. ст. до 14,8±3,2 мм рт. ст. Крім того, після переходу на безконсервантний тафлупрост стан очей пацієнтів покращився і за суб’єктивними, і за об’єктивними ознаками. Кількість осіб з помірно вираженою та тяжкою гіперемією ПО після лікування тафлупростом знизилася з 43,2% до 1,9%. Після завершення клінічного дослідження 89,8% пацієнтів прийняли рішення продовжувати монотерапію безконсервантним тафлупростом.
Автори дійшли висновку, що безконсервантний тафлупрост у концентрації 0,0015% був дієвим та безпечним, а також відмінно переносився пацієнтами. Перехід з консервантних латанопросту, травопросту чи біматопросту на безконсервантний тафлупрост давав можливість не лише удосконалити контроль ВОТ, а й поліпшити стан ПО. Отже, перехід на безконсервантний тафлупрост доцільний для пацієнтів з подразненням ПО у відповідь на консервантні антиглаукомні препарати, а також для осіб з недостатньою відповіддю на інші АПГ.
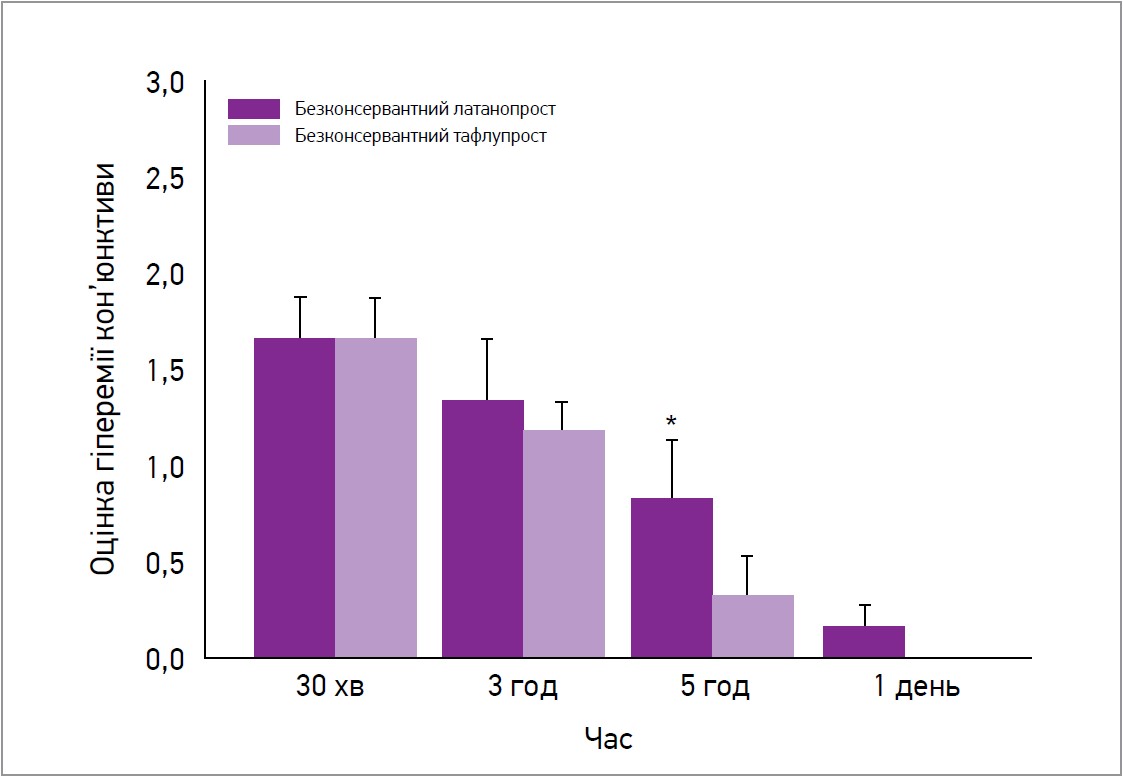
Слід зауважити, що навіть за відсутності консервантів різні АПГ мають різний вплив на ПО. Безконсервантний латанопрост спричиняє більш виражене подразнення in vivo та знижує виживаність епітеліальних клітин рогівки людини in vitro, ніж безконсервантний тафлупрост (рис. 2) (Esaki Y. et al., 2016).
Рис. 2. Оцінка гіперемії кон’юнктиви після інстиляції безконсервантних препаратів латанопросту та тафлупросту
T. T. Wong та співавт. (2018) оцінили результати переходу пацієнтів з ПВКГ чи офтальмогіпертензією з 0,005% латанопросту на низькоконсервантний 0,0015% тафлупрост. Через 3 міс лікування тафлупростом оцінка забарвлення флуоресцеїном знизилася з 6,9±3,1 до 3,3±2,7 бала (р<0,001). Було також зафіксовано достовірне збільшення часу розриву слізної плівки, зменшення гіперемії та зниження вираженості суб’єктивних симптомів з боку ПО (відчуття стороннього тіла, подразнення, печіння, свербіж, фотофобія).
Нещодавній метааналіз J. A. Tumbocon та співавт. (2022) підтвердив описані вище результати. Цікаво, що у цьому метааналізі оцінювали перехід зі стандартних консервантних АПГ не лише на безконсервантний тафлупрост, а й на тафлупрост зі зниженим вмістом БАХ. Перехід на ці форми тафлупросту забезпечував середнє зниження ВОТ на 5,9% (0,91 мм рт. ст.), хоча різниця не досягла рівня статистичної достовірності. Водночас мало місце достовірне зменшення інтенсивності забарвлення рогівки флуоресцеїном на 47,9% та достовірне збільшення часу розриву слізної плівки на 1,06 с. Побічні ефекти спостерігали лише в 3% пацієнтів. Таким чином, у реальній клінічній практиці перехід з інших АПГ, які дають задовільний контроль ВОТ і нерідко застосовуються роками, на безконсервантний або низькоконсервантний тафлупрост удосконалює контроль офтальмотонусу та забезпечує виражене поліпшення стану ПО. Останнє покращує прихильність пацієнта до лікування, дозволяючи йому тривало дотримуватися призначеного режиму терапії. Перелічені фактори сприяють уповільненню прогресування глаукоми.
Постмаркетингові дослідження демонструють, що тафлупрост володіє сприятливим профілем безпеки не лише як монотерапія, а й у поєднанні з іншими класами гіпотензивних препаратів: інгібіторами карбоангідрази, симпатоміметиками, β-блокаторами, іншими АПГ тощо. Найчастіше побічні явища спостерігали в осіб, які комбінували тафлупрост з іншими АПГ, а найрідше – при сполученні з інгібіторами карбоангідрази (Chen X. L. et al., 2023).
Окрім описаних вище переваг, протягом останніх років збільшується доказова база іще одного сприятливого ефекту тафлупросту – здатності покращувати кровоплин в оці. Поліпшення кровообігу в голівці зорового нерва та сітківці, зокрема в макулярній ділянці, а також зниження амплітуди кров’яного пульсу в оці (різниці між систолічним та діастолічним ВОТ) є незалежними від зниження ВОТ позитивними впливами тафлупросту, які забезпечують йому лідерські позиції серед інших АПГ. Ці впливи мають вагоме клінічне значення при глаукомі, оскільки цій хворобі притаманне зниження швидкості кровоплину, його об’ємних показників, а також щільності кровоносних судин (Zhang X. et al., 2022). Встановлено, що тафлупрост має виражену нейропротекторну дію. В експериментальному дослідженні тафлупрост пригнічував апоптоз гангліонарних клітин сітківки та підвищував їхню виживаність при механічному пошкодженні (Kanamori А. et al., 2009).
Висновки
У лікуванні глаукоми важливе значення має не лише нормалізація ВОТ, а і його стабілізація із відсутністю перепадів протягом доби. Досягти такого результату дозволяють АПГ, які не лише знижують ВОТ, а й вирівнюють його добовий профіль. Ще одним важливим питанням терапії глаукоми, як і всіх хронічних мало- і безсимптомних хвороб, є підтримка довготривалої прихильності (персистенції) до лікування.
АПГ тафлупрост дієво знижує ВОТ без добових коливань та завдяки хорошій переносимості забезпечує високу довгострокову прихильність пацієнтів до лікування. Як наслідок, застосування тафлупросту уповільнює прогресування глаукоми. Доказова база тафлупросту побудована на оригінальному препараті Тафлотан® («Сантен Ой», Фінляндія), який було випробувано у понад 300 багатоцентрових досліджень.
Тафлотан® містить знижену концентрацію БАХ, тому його переносимість є досить високою, а побічні ефекти виникають рідко. Якщо ж у пацієнта наявна непереносимість навіть низьких концентрацій БАХ, доцільно застосування Тафлотан® Мульті – безконсервантного тафлупросту в мультидозовому флаконі. Тафлотан® Мульті дає можливість ефективно знижувати ВОТ та мінімізувати його добову варіабельність, уникаючи усіх побічних ефектів, асоційованих із БАХ.
Підготувала Лариса Стрільчук
Медична газета «Здоров’я України 21 сторіччя» № 13-14 (549-550), 2023 р