12 червня, 2016
Репродукция и энергетический баланс: интегративная роль пролактина

Cимптоматика гиперпролактинемического гипогонадизма (ГГ), как следует из определения нозологии, прежде всего характеризуется нарушениями функции репродуктивной системы. В то же время к частым проявлениям заболевания относятся избыточная масса тела и ожирение. Применение патогенетических препаратов – агонистов дофамина – сопровождается не только подавлением роста пролактинсекретирующей опухоли, восстановлением репродуктивной функции, но и устранением негативных метаболических последствий патологической гиперпролактинемии. Результаты исследований, выполненных в последние годы, позволили уточнить роль пролактина в регуляции энергетического баланса.
Избыточная масса тела и ожирение у больных с ГГ
По данным M. Orbetzova и соавт. (2002), среди 126 обследованных пациентов с ГГ наличие избыточной массы тела отмечено в 60% случаев, в т. ч. непосредственно ожирение – у 23% больных.
В исследовании J. Pereira Lima и соавт. (2013), включавшем 138 пациентов с гиперпролактинемией различного генеза, наличие пролактинсекретирующей аденомы гипофиза отмечено у 115 больных. Наличие избыточной массы тела либо ожирения подтверждено в целом у 65% пациентов. Ожирение выявлено у 50% пациентов с макропролактиномами, значение индекса массы тела (ИМТ) в среднем составило 30 кг/м2. Избыточная масса тела отмечалась преимущественно при других причинах развития гиперпролактинемии (у 38% больных). В выводах авторы подчеркивают необходимость мониторинга массы тела у пациентов с гиперпролактинемией с целью принятия своевременных мер, направленных на предотвращение заболеваний, ассоциированных с ожирением.
Как свидетельствуют результаты исследования, проведенного C. Schmid и соавт. (2006), у 1/4 больных (у 25 из 100 пациентов) с макропролактиномами диагностировано ожирение (ИМТ >30 кг/м2). Данные показатели превышали частоту ожирения при микропролактиномах –10% (у 8 из 81 больных), гормонально неактивных аденомах гипофиза – 17 % (у 18 из 105), акромегалии – 21% (у 15 из 70), болезни Иценко-Кушинга – 22% (у 8 из 36).
Частота морбидного ожирения (ИМТ >40 кг/м2) составила 6% при макропролактиноме, 1,5% – при соматотропиноме и 3% – при кортикотропиноме. В выводах работы авторы подчеркивают, что распространенность ожирения при макропролактиномах превышает показатели в общей популяции.
По данным отечественных исследований, увеличение массы тела в целом наблюдается у 40 60% больных с гиперпролактинемией. Избыточная масса тела и ожирение I степени отмечаются у 1/3 женщин вне зависимости от формы заболевания. Ожирение II III степени в 2 раза чаще наблюдается при пролактиномах, чем при идиопатической гиперпролактинемии. Наличие избыточной массы тела и/или ожирения выявлено у 35% пациентов с идиопатической гиперпролактинемией, у 40% – с умеренной гиперпролактинемией в сочетании с микропролактиномой и у 46% – с выраженной гиперпролактинемией, обусловленной макропролактиномой.
Уровень пролактина у пациентов с ожирением
Ряд авторов отмечают увеличение продукции пролактина у больных с экзогенноконституциональным ожирением.
В работе P. Kok и соавт. (2004) проведена оценка секреции пролактина в течение суток у 11 пациенток с ожирением (среднее значение ИМТ – 33,3 кг/м2). В контрольную группу вошли 10 женщин с нормальными показателями ИМТ. Уровень пролактина повышался пропорционально показателям ИМТ и был тесно ассоциирован прежде всего с количеством висцеральной жировой ткани.
Как отмечает P.G. Kopelman в обзорной статье Physiopathology of prolactin secretion in obesity, изменения секреции пролактина у больных с ожирением являются маркером нарушения функции нейроэндокринной системы при данном заболевании.
Отечественные стандарты оказания специализированной медицинской помощи больным с ожирением предусматривают необходимость проведения оценки содержания пролактина.
Основные принципы регуляции энергетического баланса
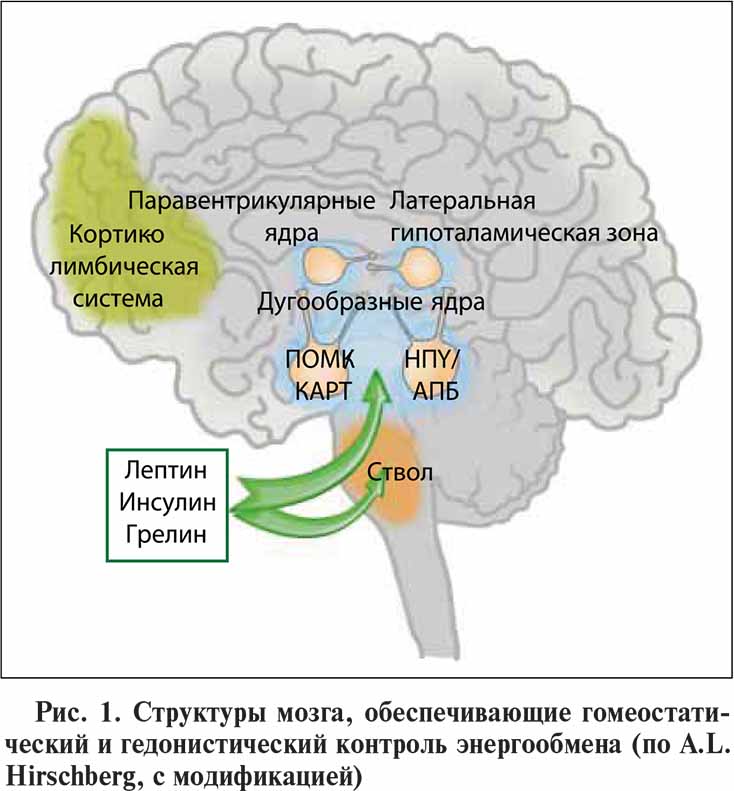
Масса тела определяется балансом между потреблением энергии и ее расходом. Несмотря на ежедневную вариабельность состава пищи и физических нагрузок, у взрослого здорового человека масса тела остается стабильной на протяжении многих лет. При ожирении поступление энергии превышает ее затраты. В регуляции энергетического обмена участвуют центральные и периферические механизмы. Центральный контроль реализуется с участием эффекторных систем головного мозга (нейропептидов, моноаминов, эндоканнабиноидов и др.). Периферическая регуляция обеспечивается сигналами, исходящими от гормонов, характеризующих объем жировых депо (лептина, инсулина), ряда других гормонов желудочно-кишечного тракта (глюкагоноподобного пептида 1, грелина и т. д.), нутриентов (глюкозы, свободных жирных кислот и др.). Центральная нервная система (ЦНС) получает информацию о состоянии энергетического статуса организма от периферических органов с помощью метаболических, эндокринных и нейрональных сигналов. На основании анализа поступившей информации формируются адекватные реакции, направленные на обеспечение долгосрочного (поддержания массы тела) и краткосрочного (инициации либо прекращения приема пищи) контроля гомеостаза. В реализации гомеостатических механизмов участвуют прежде всего гипоталамус и ствол, эти отделы мозга тесно взаимодействуют с кортиколимбическими структурами, обеспечивающими когнитивный, мотивационный и эмоциональный контроль пищевого поведения (рис. 1).
Дугообразные ядра гипоталамуса играют приоритетную роль в интеграции сигналов, регулирующих энергетический гомеостаз. Привилегированность дугообразных ядер в гомеостатическом контроле энергообмена определяется их соседством со срединным возвышением – одним из циркумвентрикулярных органов головного мозга, капилляры которых имеют фенестры (окошки). Наличие фенестр создает благоприятные условия для преодоления гематоэнцефалического барьера множеству периферических гормональных сигналов. Дугообразные ядра содержат два дискретных пула нейронов. Один из них продуцирует нейропептид Y (НПY) и агутиподобный белок (АПБ), другой – проопиомеланокортин (ПОМК) и кокаин/амфетаминрегулируемый транскрипт (КАРТ). Учитывая, что именно эти группы клеток в первую очередь получают и преобразовывают поступающую с периферии информацию о состоянии энергетического баланса, их относят к нейронам первого порядка.
Нейроны, содержащие НПY и АПБ, стимулируют прием пищи, т. е. оказывают анаболическое действие, в то время как другой пул клеток, содержащий ПОМК и КАРТ, подавляет процессы потребления пищи, т. е. обладает катаболическим эффектом. Обе группы нейронов связаны с паравентрикулярными и вентромедиальными ядрами, дорсомедиальной, латеральной и перифорникальной областями гипоталамуса, где содержатся нейроны второго порядка, также участвующие в регуляции питания и расхода энергии. ПОМК и АПБ содержащие нейроны дугообразных ядер прямо или косвенно взаимо действуют с множеством гормонов, нейромедиаторов и нутриентов, вовлеченных в регуляцию энергетического баланса, в т. ч. с лептином, инсулином, глюкозой, грели ном, пептидом YY, НПY, b эндорфином, эндогенными каннабиноидами, g аминомасляной кислотой, орекси нами, дофамином, серотонином и т. д. Инсулин и лептин ингибируют активность НПY/АПБ содержащих нейронов и стимулируют ПОМК/КАРТ продуцирующие нейроны, что приводит к подавлению аппетита и снижению массы тела. Грелин повышает аппетит путем блокады ПОМК/КАРТ нейронов и активации НПY/АПБ нейронов.
Помимо гипоталамуса, важнейшую роль в гомео статической регуляции энергообмена играет ствол мозга. Основной структурой ствола, принимающей участие в энергообмене (интерпретации периферических сигналов и дальнейшей их трансляции в гипоталамус), является дорсальный вагусный комплекс. Он включает дорсальные ядра блуждающего нерва, ядра одиночного тракта и заднюю крайнюю область (area postrema). Задняя крайняя область (участок ромбовидной ямки, расположенный кзади и латерально от треугольника блуждающего нерва), как и срединное возвышение, относится к числу циркумвентрикулярных органов. Благодаря неполному гематоэнцефалическому барьеру в этой зоне периферические сигналы насыщения имеют возможность непосредственно поступать в ствол мозга. Кроме того, обширные нейрональные связи между стволом и гипоталами ческими ядрами обеспечивают альтернативный путь коммуникации циркулирующих сигналов голода и насыщения с гипоталамусом. Нейроанатомическую связь между желудочно-кишечным трактом и мозгом обеспечивает блуждающий нерв, его афферентные волокна передают информацию о состоянии наполнения желудка, уровне гастроинтестинальных гормонов и свободных жирных кислот.
Как у животных, так и у человека нейрональные структуры, обеспечивающие гомеостатический контроль энергообмена, взаимодействуют с гораздо более объемными и сложно организованными отделами мозга, вовлеченными в когнитивный и эмоциональный контроль аппетита. В целом данный комплекс не только регулирует внутренний обмен, но и обеспечивает адаптацию метаболических потребностей организма к условиям окружающей среды. Например, именно поэтому голодная полевая мышь в течение длительного времени не покидает нору, вблизи которой охотится лиса. Вкусная пища как один из видов удовольствия является мощным орексигенным стимулом даже при отсутствии истинного дефицита энергии в организме. Чувство удовольствия обеспечивается рядом структур и медиаторных систем головного мозга, формирующих систему награды (reward system). У человека церебральная система награды включает не сколько отделов неокортекса (орбитофронтальную кору, островковую долю коры, поясную извилину), старую лимбическую кору (гиппокамп, миндалину), полосатое тело (прилежащие ядра, бледный шар), гипоталамус (латеральную и перифорникальную зоны), вентральную тегментальную область. Указанные структуры вовлечены в процессы получения удовольствия от физиологических стимулов, направленных на выживание вида (прием пищи и жидкости, половое поведение), а также являются нейрональным субстратом патологической склонности к азартным играм и наркотической зависимости. Как полагают исследователи, у большинства больных ожирение в первую очередь связано с употреблением чрезмерного количества вкусной, т. е. сладкой и/или богатой жирами пищи. В основе подобного поведенческого стереотипа лежит дисбаланс между гомеостатическими (направленными на поддержание постоянства внутренней среды) и гедонистическими (направленными на получение удовольствия, наслаждения) сигналами, регулирующими аппетит.
Энергетическая стоимость репродукции
Обеспеченность энергией – ключевое условие жизни. Возможность запасания энергии в форме гликогена в печени и мышцах достаточно ограничена и составляет 1 ккал/г, в то время как энергетическая ценность жира, со средоточенного в адипоцитах в форме триглицеридов, соответствует 8 ккал/г.
Существует отчетливый половой диморфизм, предопределяющий количество жировой ткани и характер ее распределения в организме. С учетом поправки на рост общее содержание жира в мужском организме на 34% меньше, чем в женском. Количество висцерального жира у мужчин вдвое больше, чем у женщин. В молодом возрасте общее содержание жира составляет 10 кг (15% массы тела) у мужчин и 15 кг (25% массы тела) – у женщин. Условно выделяют эссенциальный и депонируемый жир, на долю которых соответственно приходится 3 и 12% массы тела у мужчин, 9 и 15% – у женщин. Эссенциальный жир сосредоточен в костном мозге, сердце, легких, почках, кишечнике, мышцах. Данный жир, помимо триглицеридов, хранится в форме фосфолипидов. Депонируемый жир обеспечивает энергозапасы в 88 500 ккал у мужчин и 132 500 ккал – у женщин. Таким образом, присуточных энергозатратах в 1350 ккал энергетические по требности организма могут удовлетворяться в течение 60-90 дней.
В 2013 г. Американским обществом бариатрических врачей предложены алгоритмы диагностики и лечения ожирения. Данные алгоритмы, помимо оценки ИМТ, предусматривают целесообразность определения количества жировой ткани с помощью биоимпедансометрии, двухэнергетической рентгеновской абсорбциометрии либо плетизмографии всего тела (рис. 2).
Поддержание нормальной функции репродуктивной системы как у животных, так и у человека является чрезвычайно энергоемким процессом. Отрицательный энергетический баланс сопровождается нарушением полового развития и бесплодием. Поиск брачного партнера, гаметогенез, беременность, лактация и продукция соответствующих гормонов предопределяют необходимость дополнительного поступления нутриентов и адекватного изменения энергозатрат. Очевидно, что энергетическая стоимость репродукции у женщин выше, чем у мужчин.
В пубертатный период увеличение массы тела у подростков происходит за счет всех ее композиционных компонентов. Тем не менее у мальчиков в большей мере отмечается повышение массы тощей ткани, абсолютное количество жировой ткани существенно не изменяется. У девочек в этом возрасте ежегодная прибавка жировой ткани в среднем составляет 1,14 кг.
В 1970 г. эпидемиолог R. Frisch сформировала гипотезу критической массы тела. Учитывая, что менархе у более полных девушек наступает раньше, чем у худых сверстниц, предполагалось, что масса тела 46-47 кг является необходимым условием для инициации данной стадии полового созревания, при этом утверждалось, что 17% жира обеспечивают менархе, а 22% – регулярный менструальный цикл. Согласно мнению R. Frisch, у женщин, масса тела которых снизилась на 10-15% от нормальных значений, закономерно развивается аменорея.
С течением времени стало очевидным, что взаимоотношения между количеством жировой ткани и фертильностью не являются столь линейными. Нередко менархе наступает у девушек до достижения указанных критических значений веса, как и снижение массы тела у худеющих на фоне диеты женщин далеко не всегда приводит к нарушению менструального цикла.
Гипотеза критической массы тела подверглась определенной критике, тем не менее современные данные о механизмах регуляции энергобаланса свидетельствуют, что адипокины, вырабатывающиеся жировой тканью, и де понированный в ней жир играют важнейшую роль в поддержании функции репродуктивной системы. Нервная анорексия и голод приводят к аменорее и бесплодию. «Триада спортсменок» – клинически дифференцируемое состояние, включающее нарушение питания, аменорею и остеопороз. Как и анорексия, «триада спортсменок» сопровождается целым рядом негативных метаболических последствий: снижением уровней лептина и тиреоидных гормонов, повышением содержания кортизола, гипогликемией, уменьшением скорости основного обмена. Развитие указанных патологических изменений обусловлено состоянием хронического отрицательного энергетического баланса. В ходе исследований определено, что минимальный положительный энергетический баланс, необходимый для обеспечения тонической секреции гонадо тропных гормонов и нормального созревания фолликулов, составляет 30 ккал/день/кг тощей ткани.
Увеличение массы тела в период беременности происходит за счет субстратов зачатия (плод, плацента, амниотическая жидкость), увеличения объема материнских органов и тканей (матка, грудные железы, кровяное русло, внеклеточная жидкость), в т. ч. увеличения материнских жировых депо. Как показали биоэнергетические расчеты, энергетическая стоимость беременности составляет 240 ккал/день, что на 10% превышает энергетические потребности небеременных женщин. Дополнительная потребность в энергии обеспечивается не за счет мобилизации внутренних энергетических депо, а за счет накопления добавочных 2-5 кг жировой ткани. Лишь 15% энергетической стоимости беременности необходимо для развития плода, оставшаяся часть приходится на увеличение скорости метаболизма (45%) и накопление жира в организме матери (40%). Количество жировой ткани начинает увеличиваться с 6-й недели после зачатия. Во II триместре прибавка в весе составляет 65% от общего увеличения массы тела, причем половина прибавки веса в данный период приходится на жировую ткань. В III тримес тре существенного увеличения количества жира не отмечается. Под влиянием эстрогенов и прогестерона жировая ткань накапливается преимущественно в глютеофеморальных зонах, эти отложения являются стратегическим запасом для обеспечения энергетических нужд лактации.
Энергетическая стоимость лактации – 500-600 ккал/день, т. е. на 25-33% выше энергетических потребностей у некормящих женщин. Дополнительная энергия в этот период обеспечивается за счет увеличения ее потребления, снижения физической активности и мобилизации жировых депо.
Как свидетельствуют исследования в области эволюционной биологии, успешность естественного отбора предопределяется выбором наиболее оптимального варианта перераспределения энергии. На каждом этапе жизни энергетические ресурсы перераспределяются на соматический рост, репродукцию и выживание. Преимущество эволюционного отбора определяется прежде всего репродуктивными возможностями. Живые организмы могут рассматриваться как системы, захватывающие энергию из окружающей среды с целью самовоспроизведения. Соответственно, механизмы, контролирующие энергетический баланс, должны быть тесно интегрированы с механизмами, обеспечивающими репродуктивную функцию.
Примером такой интеграции являются эффекты лептина – классического метаболического гормона. При достаточных запасах энергии продукция лептина увеличивается, реализация его сигналов на уровне ЦНС приводит к снижению аппетита и массы тела. Помимо регуляции метаболизма, сигналы лептина необходимы для инициации пубертата и нормальной работы репродуктивной системы в целом. Как у животных, так и у человека мутации геналептина сопровождаются развитием ожирения, инсулинорезистентности и гипогонадотропного гипогонадизма; введение лептина способствует снижению массы тела, восстановлению чувствительности тканей к инсулину, прогрессии пубертата и устранению бесплодия. Лептин нивелирует негативное влияние голода на продукцию лютеинизирующего гормона (ЛГ) и фертильность: назначение препаратов гормона пациентам с нервной анорексией, спортсменкам с выраженным дефицитом массы тела при водит к нормализации секреции ЛГ и менструального цикла. Практически все гормоны, регулирующие энергетический обмен, задействованы в контроле репродуктивной функции.
Пролактин как интегратор контроля репродукции и энергетического баланса
Пролактин: регуляция синтеза и секреции
Пролактин был идентифицирован у животных в 1928 г., у человека – в 1971 г. Свое название гормон получил благодаря способности инициировать лактацию у млеко питающих. Уже к 1998 г. насчитывалось более 300 биологических эффектов пролактина. В последующие годы было открыто множество новых свойств гормона: участие в реализации стрессорного ответа, регуляция функции иммунной системы, контроль нейрогенеза, туморогенеза и др. Синтез и секреция пролактина не являются исключительной прерогативой гипофиза, многочисленные ткани и органы обладают такими же возможностями.
Геном человека содержит единственный кодирующий ген пролактина, располагающийся на 6 хромосоме. Молекула пролактина представлена полипептидной цепью, состоящей из 199 аминокислот, объединенных тремя дисульфидными мостиками между цистеиновыми остатками (Суs4 Суs11, Су858 Суs174, Суs191 Суs199).
Помимо классических мишеней пролактина (органов репродуктивной системы), рецепторы гормона широко представлены в различных структурах головного мозга: сосудистом сплетении, миндалине, таламусе, гипоталамусе, гипофизе, коре и обонятельных луковицах. Кроме того, рецепторы пролактина содержат многочисленные периферические органы и ткани – сердце, легкие, тимус, селезенка, печень, поджелудочная железа, надпочечники, скелетная мускулатура, кожа, а также жировая ткань.
Дофамин является основным фактором, угнетающим секрецию пролактина через систему D2-рецепторов, локализованных на мембранах лактотрофов. С другой стороны, пролактин способен активировать дофаминергические нейроны, обеспечивая тем самым гипоталамический контроль собственной продукции (короткая петля механизма обратной связи). В норме повышение уровня пролактина сопровождается увеличением концентрации дофамина в гипоталамо-гипофизарной портальной системе. Скорость синтеза дофамина снижается после гипофизэктомии. Помимо дофамина, высвобождение пролактина ингибируют g аминомасляная кислота, гастрин, гастрин-рилизинг-пептид, соматостатин и др. Секреция пролактина усиливается при приеме обогащенной белком пищи, во время сна, стресса, полового акта, стимуляции сосков грудных желез, при физических нагрузках. Эстрогены, гонадотропин рилизинг-гормон, серотонин, холецистокинин, нейротензин, окситоцин, вазопрессин, галанин, вазоактивный интестинальный полипептид, эндогенные опиоиды также оказывают стимулирующее действие на продукцию пролактина. Наиболее изучена роль пролактина в регуляции репродуктивной системы. В исследованиях последних лет особое внимание уделяется метаболическим эффектам гормона.
Роль пролактина в регуляции аппетита
Период беременности и лактации – идеальная модель изучения метаболических эффектов пролактина. Данный отрезок времени, характеризующийся физиологической гиперпролактинемией и физиологической гиперфагией, позволяет уточнить роль пролактина в регуляции энергетического баланса в норме, а также определить генез ряда метаболических нарушений, развивающихся у больных с ГГ.
Беременность и лактация связаны с реорганизацией синтеза и секреции множества гормонов. Данная реорганизация необходима для успешной адаптации организма матери к новым физиологическим условиям, включающим изменения функции сердечно-сосудистой, дыхательной, иммунной систем, поведенческих реакций и энергетического баланса. Преобразования энергообмена направлены на обеспечение дополнительных энергетических ресурсов.
Увеличение аппетита и массы тела в течение беременности является благоприятным фактором, создающим оптимальные условия для роста плода и подготовки организма матери к предстоящим энергетическим потерям, связанным с периодом лактации. Повышение аппетита у грызунов наблюдается на самых ранних сроках беременности, еще до имплантации. Наиболее весомой причиной развития гиперфагии является гиперпролактинемия. Пролактин – классический орексигенный гормон, его рецепторы сосредоточены в целом ряде зон ЦНС, ассоциированных с регуляцией аппетита, включая дугообразные, вентромедиальные, паравентрикулярные и дорсомедиальные ядра гипоталамуса. В отсутствие беременности как периферическое, так и центральное внутрижелудочковое введение пролактина сопровождается увеличением приема пищи у животных. Этот эффект прослеживается также у самок крыс после овариэктомии. Введение специфических антител к рецепторам пролактина либо их нокаутирование способствует уменьшению объема потребляемой пищи. Влияние пролактина на аппетит связано с увеличением содержания в ЦНС НПY и АПБ.
Гиперфагия, индуцированная пролактином на ранних сроках беременности, в определенной мере опосредована половыми стероидами. В этот период пролактин повышает содержание прогестерона и подавляет циклическую продукцию эстрадиола. При циклическом характере секреции эстрадиол снижает аппетит благодаря активации ПОМК-нейронов дугообразных ядер. Кроме того, под влиянием эстрадиола повышаются энергозатраты, что связано со стимуляцией a-рецепторов на уровне вентромедиальных ядер, экспрессирующих фактор транскрипции стероидогенеза - 1.
Прогестерон также обладает отчетливым орексигенным эффектом, реализующимся вследствие активации рецепторов, локализованных в дугообразных и вентромедиальных ядрах гипоталамуса.
Гиперфагия, характерная для более поздних сроков беременности, преимущественно обусловлена нарушением эффектов лептина. По мере увеличения массы тела концентрация лептина начинает повышаться (вследствие его гиперпродукции адипоцитами и активации секреторной функции плаценты), тем не менее гормон теряет свои анорексигенные свойства. Таким образом, развитие лептинорезистентности в период беременности носит физиологический характер – это один из важнейших механизмов, обеспечивающих повышение аппетита и, соответственно, поступление дополнительной энергии.
Лактация – идеальная модель интеграции энергетического баланса и репродукции. Этот период характеризуется активацией мощных орексигенных сигналов, а также факторов, обеспечивающих подавление пульсирующей секреции гонадотропинрилизинг-гормона и ЛГ.
Пролактин играет важную роль в развитии лактационной гиперфагии, что обусловлено целым рядом факторов. Прежде всего пролактин играет приоритетную роль в поддержании чрезвычайно энергоемких процессов – лактогенеза (синтеза важнейших составляющих молока) и галактопоэза (обеспечение секреции молока). Грудное вскармливание повышает риск развития отрицательного энергетического баланса у матери и, соответственно, способствует повышению аппетита.
Подавление циклической овариальной функции в период лактации необходимо для предотвращения дополнительных потерь энергии, связанных с повторной беременностью и, соответственно, создания оптимальных условий для выживания уже имеющегося потомства.
Как уже отмечалось, энергетические потребности во время лактации гораздо выше, чем в период беременности. У большинства млекопитающих увеличение приема пищи не может обеспечить необходимые метаболические потребности, что приводит к состоянию отрицательного энергетического баланса и, как следствие, мобилизации внутренних жировых депо.
Пролактин и жировая ткань
У человека пролактин секретируется не только в гипофизе, но и в целом ряде других органов и тканей, включая адипоциты. Открытие в 2003 г. адипоцитарной секреции пролактина произошло случайно, в данном эксперименте исходно планировалось использовать жировую ткань лишь в качестве негативного контроля. Оказалось, что экспланты жировой ткани грудной железы секретируют в 10-15 раз больше пролактина, чем экспланты железистой ткани. Продукция пролактина осуществляется также подкожными и висцеральными адипоцитами (как зрелыми, так и дифференцирующимися клетками). Потенциал продукции пролактина каждым адипоцитом в 4-5 раз ниже секреторных возможностей лактотрофа, в то же время масса гипофиза (1 г) не сопоставима с массой жировой ткани при морбидном ожирении (50 кг). Тем не менее вклад адипоцитарного пролактина в общую концентрацию гормона остается предметом дискуссий. Исследователи предполагают, что местно продуцирующийся пролактин осуществляет преимущественно ауто- и паракринные функции.
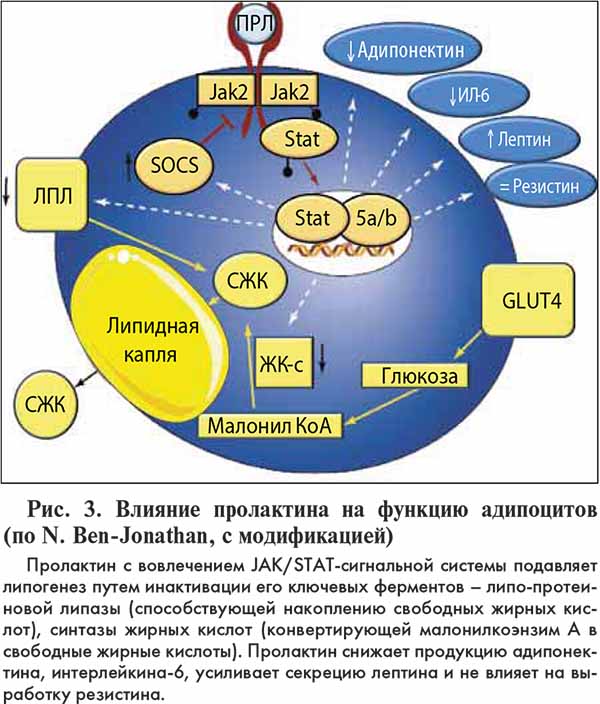 Пролактин принимает активное участие в адипогенезе. Рецепторы пролактина присутствуют в жировой ткани как у человека, так и у животных, экспрессия гена рецепторов увеличивается в период лактации, а также во время дифференциации адипоцитов.
Пролактин принимает активное участие в адипогенезе. Рецепторы пролактина присутствуют в жировой ткани как у человека, так и у животных, экспрессия гена рецепторов увеличивается в период лактации, а также во время дифференциации адипоцитов.
В период лактации у крыс пролактин подавляет липогенез путем инактивации всех ключевых ферментов, участвующих в данном процессе. Подавление липогенеза под влиянием пролактина отмечено также и в жировой ткани человека. Пролактин блокирует секрецию адипонектина. Концентрация адипонектина, в частности, резко снижена у женщин в период беременности и лактации (рис. 3).
Пролактин с вовлечением JAK/STAT сигнальной системы подавляет липогенез путем инактивации его ключевых ферментов – липопротеиновой липазы (способствующей накоплению свободных жирных кислот), синтазы жирных кислот (конвертирующей малонилкоэнзим А в свободные жирные кислоты). Пролактин снижает продукцию адипонектина, интерлейкина-6, усиливает секрецию лептина и не влияет на выработку резистина.
Роль дофамина в регуляции энергетического баланса
Дофамин – важнейший регулятор не только синтеза исекреции пролактина, но и энергетического баланса. Предположительно, патологическая гиперпролактинемия приводит к снижению дофаминергического тонуса (нарушениям в системе короткой петли механизма обратной связи). Нейротрансмиттеры дофамин, норадреналин и адреналин относятся к классу катехоламинов. Их структура характеризуется наличием катехолового кольца и боковой аминогруппы. Катехоламины и индоламины, к которым относится серотонин, определяются как моноамины. Взаимодействуя с нейропептидами и гормонами, практически все моноаминергические нейротрансмиттеры вовлечены в контроль энергообмена.
Несмотря на то что дофаминергические нейроны составляют менее 1% нейрональной популяции мозга, дофамин регулирует множество процессов в организме, включая когнитивные функции, локомоторную активность, секрецию гормонов, прием пищи.
Дофамин играет важнейшую роль в регуляции пищевого поведения. У мышей с селективной инактивацией гена тирозингидроксилазы – ключевого фермента биосинтеза дофамина – развивается гипофагия, к концу 1- го месяца жизни животные погибают от голода. Влияние дофамина на прием пищи определяется подтипом рецепторов и свойствами конкретной области мозга. Например, на уровне гипоталамуса дофамин участвует в гомеостатической регуляции энергообмена: в области дугообразных ядер и латеральной гипоталамической зоны подавляет аппетит, в области вентромедиальных ядер – стимулирует его. В составе мезокортиколимбической системы дофамин обеспечивает нормальную функцию системы награды, включая процессы научения, формирования рабочей памяти, предопределения награждающих свойств пищи и мотивации к ее приему. Дофаминергическая система задействована в подкреплении эффектов не только вкусной пищи, но и наркотических веществ, включая алкоголь, метамфетамин, кокаин, героин.
Вовлеченность дофаминергической системы в развитие гиперфагии и ожирения подтверждена результатами многочисленных исследований. Применение агонистов дофамина у грызунов с ожирением снижает массу тела животных путем активации D1- и D2-подобных рецепторов. У человека длительный прием антипсихотических препаратов (нейролептиков), являющихся блокаторами D2-рецепторов, связан с риском увеличения массы тела. Напротив, фармакологические препараты, повышающие продукцию дофамина либо блокирующие его обратный захват, способствуют снижению аппетита, повышению энергозатрат. Результаты серии работ N.D. Volkow и соавт. показали, что у больных с морбидным ожирением количество D2-рецепторов в области полосатого тела обратно пропорционально ИМТ. Эти данные позволили выдвинуть гипотезу, согласно которой в основе ожирения лежит снижение активности дофаминергической системы, а патологическое переедание является закономерной компенсаторной реакцией, направленной на преодоление дефицита дофамина. У больных, перенесших бариатрические операции, плотность D2-рецепторов постепенно восстанавливается; увеличение количества рецепторов происходит пропорционально снижению массы тела.
Взаимодействуя с D2-рецепторами, дофамин ингибирует синтез пролактина адипоцитами.
Метаболический синдром, ассоциированный с патологической гиперпролактинемией
Учитывая механизмы, реализующие метаболические эффекты пролактина в норме, наиболее вероятными причинами увеличения массы тела при ГГ являются:
1) повышение аппетита, что обусловлено как орексигенным эффектом пролактина, так и ассоциированным с гиперпролактинемией изменением содержания других гормонов (снижение уровня эстрогенов, тестостерона, кисспептина);
2) активация адипогенеза, ингибирование липогенеза, изменения выработки и эффектов адипокинов – подавление секреции адипонектина, лептинорезистентность;
3) снижение энергозатрат вследствие нарушения трансдифференциации белых адипоцитов в бурые;
4) снижение дофаминергического тонуса.
В последние годы появились сведения о том, что, помимо увеличения массы тела, патологическая гиперпролактинемия сопровождается гиперинсулинемией, инсулинорезистентностью, артериальной гипертензией, дислипидемией, нарушением эндотелиальной функции, активацией медленно прогрессирующего воспаления. Пролактин продуцируется не только адипоцитами, но и макрофагами жировой ткани, а также макрофагами атеросклеротических бляшек. Синтез пролактина макрофагами повышается при ожирении как у животных, так и у человека, что может обусловливать развитие атеросклероза и сахарного диабета (СД). В популяционном исследовании, включавшем 3929 человек, наблюдавшихся в течение 10 лет, выявлено, что верхний терциль уровня пролактина даже в пределах его референсных значений ассоциирован с повышением риска общей смертности и смертности вследствие сердечно-сосудистых заболеваний. Как отмечают авторы статьи «Metabolic syndrome associated with hyperprolactinemia: a new indication for dopamine agonist treatment?», метаболическим последствиям гиперпролактинемии в течение многих лет не уделялось должного внимания, в настоящее время при обследовании пациентов с ГГ необходимо учитывать плейотропные эффекты пролактина, а также оценивать перспективность применения агонистов дофамина в отношении снижения кардиоваскулярного риска. В США для лечения СД 2 типа зарегистрирован бромокриптин (быстро абсорбирующаяся форма – Эргосет, Циклозет). У больных СД препарат способствует уменьшению массы тела, снижению инсулинорезистентности и улучшению липидного спектра.
Эффективность каберголина в устранении метаболических последствий патологической гиперпролактинемии
Методом выбора в лечении больных с ГГ является медикаментозная терапия агонистами дофамина. В Российской Федерации, как и в большинстве стран мира, с этой целью зарегистрированы бромокриптин, хинаголид и каберголин. Каберголин (Достинекс) – селективный, длительно действующий агонист D2-рецепторов дофамина. На сегодняшний день каберголин – наиболее предпочтительный препарат с учетом его максимальной эффективности в отношении нормализации уровня пролактина, восстановления функции репродуктивной системы и антимитотического влияния на пролактинсекретирующие опухоли, в т. ч. в случаях гигантских пролактином.
В ряде работ особое внимание было уделено воздействию каберголина на метаболические проявления патологической гиперпролактинемии.
В исследование, выполненное J. Korner и соавт. (2003), было включено 16 пациентов (10 женщин и 6 мужчин) с ГГ. Исходная масса тела составила 86 кг, ИМТ – 30 кг/м2. Терапия каберголином продолжалась в течение 13,5 мес при средней дозе препарата 0,92±0,14 мг/нед. У 10 пациентов отмечено снижение массы тела, у 1 больного масса тела не изменилась, у 2 – увеличилась. В среднем показатели массы тела снизились на 6 кг. Клинически значимое снижение массы тела (на 5-10% от исходных значений) зарегистрировано у 9 больных.
Влияние каберголина на показатели медленно прогрессирующего воспаления изучалось в работе O. Serri и соавт. (2006). Выборка включала 13 больных с микропролактиномой и 2 пациентов с макропролактиномой, в контрольную группу вошли 20 здоровых добровольцев.
Каберголин назначался по 0,5 мг 2 раза в неделю при на личии микроаденомы, по 1 мг 2 раза в неделю – при макроаденоме. Исходно средние показатели уровня пролактина составили 1880 мкЕд/мл, массы тела – 82,5 кг, ИМТ – 28,9 кг/м2. Содержание инсулина, индекса НОМА, С - реактивного белка и растворимого Е-селектина (маркера активации мононуклеарных клеток) было существенно выше у больных с пролактиномами, чем в контрольной группе. Через 12 мес уровень пролактина в выборке достиг нормальных значений и в среднем составил 220 мкЕд/мл. Статистически значимых изменений массы тела не отмечено, тем не менее применение каберголина способствовало нормализации показателей инсулина, С-реактивного белка и растворимого Е-селектина.
Эффект каберголина на проявления метаболического синдрома изучался у пациентов с пролактиномами в исследовании R.S. Auriemma и соавт. (2013). В выборку был включен 61 человек, в т. ч. 41 больной с микроаденомой и 20 – с макроаденомой. Диагностика метаболического синдрома осуществлялась согласно критериям NСЕРАТР III. Продолжительность лечения составила 60 мес. К концу периода наблюдения нормальный уровень пролактина был достигнут у 93% больных. Распространенность метаболического синдрома статистически значимо уменьшилась через 12 мес (11,5%) и 60 мес (5%) лечения каберголином по сравнению с исходными значениями (28%). На фоне применения каберголина отмечено также существенное улучшение показателей липидного профиля, снижение индекса висцерального ожирения и индекса НОМА.
Целью работы А.А. Осиповой и В.П. Сметник (2003) являлась оценка значения ИМТ, типа ожирения, а также влияния терапии парлоделом, норпролаком и достинексом у пациенток с ГГ. Исследуемая выборка включала 130 женщин репродуктивного возраста, в т. ч. 88 больных с пролактиномами и 42 пациентки с неопухолевым генезом гиперпролактинемии. Уровень пролактина до лечения в среднем составил 3104±263,3 мкЕд/мл. Бромокриптин в дозах 2,5-12,5 мг/сут получали 33 пациентки, хинаголид (по 75-300 мкг/сут) – 19 человек, каберголин (0,125-2 мг/нед) был назначен 36 больным. Исходно у половины больных выявлено наличие избыточной массы тела либо ожирения. Повышение ИМТ и абдоминальное ожирение чаще наблюдались при опухолевом генезе заболевания. На фоне проводимой терапии отмечено значительное снижение уровня пролактина, подтверждена более высокая эффективность достинекса: через 6 мес нормализация уровня гормона при приеме достинекса, парлодела и норпролака составила у пациенток с пролактиномами гипофиза 94,4, 63,6, 63,2% соответственно, у больных с неопухолевым генезом заболевания – 100, 78,6, 85,7% соответственно. Снижение массы тела было статистически значимым на фоне приема каберголина, в среднем динамика составила 2,6 кг у больных с пролактиномами и 1,9 кг у пациенток с неопухолевым генезом ГГ. Применение других агонистов дофамина сопровождалось лишь тенденцией к уменьшению массы тела.
Задачи работы А. Ciresi и соавт. предусматривали оценку эффективности метаболических эффектов каберголина с учетом дозы препарата. В ретроспективном исследовании приняли участие 43 пациента (8 мужчин, 35 женщин) с пролактиномами. До лечения исходный уровень пролактина составил в среднем 3715 мкЕд/мл, объем аденомы гипофиза – 10,56 мм3, ИМТ – 25,6 кг/м2, масса тела – 88,8 кг. В течение 12 мес наблюдения 29 больных получали каберголин в средней дозе, не превышающей 0,5 мг/нед, остальные 14 человек – в более высоких дозах. В данном исследовании динамика уровня пролактина и объема опухоли не зависела от дозы препарата, через 1 год эти показатели составили 529 мкЕд/мл и 8,16 мм3 соответственно. В то же время у больных, получавших каберголин в дозах >0,5 мг/нед, отмечено более выраженное снижение значений ИМТ, а также индексов НОМА, Маtsuda и висцерального ожирения.
Динамика массы тела на фоне применения агонистов дофамина в течение 2 лет прослежена в работе А.Р. Athanasoula и соавт. (2013). В исследование были включены 44 пациента (17 мужчин, 27 женщин) с пролактиномами (26 больных с макроаденомой и 18 – с микроаденомой). Наличие избыточной массы тела либо ожирения выявлено у 21 человека. Большинство больных (n=32; 73%) принимали каберголин. Исходно показатели ИМТ в среднем составили 26,19 кг/м2, массы тела – 78,55 кг, уровня пролактина – 1284 нг/мл. Через 2 года лечения ИМТ в исследуемой выборке уменьшился на 0,99 кг/м2, масса тела – на 3,1 кг. В целом клинически значимое снижение массы тела (на 5% и более от исходных значений) отмечено у 47,7% больных. У пациентов с исходными значениями ИМТ >25 кг/м2 масса тела в среднем снизилась на 5,3%, клинически значимых результатов достигли 57% больных.
Влияние каберголина на инсулинорезистентность, провоспалительные маркеры и толщину комплекса интима-медиа сонных артерий у 21 пациентки с пролактиномами изучались в работе S.S. Inancli и соавт. Через 6 мес терапии уровень пролактина достиг нормальных значений у всех больных и составил в среднем 12,4 нг/мл (vs 151 нг/мл исходно). Отмечено статистически значимое снижение массы тела (ИМТ исходно – 27,1 кг/м2, в динамике – 26,7 кг/м2). Применение препарата сопровождалось положительной динамикой показателей липидного спектра, уменьшением инсулинорезистентности, С-реактивного белка и толщины комплекса интима-медиа.
Учитывая, что снижение тонуса дофаминергической системы может непосредственно влиять на патогенез ожирения и его осложнений, C.D. Gibson и соавт. (2012) провели пилотное двойное слепое рандомизированное исследование, целью которого являлась оценка влияния каберголина на массу тела и показатели углеводного обмена у больных с экзогенно-конституциональным ожирением с нормальным уровнем пролактина. Продолжительность исследования составила 16 нед. В выборку было включено 40 человек, ИМТ варьировал от 30 до 42 кг/м2. Всем пациентам было рекомендовано ограничить суточный рацион на 500 ккал. Исходно и в динамике проводился тест толерантности к глюкозе. Исследование завершили 29 больных, получавших либо каберголин (n=13, препарат назначался по 0,25 мг 2 раза в неделю в течение 1- го месяца с последующим удвоением дозы), либо плацебо (n=16). В выводах авторы отмечают, что вне зависимости от динамики массы тела и уровня пролактина каберголин способствует повышению чувствительности тканей к инсулину.
Таким образом, у больных с ГГ назначение каберголина сопровождается снижением массы тела, улучшением показателей углеводного обмена, липидного спектра, эндотелиальной функции, нормализацией провоспалительных атеро- и диабетогенных маркеров. Принимая во внимание важнейшую роль дофамина в регуляции энергетического баланса, чрезвычайно интересны и перспективны сведения об эффективности препарата у больных с экзогенно-конституциональным ожирением. Для дальнейшего изучения терапевтического потенциала каберголина необходимы долгосрочные исследования, предусматривающие более масштабные выборки.
Список литературы находится в редакции.
Ожирение и метаболизм, 2014, № 1 (38).
Медична газета «Здоров’я України» № 21 (346), травень 2014 p.