25 вересня, 2016
Чем еще мы можем улучшить прогноз пациентов после инвазивной реваскуляризации миокарда?
20-22 апреля в г. Киеве состоялся XV Киевский курс по коронарным реваскуляризациям, в рамках которого обсуждались не только актуальные проблемы хирургического и инвазивного лечения, но и вопросы медикаментозной терапии у пациентов с инфарктом миокарда (ИМ).
Возможностям дополнительного влияния на прогноз этих больных посвятила свой доклад доктор медицинских наук, профессор Елена Акиндиновна Коваль (Днепропетровская государственная медицинская академия):
 – На исходы у пациентов, перенесших чрескожное коронарное вмешательство (ЧКВ), влияет множество факторов, зависящих и не зависящих от оперирующего врача или специалиста, который ведет больных на амбулаторном этапе. В частности, имеют значение анатомические особенности, вид стента, полнота реваскуляризации, характер атеросклеротического процесса, выраженность фиброза и ремоделирования миокарда. Но есть и факторы, которые напрямую связаны с тем, какую терапию назначат пациенту периоперационно, после вмешательства, а также с тем, насколько настойчив будет лечащий врач в стремлении убедить больного принимать препараты постоянно и в адекватных дозах.
– На исходы у пациентов, перенесших чрескожное коронарное вмешательство (ЧКВ), влияет множество факторов, зависящих и не зависящих от оперирующего врача или специалиста, который ведет больных на амбулаторном этапе. В частности, имеют значение анатомические особенности, вид стента, полнота реваскуляризации, характер атеросклеротического процесса, выраженность фиброза и ремоделирования миокарда. Но есть и факторы, которые напрямую связаны с тем, какую терапию назначат пациенту периоперационно, после вмешательства, а также с тем, насколько настойчив будет лечащий врач в стремлении убедить больного принимать препараты постоянно и в адекватных дозах.
Одно из важнейших направлений в медикаментозном лечении пациентов после ЧКВ – антитромботическая терапия, однако лечение антиагрегантами и антикоагулянтами способствует подавлению лишь части патологических процессов, которые активируются во время вмешательства на коронарных сосудах. В частности, эти препараты не устраняют полностью контактную активацию каскадных систем плазмы крови, с помощью которой протеиназы активируются на поверхности разрушенной атеросклеротической бляшки. Контактная активация – триггерный механизм, запускающий активацию всех пяти протеолитических систем плазмы крови: калликреин-кининовую, ренин-ангиотензиновую, свертывание, фибринолиз, комплемент. Следствием этого является увеличение риска и кровотечений, и тромбозов на фоне антитромботической терапии. Дополнительно повлиять на механизм контактной активации можно с помощью статинов, которые, помимо снижения выраженности воспаления за счет подавления выработки целого ряда цитокинов и молекул адгезии, обладают способностью стабилизировать последующие долговременные протеолитические процессы вследствие модуляции активности матриксных металлопротеиназ (ММП). Это очень важные моменты, поскольку высокий уровень ММР, в частности ММP-9, является независимым предиктором сердечно-сосудистых заболеваний и сердечно-сосудистой смерти у пациентов с ишемической болезнью сердца. Повышенный уровень ММР-9 имеет прогностическое значение в отношении развития рестенозов. Установлено, что у пациентов с острым коронарным синдромом (ОКС) наблюдается значимое повышение уровня ММП-9 в коронарных артериях до и непосредственно после процедуры ЧКВ (А.С. Скоромная, 2013). Активность ММП-9 коррелирует с динамикой восстановления микроциркуляции миокарда, а степень ее снижения зависит от выраженности гиполипидемического действия статина, то есть, чем более «сильный» статин мы используем, тем более выраженное воздействие оказываем на этот значимый прогностический маркер.
Столь же клинически важным является и холестериннезависимый антитромботический эффект статинов. Установлено, что статины подавляют процесс конверсии протромбина в тромбин, снижая активность факторов V, VIIa и экспрессию рецептора PAR-1, что приводит к уменьшению содержания тканевого фактора (индуктора атеротромбоза) и снижению последующего образования активного тромбина. Кроме того, применение статинов способствует уменьшению содержания микрочастиц, которые высвобождаются из тромбоцитов, эндотелиальных клеток, моноцитов и поддерживают коагуляцию в крови.
Антитромботический эффект статинов вызвал клинический интерес после появления результатов субанализа исследования JUPITER о беспрецедентной эффективности статинотерапии в профилактике венозного тромбоза и его последствий, в том числе и тромбоэмболии легочной артерии, в широкой (более 17 тыс.) популяции больных. Согласно полученным данным длительный прием статина приводил к высокодостоверному снижению частоты тромбоза глубоких вен на 43%.
Очевидно, что антитромботический эффект статинов вносит значимый вклад в увеличение показателя выживаемости и отдаленных клинических исходов у пациентов c ОКС, в том числе – после ЧКВ, что было доказано в рандомизированных клинических исследованиях. Одним из первых крупных исследований, в котором была показана польза ранней интенсивной статинотерапии при ОКС, стало исследование MIRACLE с использованием аторвастатина в дозе 80 мг. В сравнительных исследованиях IDEAL и PROVEIT-TIMI 22 аторвастатин в максимальной дозе 80 мг/сут продемонстрировал преимущества в снижении риска развития различных сердечно-сосудистых осложнений по сравнению с симвастатином (20-40 мг/сут) и правастатином (40 мг/сут). Исследования эффектов статинотерапии при ОКС показали, что увеличение дозы статина не всегда приводит к дополнительному снижению риска развития сердечно-сосудистых осложнений. Так, в исследовании A to Z более интенсивный режим лечения симвастатином (80 мг/сут) не имел статистически достоверных преимуществ по сравнению с приемом симвастатина в дозе 40 мг/сут.
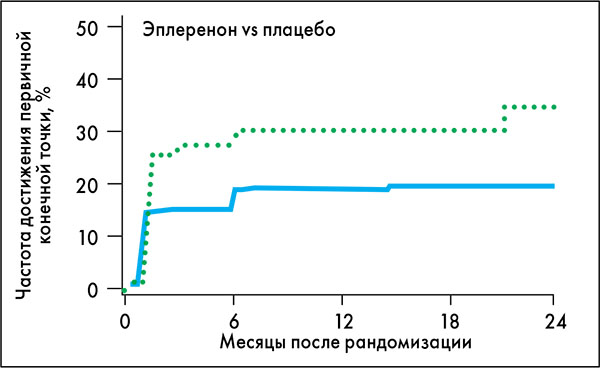
Рис. Снижение частоты достижения первичной конечной точки на фоне терапии эплереноном в исследовании REMINDER
Таким образом, именно в исследованиях с оригинальным аторвастатином (Липримар®) были продемонстрированы преимущества интенсивной статинотерапии у пациентов с ОКС. Результаты этих исследований стали основанием для того, чтобы официально рекомендовать использование статинов в высоких дозах с первых часов развития ОКС независимо от исходного уровня липидов в крови.
В дальнейшем была показана польза рутинного применения высоких доз статинов (аторвастатина и розувастатина) перед вмешательствами у больных с ОКС, которая выражалась в снижении частоты перипроцедурного ИМ и других кардиальных осложнений. Сегодня этот подход также стал стандартным в лечении данной категории больных.
Следует обратить внимание, что понятие «высокоинтенсивная статинотерапия» подразумевает назначение высоких доз статинов с наиболее выраженным гиполипидемическим эффектом – аторвастатина (40, 80 мг) и розувастатина (20, 40 мг), что, в частности, отражено в современных рекомендациях по применению статинов у взрослых пациентов Американской ассоциации сердца и Американской коллегии кардиологов (2013).
Интерес к плейотропным эффектам статинов сегодня не ослабевает, и совершенно очевидно, что польза от их использования намного превышает возможные риски. Тем более удивительны данные украинских исследований, демонстрирующие крайне беспечное отношение врачей и пациентов к жизнеспасающей терапии после проведения процедуры ЧКВ. Восприятие процедуры реваскуляризации миокарда в качестве гарантии жизни и отсутствия в дальнейшем каких-либо осложнений – наиболее частое заблуждение, которое еще и сегодня широко распространено не только среди пациентов, но также среди терапевтов, семейных врачей и даже кардиологов.
По данным 2015 года, не более 46% пациентов с ишемической болезнью сердца с поражением коронарных артерий принимали статины через 3 мес после вмешательства, что свидетельствует о недооценке послеоперационных рисков. Профессор Е.А. Коваль отметила, что более чем в 50% случаев пациенты после ЧКВ принимают неевропейские генерики статинов, и это, по мнению лектора, создает дополнительные риски для данной категории больных и, возможно, является одной из причин низкой частоты достижения целевых уровней липидов. Более того, врачи часто используют неадекватные дозы статинов и при этом контролируют уровень общего холестерина вместо главной липидной цели – уровня холестерина липопротеинов низкой плотности. В совокупности эти факторы способствуют тому, что клинический эффект статинотерапии в общей популяции нивелируется.
Еще одна возможность дополнительного улучшения исходов у пациентов, перенесших ЧКВ, связана с применением средств нейрогуморальной модуляции. В качестве таких средств традиционно используют ингибиторы ангиотензинпревращающего фермента (ИАПФ), бета-адреноблокаторы, антагонисты кальция. Не следует забывать еще об одной важной возможности нейрогуморальной модуляции при ОКС – блокаде эффектов альдостерона. Известно, что высокий уровень альдостерона в крови является независимым предиктором смертности при остром ИМ (ОИМ), соответственно, его снижение должно обеспечивать дополнительную пользу у пациентов.
Важный вопрос: имеет ли значение, с помощью какого препарата мы достигаем снижения уровня альдостерона у больных ОИМ?
Для получения ответа на этот вопрос рассмотрим результаты клинических исследований с использованием при ОИМ препаратов из группы антагонистов альдостерона.
Острые эффекты антагониста минералокортикоидных рецепторов спиронолактона при ОИМ были изучены в исследовании ALBATROSS. В этом исследовании применение антагониста альдостерона у пациентов, поступавших в стационар в течение первых 72 ч после развития симптомов, не обеспечило преимуществ по сравнению со стандартной терапией в снижении показателя достижения комбинированной конечной точки, включавшей общую смертность, частоту остановки кровообращения с успешной реанимацией, развития жизнеугрожающих аритмий, определения показаний к имплантации кардиовертера-дефибриллятора и повышения степени тяжести сердечной недостаточности (СН).
В то же время в исследовании REMINDER ранняя (в течение 24 ч) терапия эплереноном (Инспра®) в дозе 25-50 мг 1 раз в сутки при ОИМ с подъемом сегмента ST без СН приводила к достоверному снижению частоты достижения первичной конечной точки (время до первого события – смерть от сердечно-сосудистых причин, повторная госпитализация, устойчивая желудочковая тахикардия или фибрилляция, фракция выброса <40% или повышение уровня N-терминального фрагмента мозгового натрийуретического пептида – BNP/NT-proBNP) после месяца лечения (рис.). REMINDER – первое крупное исследование, продемонстрировавшее безопасность раннего применения эплеренона при ОИМ с титрацией дозы с 25 до 50 мг уже на 2-е сутки без предварительной оценки уровня калия.
Таким образом, добавление эплеренона на ранних этапах ведения пациентов с ОИМ без СН (или снижения фракции выброса левого желудочка <40%) в дополнение к ЧКВ и стандартной терапии можно рассматривать как подход, направленный на улучшение результатов вмешательства и исходов. Столь значимая разница в результатах двух исследований с применением различных антагонистов альдостерона свидетельствует о том, что преимущества терапии эплереноном при ОИМ обусловлены его уникальными свойствами, которые реализуются в виде важных клинических эффектов. Высокоселективная блокада минералокортикоидных рецепторов с помощью эплеренона приводит к увеличению плотности капилляров и пролиферации эндотелиальных клеток-предшественников, мигрирующих в зону некроза и апоптоза эндотелия для его замещения. Это способствует улучшению эндотелиальной функции, что является важным моментом, когда речь идет о такой острой ситуации, как развитие ОИМ и проведение реваскуляризации миокарда. Кроме того, эффективное устранение гиперэкспрессии минералокортикоидных рецепторов ослабляет ремоделирование предсердий, снижая риск возникновения опасных аритмий. Эплеренон обладает способностью уменьшать экспрессию АПФ в ранние сроки развития ОИМ и, таким образом, происходит потенцирование его эффектов с эффектами ИАПФ, что обеспечивает дополнительные преимущества. В конечном итоге применение эплеренона снижает риск разрыва миокарда при ОИМ и способствует более быстрому формированию полноценного рубца.
Следует сделать вывод, что в современной клинической практике есть дополнительные возможности для улучшения прогноза у пациентов, перенесших ЧКВ. Использование этих возможностей продлевает жизнь пациентам с показаниями к реваскуляризации миокарда, поэтому подход к ведению таких больных не должен быть формальным.
Статья в формате PDF.
Подготовила Наталья Очеретяная
Тематичний номер «Кардіологія, Ревматологія, Кардіохірургія» № 4 (47), вересень 2016 р.