30 липня, 2021
Патологія серця і судин при хворобі Бехчета
Серцево-судинні захворювання (ССЗ) залишаються основною причиною смерті серед дорослого населення: щорічно у Європі від патологій серцево-судинної системи (ССС) помирає понад 4 млн осіб. Однією із причин ураження ССС є системні васкуліти (СВ), зокрема хвороба Бехчета (ХБ). При ХБ мають місце ураження будь-якого типу і калібру судин, тому вона характеризується мультисистемним характером пошкодження та гетерогенністю клінічних проявів. Це ускладнює своєчасне встановлення діагнозу і призначення відповідного лікування.
Ураження ССС при ХБ зустрічаються відносно рідко, але ця патологія є однією із прогностично несприятливих. Виживаність без подій протягом середньої періоду спостереження 67±46 місяців значно нижча в осіб із ХБ і хворобою серця, ніж без неї (63 vs 14%; р=0,0001) [63]. Ураження судин, особливо артерій, є тяжким проявом ХБ і залишається основною причиною смерті пацієнтів [56].
За словами N. Akdeniz et al., ХБ є «великим імітатором» дерматології [4]. ХБ є хронічним, рецидивувальним, мультисистемним СВ, для якого характерні ураження слизових оболонок і шкіри, очей, судин, суглобів, ССС, нервової системи та шлунково-кишкового тракту [4, 56, 79]. У лікарів вузького профілю відсутня діагностична настороженість щодо ХБ, тому частіше вони ставлять діагноз локальної патології. Необхідно підкреслити, що діагностика ХБ базується на аналізі клінічних проявів, оскільки відсутні патогномонічні лабораторні дослідження, що дозволяють верифікувати діагноз ХБ, а своєчасне встановлення діагнозу необхідне для оптимізації ведення таких хворих [24, 46, 56].
Згідно з переглянутою на Міжнародній консенсусній конференції номенклатурою васкулітів (Чапел-Гілл, США, 2012), до СВ без переважаючого типу уражених судин відносять ХБ і синдром Когана, які вражають судини будь-якого калібру (малого, середнього, великого) і типу (артерії, вени, капіляри). ХБ характеризується рецидивними афтозними виразками ротової порожнини та/або статевих органів, що супроводжуються запальними ураженнями шкіри, очей, суглобів, шлунково-кишкового тракту та/або центральної нервової системи. При ХБ можуть розвиватися васкуліти дрібних судин, тромбоангіїти, тромбози, артеріїти та артеріальні аневризми [51].
Історія
У 1937 р. турецький дерматолог H. Behçet вперше описав захворювання у трьох пацієнтів із клінічною тріадою – афтозним стоматитом, виразками статевих органів і переднім увеїтом з гіпопіоном [14]. Згодом були зареєстровані інші клінічні прояви ХБ [24, 46].
Епідеміологія
ХБ зустрічається в різних географічних зонах світу, хоча існують значні регіональні відмінності з найвищою захворюваністю у країнах, розташованих уздовж Шовкового шляху, що простягається від Східної Азії до Середземномор’я [38, 47]; тому ХБ ще називають «хвороба шовкового шляху» [53]. Найвищу поширеність ХБ відзначають у Туреччині, яка становить 421 випадок, у Японії, Ірані, Іраку, Саудівській Аравії, Кореї – 13‑20 випадків, у США – 5,2 випадку, у Великій Британії – 0,64 випадку на 100 тис. населення відповідно [27, 69]. Однак унаслідок міграції географічна поширеність цього захворювання змінюється [24, 28]. Так, у країнах із низькою частотою ХБ більший відсоток захворюваності спостерігають в осіб, які є вихідцями з регіонів із високою поширеністю ХБ [64].
ХБ переважно розвивається у віці 20‑40 років, рідко зустрічається серед дітей та осіб після 55 років [78]. Здебільшого хворіють чоловіки, зокрема частіше – із Середземноморського регіону, а жінки – на Далекому Сході [1, 12].
Етіопатогенез
Етіопатогенез ХБ до кінця не з’ясований і має мультифакторіальну природу [27, 54, 56, 61, 79, 103]. Відомо, що у розвитку ХБ відіграють роль інфекційні (вірусні, бактеріальні), генетичні, екологічні та токсичні фактори [27, 37, 64, 79, 103]. Зокрема, інфекція (вірусна, бактеріальна) або інші чинники можуть індукувати автоімунну реакцію у генетично схильних людей із виникненням васкуліту [20, 87]. Те, що ХБ частіше зустрічається у деяких етнічних групах, вказує на роль генетичних факторів у її розвитку [30]. Встановлено, що на ХБ частіше хворіють у регіонах із високою поширеністю HLA-B51, з якими виявлено сильну кореляцію [24, 37, 54, 78, 103]. До того ж наявність HLA-B51 пов’язана з тяжким перебігом цього захворювання та асоційована із сімейною ХБ [71].
Патогенез ХБ розглядається як посилена реакція імунної системи на антигени навколишнього середовища чи автоантигени у генетично схильних осіб.
Клінічні і патогенетичні аспекти ХБ [30]
- Активація нейтрофілів
- Клітинний та гуморальний імунітет
- Антигенні стимули
- Вірус простого герпесу
- Стрептококи та суперантигени
- Білки теплового шоку (молекулярна маса 65 кДа, αβ-кристалін)
- HLA-B51 та презентація антигену
- Retinal-S як антиген та HLA-B51 як автоантиген
- Патологія судин та антитіла до ендотеліальних клітин
- Гендерні аспекти
Автоімунна відповідь, що зумовлена генетичними та екологічними факторами, призводить до розвитку СВ та пов’язаних із ним клінічних проявів [4]. У дослідженнях показано, що ген фактора некрозу пухлини α (алель ФНП-α‑1031C) і поліморфізм генів інтерлейкіну (ІЛ)-21, ІЛ‑10 та ІЛ‑8 асоційовані з патогенезом ХБ, зокрема розглядається роль осі ІЛ‑23/ІЛ‑17 в індукції ХБ. Окрім того, гіперчутливість уповільненого типу до таких інфекцій, як стрептококи може бути важливим фактором розвитку ХБ. Показано, що бактеріальні антигени разом із білком теплового шоку (60/65 кДа) активують Т-клітини із посиленням запальної реакції [71].
Основними патогенетичними ланками ХБ є:
- зниження активності Т-лімфоцитів-хелперів, збільшення кількості циркулювальних автоантитіл до клітин слизових оболонок;
- синтез циркулювальних Т-лімфоцитів, які мають цитотоксичність до епітелію слизової оболонки ротової порожнини;
- висока хемотаксична і фагоцитарна активність сегментоядерних нейтрофілів.
Ці фактори насамперед призводять до пошкодження ендотелію судин із розвитком запалення та тромбозу [30, 59]. На додаток, у хворих на ХБ відзначають підвищення сироваткового рівня цитокінів, таких як ФНП-α, ІЛ‑6 та ІЛ‑8, виявляють антитіла до ендотеліальних клітин, лімфоцитів, кардіоліпіну та антинуклеарні антитіла, а також виразну активацію нейтрофілів і моноцитів [27, 30, 99].
Порушення згортання крові та надмірна активність тромбоцитів можуть відігравати додаткову роль у пошкодженні ендотелію, запаленні та судинній патології при ХБ (рис. 1).
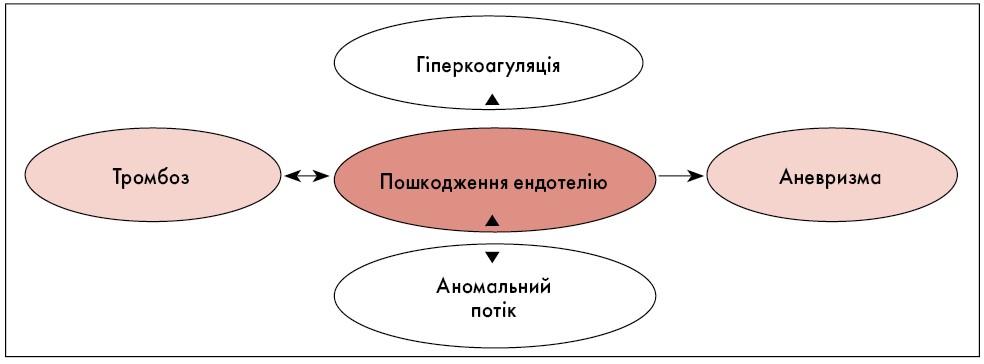 Рис. 1. Зв’язок між гіперкоагуляцією, пошкодженням ендотелію, тромбозом, аневризмою та аномальним потоком у патофізіології ураження судин при ХБ
Рис. 1. Зв’язок між гіперкоагуляцією, пошкодженням ендотелію, тромбозом, аневризмою та аномальним потоком у патофізіології ураження судин при ХБ
Примітка: Адаптовано за M.B. Owlia та G. Mehrpoor [71].
Патогенез підвищеного ризику тромбоутворення при ХБ до кінця не відомий [71]. Виявлено значну тромботичну тенденцію, пов’язану із запаленням судин, що може бути спровокована навіть внутрішньовенним введенням голки або канюлі [86]. Запалення судинної стінки є основною причиною тромбоутворення при ХБ [10, 56]. У його розвитку відіграє роль дисфункція ендотелію в результаті запалення та підвищення згортання крові, пригнічення фібринолізу, відкладення імунних комплексів у стінці судин, підвищення рівня протромботичних факторів, надмірна активація тромбоцитів зі збільшенням їх агрегації [10].
У літературі є дані, що високий ризик тромбозу при ХБ пов’язаний із Т-клітинно-опосередкованим нейтрофільним запаленням [102]. Висунуте припущення, що комплекси тромбоцитів-нейтрофілів можуть відігравати важливу роль у тромбозі та запаленні, яке спостерігається при деяких судинних подіях, зокрема при ХБ. Утворення цих комплексів зумовлює трансендотеліальний рух тромбоцитів і розвиток запалення та тромбозу in vitro й in vivo [71].
Підвищення рівня деяких маркерів дисфункції ендотелію (зокрема, молекул адгезії) та запалення (прозапальні цитокіни, С-реактивний білок) підтверджують їх важливе місце у патофізіології більшості імуноопосередкованих серцево-судинних подій при ХБ [71]. Встановлено, що фактор V (фактор Лейден) та HLA-B5 (B51) підвищують ризик тромбофлебіту у певних етнічних групах [16]. Дисфункція ендотелію призводить до збільшення продукції фактора Віллебранда, VIII фактора згортання крові та до зниження – простацикліну (PGI2) [10, 16, 42, 43]. Також виявлено зростання рівня фібриногену та зниження фібринолітичної активності у пацієнтів з активним ХБ [10, 102]. Високий рівень фактора активації тромбоцитів і Р-/Е-селектину в осіб із ХБ при тромбозі підтримує асоціацію ендотеліальної активації та тромбозу [16, 71]. Окрім того, встановлений зв’язок мутації гена MEFV із патологією судин великого калібру в населення Туреччини та із тромбозом вен – Ізраїлю [76].
У рекомендаціях Європейської антиревматичної ліги (EULAR, 2018) зазначено, що у пацієнтів із ХБ тромбоз глибоких вен (ТГВ) виникає внаслідок запалення стінки судини, а не гіперкоагуляції [45]. За даними дослідження M. Leiba et al. не виявлено постійних первинних порушень у коагулянтній, антикоагулянтній чи фібринолітичній системах у хворих на ХБ [60].
Гістопатологія
Основною гістопатологічною ознакою ХБ є васкуліт судин великого, середнього та малого калібру з периваскулярним запаленням і розвитком тромбозу [27, 29, 56, 82, 87]. У місцях ураження виявляють інфільтрацію лімфоцитами, моноцитами, еозинофілами й нейтрофілами, набряк ендотелію, лейкоцитоклазію (фрагментація, дегрануляція нейтрофілів) та лейкоцитокластичний васкуліт [27, 79, 87].
Для ураження артерій на ранній стадії захворювання характерні активне запалення з інфільтрацією переважно медії та адвентиції, у пізній спостерігають зникнення еластичних і м’язових волокон, фіброз інтими й адвентиції, проліферацію і тромбоз vasa vasorum, у деяких випадках – поєднання цих патологічних процесів [79]. При ураженні артерій частіше виявляють розвиток аневризм [80].
Клінічна картина
ХБ має хронічний перебіг із періодами загострення та ремісій, гетерогенними клінічними проявами, проте тягар хвороби має тенденцію зменшуватися через 5‑10 років [45, 58, 61]. Необхідно зазначити, що у чоловіків спостерігається тяжчий перебіг ХБ, що, ймовірно, пов’язано з дією естрогенів. У них виявляють, зокрема, тяжку патологію судин, центральної нервової системи, легень та аневризми легеневої артерії [30, 50, 58, 79].
Для ХБ, як зазначено вище, характерна мультисистемність ураження із залученням шкіри, слизових оболонок, очей, суглобів, нервової системи, серця, судин, шлунково-кишкового тракту та інших органів і систем [45, 71, 87]. ХБ притаманні рецидивні виразки слизової оболонки очей (у 90‑100% хворих) і статевих органів, ураження шкіри (псевдофолікуліт, вузлувата еритема, пустули), ураження очей (увеїт), артрит/артралгії, невропатія, ураження шлунково-кишкового тракту, вен, артерій, серця тощо [1, 19, 45, 63].
Ураження судин
Ураження судин є частим ускладненням ХБ, що діагностують у 1,8‑52% випадків (табл. 1); також воно є несприятливим прогностичним фактором [6, 29, 32]. У літературі наявні дані про ураження судин у 78% хворих на ХБ з аневризмами легеневої артерії [96]. Слід зазначити, що поняття vasculo-Behçet застосовують у випадках, коли судинні прояви домінують у клінічній картині [29, 79]. Патологію судин частіше виявляють у молодих чоловіків у перші роки після початку захворювання [29, 89]. Ураження судин як перший прояв ХБ спостерігали у 27,5% хворих [32].
Як вказано вище, для ХБ характерним є залучення у патологічний процес вен, артерій, капілярів із розвитком васкуліту судин різного калібру [95]. Ураженню судин при ХБ притаманна значна тромботична тенденція, що пов’язана з їх запаленням. Необхідно зазначити, що при патології судин мають місце регіональні відмінності, зокрема, ушкодження судин досить рідко відзначають у населення країн Далекого Сходу. Воно може сформуватися як окремий клінічний кластер, при якому в одного і того ж пацієнта діагностують кілька типів артеріальних або венозних подій [86]. Слід звернути увагу, що, за даними дослідження M. Abdo et al., не виявлено асоціації між патологією судин при ХБ і факторами ризику ССЗ (як-то куріння, артеріальна гіпертензія, ожиріння, дисліпідемія, цукровий діабет) [1].
За результатами випробування E. Kural-Seyahi et al., ураження судин діагностували у 49,2% чоловіків та 5,6% жінок, артерій великого калібру – у 7,6 і 0,8% відповідно, патологію вен великого калібру (оклюзію верхньої чи нижньої порожнистих вен, синдром Бадда – Кіарі) – у 13,7% чоловіків, ТГВ нижніх кінцівок – у 27,9 та 3,2% чоловіків і жінок відповідно [58]. Згідно з даними дослідження, проведеного T. Aksu et al., середній вік хворих із пошкодженням судин становив 27 років, переважали чоловіки (81:12), венозний тромбоз діагностували у 42% (ТГВ нижніх кінцівок – у 33%, нижньої порожнистої вени – у 6%, верхньої порожнистої вени – у 11%), ураження артерій – у 38% (тромбоемболію легеневої артерії – у 35%), синдром Бадда – Кіарі – у 7% [5].
За результатами іншої роботи, венозний тромбоз було виявлено приблизно у 70% пацієнтів, аневризми – у 20% та тромбоемболію легеневої артерії – у 19%. Середній період від діагностики ХБ до розвитку ураження судин становив біля семи років, однак судинну патологію виявляли орієнтовно у 26% випадків при встановленні діагнозу ХБ [50].
Ураження вен
Патологія вен – це найпоширеніше ураження судин, що діагностують у 10,5‑42% пацієнтів із ХБ, і які зазвичай є раннім проявом цього захворювання [1, 19, 29, 32, 82]. У літературі є дані щодо частішого ураження вен (за результатами роботи Y. Ishigatsubo у 70% хворих мав місце тромбоз вен) [50]. Частоту ураження вен і артерій наведено у таблиці 2.
Для уражень вен характерні тромбози [56]. Своєю чергою ТГВ відносять до найпоширенішого типу ушкодження судин (дві третини всіх випадків тромбозу), що зазвичай є двостороннім і має рецидивний перебіг [28, 86]. ТГВ нижніх кінцівок спостерігають у 5‑29,8% хворих на ХБ [1, 81]. Однак є повідомлення про вищу частоту ТГВ нижніх кінцівок – у 67,1% випадків [91]. Тромбоз поверхневих вен також відносять до частих уражень вен при ХБ [29, 82].
Венозний тромбоз виникає переважно в судинах нижніх кінцівок, але може розвиватися в інших венах, зокрема нижній і верхній порожнистих венах, венах печінки, синусів головного мозку [28, 32]. Так, третину венозних тромбозів виявляють у судинах великого калібру (як-от легенева артерія, нижня або верхня порожниста вена, мозковий венозний тромбоз тощо) [29, 82]. За даними дослідження, тромбоз верхньої та нижньої порожнистих вен діагностували у 9 та 2,5% випадків відповідно [65]. Слід зазначити, що синдром Бадда – Кіарі є несприятливим прогностичним фактором, що збільшує смертність хворих на ХБ у дев’ять разів [29]. Сукупний ризик повторних судинних подій становив 38,4% за п’ять років [91].
Ураження артерій
Ураження артерій спостерігають рідше, ніж патологію вен і діагностують у 0,5‑17% хворих на ХБ [1, 29, 41, 50, 95]. Однак є дані щодо вищої частоти пошкодження артерій – у 36,8‑38% випадків [5, 19]. Ураження артерій як перший прояв ХБ відзначали у 7,8% осіб із ХБ [79]. Основними місцями ушкодження артерій є аорта, стегнові, сонні, легеневі, клубові, підколінні артерії [29]. Патологія артерій включає аневризми, тромбози, оклюзії чи стенози: у 2/3 випадків ураження артерій діагностують аневризми, у третині – оклюзії [1, 29, 50, 56, 95]. Потрібно зазначити, що ураження артерій часто буває множинним [56]. Патологія грудної аорти та легеневої артерії є найтяжчими ураженнями, які у 40% випадків були причиною смерті хворих на ХБ [79]. Аортит відносять до рідкісних проявів ХБ, який діагностували у 3% пацієнтів [79].
Деструкція судинної стінки внаслідок запальної клітинної інфільтрації призводить до ослаблення та витончення артеріальної стінки і формування аневризми [28, 71]. Аневризми артерій можуть призводити до розриву, особливо аневризми легеневої артерії, що пов’язані з високим ризиком масивної кровотечі та смерті [29, 79].
За даними дослідження D. Saadoun et al., артеріальні ураження діагностували у 12,3% осіб із ХБ, з яких 91,2% були чоловічої статі (порівняно з 62,4% без пошкодження артерій; p=0,017), що мали вищі показники ураження вен – 80,4% (порівняно з пацієнтами без ураження артерій – 29,8%; p<0,001). Середній вік хворих при встановленні діагнозу ХБ складав 33 (27‑41) роки, ураження артерій – 38 (30‑43) років. Необхідно зазначити, що відмінності у частоті тютюнокуріння у групі пацієнтів з/без ушкодження артерій були відсутні. Патологія артерій включала аневризми (47,3%), оклюзії (36,5%), стенози (13,5%) та аортити (2,7%). До патологічного процесу переважно були залучені аорта (16,9%), стегнова (15,5%) й легенева (14,1%) артерії. У 68,2% випадків спостерігали ізольоване ураження артерій, у 31,7% – множинне. В осіб із пошкодженням артерій патологія вен мала місце у 2,5 рази частіше, ніж у пацієнтів без нього [79].
Ці дані підтверджують результати роботи H. Ceyran et al., за якими аневризми артерій діагностували частіше, ніж оклюзії, а у третині випадків ураження були множинними [18]. За даними досліджень, аневризми артерій виявляли у 9,8‑20%, а легеневу емболію – у 11‑19% хворих [1, 41, 50]. Аневризми артерій були причиною смерті у 100% випадків внаслідок їх розриву і кровотечі [1].
Серед патологій артерій ураження легеневої артерії зустрічається найчастіше, яке діагностують у ~5% випадків ХБ і частіше спостерігають у чоловіків [16, 86, 96]. Патологія легеневої артерії асоційована з несприятливим прогнозом, за якої смертність становить 26% [16, 83, 86, 96]. Васкуліт судин легень може спричинити тромбоз, інфаркт, крововиливи і аневризми [96].
Аневризми легеневої артерії є причиною зростання захворюваності та летальних випадків при ХБ [42, 83]. Так, смертність хворих становить близько 25% протягом семи років незважаючи на жорсткий контроль, часті візити до лікаря та агресивне ведення. Збільшення діаметра аневризми та високий тиск у легеневій артерії є несприятливими прогностичними факторами виживаності пацієнтів [85, 97]. Встановлено, що поширеність рецидивів становить близько 20% [20]. Частоту клінічних проявів аневризми легеневої артерії представлено у таблиці 3.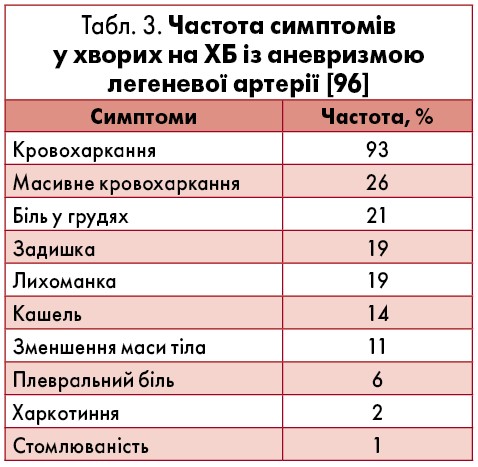
Аневризми легеневої артерії бувають одиночними, множинними, одно- чи двосторонніми, істинними та можуть формуватися псевдоаневризми. Супутні позалегеневі венозні тромбози чи тромбофлебіт та артеріальні аневризми і/або оклюзії мають 78% пацієнтів з аневризмами легеневої артерії [96]. Однак ураження легеневої артерії при ХБ не обмежується аневризмами – також мають місце розвиток тромбозу легеневої артерії (in situ) та пошкодження паренхіми легень, асоційованої із залученням до патологічного процесу легеневої артерії [83]. Тромбоз легеневої артерії діагностують приблизно у третини пацієнтів з ураженням легеневої артерії [5, 56, 83, 85, 97].
Варто підкреслити, що аневризми або тромбози можуть зникати чи регресувати приблизно в 70% випадків у разі використання імуносупресивних препаратів [83].
Ураження серця
Патологію серця діагностують у 0,6‑8,8% хворих, яка погіршує прогноз хворих на ХБ [29, 37]. Однак є повідомлення про вищу частоту ураження серця, яка становить 20,6% (табл. 4) [32]. Пошкодження ССС включає перикардит, ендокардит (із розвитком аортальної регургітації та рідше – мітральної недостатності), пролапс мітрального клапана, внутрішньосерцевий тромбоз, коронарит, стенокардію (стабільну та нестабільну), інфаркт міокарда (ІМ), міокардит, кардіоміопатію, ендоміокардіальний фіброз, аневризми міжпередсердної перегородки і шлуночка, аневризми синуса Вальсальви, порушення ритму та провідності серця, застійну серцеву недостатність (СН) [27, 29, 37, 77]. Ураження серця є першим клінічним проявом у 40‑69,23% хворих [2]. За даними дослідження T. Ahmed et al., 84,6% осіб із патологією серця були чоловіки, середній вік яких становив 34,2 року [2]. Результати випробувань показали, що саме ХБ підвищує ризик ураження серця, а не наявність факторів ризику ССЗ [3, 34, 68].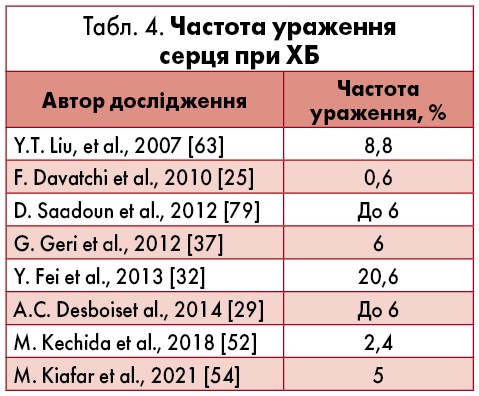
За даними дослідження, проведеного N. Gao et al., серед хворих з ураженням ССС чоловіків було 77,1% за середнього віку 37,19+10,4 року, а жінок – 36,0+8,6 року. Патологія серця включала:
- недостатність клапанів – 20,57%;
- порушення провідності серця – 28,6%;
- внутрішньосерцевий тромбоз – 2,9%;
- аневризми артерій – 37,1%;
- стеноз/оклюзію артерій – 14,3%;
- ураження легеневої артерії – 8,6%;
- тромбоз вен – 11,4%.
Варто зазначити, що у 20 пацієнтів було більш ніж одне з цих уражень серця. Показники запалення не мали суттєвої різниці між вищевказаними підгрупами (р>0,05). Лікування включало глюкокортикоїди (ГК) та імуносупресивні препарати, симптоматичну терапію, а також інтервенційне й хірургічне втручання [35]. За даними іншої роботи, перикардит діагностували у 38,5%, ендокардит – у 26,9% (аортальну недостатність – у 17,3%, мітральну – у 5,8%), внутрішньосерцевий тромбоз – у 19,2% (у правих відділах серця), ІМ – у 17,3%, ендоміокардіальний фіброз – у 7,7%, ішемічні зміни на ЕКГ – у 9,2%, порушення внутрішньошлуночкової провідності серця – у 7,7% хворих [37].
За результатами випробування Y.T. Liu et al., недостатність клапанів аорти діагностовано у 53%, тромби у правому шлуночку – у 32%, ІМ – у 11%, міокардит – у 5% осіб із ХБ [63]. Згідно з даними дослідження T. Ahmed et al., ураження серця включало ІМ з елевацією сегмента ST – у 22,22%, стабільну стенокардію – 5,5%, правошлуночкову СН – 11,1%, випіт у перикард – 22,22%, внутрішньосерцевий тромбоз – 11,1%, легеневу гіпертензію – 22,22% (у 16,7% внаслідок тромбоемболії легеневої артерії), мітральну недостатність – 5,5% випадків. За середній період спостереження (59,73 місяця) смертність у результаті патології серця становила 15,4% [2].
Перикардит – найпоширеніше ураження серця при ХБ, яке виявляють у 22,22‑38,5% випадків [2, 37, 71]. У хворих на ХБ діагностують гострий, ексудативний перикардит (асимптоматичний), тампонаду серця, констриктивний перикардит [71]. При ХБ частіше розвивається аортальна недостатність – у 17,3%, рідше діагностують мітральну – у 5,8%, трикуспідальну і недостатність клапана легеневої артерії – у 1,9% випадків [37].
У хворих на ХБ можуть розвиватися порушення провідності серця, зокрема атріовентрикулярні (АВ) блокади різного ступеня, блокада правої ніжки пучка Гіса та порушення ритму серця (екстрасистолічна аритмія, шлуночкова тахікардія) [6, 10, 19, 37, 71, 87]. АВ-блокади – рідкісний прояв ХБ, розвиток яких може бути пов’язаний із запаленням АВ-вузла та оточуючих тканин; також вони можуть потребувати імплантації електрокардіостимулятора [37].
Рідкісним ураженням серця при ХБ є ішемічна, неішемічна або запальна кардіоміопатія з розвитком безсимптомної діастолічної та/або систолічної дисфункції чи СН [87]. У літературі є повідомлення про розвиток у 33-річного пацієнта дилатаційної кардіоміопатії та повної АВ-блокади [6].
Ураження коронарних артерій
Атеросклероз залишається основною причиною гострого ІМ, але, як відомо, є інші більш рідкісні причини його розвитку, які слід враховувати, особливо у молодих пацієнтів. Ураження коронарних артерій (КА) доволі рідко зустрічається у хворих на ХБ із поширеністю 0,5-12,1% випадків [19, 70‑73, 79]. Патологія КА є потенційно фатальним ускладненням ХБ і може проявлятися стабільною чи нестабільною стенокардією, безбольовою ішемією міокарда, ІМ, порушенням ритму серця, раптовою кардіальною смертю [19, 70, 71].
Артеріїт, аневризми/псевдоаневризми, стеноз/оклюзія, тромбоз КА є причиною розвитку ішемічної хвороби серця (ІХС) при ХБ [10, 19, 71]. Лейкоцитокластичний васкуліт, підвищення тромбоутворення (внаслідок дисфункції ендотелію, зменшення активності фібринолітичної системи крові, підвищення рівнів факторів згортання крові (зокрема, 8-го фактора), фібриногену та аневризми КА відіграють роль у патогенезі ІХС при ХБ [87]. Окрім коронариту, зазначають додаткові механізми розвитку ІХС при ХБ, як-то спонтанна дисекція КА і субклінічний атеросклероз [28].
За даними роботи H. Chen et al., ураження КА при ХБ відзначали у 4% хворих, з яких 89,5% становили чоловіки. Середній вік пацієнтів із пошкодженням КА був 34 роки, а середня тривалість розвитку патології КА від початку захворювання – 2,8 року.
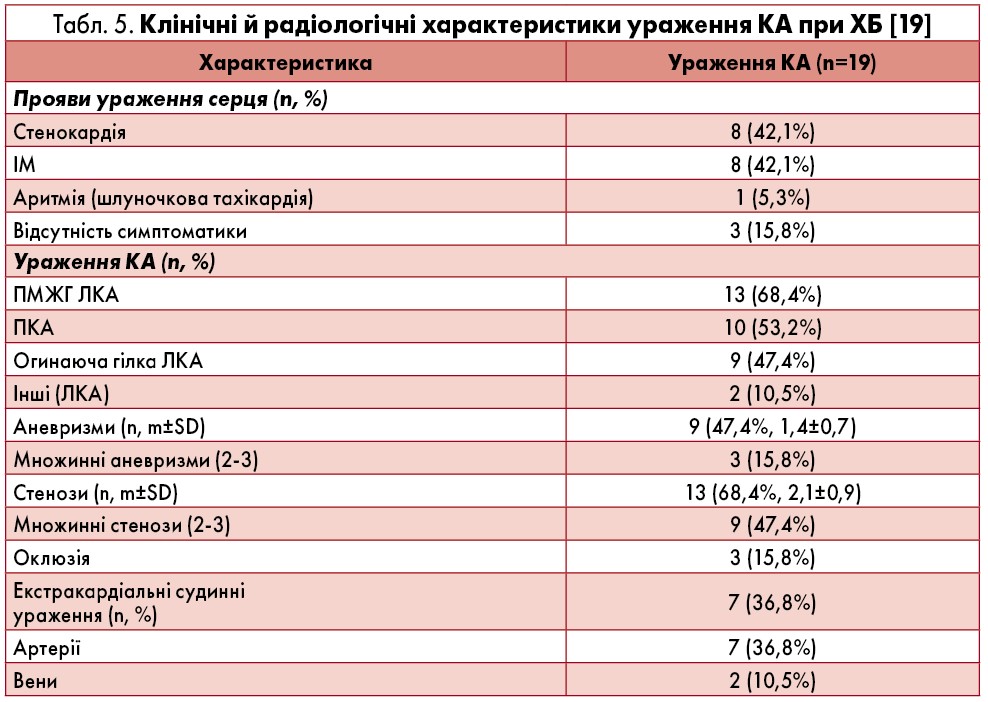
Стенокардію спостерігали у 42,1%, ІМ – у 42,1%, шлуночкові порушення ритму серця – у 5,3% осіб з ураженням КА, 15,8% пацієнтів були асимптоматичними, але на ЕКГ виявляли зміни. За даними коронарографії та комп’ютерно-томографічної (КТ) ангіографії найчастіше мали місце стенози КА – у 68,4%, аневризми – у 47,4%, оклюзії – у 15,8% випадків (табл. 5) [19].
Характерним було множинне ушкодження КА, найчастіше уражалася передня міжшлуночкова гілка (ПМШГ) лівої коронарної артерії (ЛКА) і права коронарна артерія (ПКА). При проведенні мультиваріантного аналізу тест патергії був незалежним фактором ураження КА [19]. Необхідно зазначити, що при ХБ частіше страждають проксимальні відділи КА [86].
ІМ діагностують у 11‑22,22% хворих на ХБ та патологію серця [2, 37, 63], хоча є повідомлення про вищу частоту – 42,1% [19]. Ризик ІМ (відношення шансів [ВШ] 1,72; 95% довірчий інтервал [ДІ] 1,01‑2,73) та інсульту (ВШ 1,65; 95% ДІ 1,09‑2,50) значно вищий у пацієнтів із ХБ порівняно із групою контролю, який зберігається після корегування, що пояснюється наявністю васкуліту [3]. ІМ при ХБ є наслідком артеріїту КА, проте його розвиток спостерігали і при незмінених КА [71, 87]. У літературі є дані про дисфункцію ендотелію, зокрема коронарних мікросудин в осіб із ХБ, що призводить до суттєвого порушення резерву коронарного кровотоку порівняно з контролем [17]. У метааналізі у пацієнтів із ХБ було виявлено погіршення потікопосередкованої вазодилатації та більшу товщину комплексу інтима-медіа сонних артерій порівняно з контролем [66].
На додаток, описано розвиток ІМ з елевацією сегмента ST нижньої стінки лівого шлуночка, який був першим проявом ХБ. ІМ розвинувся внаслідок тромбозу дистального відділу ПКА у 50-річної жінки, якій провели аспірацію тромбу та призначено еноксапарин, аспірин і клопідогрель [70]. У літературі наведений випадок розвитку ІМ у 66-річного пацієнта, в якого за даними коронарографії виявили трисудинне ураження КА (стеноз ПКА, огинаючої гілки ЛКА, ПМЖГ ЛКА) і гігантську аневризму ПМЖГ ЛКА. Було проведено аортокоронарне шунтування та виключення аневризми з коронарного кровотоку [9]. Також описаний тромбоз дистального сегменту ЛКА у 38-річного хворого з розвитком ІМ з елевацією сегмента ST переднього відділу лівого шлуночка, що ускладнився кардіогенним шоком та нестійкою шлуночковою тахікардією [10].
Аневризми КА – одне з ускладнень ХБ, які діагностують у 0,5‑5% пацієнтів [75]. За даними роботи H. Chen et al., у хворих з ураженням КА аневризми виявляли у 47,4%, частіше – одиничні аневризми (переважно з локалізацією у ПКА) [19]. Аневризми КА можуть мати безсимптомний перебіг, але також призводити до розвитку гострого коронарного синдрому у разі поєднання зі стенозом КА. Аневризми бувають сакулярними, кальцинованими, тромбованими [89]. В основі формування аневризми лежать облітерувальний ендартеріїт vasa vasorum та периваскулярна інфільтрація мононуклеарними клітинами з деструкцією медії та стоншенням стінки судин [19, 89].
У літературі описаний випадок розвитку аневризм КА у 56-річного чоловіка із ХБ, який раніше переніс лобектомію правої легені з приводу аневризм легеневої артерії та був госпіталізований через стенокардію. На ЕКГ зареєстровано АВ-блокаду 2:1, блокаду правої ніжки пучка Гіса і передньоверхньої гілки лівої ніжки пучка Гіса. За даними інвазивної коронарографії, виявлено дві кальцифіковані аневризми у проксимальному сегменті ПМЖГ ЛКА та огинаючої гілки ЛКА (із тромбозом і дистальним уповільненням кровотоку). КТ-ангіографія підтвердила наявність двох сакулярних аневризм. Хворому проведено імплантацію двокамерного кардіостимулятора та аортокоронарне шунтування [77].
Внутрішньосерцевий тромбоз
В осіб із ХБ виявляють внутрішньосерцеві тромби у 32% пацієнтів, що часто передують іншим проявам цього захворювання [36]. Чоловіки страждають частіше за жінок із співвідношенням 23:2, середній вік хворих – 27 років. Внутрішньосерцевий тромбоз асоційований з ураженням легеневої артерії та здебільшого локалізується у правій половині серця [5]. У 40‑56% пацієнтів із внутрішньосерцевим тромбозом виявлено патологію легеневої артерії, 42‑56% із них мали венозний тромбоз, а 52‑55% – тромбоз легеневої артерії [5, 32, 68]. За даними роботи T. Aksu et al., тромбоз правої половини серця мав місце у 95% хворих (тромбоз правого шлуночка – у 74%, правого передсердя – у 43%), тромбоз синусів – у 6% [5]. Той факт, що тромби переважно локалізуються у правому шлуночку, підтверджують і результати іншого дослідження. До того ж встановлено асоціацію з аневризмою легеневої артерії [36].
Слід зазначити, що рецидиви є нечастими, та під впливом імуносупресивного лікування тромби регресують. При виявленні внутрішньосерцевого тромбозу рекомендовано проводити дослідження легеневої артерії за допомогою КТ органів грудної клітки. Кардіохірургічне втручання не рекомендоване, якщо відсутні ускладнення, такі як недостатність клапана або легенева гіпертензія [86]. Внаслідок високої специфічності тромбозу у правих відділах серця при ХБ, у разі його виявлення необхідно виключити ХБ, особливо у молодих осіб із країн Ближнього Сходу чи Середземномор’я [36].
Атеросклероз
Дані щодо атеросклерозу в осіб із ХБ суперечливі. E. Seyahi et al. вважають, що прискорений розвиток атеросклерозу не є характерною рисою ХБ (на основі виявлення атеросклеротичних бляшок та оцінки товщини комплексу інтима-медіа сонних і стегнових артерій) [84]. Однак за результатами іншої роботи, встановлений субклінічний атеросклероз у хворих на ХБ [44]. Є точка зору, що передчасний розвиток атеросклерозу пов’язаний із застосуванням ГК [88].
Діагностика
Через відсутність специфічних маркерів діагностика ХБ є складним завданням. Діагноз ХБ, по суті, базується на клінічних проявах, а діагностичні критерії дають можливість встановити діагноз із достатньою чутливістю та специфічністю [56]. У крові виявляють неспецифічні зміни, зокрема підвищення швидкості осідання еритроцитів, рівня С-реактивного білка [19, 79]. HLA-B51 є поширенішим в осіб із ХБ, ніж у загальній популяції: 60% хворих на ХБ були позитивними щодо HLA-B51 [98]. Позитивний тест патергії відмічали у 45% випадків [98]; за даними іншої роботи – у 82% пацієнтів із ХБ [96]. Окрім того, у хворих на ХБ виявляють антитіла до ендотелію тощо [19].
Із діагностичною метою для виявлення ураження серця і судин при ХБ перевагу слід віддавати неінвазивним методам дослідження із візуалізацією, як-то доплерівське ультразвукове дослідження, КТ, магнітно-резонансна томографія (МРТ), КТ-ангіографія, МРТ-ангіографія, позитронно-емісійна томографія із використанням 18F-фтородезоксиглюкози [33, 77, 79, 89]. На додаток, за показаннями можна проводити інвазивну коронарографію, внутрішньосудинне ультразвукове дослідження та інші методи [19, 26]. При виконанні коронарографії виявляють стеноз, оклюзію, тромбоз, аневризми КА. На рисунку 2 представлені дані коронарографії хворого на ХБ з ураженням КА [19].
Діагностичні критерії ХБ
Через відсутність специфічних клінічних та лабораторних діагностичних тестів доступні декілька діагностичних критеріїв ХБ, одними з яких є запропоновані Міжнародною дослідною групою (ICBD). Встановлення діагнозу ХБ потребує наявності рецидивних виразок ротової порожнини та принаймні двох інших критеріїв (як-от рецидивні виразки статевих органів, ураження очей, шкіри, позитивний тест на патергію) [22].
Лікування
Метою терапії є своєчасне пригнічення запалення і попереджання рецидивів, підтримання ремісії та покращання якості життя хворих [4, 45]. Для оптимального ведення осіб із ХБ необхідний мультидисциплінарний підхід, а лікування має бути індивідуалізованим відповідно до віку, статі, типу, тяжкості ураження органів та уподобань пацієнтів [45]. Хворі на ХБ потребують тривалого лікування та спостереження, а медикаментозна терапія залежить від клінічних проявів [56].
EULAR (2018) рекомендує призначати ГК, колхіцин, зокрема, при ураженні шкіри і слизових оболонок. У деяких випадках можна розглядати застосування азатіоприну, талідоміду, інтерферону α, інгібіторів ФНП-α чи апреміласту. Для терапії гострого ТГВ рекомендоване призначення ГК та імуносупресивних препаратів, таких як азатіоприн, циклофосфамід або циклоспорин А (рівень доказовості ІII, сила рекомендацій С).
У разі рефрактерного тромбозу варіантом вибору можуть бути моноклональні антитіла до ФНП-α та антикоагулянтів, за умови низького ризику кровотечі та виключення аневризми легеневої артерії (рівень доказовості ІII, сила рекомендацій С). Для лікування аневризм легеневої артерії рекомендовані високі дози ГК та циклофосфаміду, а застосування моноклональних антитіл до ФНП-α слід розглядати у рефрактерних випадках. У пацієнтів із кровотечею або високим ризиком значної кровотечі емболізація доцільніша за відкриту операцію. При аневризмах аорти, периферичних артерій рекомендовано фармакотерапію циклофосфамідом та ГК перед втручанням. У разі наявності симптоматики не слід відкладати хірургічне втручання або стентування (рівень доказовості ІII, сила рекомендацій С) [45].
Проведення антикоагулянтної терапії з метою лікування і профілактики тромбоемболічних ускладнень ХБ є предметом дискусій [27, 86, 101]. Результати дослідження E. Seyahi показали неефективність антикоагулянтної терапії без імуносупресивних препаратів для запобігання рецидивів венозного тромбозу, тому науковці вважають, що лікувати венозний тромбоз потрібно імуносупресивними засобами [86].
Діагностичні критерії ХБ [22]
- Невеликі афтозні, великі афтозні або герпетиформні виразки, що спостерігає лікар або пацієнт, які рецидивують принаймні тричі протягом 12 місяців
Плюс два з наступного:
- Рецидивні виразки статевих органів: афтозні виразки або рубці, що спостерігає лікар чи пацієнт
- Ураження очей: передній/задній увеїт або помутніння склоподібного тіла при дослідженні щільовою лампою чи васкуліт сітківки, який виявляє офтальмолог
- Ураження шкіри: вузлувата еритема, що виявляє лікар або спостерігає хворий, псевдофолікуліт, папулопустульозні ураження чи акнеподібні вузлики, що виявляє лікар у пацієнтів після підліткового віку, які не отримують ГК
- Позитивний тест патергії: оцінює лікар через 24‑48 год (результати застосовують лише за відсутності інших клінічних пояснень)
На основі метааналізу трьох ретроспективних досліджень (рекомендації EULAR, 2018) узагальнена оцінка ризику рецидиву ТГВ у пацієнтів із ХБ, які отримували імуносупресивні препарати та антикоагулянти, порівняно з тими, хто приймав лише антикоагулянти, підтримує застосування імуносупресивних засобів (відносний ризик [ВР] 0,17; 95% ДІ 0,08‑0,35). З іншого боку, терапія антикоагулянтами та імуносупресивними ліками порівняно з лише імуносупресивними препаратами не забезпечує значних переваг у запобіганні рецидивам (ВР 0,75; 95% ДІ 0,48‑1,17) [45].
Як зазначено вище, до терапії при рефрактерному венозному тромбозі можна додати антикоагулянти, однак слід враховувати ризик кровотечі при їх застосуванні у хворих на ХБ, оскільки аневризми артерій тісно пов’язані з ТГВ. При застосуванні антикоагулянтів необхідно проводити обстеження пацієнтів із метою виявлення аневризм. До того ж лікарі повинні мати на увазі ризик розвитку аневризми протягом курсу терапії, оскільки майже у всіх осіб із ХБ та аневризмами є ТГВ в анамнезі [45].
Лікування ураження серця при ХБ переважно емпіричне, спрямоване на зменшення активності васкуліту і базується на призначенні ГК, імуноcупресивних препаратів та колхіцину [27, 29]. Окрім того, проводять стандартне лікування відповідно до патології серця [10, 19, 70]. Терапія уражень КА полягає у зменшенні симптомів і запобіганні подальшого ушкодження. Ремісія патології серця пов’язана із застосуванням ГК, імуносупресивних, антитромботичних засобів та колхіцину [27, 37, 89].
S. Hattori та S. Kawana проводили пульс-терапію метилпреднізолоном із наступним призначенням преднізолону при ураженні КА. Через три тижні така терапія привела до зменшення симптомів [48]. H. Chen et al. при лікуванні осіб із патологією КА призначали ГК, імуносупресивні препарати (циклофосфамід, талідомід, азатіоприн, метотрексат). Також пацієнти отримували аспірин, гепарин та варфарин (за високого ризику тромбозу), β-адреноблокатори та інгібітори ангіотензинперетворювального ферменту (хворі на ІМ). Після лікування (середній період спостереження – 15 місяців) ремісія мала місце у 78,9% хворих, а летальність становила 10,5% (внаслідок СН та раптової серцевої смерті) [19]. Інші автори вважають, що антитромботичну терапію при ураженні серця необхідно застосовувати з обережністю, враховуючи схильність хворих на ХБ до кровотеч, особливо при аневризмах легеневої артерії [27].
У літературі описаний рецидивний тромбоз КА при розвитку ІМ з елевацією сегмента ST у 39-річного чоловіка. Лише після встановлення діагнозу ХБ і 8-денної терапії ГК та колхіцином при виконанні КТ-ангіографії тромбів у КА не було виявлено [94].
При ІМ, окрім ГК та імуносупресивних препаратів, проводять терапію ІМ за сучасними стандартами (антитромбоцитарна терапія, β-адреноблокатори, інгібітори ангіотензинперетворювального ферменту, статини тощо) [10, 70]. У літературі доступні дані щодо успішного тромболізису за відсутності можливості виконання первинного коронарного втручання (ПКВ), застосування інгібіторів глікопротеїнових рецепторів IIb-IIIa [10].
При лікуванні внутрішньосерцевого тромбозу H. Wang et al. показали, що імуносупресивна терапія у комбінації з антикоагулянтами пов’язана з резолюцією тромба, а ремісія внутрішньосерцевого тромбозу асоційована із використанням ГК, імуносупресивних препаратів та антикоагулянтів у 83,3% випадків [101]. За даними дослідження G. Geri et al., у 8 з 10 випадків внутрішньосерцевий тромбоз регресував при лікуванні азатіоприном (n=7) або ГК (n=5). Потрібно зазначити, що ці пацієнти отримували також антикоагулянти [37].
Інтервенційне та хірургічне лікування
При патології ССС за наявності показань можна проводити інтервенційне та хірургічне лікування [62]. У літературі є дані про успішне проведення ПКВ з імплантацією стента при ІМ та ПКВ без стентування [31, 37]. Проте довгострокові результати після успішної ангіопластики чи імплантації стента залишаються нез’ясованими [92]. У деяких випадках при проведенні ПКВ спостерігали тенденцію до зростання частоти тромбозів стентів і рецидивів тромбозів під час тривалого спостереження [48]. Тому автори вважають за доцільне застосовувати імуносупресивну терапію разом з антитромботичними препаратами до та після ПКВ при ХБ для запобігання рецидиву чи загострення. У таких випадках найчастіше використовують ГК, колхіцин, азатіоприн та циклофосфамід [94]. Як альтернативу ПКВ можна проводити тромболітичну терапію у рекомендовані терміни при ІМ (за відсутності можливості проведення ПКВ) [10, 57]. F. Kosar et al. повідомили про успішний фібриноліз у пацієнта із ХБ [57].
У хворих на ХБ потрібно за можливості уникати хірургічного втручання при ураженні артерій у гострій фазі запалення через часті післяопераційні ускладнення, зокрема кровотечі, утворення аневризм, псевдоаневризм, рецидиви, тромбози [8, 13, 28, 32, 49, 74, 105]. ГК та імуносупресупресивні препарати рекомендовано застосовувати до і після операції [62, 105]. Екстрені хірургічні втручання показані у випадках підозри на розрив аневризми або кровотечі [62]. Оперативне втручання може бути необхідним у разі рецидивного масивного внутрішньосерцевого тромбозу, незважаючи на фармакотерапію, або якщо він пов’язаний із СН [23]. Аневризми КА можуть потребувати хірургічного лікування при значних розмірах (більш як 20 мм), швидкому збільшенні розмірів та загрозі розриву, а також симптомах тяжкої рецидивної ішемії, що не піддається медикаментозному лікуванню [21, 89].
У ретроспективному дослідженні 32,6% хірургічних втручань у хворих на ХБ ускладнювалися дегісценцією рани, інфікуванням та оклюзією чи недостатністю трансплантата. Сукупна частота післяопераційних ускладнень становила 7,7% через три, 25,6% – шість, 33,3% – 12 та 35,9% –18 місяців. Післяопераційні ускладнення виникали частіше внаслідок тих операцій, які проводили у пацієнтів із позитивною пробою патергії (р<0,001), та при втручаннях на судинах порівняно із процедурами не на судинах (р<0,05). Однак застосування ГК разом з імуносупресивними препаратами значно знижувало частоту післяопераційних ускладнень порівняно із хворими, які отримували лише ГК, і тими, хто їх не приймав (р<0,05).
Багатофакторний аналіз показав, що позитивна реакція патергії (ВР 1,91; р<0,05) й операції, які не супроводжувалися лікуванням ГК та імуносупресивними препаратами (ВР 2,11; р<0,01), були незалежними факторами ризику виникнення післяопераційних ускладнень. Ці результати підтверджують необхідність проведення імуносупресивного лікування і після хірургічних втручань [74].
При клапанних вадах серця за показаннями рекомендоване оперативне втручання разом з імуносупресивною терапією. Післяопераційні ускладнення включали дисфункцію протезованого клапана, яка може потребувати повторного хірургічного втручання [86]. Y.J. Ha et al. повідомили, що пацієнти із ХБ, які перенесли протезування клапанів серця, мали часті хірургічні ускладнення та високий рівень післяопераційної смертності [39]. Однак є дані, за якими 35,7% осіб з ураженням ендокарда та розвитком клапанних вад серця перенесли протезування клапана без ускладнень [37].
Прогноз
Прогноз при ХБ залежить від типу і тяжкості ураження, а наслідки цього захворювання можуть бути несприятливими. Ураження слизових оболонок і шкіри бувають дуже виснажливими та погіршують якість життя пацієнта. Патологія очей може призводити до погіршення зору із ризиком його втрати, а нервової системи – до серйозних неврологічних наслідків [56]. Ураження очей, судин, нервової системи та шлунково-кишкового тракту пов’язане з гіршим прогнозом [45]. ХБ може корелювати із суттєвою захворюваністю (сліпота, фізичні вади, когнітивні порушення) і зростанням летальних випадків. Судинні прояви, такі як ураження легеневої артерії (смертність протягом трьох років становила 50%) та синдром Бадда – Кіарі є провідними причинами смерті з-поміж хворих на ХБ [27, 32, 86].
У чоловіків відзначають гірший прогноз; причина цього поки не зрозуміла, але, ймовірно, пов’язана з дією естрогенів [30, 79]. В експериментальному дослідженні на щурах з ендотоксин-індукованим увеїтом, подібним до такого при ХБ, клітинна інфільтрація була виразнішою у щурів-самців, ніж самок, в яких після оваріоектомії спостерігали посилення запалення. Лікування 17-бета-естрадіолом сприяло значному зменшенню запалення у щурів-самців та щурів-самок із видаленими яєчниками [67].
Незважаючи на оптимальне медикаментозне лікування, ураження ССС асоційоване із більшою захворюваністю та смертністю [89]. Наявність внутрішньосерцевого тромбозу пов’язана з гіршим прогнозом, але застосування імуносупресивних препаратів покращує прогноз таких хворих [68, 86]. За даними C. Darie et al., річна летальність пацієнтів при ХБ становить 2‑4%. Найпоширенішими причинами смерті є розриви аневризм судин і перфорації виразок кишечника. Аневризми легеневої артерії та синдром Бадда – Кіарі корелюють із вищими показниками смертності. Загалом виживаність хворих на ХБ і патологію серця нижча, ніж у таких без неї [23].
За результатами роботи D. Saadoun et al., смертність хворих за 1 і 5 років склала 1,2 та 3,3% відповідно. Загальна летальність становила 5% після 7,7 року спостереження. Основними причинами смерті були патологія судин великого калібру (переважно аневризми артерій та синдром Бадда – Кіарі) (43,9%), онкологічні захворювання (14,6%), ураження центральної нервової системи (12,2%) та сепсис (12,2%). При проведенні багатофакторного аналізу виявлено, що чоловіча стать (ВР 4,94; 95% ДІ 1,53‑16,43), ураження артерій (ВР 2,51; 95% ДІ 1,07‑5,90) і часті загострення (ВР 2,37, 95% ДІ 1,09‑5,14) незалежно пов’язані з ризиком смерті [80]. Багатофакторний аналіз пошкодження вен (ВШ 0,29; 95% ДІ 0,08‑1,11) та оклюзійних уражень артерій (ВШ 0,13; 95% ДІ, 0,01‑1,25) показав, що вони негативно асоційовані з повною ремісією. Хворі з оклюзією артерій у сім разів рідше повністю відповідали на призначену терапію, а з патологією артерій лише 38,6% досягли цілковитої ремісії [79].
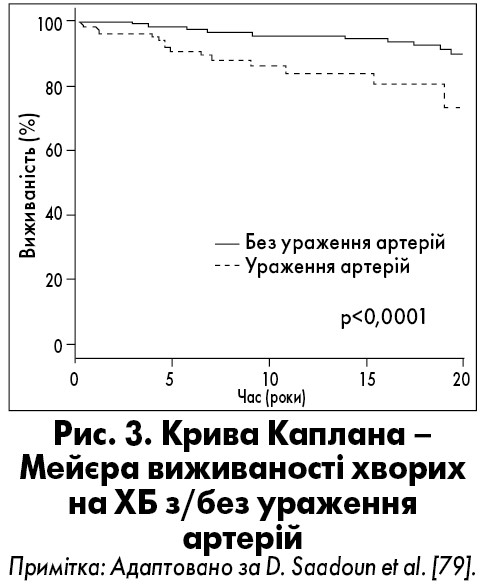 Довгостроковий прогноз в осіб з ураженням артерій гірший, особливо у випадках з оклюзійними ушкодженнями та патологією вен. Виживаність значно нижча у хворих на ХБ з ураженням артерій, ніж без нього (p<0,0001) (рис. 3). Виживаність за 5, 10, 15 і 20 років у пацієнтів із ХБ та ураженням артерій порівняно із хворими без нього становила 90 vs 98%, 86 vs 95%, 84 vs 94% та 73 vs 89% відповідно. Призначення імуносупресивних препаратів покращувало прогноз таких хворих: мало місце різке зниження щорічної частоти артеріальних подій після їх застосування [79].
Довгостроковий прогноз в осіб з ураженням артерій гірший, особливо у випадках з оклюзійними ушкодженнями та патологією вен. Виживаність значно нижча у хворих на ХБ з ураженням артерій, ніж без нього (p<0,0001) (рис. 3). Виживаність за 5, 10, 15 і 20 років у пацієнтів із ХБ та ураженням артерій порівняно із хворими без нього становила 90 vs 98%, 86 vs 95%, 84 vs 94% та 73 vs 89% відповідно. Призначення імуносупресивних препаратів покращувало прогноз таких хворих: мало місце різке зниження щорічної частоти артеріальних подій після їх застосування [79].
Згідно з результатами роботи H.S. Ahn et al., хворі на ХБ (рис. 4) мають нижчу виживаність при ІМ, інсульті та вищий ризик смерті від усіх причин (ВШ 1,82; 95% ДІ 1,40‑2,37) порівняно з контрольною групою [3].
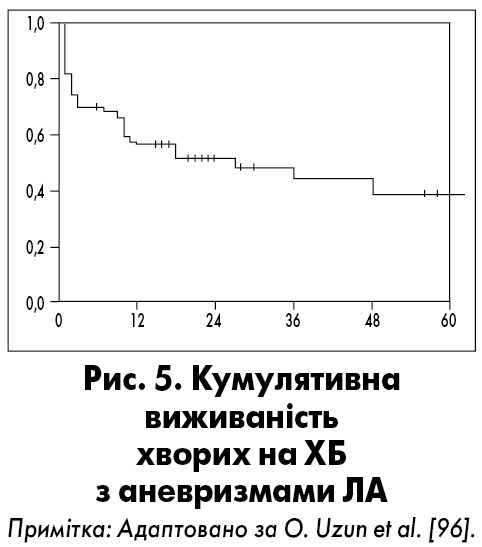
V. Hamuryudan et al. показали, що 5-річна виживаність хворих з аневризмами легеневої артерії становила 80% [42]. За даними роботи O. Uzun et al., кумулятивна 1- і 5-річна виживаність осіб з аневризмами легеневої артерії була 57 і 39% відповідно (рис. 5) [96].
 Рис. 4. Порівняння СС-подій та смерті від усіх причин у хворих на ХБ та групі контролю
Рис. 4. Порівняння СС-подій та смерті від усіх причин у хворих на ХБ та групі контролю
Примітка: Адаптовано за H.S. Ahn et al. [3].
Висновки
 Таким чином, ХБ – це захворювання, для якого притаманне ураження багатьох органів і систем, а своєчасна діагностика та призначення відповідного лікування мають велике значення. При ХБ страждають судини будь-якого калібру і типу (вени, артерії, капіляри). Для цього захворювання характерна тріада: афтозний стоматит, виразки слизових оболонок і шкіри статевих органів, пошкодження очей у вигляді увеїту або іридоцикліту. Патологія серця при ХБ включає перикардит, міокардит, внутрішньосерцевий тромбоз, ендоміокардіальний фіброз, ендокардит із недостатністю клапанів серця, ураження коронарних артерій із розвитком стенокардії, ІМ, безбольової ішемії міокарда, аневризми серця і синуса Вальсальви, порушення ритму та провідності серця.
Таким чином, ХБ – це захворювання, для якого притаманне ураження багатьох органів і систем, а своєчасна діагностика та призначення відповідного лікування мають велике значення. При ХБ страждають судини будь-якого калібру і типу (вени, артерії, капіляри). Для цього захворювання характерна тріада: афтозний стоматит, виразки слизових оболонок і шкіри статевих органів, пошкодження очей у вигляді увеїту або іридоцикліту. Патологія серця при ХБ включає перикардит, міокардит, внутрішньосерцевий тромбоз, ендоміокардіальний фіброз, ендокардит із недостатністю клапанів серця, ураження коронарних артерій із розвитком стенокардії, ІМ, безбольової ішемії міокарда, аневризми серця і синуса Вальсальви, порушення ритму та провідності серця.
Сімейні лікарі, кардіологи, ревматологи мають пам’ятати про ураження ССС у хворих на ХБ і потенційні ризики для їхнього життя, особливо за розвитку аневризм судин, та призначити необхідне обстеження для своєчасної діагностики й терапії. До того ж у літературі описані випадки ХБ, при яких першими проявами захворювання були симптоми патології серця. Прогноз пацієнтів із ХБ та ураженням серця гірший, ніж при патології інших органів, але відповідне лікування покращує прогноз хворих.
Література
- Abdo M., Alkemary A., El Mallah R. What is the impact of traditional risk factors for vascular affection on Behcet’s disease vascular involvement: a retrospective cohort study // Egypt Rheumatol Rehabil. – 2019. – 46. – Р. 257‑261.
- Gemici T., Leila A., Feten F. et al. Cardiac involvement in Behcet’s disease // Archives of Cardiovascular Diseases Supplements. – 2015. – Vol. 7. – Р. 44‑57.
- Ahn H.S., Lee D., Lee S.Y. et al. Increased cardiovascular risk and all-cause death in patients with Behçet’s disease: a nationwide population-based dynamic cohort study // J Rheumatol, 2019; pii: jrheum.190408.
- Akdeniz N., Elmas Ö.F., Karadağ A.S. Behçet syndrome: A great imitator // Clin Dermatol. – 2019. – 37 (3). – Р. 227‑239.
- Aksu T., Tufekcioglu O. Intracardiac thrombus in Behçet’s disease: Four new cases and a comprehensive literature review // Rheumatol Int. – 2015. – 35. – Р. 1269‑1279.
- Al-Izzi M., El Bur M., Arif M. A diagnosis not to be missed: Behcet’s disease as a cause of dilated cardiomyopathy in a young Arab male patient // Int J Rheum Dis. – 2010. – 13. – Р. 97‑99.
- Altenburg A., Davatchi F., Sadeghi B. et al. Update of demographic data of Adamantiades-Behçet disease patients in Germany with focus on juvenile vs. adult onset and Turkish vs. German descent. 16th International Conference on Behcet’s Disease, 18‑20 September 2014, Paris, France, P. 36.
- Arnáiz-García M.E., Sarralde-Aguayo J.A., Arnáiz J., Arnáiz-García A.M. Aneurisma gigante de arteria coronaria descendente anterior/Giant aneurysm of the left anterior descending coronary artery // Archivos de cardiología de México. – 2018. – 88 (3). – Р. 230‑231.
- Ayari J., Mourali M.S., Farhati A., Mechmeche R. Left main coronary artery thrombosis revealing angio-Behçet syndrome // Egypt J Intern Med. – 2014. – 26 (2). – Р. 88‑90.
- Bang D., Lee J.H., Lee E.S. et al. Epidemiologic and Clinical Survey of Behcet’s Disease in Korea: the First Multicenter Study // J Korean Med Sci. – 2001. – 16. – Р. 615‑618.
- Bang D., Oh S., Lee K.-H. et al. Influence of sex on patients with Behçet’s disease in Korea // J Korean Med Sci. – 2003. – 18 (2). – Р. 231‑235.
Повний список літератури знаходиться в редакції
Тематичний номер «Кардіологія, Ревматологія, Кардіохірургія» № 3 (76) 2021 р.