30 жовтня, 2021
Можливості лікування місцево-поширеного та метастатичного раку передміхурової залози та сечового міхура
 29 червня відбувся вебінар «Мультидисциплінарне лікування місцево-поширених та метастатичних форм раку простати та сечового міхура в українських реаліях в 2021». Фахівці обговорили стан проблеми в Україні, діагностику та вибір тактики лікування пацієнтів із поширеним раком сечового міхура (РСМ), можливості системної терапії поширених та метастатичних форм РСМ та участі таких пацієнтів у клінічних дослідженнях, а також розглянули клінічні випадки.
29 червня відбувся вебінар «Мультидисциплінарне лікування місцево-поширених та метастатичних форм раку простати та сечового міхура в українських реаліях в 2021». Фахівці обговорили стан проблеми в Україні, діагностику та вибір тактики лікування пацієнтів із поширеним раком сечового міхура (РСМ), можливості системної терапії поширених та метастатичних форм РСМ та участі таких пацієнтів у клінічних дослідженнях, а також розглянули клінічні випадки.
Про системну терапію поширеного та метастатичного РСМ розповіла завідувачка відділення хіміотерапії № 1 Київського міського клінічного онкологічного центру, доцент кафедри онкології Національного університету охорони здоров’я України імені П.Л. Шупика, кандидат медичних наук Ольга Володимирівна Пономарьова.
– Класичною схемою лікування пацієнтів з РСМ сьогодні залишається цисплатиновмісна хіміотерапія (ХТ). ХТ на основі цисплатину є стандартом лікування як у неоад’ювантному, так і в ад’ювантному режимах. Проте через її високу токсичність не всі пацієнти отримують клінічну перевагу від такого підходу. Високу ефективність у лікуванні пацієнтів з місцево-поширеним та метастатичним РСМ, яким протипоказана платиновмісна ХТ, продемонстрували інгібітори контрольних точок – атезолізумаб і пембролізумаб (Кітруда®).
Пембролізумаб (Кітруда®) є першим інгібітором білка програмованої клітинної смерті 1 (PD‑1), який у рандомізованих клінічних дослідженнях забезпечував вищу загальну виживаність (ЗВ) порівняно з ХТ у пацієнтів із поширеною урогенітальною карциномою після неефективного лікування препаратами платини. Так, на підставі даних рандомізованого клінічного дослідження III фази KEYNOTE‑045 пембролізумаб було схвалено Управлінням з контролю якості харчових продуктів і лікарських препаратів США, Європейським агентством з лікарських засобів та Міністерством охорони здоров’я, праці й добробуту Японії для лікування дорослих пацієнтів з місцево-поширеною та метастатичною резистентною або рефрактерною до препаратів платини урогенітальною карциномою незалежно від експресії ліганду PD‑1 (PD‑L1). Крім цього, на підставі даних відкритого клінічного дослідження II фази KEYNOTE‑052 пембролізумаб було схвалено для використання у 1-й лінії терапії пацієнтами з місцево-поширеною та метастатичною урогенітальною карциномою, яким протипоказане призначення платиновмісної ХТ. Загалом у дослідженні взяло участь 370 пацієнтів. Пембролізумаб застосовували у дозі 200 мг через кожні 3 тижні впродовж 24 місяців. Частота об’єктивної відповіді (ЧОВ), отримана в цьому дослідженні, склала 24% (95% довірчий інтервал – ДІ – 20-29) при медіані спостереження 5 місяців (A.V. Balar et al., 2017) та 28,6% (95% ДІ 24,1-33,5) при медіані спостереження 24 місяці (J. Vuky et al., 2020).
На цьогорічному конгресі Американського товариства клінічної онкології (ASCO) Peter O’Donnell та співавт. представили оновлені результати дослідження KEYNOTE‑052, отримані після 5 років спостереження. Повністю завершили 24‑місячний курс лікування 43 пацієнти (11,6%), а 326 (88,1%) учасників були змушені припинити терапію з тих чи інших причин. Зокрема, у 59,5% пацієнтів такою причиною слугувало прогресування захворювання, а у 16,8% – розвиток побічних проявів. ЧОВ склала 28,9% (95% ДІ 24,3-33,8), у 9,5% випадків вдалося досягнути повної відповіді на лікування та ще у 19,5% – часткової. При медіані спостереження 56,3 місяця (51,2-65,3) медіана ЗВ у загальній популяції сягала 11,3 місяця (95% ДІ 9,7-13,1; рис. 1А). При цьому кращі результати отримано у пацієнтів із високим рівнем експресії PD-L1 (рис. 1Б).
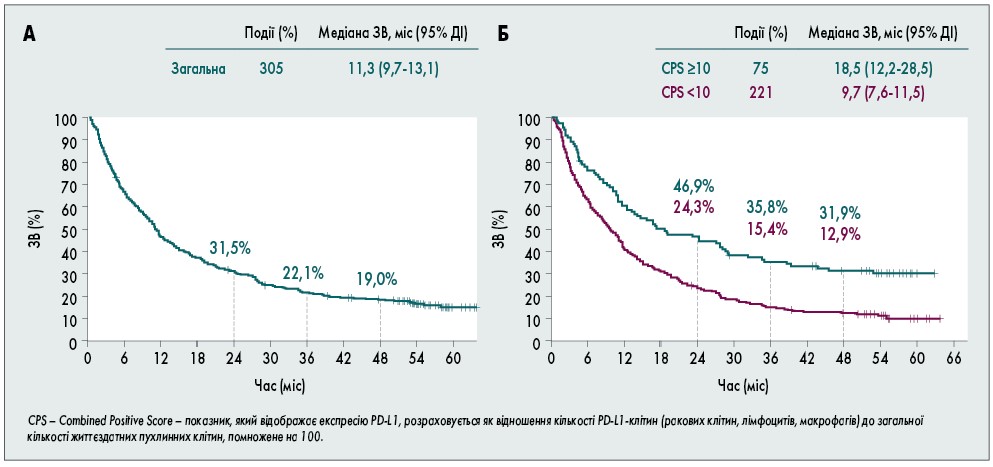 Рис. 1. Розрахунок ЗВ за методом Каплана – Маєра у загальній популяції хворих (А) та у групах хворих із різним PD-L1 статусом (Б)
Рис. 1. Розрахунок ЗВ за методом Каплана – Маєра у загальній популяції хворих (А) та у групах хворих із різним PD-L1 статусом (Б)
ЧОВ склала 28,9% у загальній популяції та була більш ніж удвічі вищою у пацієнтів із високим рівнем експресії PD-L1 порівняно з пацієнтами із негативним PD-L1 статусом (47,3 проти 20,7%).
При оцінюванні рентгенологічних даних зменшення розміру пухлини виявлено у 58,7% пацієнтів, з них у 41,1% вогнище зменшилося більш ніж на 30%, а у 27,2% – більш ніж на 60%. Варто зауважити, що кращі показники зафіксовано у пацієнтів з позитивним PD-L1 статусом (рис. 2).

Рис. 2. Найкраща зміна розміру пухлини від початкового рівня у таргетних вогнищах залежно від PD-L1 статусу
Медіана тривалості відповіді становила 33,4 місяця у загальній популяції, 21,2 місяця – у пацієнтів із негативним PD-L1 статусом, а в осіб із високим рівнем експресії PD‑L1 медіана тривалості відповіді досягнута не була.
У більшості учасників дослідження побічні явища, пов’язані з застосуванням пембролізумабу, були нетяжкими. До них належали свербіж (18,4%), підвищена втомлюваність (18,1%), висип (12,2%), зниження апетиту (10,8%), гіпотиреоз (10,0%), діарея (9,2%) та нудота (8,6%). Побічні явища ≥3 ступеня тяжкості спостерігали у 21,1% хворих, які отримували пембролізумаб (P.H. O’Donnell, 2021).
Таким чином, монотерапія пембролізумабом у 1-й лінії продовжує демонструвати стійку протипухлинну активність через 5 років з моменту включення останнього пацієнта у дослідження з ЧОВ 28,9%, медіаною тривалості відповіді 33,4 місяця та медіаною ЗВ 11,3 місяця. Пацієнти з високим рівнем експресії PD-L1 мають вищу та тривалішу відповідь на лікування. Профіль безпеки пембролізумабу у дослідженні KEYNOTE‑052 не відрізнявся від такого у попередніх дослідженнях препарату. Отримані дані свідчать на користь застосування пембролізумабу як препарату 1-ї лінії у пацієнтів із місцево-поширеною та метастатичною урогенітальною карциномою, яким протипоказане призначення платиновмісної ХТ.
Завдяки появі нових безпечніших та ефективніших лікарських засобів і можливості залучення пацієнтів до клінічних досліджень лікування РСМ в Україні з кожним роком стає успішнішим та доступнішим.
Підготувала Ольга Нестеровська
Тематичний номер «Онкологія, Гематологія, Хіміотерапія» № 4 (71) 2021 р.



