Серцево-легенева реанімація у дітей
Серцево-легенева реанімація (СЛР) – комплекс лікувальних заходів, спрямованих на оживлення, тобто на відновлення життєво важливих функцій у пацієнтів, що перебувають у стані клінічної смерті.
Клінічна смерть – стан, за якого при зупинці кровообігу та дихання в головному мозку людини ще не виникли незворотні зміни, і комплекс серцево-легеневої та церебральної реанімації, спрямований на відновлення або тимчасове заміщення втраченої чи істотно порушеної функції серця та дихання, може повернути хворого до життя без клінічно значущого неврологічного дефекту.
Біологічна смерть – стан незворотних змін в організмі людини, насамперед у центральній нервовій системі (ЦНС), коли повернення до життя неможливе.
Соціальна смерть – стан, за якого відсутня функція кори головного мозку й людина не може функціонувати як частина суспільства (соціуму).
Критичний стан (термінальний стан) – крайній ступінь будь-якої патології, що потребує підтримки чи заміщення життєво важливих функцій. Іншими словами, кінцевий період згасання життєдіяльності організму. Фінальними етапами критичного стану є преагонія і агонія.
Преагонія характеризується загальмованістю, падінням систолічного артеріального тиску до 50-60 мм рт. ст., тахікардією і зменшенням наповнення пульсу, задишкою, зміною кольору шкіри (блідість, ціаноз, «мармуровий» малюнок). Триває від декількох хвилин і годин до доби. Прогресують розлади дихання та гемодинаміки і врешті-решт розвивається агонія.
Агонія – стан, за якого свідомість і очні симптоми відсутні. Тони серця глухі, артеріальний тиск не визначається, пульс на периферичних судинах відсутній, а на сонних артеріях – слабого наповнення. Дихання нечасте, судомне або глибоке. Тривалість агонії – від декількох хвилин до декількох годин. Нерідко спостерігається короткочасна активізація серцево-судинної та дихальної систем, іноді повертається свідомість, але виснажені органи швидко втрачають здатність функціонувати, і відбувається зупинка дихання та кровообігу, тобто настає клінічна смерть.
Причини зупинки серцевої діяльності та дихання у дітей
• Поза лікувальними установами:
– синдром раптової смерті немовлят;
– травми;
– кровотечі;
– утоплення;
– порушення прохідності верхніх дихальних шляхів;
– отруєння.
• У лікувальних установах:
– важка асфіксія при народженні;
– інфекційні й інші захворювання дихальних шляхів;
– вроджена патологія;
– сепсис;
– ексикози;
– рефлекторна зупинка серця при проведенні діагностичних і лікувальних маніпуляцій у певної категорії дітей (санація ротоглотки, зондування шлунка, ендотрахеальна інтубація, ввідний інгаляційний наркоз тощо).
У дітей зупинка серця – це фінал поступового згасання фізіологічних функцій організму, ініційованого, як правило, дихальною недостатністю. Первинна зупинка серця зустрічається дуже рідко, шлуночкові фібриляція та тахікардія є її причиною менше ніж у 15% випадків. Клінічна смерть по суті є періодом з моменту зупинки дихання та кровообігу до незворотних змін найбільш чутливих до гіпоксії клітин ЦНС. За звичайних умов навколишнього середовища запас часу, необхідного для оживлення дитини у разі відсутності дихання та кровообігу, становить до 3-5 хв (у новонароджених і дітей раннього віку – до 5-7 хв), а за низької температури навколишнього середовища термін може бути трохи подовжений, але незначно.
Діагностичні критерії клінічної смерті
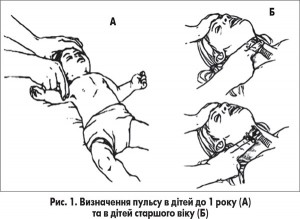 1. Відсутність кровообігу, що визначається відсутністю пульсу на магістральних судинах (сонних, стегнових, плечових артеріях). У дітей до 1 року пульс краще оцінювати на плечовій артерії і рідше – на стегновій, оскільки в них коротка й широка шия, через що іноді складно швидко знайти сонну артерію (рис. 1).
1. Відсутність кровообігу, що визначається відсутністю пульсу на магістральних судинах (сонних, стегнових, плечових артеріях). У дітей до 1 року пульс краще оцінювати на плечовій артерії і рідше – на стегновій, оскільки в них коротка й широка шия, через що іноді складно швидко знайти сонну артерію (рис. 1).
Відсутність пульсу на периферичних артеріях (наприклад, на променевих) не є ознакою клінічної смерті, оскільки пульсація судин може не визначатися при вираженій гіпотензії та/або спазмі периферичних судин. Крім того, реаніматор може сприйняти пульсацію дрібних артерій власних пальців за пульсацію периферичної артерії хворого.
Відсутність серцевих тонів при аускультації (фонендоскопом чи безпосередньо вухом) також свідчить про зупинку серця.
2. Відсутність спонтанного зовнішнього дихання, що визначається за відсутністю дихальної екскурсії грудної клітки. Як неефективні можна трактувати агональні подихи, поодинокі конвульсивні рухи з участю допоміжної мускулатури. За умови первинної зупинки кровообігу спонтанне ритмічне дихання зупиняється через 15-30 с унаслідок виснаження дихального центру, але можливі термінальні види дихання – Чейна-Стокса, Біота, гаспінг-дихання.
3. Розширення зіниць без реакції на світло. Паралітичний мідріаз фіксується вже через 60-90 с після зупинки серцевої діяльності.
4. Відсутність свідомості, арефлексія (на оклик, больове подразнення тощо). Дитина може втрачати свідомість вже через 10-20 с після зупинки серця внаслідок виснаження в головному мозку енергетичних субстратів, насамперед глюкози.
5. М’язова атонія.
6. Виражені зміни кольору шкіри та слизових (ціаноз за первинної зупинки дихання чи мертвенна блідість за первинної зупинки кровообігу).
7. Асистолія, фібриляція шлуночків, пульсвідсутня шлуночкова тахікардія, електромеханічна дисоціація та брадиаритмія з неефективною механічною діяльністю серця (діагностується за можливості зробити електрокардіографію – ЕКГ), зниження електричної активності головного мозку (якщо є можливість зробити електроенцефалографію).
Основні діагностичні критерії біологічної смерті: ранні ознаки – симптом «крижинки, яка тане» (висихання та помутніння зіниць), симптом «котячого ока» (після натискання на очне яблуко зіниця приймає і зберігає веретеноподібну горизонтальну форму), трупні плями та трупне задубіння.
Невідкладна допомога при зупинці дихання та кровообігу
Оживлення дитини (ресусцитацію, серцево-легеневу реанімацію) необхідно починати негайно після констатації клінічної смерті, швидко й енергійно в певній послідовності, з фіксацією часу настання клінічної смерті й моменту початку реанімаційних заходів, поданням сигналу тривоги та залученням допоміжного персоналу й викликом реанімаційної бригади, з’ясуванням, за можливістю, часового відрізку (у хвилинах) тривалості зупинки дихання та кровообігу. Якщо точно відомо, що цей час перевищує 10 хв, або в дитини є ранні ознаки біологічної смерті (симптоми «крижинки, яка тане», «котячого ока»), то необхідність проведення СЛР сумнівна.
Серцево-легенева реанімація може бути базова, коли комплекс оживлення дитини включає неінвазивну штучну вентиляцію легень простими методами («рот у рот», «рот у рот і ніс») та компресію грудної клітки й застосовується в будь-яких умовах, і розширена, яка проводиться переважно медичними працівниками із застосуванням інвазивних методик для відновлення ефективного дихання і кровообігу.
Основні положення первинної СЛР сформульовані P. Safar (1984) у вигляді «Правил АВС» з відповідною абревіатурою заголовних англійських букв: крок А (Airway open – відкрий дорогу повітрю) – відновлення прохідності дихальних шляхів; крок В (Breath for victim – дихання для жертви) – відновлення дихання, штучна вентиляція легень (ШВЛ); крок С (Circulation his blood – циркуляція його крові) – відновлення кровообігу, закритий масаж серця. В.А. Міхельсон та співавт. (2001) доповнили ці правила ще трьома буквами: D (Drag) – введення ліків; E (ECG) – електрокардіографічний контроль; F (Fibrillation) – дефібриляція як метод лікування порушень ритму.
А. Відновлення прохідності дихальних шляхів
 1. Покласти дитину на спину на тверду поверхню (стіл, підлога, асфальт).
1. Покласти дитину на спину на тверду поверхню (стіл, підлога, асфальт).
2. Механічно очистити ротоглотку від слизу, блювотних мас, згустків крові, сторонніх тіл тощо за допомогою електровідсмоктувача, груші або пальця (обгорнутого хустиною чи бинтом).
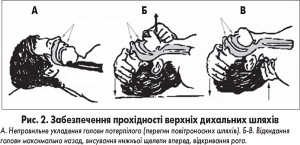
3. За відсутності травми в шийному відділі хребта у випадку обтурації гіпофарингеальної області коренем язика внаслідок гіпотонії м’язів для відновлення прохідності дихальних шляхів виконати потрійний прийом Сафара: запрокинути голову (перерозгинання голови в шийному відділі хребта), вивести вперед нижню щелепу та відкрити рот (рис. 2, 3).
У результаті цих дій натягуються тканини між нижньою щелепою і гортанню, корінь язика відходить від задньої стінки глотки.
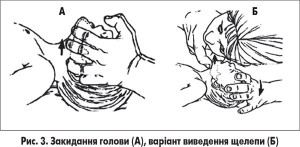 За підозри на перелом чи вивих у шийному відділі хребта розгинання в атланто-окципітальному суглобі неприпустиме. Травму шийного відділу хребта можна запідозрити ситуаційно при катастрофах, пірнанні, падінні з висоти. У цих випадках лише виводять уперед нижню щелепу, фіксують голову та шийний відділ хребта.
За підозри на перелом чи вивих у шийному відділі хребта розгинання в атланто-окципітальному суглобі неприпустиме. Травму шийного відділу хребта можна запідозрити ситуаційно при катастрофах, пірнанні, падінні з висоти. У цих випадках лише виводять уперед нижню щелепу, фіксують голову та шийний відділ хребта.
4. Після відновлення прохідності дихальних шляхів необхідно оцінити наявність самостійного дихання (візуально, аускультативно, тактильно). Часто відновлення прохідності дихальних шляхів і її підтримання буває достатньо для того, щоб надалі дихання пацієнта було досить ефективним. Якщо самостійне дихання після проведених заходів відсутнє (оцінка проводиться швидко, за 3-5 с), то необхідно розпочинати вентиляційну підтримку пацієнта – крок В.
В. Штучна вентиляція легень
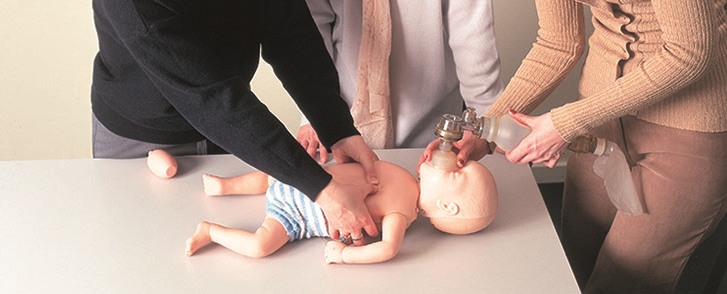
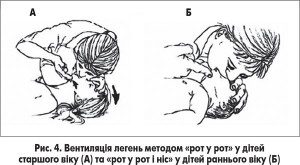 Основні методи первинної підтримки відновлення дихання – це експіраторні методи ШВЛ: «рот у рот» і «рот у рот і ніс». При диханні за методикою «рот у рот і ніс» (у дітей віком до 1 року) реаніматор після попереднього вдиху щільно обхоплює своїми губами рот і ніс дитини, при диханні за методикою «рот у рот» (у дітей старше 1 року) обхоплює своїми губами рот дитини, її ніс затискає пальцями руки та вдуває повітря в дихальні шляхи (рис. 4). Достатній об’єм кожного активного вдування – це об’єм, який забезпечує візуальне підняття грудної клітки дитини на вдиху, у середньому він становить 6-7 мл/кг. Видих (опускання грудної клітки) відбувається пасивно.
Основні методи первинної підтримки відновлення дихання – це експіраторні методи ШВЛ: «рот у рот» і «рот у рот і ніс». При диханні за методикою «рот у рот і ніс» (у дітей віком до 1 року) реаніматор після попереднього вдиху щільно обхоплює своїми губами рот і ніс дитини, при диханні за методикою «рот у рот» (у дітей старше 1 року) обхоплює своїми губами рот дитини, її ніс затискає пальцями руки та вдуває повітря в дихальні шляхи (рис. 4). Достатній об’єм кожного активного вдування – це об’єм, який забезпечує візуальне підняття грудної клітки дитини на вдиху, у середньому він становить 6-7 мл/кг. Видих (опускання грудної клітки) відбувається пасивно.
Останнім часом фірма Аmbu International випускає простий пристрій для проведення ШВЛ, що називається «ключ життя» і являє собою вкладений у брелок від ключів поліетиленовий листок з односпрямованим клапаном у центрі, через який здійснюється вдування повітря.
 Бокові краї листочка чіпляються за вушні раковини хворого за допомогою тонких резинок. Неправильно застосувати «ключ життя» майже неможливо, тому що на ньому все намальовано – губи, зуби, вуха. Цей пристрій одноразовий і позбавляє необхідності безпосереднього контакту з пацієнтом.
Бокові краї листочка чіпляються за вушні раковини хворого за допомогою тонких резинок. Неправильно застосувати «ключ життя» майже неможливо, тому що на ньому все намальовано – губи, зуби, вуха. Цей пристрій одноразовий і позбавляє необхідності безпосереднього контакту з пацієнтом.
Показаннями до ШВЛ за методикою «рот у ніс» можуть бути такі стани, коли в пацієнта судомно затиснуті щелепи, є рани губ, язика, нижньої щелепи або утруднення в забезпеченні проведення ШВЛ за методикою «рот у рот» (рис. 5).
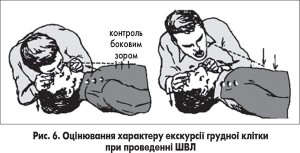 Після 1-2 пробних вдихів реаніматор оцінює характер екскурсії грудної клітки (рис. 6).
Після 1-2 пробних вдихів реаніматор оцінює характер екскурсії грудної клітки (рис. 6).
Якщо вона відсутня, необхідно повторно виконати всі заходи з відновлення прохідності дихальних шляхів. У разі неефективності цих дій можна запідозрити обтурацію дихальних шляхів стороннім тілом.
Очищення всліпу пальцем верхніх дихальних шляхів у дітей не рекомендується, тому що при грубих маніпуляціях можна проштовхнути стороннє тіло глибше. Якщо його видно, то краще для видалення використати затискач Келлі або пінцет Меджіла.
Дітям до 1 року натискати на живіт з метою підвищення внутрішньолегеневого тиску й видалення стороннього тіла не слід, оскільки існує реальна загроза травматичного ушкодження органів черевної порожнини, особливо печінки.
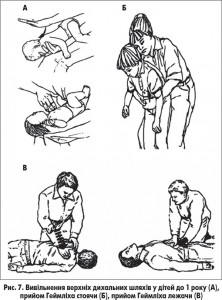 У цьому віці краще надавати допомогу, утримуючи дитину на руці лицем донизу в позі «вершника» з головою, опущеною нижче тулуба, а іншою рукою завдати 4 коротких удари проксимальною частиною долоні по спині в міжлопатковій ділянці.
У цьому віці краще надавати допомогу, утримуючи дитину на руці лицем донизу в позі «вершника» з головою, опущеною нижче тулуба, а іншою рукою завдати 4 коротких удари проксимальною частиною долоні по спині в міжлопатковій ділянці.
Далі укласти дитину на спину таким чином, щоб голова була нижче тулуба, й виконати чотири натискання на грудну клітку.
Методика видалення стороннього тіла залежить від віку дитини (рис. 7).
Для видалення стороннього тіла з дихальних шляхів дітей старшого віку або дорослих, якщо 5 ударів по спині не дали результату, рекомендовано застосовувати прийом Геймліха – серію (до 5 разів) субдіафрагмальних поштовхоподібних натискань у краніальному напрямі через епігастрій та нижній відділ грудної клітки, щільно охопивши тулуб пацієнта обома руками (чи пальцями, якщо це маленька дитина).
Різке натискання на епігастральну область спричиняє як мінімум удвічі більше підвищення тиску в трахеобронхіальному дереві, ніж постукування по спині.
 Для ефективної вентиляції легень можна використовувати вікові повітроводи, S-подібну трубку (трубку Сафара) (рис. 8).
Для ефективної вентиляції легень можна використовувати вікові повітроводи, S-подібну трубку (трубку Сафара) (рис. 8).
Широко застосовуються ротоносові маски з підключенням їх до ручних дихальних апаратів (мішок Амбу).
Короткочасна примусова ШВЛ забезпечується через ротоносову чи ларингеальну маску, а в дорослих ще й повітровід-обтуратор, тривала ШВЛ – через інтубаційну чи трахеостомічну трубку.
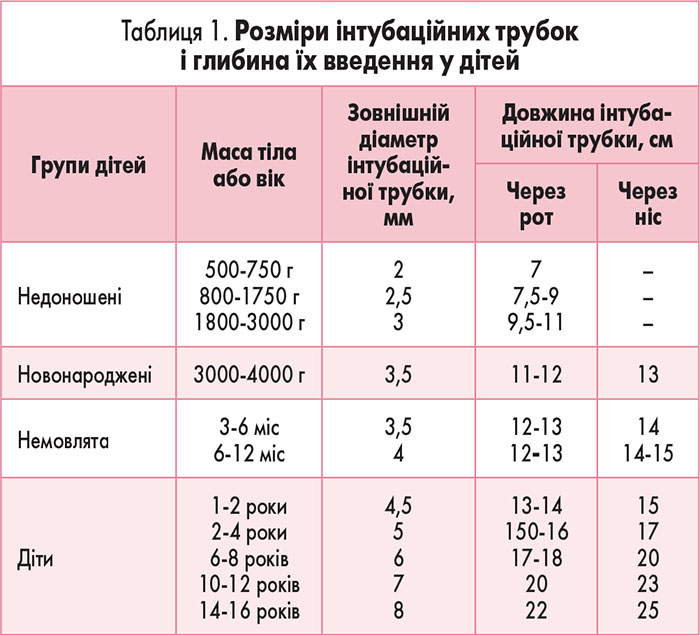
Інтубація трахеї показана при первинній реанімації за необхідності ШВЛ більше 5 хв або санації трахеобронхіального дерева при аспірації грудного молока та шлункового вмісту. Інтубація трахеї проводиться при прямій ларингоскопії методикою оротрахеальної і значно рідше – рінотрахеальної інтубації з використанням відповідних вікові трубок (табл. 1).
Приблизний розрахунок величини вікового діаметра інтубаційної трубки можна визначити за емпіричною формулою: діаметр (мм) = вік (роки) / 4 + 4,5. Інший метод – внутрішній діаметр трубки повинен мати приблизно такий розмір, як кінчик мізинця хворого.
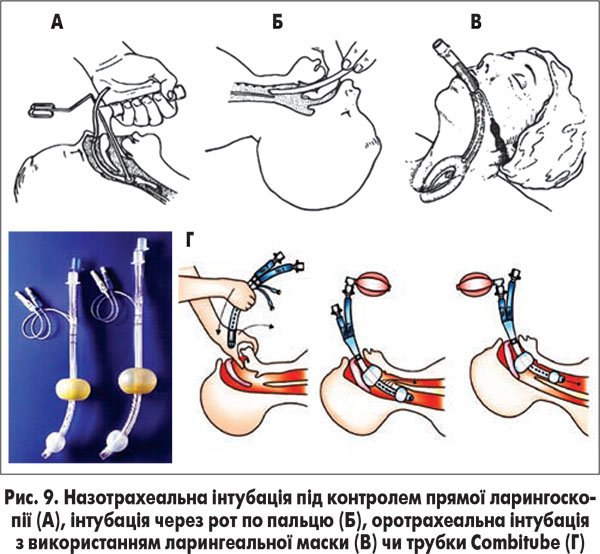
В окремих ситуаціях інтубація може бути виконана всліпу по пальцю, із застосуванням трубки Combitube або за допомогою ларингеальної маски (рис. 9).
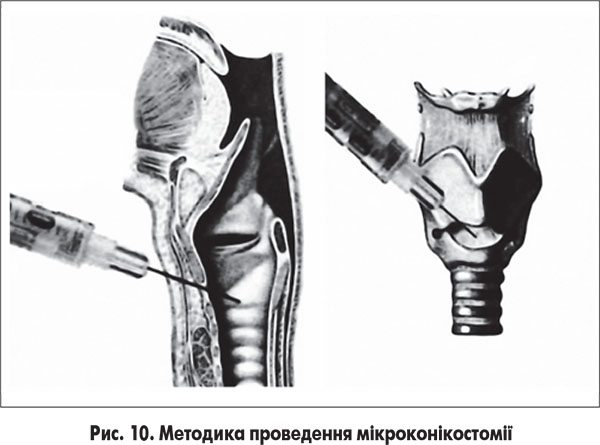
За відсутності ефекту й неможливості виконати пряму ларингоскопію можливим є проведення мікроконікостомії – перфорації крикотиреоїдної мембрани товстою голкою (рис. 10).
Крикотиреоїдна мембрана розташована між нижнім краєм щитовидного і верхнім краєм перснеподібного хряща гортані. Між нею і шкірою є незначний прошарок м’язових волокон і відсутні великі судини й нерви. Якщо орієнтуватися на верхню вирізку щитовидного хряща і спуститися за середньою лінією, то визначається невелика впадина між передньою дугою перснеподібного хряща і нижнім краєм щитовидного, це і є крикотиреоїдна мембрана. Голосові зв’язки знаходяться дещо краніальніше мембрани, тому при проведенні цієї маніпуляції вони не ушкоджуються. Для виконання мікроконікостомії необхідно декілька секунд. Техніка її проведення така: голова максимально запрокинута назад (бажано підкласти під плечі валик); великим і середнім пальцями фіксується гортань за бокові поверхні щитовидного хряща; вказівним пальцем визначається мембрана. Голка, попередньо зігнута під тупим кутом, вводиться в мембрану точно за середньою лінією до відчуття «провалу», яке вказує на те, що кінець голки потрапив у порожнину гортані.
У критичній ситуації за повної обструкції в області гортані можливе проведення розтину крикотиреоїдної мембрани – конікотомії. Як зафіксувати й визначити мембрану, зазначено вище. Над мембраною робиться поперечний розріз шкіри довжиною близько 1,5 см.
У розріз шкіри вводиться вказівний палець так, щоб верхівка нігтьової фаланги впиралася в мембрану. По нігтю, торкаючись його плоскістю ножа, перфорується мембрана і через отвір вводиться пустотіла трубка. Маніпуляція займає від 15 до 30 с, що вигідно відрізняє конікотомію від трахеостомії, для виконання якої необхідно декілька хвилин. Зараз випускаються спеціальні конікотомічні набори, які складаються з бритви-жала для розсікання шкіри, троакара для введення в гортань спеціальної канюлі і самої канюлі, надітої на троакар.
Апарати ШВЛ розрізняються за складністю конструкції. На початковому етапі частіше використовуються прості дихальні мішки типу «Амбу», Penlon або переривники постійного повітряного потоку (наприклад, за методом Ейра: через трійник – пальцем), а в стаціонарних умовах – складні апарати для проведення ШВЛ.
Якщо є можливість, то ШВЛ на етапі реанімації потрібно починати вентиляцією чистим киснем з бажаним зволоженням та підігрівом киснево-повітряної суміші.
Відсутність пульсу на магістральних судинах при забезпеченні ефективної вентиляції легень вказує на необхідність проведення зовнішнього масажу серця.
С. Зовнішній (закритий) масаж серця (ЗМС)
Показання до ЗМС:
– зупинка серця;
– гіпосистолія (навіть якщо через тонку грудну стінку дитини вдається пальпаторно визначити верхівковий поштовх, але немає пульсації магістральних судин, то серцева діяльність також трактується як недостатня);
– частота серцевих скорочень у новонароджених менше 60 за 1 хв після 30 с ефективної ШВЛ.
Відповідно до методики проведення ЗМС хворий лежить на спині на жорсткій прямій поверхні. При цьому дітям віком до 1 року під грудну клітку підставляють долоню, що дає можливість розвести плечовий пояс і підтримати голову дитини в дещо запрокинутому стані.
Можливий і інший варіант – коли тулуб дитини лежить на передпліччі, а голова – на долоні.
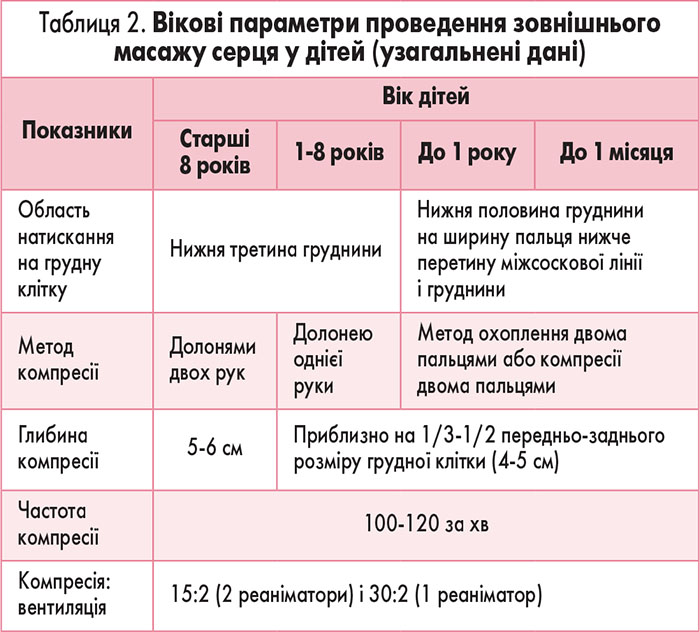
Реаніматор перебуває справа або зліва від пацієнта. З урахуванням віку дитини він обирає положення рук і здійснює ритмічне натискання на грудну клітку з частотою, відповідною віковому цензу, зіставляючи силу натискання з пружністю грудної клітки (табл. 2).
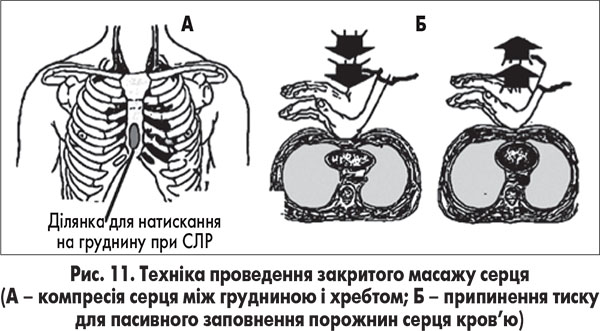
ЗМС досягається компресією (стисканням) грудної клітки в поперечному напрямку від груднини до хребта (рис. 11).
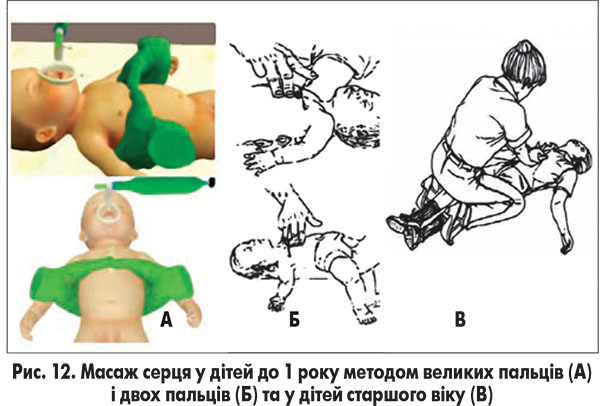
У дітей до 1 року ЗМС проводиться методом великих пальців: на груднину натискають подушечками двох великих пальців, водночас решта пальців обох рук підтримують спину дитини (А), або двох пальців: на груднину натискають кінчиками двох пальців однієї руки – другого і третього або третього й четвертого, під час цього друга рука підтримує спину дитини (Б) (рис. 12).
Область натискання на груднину у новонароджених та немовлят на ширину пальця нижче від місця перетину міжсоскової лінії і груднини.
ЗМС у дітей віком 1-8 років виконується основою долоні, що розташовується на груднині на відстані одного пальця від її дистального кінця.
ЗМС у дітей старше 8 років виконується основою долоні однієї руки і покладеною зверху долонею другої руки у вигляді замка при компресії на випрямлених руках, причому кут між руками й тілом має становити 90°, щоб максимально ефективно задіяти у масажі плечовий пояс і масу тіла реаніматора. Область натискання розташована на кордоні середньої і нижньої третини груднини.
Компресія грудної клітки повинна бути достатньою для виникнення пульсової хвилі на магістральних судинах, але й не призводити до ускладнень ЗМС (переломів груднини та ребер, пневмотораксу, розриву печінки, аспірації шлункового вмісту). У разі перелому кісткових елементів грудної клітки силу компресій необхідно зменшити.
Якщо ШВЛ проводиться одночасно із ЗМС, рекомендується почергово виконувати вдування й компресії. У дітей рекомендоване їх співвідношення 2:15 (два вдихи до п’ятнадцяти компресій) при проведенні заходів двома реаніматорами та 2:30 (два вдихи до тридцяти компресій грудної клітки) одним реаніматором (табл. 2).
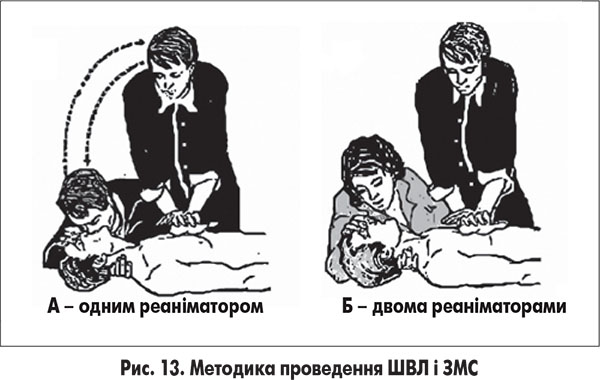
У той момент, коли здійснюється вдих у легені, компресія грудної клітки не відбувається, і навпаки, тобто процедури ШВЛ і ЗМС чергуються та змінюють одна одну (рис. 13).
На сучасному етапі можливим є застосування автоматичних апаратів для зовнішнього масажу серця (рис. 14), особливо під час транспортування пацієнта в лікарні чи поза нею.
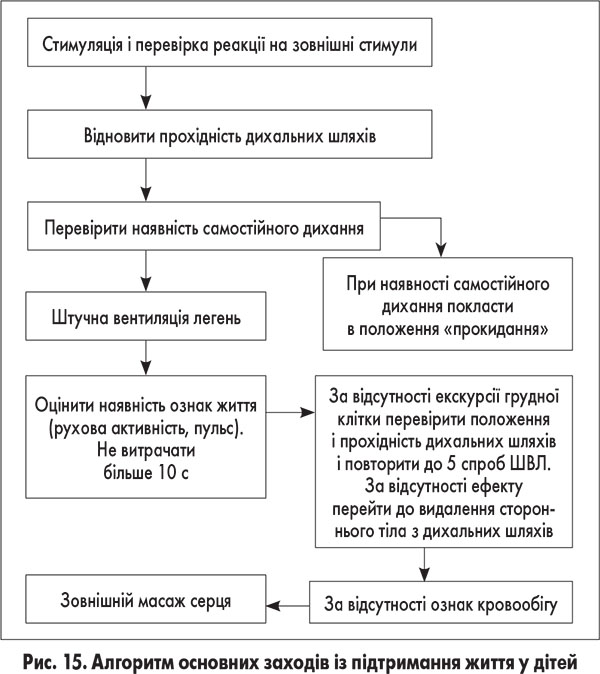
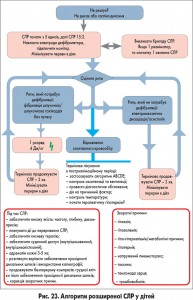
Схему-алгоритм основних заходів з підтримання життя в дітей подано на рисунку 15.
Прямий (відкритий) масаж серця застосовується, як правило, коли зупинка серця відбулася під час торакотомії або лапаротомії, і компресію серця виконують між двома долонями чи між першим та іншими пальцями реаніматора.
Основні критерії правильності виконання серцево-легеневої реанімації:
– при проведенні ЗМС у момент натискання на груднину фіксується пульс на магістральних судинах;
– при проведенні ШВЛ під час вдування повітря спостерігається підняття (екскурсія) грудної клітки, після закінчення вдиху грудна клітка внаслідок еластичних характеристик спадається і одночасно реєструється потік повітря з ротової та/або носової порожнини. Стан дитини повторно оцінюється через 1 хв після початку реанімації і далі кожні 2-3 хв.
Критерії ефективності ШВЛ та ЗМС на етапі елементарної підтримки життя:
– звуження зіниць та поява реакції на світло;
– поява тонусу повік (заплющується очна щілина);
– виникають спонтанні рухи гортані, самостійні вдихи;
– зменшення ступеня ціанозу (чи блідості) шкіри та слизових оболонок;
– відновлення кровообігу;
– сатурація на рівні 94-98%.
D. Медикаментозна терапія при СЛР у дітей
Якщо серцебиття не відновлюється, продовжуючи ШВЛ і ЗМС, необхідно забезпечити доступ до венозного русла для введення медикаментозних засобів.
Основні шляхи введення ліків при здійсненні СЛР
А. Внутрішньовенний (в/в). Можливе введення як у периферичну вену, так і в центральну (пріоритетний метод). Якщо препарати вводяться в периферичну вену, то об’єм ізотонічного розчину, в якому розводять медикаменти, збільшується, і після ін’єкції слід припідняти руку пацієнта для кращого надходження засобу в центральний кровообіг. Серед центральних вен при проведенні СЛР перевагу віддають катетеризації внутрішньої і зовнішньої яремних, стегнових вен, що дозволяє не переривати реанімаційних заходів.
Рідше застосовується при СЛР катетеризація підключичної вени через необхідність переривати реанімаційні дії.
Б. Внутрішньокістковий (в/к) шлях введення медикаментозних засобів рекомендується як тимчасовий метод надання допомоги дітям, коли інші судинні доступи невідкладно забезпечити не вдається. Усі медикаменти, які використовуються при СЛР, а також усі розчини, у тому числі цільна кров, можуть бути введені внутрішньокістково. За методикою стандартну голку 16-18 G або спинномозкову голку № 18-20 з мандреном чи голку для пункції кісткового мозку вводять в передньо-медіальну поверхню великогомілкової кістки в проксимальну частину (на 1-2 см нижче її бугристості) чи дистальну частину, або в дистальний відділ стегнової кістки.
Голку вводять під тиском круговими рухами до відчуття провалу під кутом 90° до поверхні кістки, щоб не пошкодити епіфіз. Видаляють мандрен і підтверджують правильність перебування голки аспіраційною пробою (пунктат кісткового мозку). Вводять препарат під візуальним контролем, виключаючи його екстравазальне розповсюдження. Внутрішньокісткове введення протипоказане хворим з переломами кісток, гнійничковими захворюваннями шкіри, у разі невдалих попередніх спроб пункції кісткового каналу.
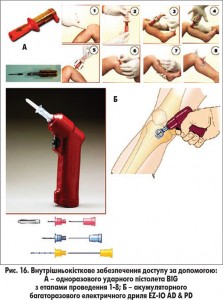 Окрім ручного введення, на сучасному етапі можливим є в/к забезпечення доступу за допомогою одноразового ударного пістолета (рис. 16А) та акумуляторного багаторазового електричного дриля (рис. 16Б).
Окрім ручного введення, на сучасному етапі можливим є в/к забезпечення доступу за допомогою одноразового ударного пістолета (рис. 16А) та акумуляторного багаторазового електричного дриля (рис. 16Б).
В. Ендотрахеальний (е/т) шлях майже втратив свою пріоритетність при проведенні СЛР. Він можливий для введення адреналіну, атропіну, лідокаїну, налоксону. Як правило, доза, яка вводиться е/т, більша від дози, що вводиться в/в (так, доза адреналіну в дітей віком до 8 років збільшується в 10 разів, а у дітей старше 8 років та дорослих – у 2-2,5 раза).
Необхідна доза препарату вводиться в фізіологічному розчині (повний об’єм рідини, введеної в трахею, не повинен перевищувати 10 мл у дорослих або 5 мл у дітей до року) і інсталюється зі шприца краще через катетер за дистальний кінець ендотрахеальної трубки або безпосередньо в ендотрахеальну трубку. Після введення препарату необхідно провести 5 штучних вдихів для його кращого розповсюдження по легенях.
Г. Внутрішньосерцевий (в/с) шлях введення ліків не рекомендується у дітей через високий ризик розвитку ускладнень (розриви коронарних судин, тампонада серця, пневмоторакс тощо).
Основні медикаментозні засоби, що використовуються при СЛР:
– адреноміметики використовуються найчастіше, особливо адреналін. Показаннями до його використання є: асистолія, прогресуюча брадикардія, неефективне серце, окремі випадки фібриляції шлуночків (переведення мілкохвильової фібриляції шлуночків у великохвильову перед дефібриляцією) або пульсвідсутня шлуночкова тахікардія. У дітей перша доза адреналіну – 0,01 мг/кг (0,1% розчин адреналіну гідрохлориду 0,01 мл/кг) при в/в та в/к введенні і 0,1 мг/кг при е/т введенні. У дорослих перша доза становить 1 мг при в/в і в/к введенні та 2-3 мг при е/т введенні. Для в/в, в/к введення препарат розводять 1:10 000 (наприклад, 1 мл офіцінального розчину розчиняють у 9 мл ізотонічного розчину), а для е/т – у 3-5 мл розчину. За необхідності повторні введення адреналіну проводять з інтервалом у 3-5 хв у дозі 0,01 мг/кг (10 мкг/кг);
– допамін (дофамін, допмін) застосовують після відновлення серцевої діяльності на тлі нестабільної гемодинаміки в дозі 5-20 мкг/кг/хв, для покращення діурезу – 1-2 мкг/кг/хв;
– М-холіноблокатор атропін показаний при прогресуючій брадиаритмії, електромеханічній дисоціації, ектопічному ритмі шлуночків, повільних ідіовентрикулярних ритмах. У дітей рекомендована доза атропіну 0,01-0,02 мг/кг (0,1% розчин атропіну сульфату 0,01-0,02 мл/кг) при в/в або в/к введенні (максимальна одноразова доза 0,5 мг, у дорослих – 1 мг при в/в введенні), але не менше 0,1 мг в дитячому віці і 0,5 мг у дорослих через небезпеку парадоксального парасимпатоміметичного ефекту. За необхідності препарат вводять кожні 5 хв у попередній дозі до сумарної дози 1 мг у дітей і 2 мг у дорослих, тому що така доза атропіну спричиняє повну блокаду блукаючого нерва. Е/т доза – 0,02 мг/кг;
– натрію гідрокарбонат показаний при тяжкому метаболічному ацидозі (гіпостази, симптом «білої плями» більше 5 сек, рН <7,25, ВЕ <-12 ммоль/л), СЛР тривалістю понад 10 хв, гіперкаліємії, передозуванні трициклічними антидепресантами або барбітуратами. Бажано вводити цей препарат під контролем кислотно-лужного стану. Вихідна доза препарату за відсутності даних про кислотно-лужний стан – 1 ммоль/кг (4,2% розчин натрію гідрокарбонату 2 мл/кг або 8,4% розчин – 1 мл/кг). Повторні введення натрію гідрокарбонату здійснюються кожні 10 хв тривалої зупинки серця в половинній дозі;
– лідокаїн застосовують при фібриляції шлуночків або пульсвідсутній шлуночковій тахікардії в дозі для в/в введення 1 мг/кг.
За необхідності можна використовувати тривалу інфузію препарату в дозі 20-50 мкг/кг/хв;
– аміодарон показаний при шлуночковій тахікардії, рефрактерній фібриляції в дозі 5 мг/кг для в/в введення з титруванням, за потреби – у дозі 5-15 мкг/кг/хв;
– препарати кальцію рекомендовані тільки при задокументованих випадках гіпокальціємії, гіпермагніємії, гіперкаліємії або передозуванні блокаторів кальцієвих каналів. Вводять 10% розчин кальцію хлориду в/в з розрахунку 0,2 мл/кг (приблизно 5,5 мг/кг іонізованого кальцію);
– глюкоза показана при задокументованих ситуаціях гіпоглікемії в/в у дозі 0,5-1 г/кг у концентрації не більше 25% протягом понад 20 хв.
Е. Електрокардіографічний контроль (за можливістю)
 Основні види (варіанти) порушення ритму серця при клінічній смерті:
Основні види (варіанти) порушення ритму серця при клінічній смерті:
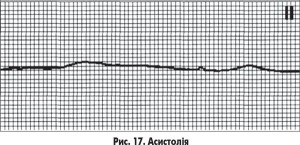
1. Асистолія, коли відсутня і електрична активність серця, і механічний викид (на ЕКГ – пряма лінія, рис. 17).
Оскільки за асистолію може бути прийнята згасаюча низькоамплітудна фібриляція, підтвердження бажане при реєстрації не менше ніж у двох відведеннях.
2. Фібриляція шлуночків і пульсвідсутня шлуночкова тахікардія, коли наявна аномальна електрична активність, що може супроводжуватися хаотичними скороченнями окремих кардіоміоцитів і відсутністю серцевого викиду (нетипові для дітей види зупинки кровообігу).
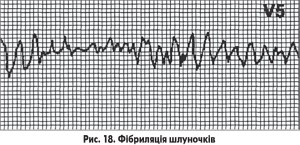 На ЕКГ при фібриляції шлуночків реєструються нерегулярні, з високою частотою (350-450 за хв) хвилі різної амплітуди, ширини і спрямованості, діастола цілком відсутня (рис. 18).
На ЕКГ при фібриляції шлуночків реєструються нерегулярні, з високою частотою (350-450 за хв) хвилі різної амплітуди, ширини і спрямованості, діастола цілком відсутня (рис. 18).
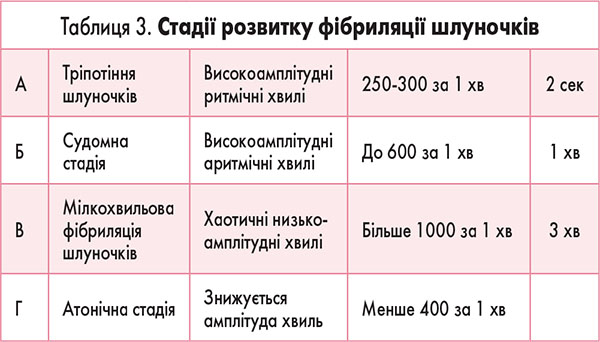
Стадії розвитку фібриляції шлуночків наведено в таблиці 3.
Через 15-30 с від початку фібриляції шлуночків хворий втрачає свідомість, через 40-50 с розвиваються типові судоми – однократне тонічне скорочення скелетних м’язів.
Розширюються зіниці, досягаючи максимальних розмірів через 1,5 хв. Шумне й часте дихання припиняється на 2-й хв клінічної смерті.
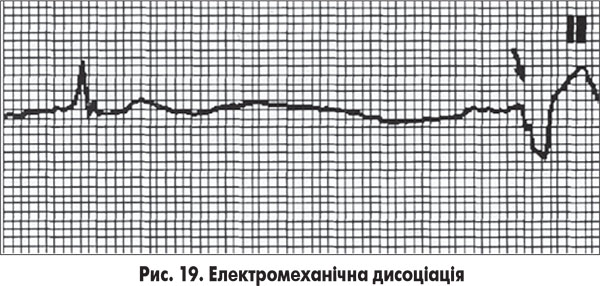
3. Електромеханічна дисоціація (неефективне серце), коли зберігається електрична активність серця і навіть, можливо, механічний викид, але в цих випадках кровообіг є недостатнім для повноцінного забезпечення киснем клітин головного мозку, що веде до розвитку термінального стану. На ЕКГ виявляють типові й нетипові шлуночкові комплекси з різним ритмом (рис. 19).
F. Дефібриляція серця (ДС)
Показання до ДС:
– фібриляція шлуночків;
– пульсвідсутня шлуночкова тахікардія.
Фібриляція шлуночків типова при утопленні в прісній воді, електротравмі, странгуляційній асфіксії, передозуванні серцевих глікозидів.
Електрична дефібриляція серця (ЕДС) – застосування електроімпульсних розрядів високої напруги – є найефективнішим методом і важливим компонентом СЛР. При ЕДС через тіло хворого по розміщених на грудній клітці електродах пропускається електричний розряд з метою одномоментної деполяризації максимальної кількості кардіоміоцитів, що дозволяє ліквідувати наявні порушення серцевого ритму та дає можливість водію серцевого ритму відновити нормальний перебіг збудження.
Якщо в пацієнта фібриляція шлуночків і швидко виснажуються енергетичні ресурси, то дефібриляцію необхідно провести якнайшвидше. Якщо час, що минув з моменту зупинки серця, невідомий, то як першочерговий захід рекомендується СЛР протягом мінімум двох хвилин.
Основні правила проведення ЕДС
1. Усі розряди краще проводити під час видиху, щоб розміри грудної клітки були мінімальними – це знижує трансторакальний опір на 15-20%.
2. Інтервал між розрядами має бути мінімальним. Кожний попередній розряд знижує трансторакальний опір на 8% і наступний розряд дає міокарду більшу енергію току.
3. Під час кожного розряду всі реаніматори, крім людини, яка безпосередньо здійснює ЕДС, відходять від хворого на короткий проміжок часу (долі секунди). Перед розрядом і після нього вживаються необхідні заходи щодо підтримки вентиляції, кровообігу.
4. Перед дефібриляцією електроди змащують спеціальною електропровідною пастою або обгортають марлею, змоченою ізотонічним розчином натрію хлориду. Розміри електродів у дорослих – 13 см у діаметрі, у дітей старшого віку – 8 см, у молодшого – 4,5 см.
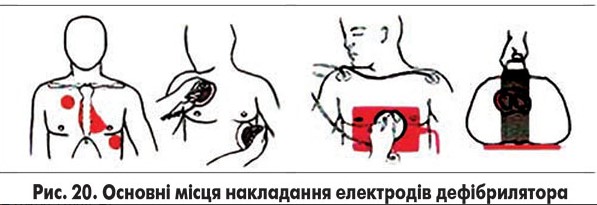
5. Залежно від конструкції електродів є два варіанти їх розміщення на грудній клітці (рис. 20): фронтальне розміщення електродів – один справа від груднини в області другого міжребер’я (+), другий за середньою аксилярною лінією на рівні верхівки серця (–), або сагітальне – один підкладають під ліву лопатку (+), а другий – на грудну клітку в області верхівки серця (–).
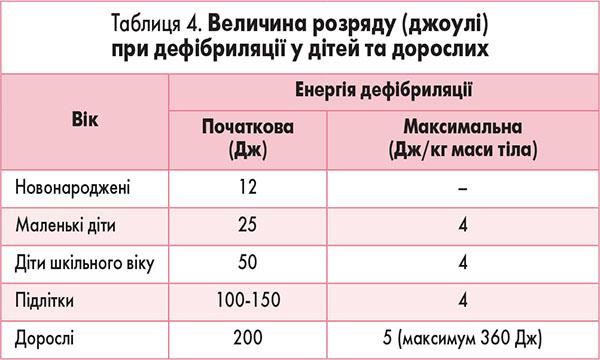
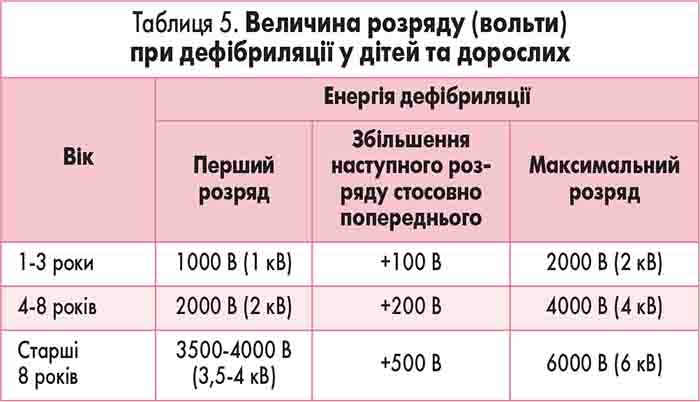
6. Рекомендовані величини електроімпульсних розрядів (ERC2000): у дорослих початкові величини приблизно 3 Дж/кг, тобто в пацієнта вагою 70 кг – приблизно 200 Дж, за повторної дефібриляції – зростання до 5 Дж/кг (максимально 360 Дж), у дітей – приблизно 4 Дж/кг (табл. 4).
В апаратах старих зразків (градація імпульсу у вольтах) рекомендовані такі величини розрядів: у дітей до року – 0,5-1 кВ; 1-3 років – 1 кВ, 3-7 років – 1,5 кВ; 7-12 років – 2-2,5 кВ; 12-16 років – 2,5-3,5 кВ; у дорослих дефібриляцію необхідно починати з 3-4 кВ, за відсутності ефекту – збільшувати кожного наступного сеансу величину розряду на 0,5 кВ – до максимальної величини 7 кВ. У таблиці 5 наведено величини розряду (вольти) при дефібриляції дітей та дорослих.
Приблизний розрахунок величини електроімпульсного розряду можна зробити за емпіричною формулою: величина розряду (В) = 500 В на рік (віком до 5 років) + 250 В на рік (віком після 5 років).
При проведенні ЕДС на відкритому серці величина розряду зменшується від загальноприйнятої у 7 разів.
Ефективність ЕДС підвищується шляхом повторного введення всього комплексу медикаментозних засобів (у тому числі поляризуючої суміші, іноді магнію сульфату, еуфіліну тощо).
Можливі причини неефективної дефібриляції:
– неправильне розміщення електродів;
– змазка на електродах відсутня або її мало (високий опір шкіри);
– електроди недостатньо щільно притиснуті до грудної клітки;
– низька енергія дефібриляції;
– недостатнє насичення міокарда киснем.
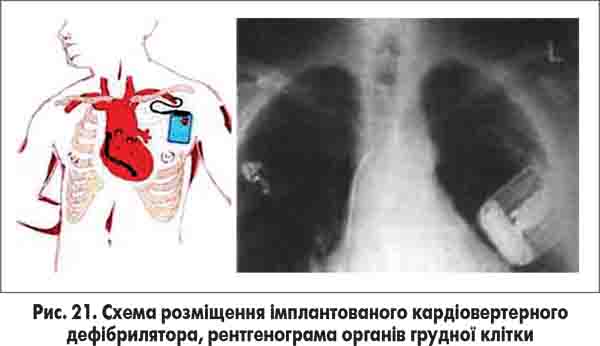
Розробка імплантованих кардіовертерних дефібриляторів, які визначають патологічні зміни серцевого ритму й переривають їх електричним шляхом, дозволила винайти нову методику лікування пацієнтів із групи ризику серйозних порушень серцевого ритму. У 1970 році М. Міровські вперше висунув ідею про імплантований пристрій, здатний визначати шлуночкову фібриляцію і у відповідь на неї проводити електричний розряд, що дефібрилює серце та нормалізує ритм. Цю ідею було реалізовано в 1980 році зі здійсненням імплантації апарату такого типу. На рисунку 21 подано варіант імплантованого кардіовертерного дефібрилятора.
Сучасні імплантовані кардіовертерні дефібрилятори останніх поколінь мають два внутрішньосерцеві дефібрилюючі електроди в одному провіднику, який проводять через v. Сephalica або v. Subclavia, як і стандартний пейсмекерний провідник, у праву половину серця. Кінчик провідника з дистальним дефібриляційним електродом (катодом) розміщують на верхівці правого шлуночка, а проксимальний електрод (анод) розташовують у місці впадіння верхньої порожнистої вени в праве передсердя. Розряд генерується між двома електродами.
В останніх моделях корпус генератора служить додатковим електродом, завдяки чому розряд охоплює область від правошлуночкового катода до корпусу генератора, що підвищує його ефективність і знижує поріг дефібриляції.
У сучасних умовах класичні підходи до надання невідкладної допомоги постійно удосконалюються.
Найважливіші зміни й доповнення в Рекомендаціях Європейської ради реанімації (ERC) в 2010 році
1. Рішення про початок СЛР слід приймати протягом не довше ніж 10 сек. Залежно від віку дитини пульс можна перевіряти на сонній артерії (діти), плечовій (немовлята) або стегновій (діти та немовлята).
2. Співвідношення натискань грудної клітки та вентиляції (compression:ventilationratio – C:V) у дітей залежить від того, скільки рятувальників надають допомогу – один або більше. Рятувальникам-немедикам, які зазвичай проходять навчання з надання допомоги у виконанні однією особою, необхідно вчитися виконувати 30 натискань грудної клітки та 2 рятувальні вдихи, тобто так само, як у рекомендаціях з надання допомоги дорослим, що дає можливість кожному, хто пройшов навчання з проведення базових реанімаційних заходів (BLS), проводити реанімацію в дітей за мінімуму додаткової інформації. Рятувальники, що мають професійний обов’язок надавання допомоги, повинні вчитися й застосовувати C:V 15:2, однак можна і 30:2, якщо рятувальник надає допомогу один, особливо якщо не вдається досягти необхідної кількості натискань.
 Вентиляція і в подальшому залишається дуже важливим елементом СЛР при зупинці кровообігу, що настала внаслідок асфіксії. Рятувальників, які не в змозі або не хочуть проводити вентиляцію «рот у рот», необхідно заохочувати виконувати СЛР тільки з натисканням грудної клітки. Співвідношення C:V без протекції дихальних шляхів чи з протекцією ларингеальною маскою або трубкою Combitube як для одного, так і для двох реаніматорів повинно бути 30:2 і проводитися з паузою на проведення ШВЛ (ризик розвитку аспірації).
Вентиляція і в подальшому залишається дуже важливим елементом СЛР при зупинці кровообігу, що настала внаслідок асфіксії. Рятувальників, які не в змозі або не хочуть проводити вентиляцію «рот у рот», необхідно заохочувати виконувати СЛР тільки з натисканням грудної клітки. Співвідношення C:V без протекції дихальних шляхів чи з протекцією ларингеальною маскою або трубкою Combitube як для одного, так і для двох реаніматорів повинно бути 30:2 і проводитися з паузою на проведення ШВЛ (ризик розвитку аспірації).
Якщо є протекція дихальних шляхів (інтубація трахеї), компресія грудної клітки проводиться з частотою 100/хв, вентиляція – з частотою 10/хв (у разі застосування мішка Амбу – 1 вдих кожні 5 с) без паузи при проведенні ШВЛ (оскільки компресія грудної клітки з одночасним роздуванням легень збільшує коронарний перфузійний тиск). За тривалої СЛР рекомендується застосування механічних пристроїв для проведення компресії грудної клітки.
3. Технічно натискання грудної клітки повинні виконуватися на відповідну глибину з якнайменшими перервами, щоб мінімізувати час без кровотоку. Необхідно натискати грудну клітку принаймні на 1/3 її передньо-заднього розміру в усіх дітей (приблизно 4 см у немовлят та 5 см у дітей). У немовлят, як і у дітей, частота натискання повинна становити принаймні 100/хв, але не більше 120/хв. Техніка їх виконання у немовлят включає натискання двома пальцями, якщо допомогу надає один рятувальник, та охоплення грудної клітки долонями й натискання двома великими пальцями, якщо рятувальників двоє або більше. У старших дітей, залежно від вибору рятувальника, можна застосовувати техніку натискання однією або двома руками.
 4. Застосування автоматичних зовнішніх дефібриляторів (AED) у дітей старше 1 року є безпечним та ефективним. Для дітей віком 1-8 років рекомендується застосовувати педіатричні електроди або спеціальне програмування, що зменшує енергію пристрою до 50-75 Дж. Якщо такий пристрій недоступний та немає можливості зменшити енергію мануально, у дітей старше 1 року можна застосувати немодифікований AED – так само, як і в дорослих. Відомо про випадки ефективного застосування AED у дітей до 1 року життя. У рідкісних випадках появи дефібриляційного ритму в дітей віком до 1 року застосування AED є обґрунтованим.
4. Застосування автоматичних зовнішніх дефібриляторів (AED) у дітей старше 1 року є безпечним та ефективним. Для дітей віком 1-8 років рекомендується застосовувати педіатричні електроди або спеціальне програмування, що зменшує енергію пристрою до 50-75 Дж. Якщо такий пристрій недоступний та немає можливості зменшити енергію мануально, у дітей старше 1 року можна застосувати немодифікований AED – так само, як і в дорослих. Відомо про випадки ефективного застосування AED у дітей до 1 року життя. У рідкісних випадках появи дефібриляційного ритму в дітей віком до 1 року застосування AED є обґрунтованим.
5. Щоб скоротити час без кровотоку, при застосуванні мануального дефібрилятора необхідно продовжувати натискання грудної клітки під час розміщення та зарядження ложок дефібрилятора або самоприклеюваних електродів (якщо дозволяє розмір грудної клітки дитини). Після зарядження дефібрилятора необхідно припинити на короткий час натискання грудної клітки й виконати дефібриляцію. Для спрощення та відповідно до стандартів BLS і спеціалізованих реанімаційних заходів у дорослих (ALS) для дефібриляції у дітей рекомендується застосовувати стратегію одиничного розряду з енергією 4 Дж/кг без подальшого її збільшення (найкраще із застосуванням двохфазного дефібрилятора, проте однофазний теж допускається).
6. У немовлят і малих дітей можна безпечно застосовувати інтубаційні трубки з манжетою. Діаметр трубки обирають, попередньо здійснивши розрахунок за відповідною формулою. Альтернативою ендотрахеальній інтубації можуть бути технічно більш прості методи із застосуванням ларингеальної маски, трубок Combitube.
 7. Кожний вдих при ШВЛ треба проводити протягом 1 с (не форсовано). Дихальний об’єм повинен становити 400-600 мл (6-7 мл/кг), частота дихання – 10/хв з метою недопущення гіпервентиляції.
7. Кожний вдих при ШВЛ треба проводити протягом 1 с (не форсовано). Дихальний об’єм повинен становити 400-600 мл (6-7 мл/кг), частота дихання – 10/хв з метою недопущення гіпервентиляції.
8. Досі не з’ясовано, чи безпечно та як важливо застосовувати натискання на перснеподібний хрящ під час інтубації трахеї. Тому, якщо цей маневр погіршує вентиляцію або загальмовує чи утруднює інтубацію, необхідно його змодифікувати або припинити виконання.
9. Моніторування концентрації видихуваного двоокису вуглецю (CO2), найкраще – за допомогою капнографу, може бути доцільним при підтвердженні правильного положення інтубаційної трубки та рекомендоване під час СЛР для оцінки й оптимізації її якості.
10. Після повернення спонтанного кровообігу необхідно регулювати концентрацію кисню в дихальній суміші, щоб обмежити ризик гіпероксемії.
 11. Запровадження системи швидкого реагування в педіатричних відділеннях може зменшити частоту зупинок кровообігу та дихання і знизити смертність.
11. Запровадження системи швидкого реагування в педіатричних відділеннях може зменшити частоту зупинок кровообігу та дихання і знизити смертність.
12. Ендотрахеальний шлях введення ліків не рекомендується, перевага віддається внутрішньовенному (центральні й периферичні вени) чи внутрішньокістковому.
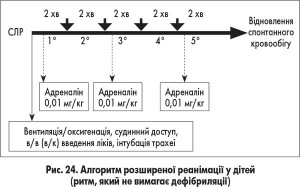
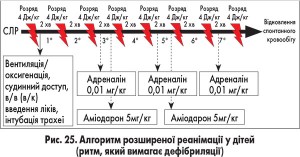
Алгоритми проведення базової та розширеної СЛР відповідно до європейських рекомендацій 2010 року подано на рисунках 22-25.
Рекомендації Американської асоціації серця щодо СЛР і невідкладної допомоги при серцево-судинних захворюваннях (2010 рік)
СЛР проводиться до ефективного відновлення функції кровообігу, дихання, ЦНС тощо. Тривалість СЛР за умов відсутності ефекту від правильно і в повному обсязі виконаних реанімаційних заходів становить 30-45 хв (щонайменше 10 хв у новонароджених), після чого СЛР можна закінчувати.
СТАТТІ ЗА ТЕМОЮ Педіатрія
Вроджена дисфункція кори надниркових залоз (ВДКНЗ) – це захворювання з автосомно-рецесивним типом успадкування, в основі якого лежить дефект чи дефіцит ферментів або транспортних білків, що беруть участь у біосинтезі кортизолу. Рання діагностика і початок лікування пацієнтів з ВДКНЗ сприяє покращенню показників виживаності та якості життя пацієнтів....
Алергічний риніт (АР) є поширеним запальним захворюванням верхніх дихальних шляхів (ВДШ), особливо серед педіатричних пацієнтів. Ця патологія може знижувати якість життя, погіршувати сон та щоденну продуктивність. Метою наведеного огляду є надання оновленої інформації щодо епідеміології АР та його діагностики, з урахуванням зв’язку з бронхіальною астмою (БА). ...
Американська академія педіатрії (AAP) оновила рекомендації щодо контролю грипу серед дитячого населення під час сезону 2023-2024 рр. Згідно з оновленим керівництвом, для профілактики та лікування грипу в дітей необхідно проводити планову вакцинацію з 6-місячного віку, а також своєчасно застосовувати противірусні препарати за наявності показань. ...
Поширеність і вплив алергічних захворювань часто недооцінюють [1]. Ключовим фактором алергічної відповіді є імуноглобулін (Ig) Е, присутній на поверхні тучних клітин і базофілів. Взаємодія алергену з IgЕ та його рецепторним комплексом призводить до активації цих клітин і вивільнення речовин, у тому числі гістаміну, які викликають симптоми алергії [2]. Враховуючи ключову роль гістаміну в розвитку алергічних реакцій, при багатьох алергічних станах, включаючи алергічний риніт і кропив’янку, пацієнту призначають антигістамінні препарати [3, 4]....