10 липня, 2017
Порівняння ефективності та безпеки двох режимів послідовного застосування системних глюкокортикостероїдів для лікування загострення бронхіальної астми

Division of Emergency Medicine, All India Institute of Medical Sciences, New Delhi, India
Гостра бронхіальна астма (БА) є поширеною причиною потрапляння до відділень невідкладної допомоги (ВНД) по всьому світу. У Сполучених Штатах щороку у ВНД із загостренням БА потрапляє приблизно 1,8 млн пацієнтів, з яких госпіталізуються майже 500 тис. [1]. Дані попередніх досліджень свідчать про те, що пацієнтам з ознаками тяжкої БА на додаток до стандартної терапії слід негайно призначати системні глюкокортикостероїди (ГКС) [3, 4].
У більшості досліджень, проведених за участю пацієнтів із загостренням БА, на початковому етапі застосовують внутрішньовенний метилпреднізолон (МП), а потім – пероральний ГКС (зазвичай МП) упродовж 1–8 тиж. Звичайно, використання внутрішньовенного гідрокортизону з подальшим пероральним прийомом преднізолону є більш дешевим, проте, оскільки МП, як відомо, має кращі фармакологічні властивості, такі як менша мінералокортикоїдна активність [5], більш виражене пригнічення запальних клітин [6] і краще проникнення в тканини легень [7], у порівнянні з гідрокортизоном і преднізолоном, вкрай бажаним є вивчення обох цих схем лікування пацієнтів із загостренням БА.
Опубліковані літературні дані щодо цього питання є досить обмеженими і суперечливими. Хоча роль внутрішьовенних ГКС при загостренні БА чітко встановлена, ми прагнемо порівняти ГКС, які найчастіше використовують при загостреннях БА в різних країнах. Таким чином, метою даного дослідження було порівняння ефективності і безпеки застосування внутрішньовенного MП з подальшим переходом на пероральний МП та внутрішньовенного гідрокортизону з подальшим переходом на пероральний преднізолон при лікуванні пацієнтів із загостренням БА.
Матеріали та методи дослідження
Дослідження проводилось упродовж 6 міс (з червня по листопад 2008 р.) у ВНД високоспеціалізованої лікарні в Північній Індії. Щороку дане ВНД приймало понад 120 тис. пацієнтів. Етичне схвалення було отримано від Комітету з професійної етики. Перед включенням пацієнта в дослідження від нього отримували письмову інформовану згоду.
В рамках пілотного рандомізованого дослідження порівнювали дві схеми застосування ГКС. Пацієнти на початку дослідження не знали, який препарат отримують внутрішньовенно – МП чи гідрокортизон. Проте на момент виписки вони знали, який препарат їм призначений для перорального прийому – МП чи преднізолон. У цьому пілотному дослідженні взяли участь 100 пацієнтів.
У дослідження увійшли пацієнти віком від 13 до 60 років, які протягом усього періоду спостере- ження перебували у ВНД з помірним (пікова швидкість видиху (ПШВ) 50–70 % від прогнозованого значення або бальна оцінка симптомів астми 8–11) або тяжким (ПШВ < 50 % від прогнозованого значення або бальна оцінка симптомів астми 12–15) загостренням БА. Пацієнтів молодше 13 років направляли у відділення дитячої невідкладної допомоги, а в пацієнтів старше 60 років часом було складно диференціювати БА з хронічним обструктивним захворюванням легень (ХОЗЛ).
Пацієнти вважалися хворими на астму, якщо раніше їм було встановлено діагноз БА або якщо дані історії хвороби та результати досліджень свідчили про наявність БА, як це визначено керівництвами Британського торакального товариства (BTS) а також керівництвами Звіту 3-ї експертної групи Національної програми з вивчення та профілактики астми [8, 9].
З дослідження виключали пацієнтів з наявністю будь-яких з наступних ознак: перший епізод свистячого дихання, температура > 38 °C, супутні захворювання, такі як пневмонія, застійна серцева недостатність або інтерстиційне захворювання легень, застосування системних ГКС упродовж останніх 30 днів, неможливість отримати від пацієнта згоду на участь у дослідженні, потреба в допоміжній вентиляції впродовж 1 год після госпіталізації у ВНД, неможливість провести вимірювання ПШВ, легке загострення БА (ПШВ > 70 % від прогнозованого значення або бальна оцінка симптомів астми 5–7), вагітність. Стан пацієнтів оцінювали впродовж перших 5 хв після їх поступлення до ВНД, щоб підтвердити, чи відповідають вони критеріям включення або виключення. Від пацієнта або його родичів отримували інформовану згоду. Визначали такі вихідні параметри, як пульс, артеріальний тиск (АТ), частота дихання (ЧД), наявність або відсутність ціанозу, наси- ченість киснем, вміст газів у артеріальній крові, ПШВ і об’єм форсованого видиху за 1-шу секунду (ОФВ1 ).
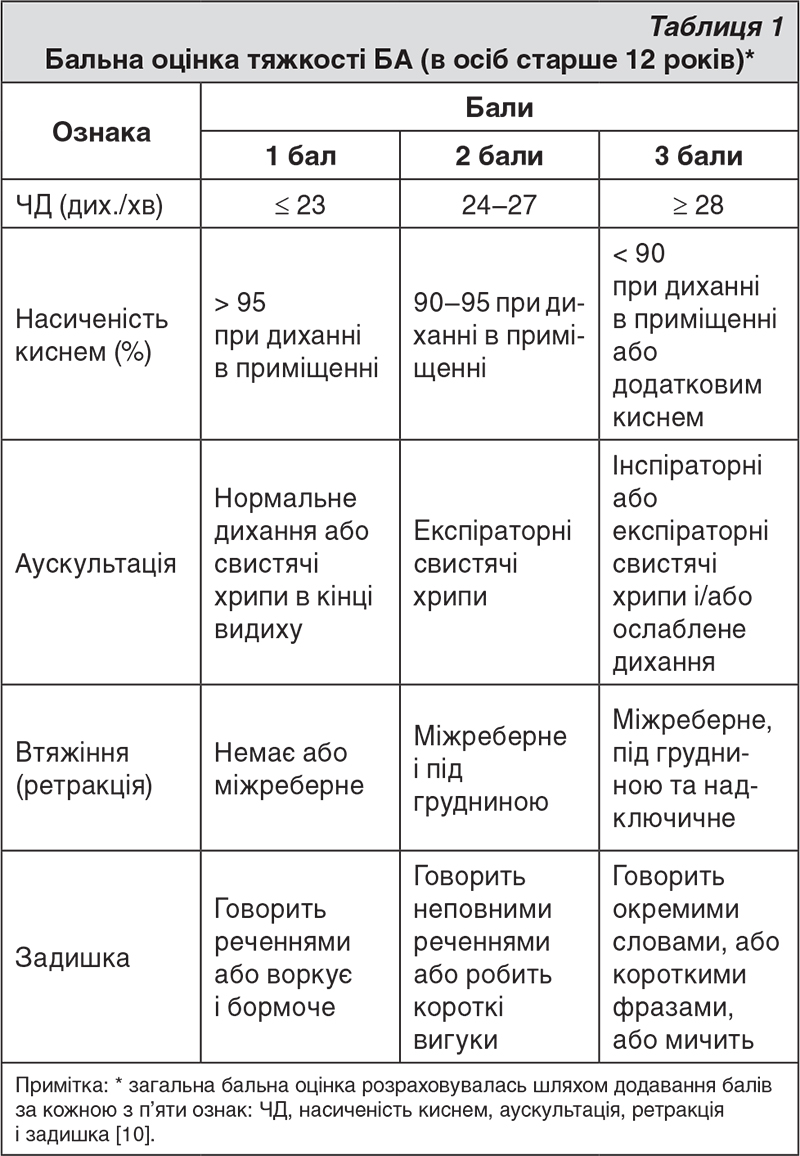 В кожен момент часу здійснювали два виміри (наприклад, при поступленні, через 1, 3 і 6 год, далі кожні 6 год упродовж перебування у ВНД, а потім – через 2 тиж спостереження), записували вищий показник. Оцінка ступеня тяжкості загострення базувалась на вимірюванні ПШВ і бальній оцінці симптомів астми. Ця бальна система оцінки астми (табл. 1) є модифікацією системи, опублікованої Національним інститутом охорони здоров’я; тяжкість епізоду визначається ознаками і симптомами [10].
В кожен момент часу здійснювали два виміри (наприклад, при поступленні, через 1, 3 і 6 год, далі кожні 6 год упродовж перебування у ВНД, а потім – через 2 тиж спостереження), записували вищий показник. Оцінка ступеня тяжкості загострення базувалась на вимірюванні ПШВ і бальній оцінці симптомів астми. Ця бальна система оцінки астми (табл. 1) є модифікацією системи, опублікованої Національним інститутом охорони здоров’я; тяжкість епізоду визначається ознаками і симптомами [10].
БА розцінювали як легку (ПШВ > 70 % від прогнозованого значення або бальна оцінка симптомів астми 5–7), помірну (ПШВ 50–70 % від прогнозованого значення або бальна оцінка симптомів астми 8–11) або тяжку (ПШВ < 50 % від прогнозованого значення або бальна оцінка симптомів астми 12–15). Після включення в дослідження пацієнти були випадковим чином розподілені в одну з двох груп лікування – група А або група В.
Пацієнти групи А отримували внутрішньовенно гідрокортизон по 200 мг кожні 6 год до виписки з подальшим пероральним прийомом преднізолону в добовій дозі 0,75 мг/кг упродовж 2 тиж. Пацієнти групи B отримували MП по 125 мг внутрішньовенно болюсно (Солюмедрол®, Pfizer Products India Pvt Ltd., Індія), а потім – по 40 мг внутрішньовенного МП кожні 6 год до виписки з подальшим переходом на пероральний МП в добовій дозі 0,6 мг/кг (Медрол®, Pfizer Products India Pvt Ltd.) упродовж 2 тиж. Крім того, пацієнти кожної групи отримували стандартну терапію: небулізований іпратропій в дозі 250 мкг і сальбутамол по 2,5 мг, розведені в 3 мл фізіологічного розчину, спочатку кожні 20 хв тричі. В залежності від відповіді пацієнта на терапію призначали відповідні дози бронходилататорів. За винятком внутрішньовенних ГКС, всі інші препарати призначали лікарі ВНД, які не брали участі в дослідженні. Антибіотики застосовували у разі необхідності.
Окрім того, всі пацієнти отримували кисневу терапію в дозі 4–6 л/хв за допомогою носових канюль або масок для обличчя. За необхідності лікарями ВНД призначалась дихальна підтримка. Всі клінічні прояви, ПШВ і ОФВ1 , оцінювали на початку дослідження, через 1, 3 і 6 год, далі – через кожні 6 год перебування у ВНД. Аналіз вмісту газів у артеріальній крові проводили на початку та повторно у разі відповідного призначення лікаря ВНД. Рішення про виписку пацієнта приймав лікар відділення. Зазвичай таке рішення приймалось після того, як ПШВ перевищувала 65 % від прогнозованого значення. Спостереження за пацієнтами велось упродовж 2 тиж, оцінювали відповідь на терапію (оцінка клінічних і спірометричних показників), а також будь- які побічні ефекти. Також враховували повторні звертання до будь-якої лікарні у зв’язку з рецидивом загострення впродовж 2 тиж спостереження.
Первинною кінцевою точкою була «невдача лікування», яка встановлювалась за наявності будь-якого з наступних критеріїв: потреба в ШВЛ, потреба в госпіталізації, летальний кінець упродовж 2 тиж після початкових проявів, повторна госпіталізація з приводу загострення впродовж 2 тиж після виписки або посилення фармакологічної терапії лікарями загальної практики впродовж 2 тиж після виписки з лікарні.
Вторинними кінцевими точками були зміни ОФВ1 і ПШВ під час перебування пацієнта у ВНД і подальшого 2-тижневого спостереження, зміна бальної оцінки симптомів астми під час 2-тижневого спостереження, тривалість перебування у ВНД (у разі ви- писки пацієнта) і тривалість перебування в стаціонарі (якщо призначалось стаціонарне лікування). Крім того, в обох групах лікування виявляли і порівнювали характер і тяжкість побічних ефектів, які реєстрували упродовж 2 тиж.
 Оскільки пошук літературних даних виявив лише одне дослідження, в якому порівнювалась ефективність МП і гідрокортизону [11], дане дослідження було проведене як пілотне, щоб допомогти оцінити розмір вибірки для підтверджувальних досліджень. Таким чином, була застосована методика цільової вибірки і був обраний розмір вибірки 100 пацієнтів. Для кожної змінної розраховували показники описової статистики (середнє значення, стандартне відхилення і медіана).
Оскільки пошук літературних даних виявив лише одне дослідження, в якому порівнювалась ефективність МП і гідрокортизону [11], дане дослідження було проведене як пілотне, щоб допомогти оцінити розмір вибірки для підтверджувальних досліджень. Таким чином, була застосована методика цільової вибірки і був обраний розмір вибірки 100 пацієнтів. Для кожної змінної розраховували показники описової статистики (середнє значення, стандартне відхилення і медіана).
Для порівняння значень між групами використовували незалежний t-критерій. Коли припущення про нормальний розподіл не підтверджувалось, використовували відповідний непараметричний тест, наприклад, U-критерій Манна–Уїтні. Порівняння показників між групами здійснювали за допомогою ксі-квадрат-(χ2) критерію. Усередині групи для перевірки різниці між початковими показниками та показниками через 2 тиж використовували парний критерій Стьюдента. Дисперсійний аналіз повторних вимірювань (ANOVA) застосовували для визначення різниці між значеннями в межах групи в різні моменти часу.
Для множинних порівнянь ОФВ1 і ПШВ в різні моменти часу застосовували критерій Тьюкі для стьюдентизованого діапазону (q). Результати вважали значущими на рівні 5 % (р < 0,05). Для обробки і аналізу даних використовували програму Microsoft Excel (версія 2000, Microsoft, Редмонд, штат Вашингтон, США) і статистичний пакет програмного забезпечення (SAS версія 9.1.3 Service Pack 4, SAS Institute Inc., Cary, NC, США).
Результати дослідження та їх обговорення
 Було обстежено 112 пацієнтів, 12 з яких відмовилися дати інформовану згоду. Загалом було відібрано 100 хворих і випадковим чином розподілено на дві групи (група А (n = 49) і група В (п = 45). Шість пацієнтів були з різних причин виключені з дослідження впродовж 1 год після рандомізації. Таким чином, тільки 94 пацієнтів зрештою були залучені до дослідження.
Було обстежено 112 пацієнтів, 12 з яких відмовилися дати інформовану згоду. Загалом було відібрано 100 хворих і випадковим чином розподілено на дві групи (група А (n = 49) і група В (п = 45). Шість пацієнтів були з різних причин виключені з дослідження впродовж 1 год після рандомізації. Таким чином, тільки 94 пацієнтів зрештою були залучені до дослідження.
Пацієнти обох груп достовірно не відрізнялися за віком, анамнезом куріння, тривалістю БА, лікарськими препаратами, що використовувались для лікування хронічної фази, тривалістю нинішнього загострення БА і лікарськими засобами, що застосовувались до поступлення у ВНД (табл. 2).
Крім того, на початку дослідження між пацієнтами обох груп не було істотних відмінностей у показниках вмісту газів у артеріальній крові. Жоден з пацієнтів не застосовував пероральні або парентеральні ГКС протягом останніх 30 днів.
Клінічні ознаки загострення у пацієнтів в основному полягали у посиленні кашлю з мокротинням, задишці, ретракції міжреберних проміжків/під грудниною/над грудниною та наявності хрипів.
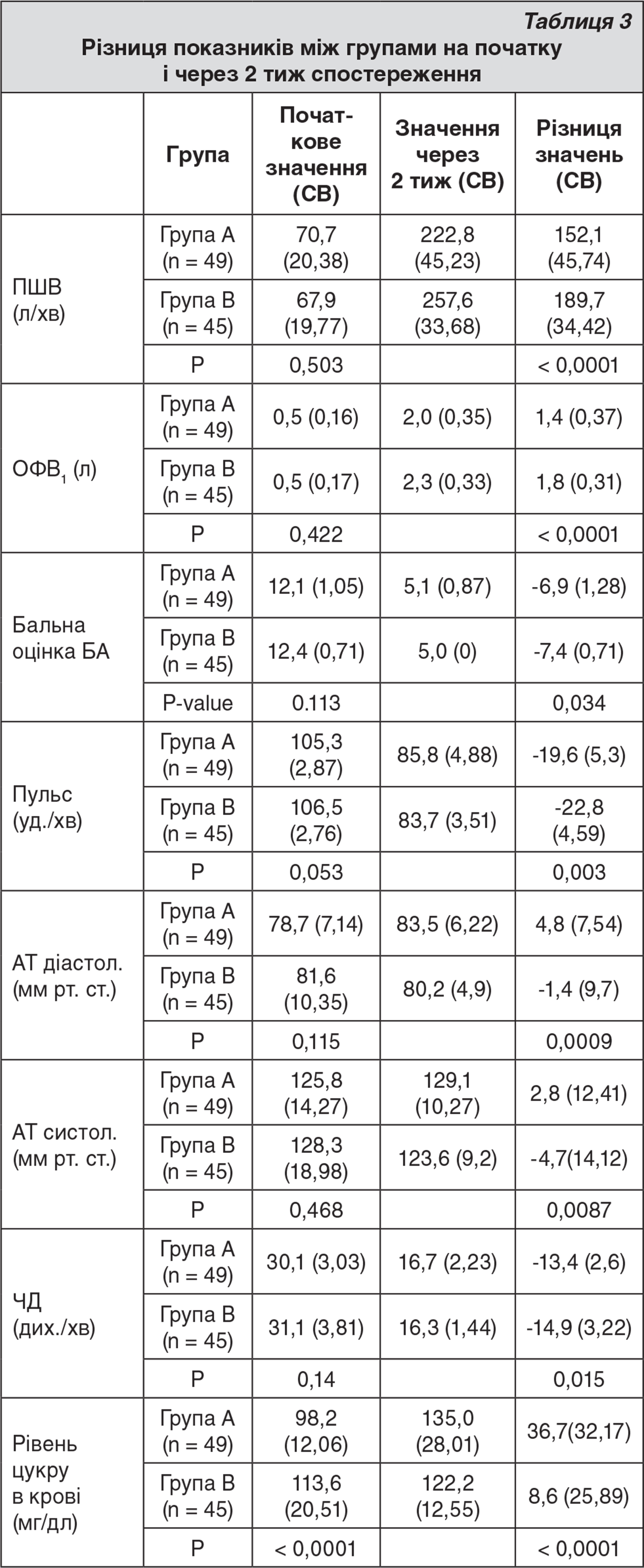
Частота пульсу, АТ, ЧД, ПШВ, ОФВ1 і бальна оцінка симптомів астми на початку між групами істотно не відрізнялися. Після лікування показники пульсу, ЧД, ПШВ, ОФВ1 і бальна оцінка симптомів астми значно покращились у пацієнтів обох груп як на момент виписки, так і через 2 тиж спостереження (табл. 3).
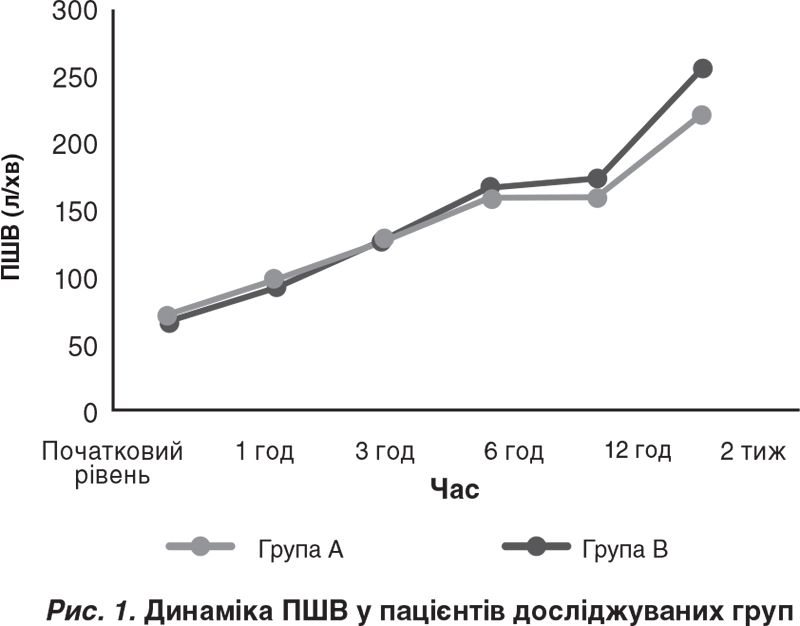
Спостерігалось стійке і значне зростання середніх значень ПШВ у пацієнтів обох досліджуваних груп у порівнянні з початковим рівнем упродовж 6 год перебування у ВНД з найбільшим значен- ням на 6-й годині (р < 0,0001).
У пацієнтів групи А середній показник ПШВ через 6 год становив 160,0 (± 40,44) л/хв, тоді як у пацієнтів групи B – 167,6 (± 33,39) л/хв. Не було виявлено істотних відмінностей між середніми значеннями ПШВ в пацієнтів обох груп у різні моменти часу під час перебування у ВНД (р = 0,431 через 1 год, р = 0,704 через 3 год, р = 0,341 через 6 год; рис. 1).
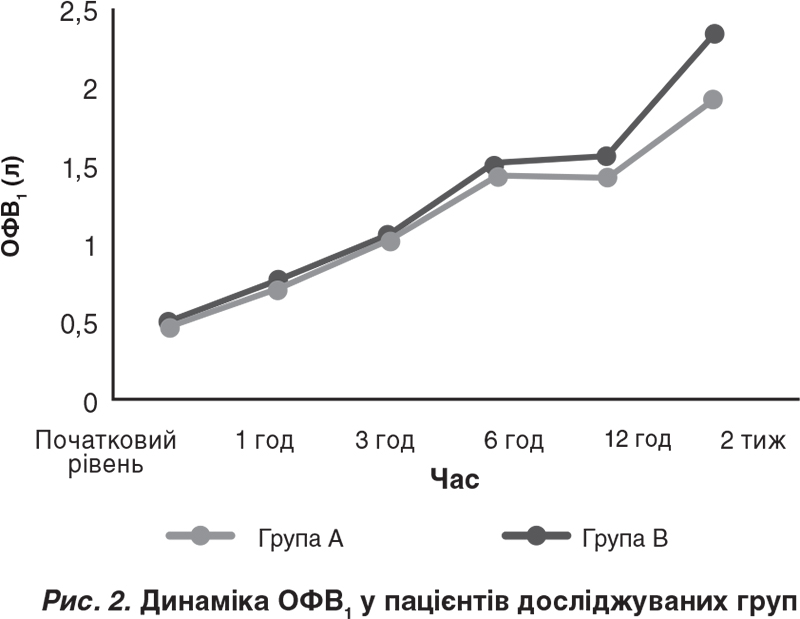
Аналогічні результати спостерігали для середнього показника ОФВ1 (р = 0,41 через 1 год, р = 0,874 через 3 год, p = 0,609 через 6 год; рис. 2).
 На момент виписки збільшення ПШВ і ОФВ1 статистично не відрізнялося між пацієнтами обох груп. Проте спостерігалася значна різниця між показниками ПШВ і ОФВ1 через 2 тиж спостереження, а саме у пацієнтів групи B продемонстровано кращі показники ПШВ і ОФВ1 порівняно з групою А (р < 0,001; див. табл. 3).
На момент виписки збільшення ПШВ і ОФВ1 статистично не відрізнялося між пацієнтами обох груп. Проте спостерігалася значна різниця між показниками ПШВ і ОФВ1 через 2 тиж спостереження, а саме у пацієнтів групи B продемонстровано кращі показники ПШВ і ОФВ1 порівняно з групою А (р < 0,001; див. табл. 3).
Середня тривалість перебування у ВНД становила 10,2 (± 6,49) год в групі А і 8,9 (± 5,99) год в групі В (р = 0,32). Один пацієнт у групі А потребував госпіталізації. Не було суттєвих відмінностей між групами у потребі в додаткових дозах інгаляторів упродовж перших 6 год загострення (р = 0,136).
Крім того, не було ніяких істотних відмінностей між групами (р = 0,74) в потребі в додаткових препаратах (пероральних бронхолітиках і антибіотиках), які призначали лікарі під час виписки.
 Початкові середні значення вмісту цукру в крові становили 98,2 (± 12,06) мг/дл і 113,6 (± 20,51) мг/дл в групі А і групі В відповідно (р < 0,0001). Через 2 тиж лікування середні значення рівня цукру в крові були значно вищими в групі А (135,0 (± 28,01) мг/дл) в порівнянні з групою B (122,2 (± 12,55) мг/дл; р < 0,0001).
Початкові середні значення вмісту цукру в крові становили 98,2 (± 12,06) мг/дл і 113,6 (± 20,51) мг/дл в групі А і групі В відповідно (р < 0,0001). Через 2 тиж лікування середні значення рівня цукру в крові були значно вищими в групі А (135,0 (± 28,01) мг/дл) в порівнянні з групою B (122,2 (± 12,55) мг/дл; р < 0,0001).
У групах спостерігалося значне розходження рівнів цукру в крові через 2 тиж в порівнянні з початковим рівнем (група A: р < 0,0001; група В: р = 0,031). В групі А діастолічний АТ значно збільшився – з 78,7 (± 7,14) до 83,5 (± 6,22) мм рт. ст. (р < 0,0001), тоді як в групі В спостерігалось зниження систолічного АТ з 128,3 (± 18,98) до 123,6 (± 9,2) мм рт. ст. (р = 0,032). Вміст газів у артеріальній крові визначали лише на початку, оскільки клінічний стан більшості пацієнтів не потребував повторного його визначення. У групі А у 2 (4,17 %) пацієнтів спостерігався рецидив загострення упродовж 2 тиж спостереження.
В одного пацієнта рецидив зареєстровано на 14-й день спостереження; його бальна оцінка симптомів астми становила 11. В іншого пацієнта рецидив розвинувся на 10-й день спостереження, він отримав допомогу в іншій лікарні. Його стан покращився через 6 год, після чого він продовжив приймати таблетки, призначені в ході дослідження. Інший пацієнт (2,04 %) з групи А потребував підтримки дихання за допомогою ШВЛ через виснаження дихальних м’язів; він помер через 48 год після поступлення до ВНД. Через 2 тиж спостереження у пацієнтів обох груп відмічали такі побічні явища: здуття живота і закрепи у 2 (8,33 %) пацієнтів групи А, пекучий біль в епігастрії в 2 (8,33 %) пацієнтів групи А і в 1 (2,22 %) пацієнта групи В і набряк обличчя у 2 (14,58 %) пацієнтів групи А і в 3 (6,67 %) пацієнтів групи B.
При тяжкому загостренні БА важливо досягти швидкого поліпшення функції легень протягом перших годин, оскільки саме в цей час спостерігаються найбільші ураження. На цьому етапі доцільним є негайне призначення ГКС [12, 13], хоча їх дія може розвинутись щонайменше через 4 год [14]. Міжнародні керівні принципи, такі як Глобальна ініціатива з астми (GINA) [14] і керівництва BTS [8], рекомендують раннє застосування системних ГКС при загостренні БА, оскільки було показано, що вони здатні зменшувати частоту та тривалість госпіталізації, а також частоту рецидивів після загострення. При загостреннях БА доцільно призначати короткий курс пероральних ГКС після виписки з ВНД, оскільки це знижує частоту рецидивів і потребу в інгаляційних бронходилататорах і не супроводжується будь-якими серйозними побічними ефектами [3, 15].
В опублікованих дослідженнях роль різних ГКС при БА описується не однаково, оскільки їх ефек- тивність може варіювати залежно від протизапальних властивостей [16]. У той час як МП виявляє велику протизапальну активність, більшу тривалість дії і менші натрій-зберігаючі властивості в порівнянні з преднізолоном і гідрокортизоном [11], в опублікованій літературі існує дуже мало досліджень, які порівнюють різні схеми ГКС-терапії при загостренні БА. Gordon et al. (1984) оцінювали вплив двох доз МП (125 мг або 60 мг) у порівнянні з гідрокортизоном у дозі 100 мг на сироваткові рівні IgE. Рівні IgE значно зменшилися у хворих, які застосовували вищу дозу МП (125 мг), тоді як не спостерігалось значного їх зниження у пацієнтів, які отримували гідрокортизон або нижчу дозу МП (60 мг) [17 ].
В іншому дослідженні 14 пацієнтів із загостренням БА отримували гідрокортизон (100 мг внутрішньовенно кожні 6 год), МП (20 мг внутрішньовенно кожні 6 год) або дексаметазон (3,75 мг внутрішньовенно кожні 6 год). Не було виявлено жодних відмінностей у ефективності цих трьох препаратів упровдож 72 год [18]. У дослідженні Hall et al. (1996) було встановлено, що гідрокортизон є ефективнішим, ніж МП, в скороченні терміну госпіталізації у хворих з тяжким загостренням БА [11]. Проте гідрокортизон вводили в дозі 200 мг внутрішньовенно кожні 4 год, тоді як МП – в дозі 125 мг внутрішньовенно кожні 12 год. В жодному з цих досліджень не порівнювали ефективність послідовного призначення внутрішньовенного ГКС у ВНД з подальшим пероральним їх застосуванням коротким курсом, що є рекомендованим.
Дане дослідження мало на меті порівняти ефективність і безпеку двох режимів лікування загостреннях БА – внутрішньовенного застосування гідрокортизону з подальшим пероральним призначенням преднізолону, а також внутрішньовенного MП з подальшим призначенням перорального МП. Проведене дослідження продемонструвало значне поліпшення функції легень протягом декількох годин внутрішньовенного введення ГКС у ВНД. Через 2 тиж спостереження поліпшення функції легень при пероральному застосуванні МП було значно більш виражене, ніж в групі преднізолону. Таку різницю результатів в кінці 2-тижневого спостереження можна пояснити численними властивостями МП.
МП, як відомо, має більш виражену протизапальну активність і меншу мінералокортикоїдну дію в порівнянні з преднізолоном [11]. Зокрема, було показано, що він чинить набагато сильнішу дію на специфічні клітини, що беруть участь у запаленні (наприклад, мононуклеари периферійної крові), в порівнянні з преднізолоном [6]. Також деякі дослідження на тваринах показали, що МП досягає значно вищих концентрацій в легеневій тканині в порівнянні з преднізолоном протягом певного періоду часу після одноразового застосування. Це може забезпечувати більшу біодоступність препарату в місці його дії [7].
Тривалість перебування у ВНД пацієнтів групи B була дещо меншою в порівнянні з такими групи А, хоча значущої різниці не було. У ході дослідження рівні глюкози в крові через 2 тиж спостереження збільшились в обох групах, проте це зростання було більш вираженим у групі А в порівнянні з групою B (р < 0,0001 проти р = 0,031). Це збільшення може бути пов’язане із застосуванням в групі А преднізолону протягом 2 тиж. Ці дані підтверджують висновки інших досліджень, які продемонстрували гіперглікемічні ефекти преднізолону [19].
Дані щодо несприятливих подій показали, що застосування внутрішньовенного MП/перорального MП є порівняно безпечнішим, ніж внутрішньовенного гідрокортизону/преднізолону, хоча це може бути підтверджено лише за умови вклю- чення більшої вибірки в ході подальших досліджень. У групі А 3 пацієнтів досягли первинної кінцевої точки, з них у 2 розвинувся рецидив упродовж 2 тиж і один помер. Дане дослідження має певні обмеження. Розмір вибірки був малим, проте, як уже зазначалось, це дослідження було пілотним.
Друге обмеження полягає в тому, що воно не було подвійним сліпим, і отже, могла мати місце певна упередженість з боку лікарів, які брали в ньому участь. Дослідження проводилось у ВНД з середньою кількістю персоналу 10 лікарів на зміну, яка змінювалась щодоби. За винятком ГКС, інші засоби призначали лікарі відділення, які не брали участь у дослідженні. Вони також приймали рішення щодо поступлення та виписки хворих і навряд чи могли вплинути на результати дослідження. Третє обмеження – дози МП і гідрокортизону/преднізолону, які застосовували в дослідженні.
Bowler et al. (1992) в своєму дослідженні показали, що нижча доза внутрішньовенного гідрокортизону (50 мг) 4 рази на добу протягом 2 днів з подальшим призначенням нижчої дози преднізону є так само ефективною при лікуванні тяжкого загострення БА, як доза гідрокортизону 200 або 500 мг з подальшим призначенням вищих доз преднізону [20]. В керівництвах BTS [8] також наведені нижчі дози гідрокортизону (100 мг внутрішньовенно кожні 6 год), а потім 40–50 мг преднізолону протягом 5 днів або до усунення загострення БА. Дози гідрокортизону і преднізолону, які застосовували в дослідженні, базувались на рекомендаціях Тейлора (2003) [21]. МП використовували в дозах, еквівалентних дозам гідрокортизону.
На основі керівництв BTS в цьому дослідженні могли бути розглянуті нижчі дози гідрокортизону/MП і менш тривале призначення перорального MП/преднізолону, оскільки крім високої вартості ГКС у високих дозах можуть спричинювати більше стероїд-пов’язаних побічних ефектів, ніж у низьких. Ще одним обмеженням дослідження було виключення пацієнтів молодше 13 років, хоча такі пацієнти із загостреннями БА складають значну групу.
Висновки
Дане дослідження продемонструвало більш високу ефективність і безпеку застосування внутрішньовенного МП з подальшим призначенням перорального МП в порівнянні з внутрішньовенним гідрокортизоном з подальшим пероральним прийомом преднізолону у хворих із загостренням БА. На підставі результатів цього пілотного дослідження внутрішньовенний МП з подальшим пероральним МП, незважаючи на більш високу вартість, можуть розглядатись як препарати вибору при порівнянні цих двох терапевтичних режимів при загостреннях БА. Проте період напіврозпаду МП в плазмі та тканинах в два-три рази більший, ніж гідрокортизону [22], у зв’язку з цим доцільно розглянути терапевтичний режим з менш частим дозуванням МП, що, імовірно, знизить загальну вартість лікування.
Список літератури – у редакції.
Реферативний огляд статті «Comparing the efficacy and safety of two regimens of sequential systemic corticosteroids in the treatment of acute exacerbation of bronchial asthma» Praveen Aggarwal, Sanjeev Bhoi підготувала Євгенія Канівець
J Emerg Trauma Shock. 2010 Jul-Sep;
3(3): 231–237. doi: 10.4103/0974-2700.66522
ЖУРНАЛ «АСТМА ТА АЛЕРГІЯ» № 1, 2017


