3 квітня, 2019
Терапевтична еквівалентність препаратів ніфуроксазиду вітчизняного і закордонного виробництва у лікуванні дітей з гострими кишковими інфекціями

 Гострі кишкові інфекції (ГКІ) займають важливе місце у структурі інфекційної патології дитячого віку. За даними Всесвітньої оранізації охорони здоров’я, у світі на ГКІ щорічно хворіє більше 1 млрд осіб, з яких 65-70% становлять діти віком до 5 років [1-3]. Дитяча смертність у зазначеній віковій категорії становить близько 1,5 млн дітей на рік [4, 5]. Останніми роками відзначається тенденція до зростання захворюваності на ГКІ й у нашій країні. Так, в Україні щорічно офіційно реєструється 45-50 тис. випадків ГКІ серед дітей, причому близько 40 дітей помирають через тяжкий і/або ускладнений перебіг [6]. У структурі дитячої смертності у нашій країні інфекційні захворювання традиційно посідають п’яте місце, а серед летальних випадків від інфекційних причин ГКІ займають перше місце (частка становить 30-35% [7]). Причинами значної поширеності ГКІ є збільшення спектра мікроорганізмів, що спричиняють інфекційні процеси, несприятливі соціально-економічні умови, недостатній рівень санітарної освіти населення, інколи – несвоєчасна та нераціональна антибіотикотерапія [8-11].
Гострі кишкові інфекції (ГКІ) займають важливе місце у структурі інфекційної патології дитячого віку. За даними Всесвітньої оранізації охорони здоров’я, у світі на ГКІ щорічно хворіє більше 1 млрд осіб, з яких 65-70% становлять діти віком до 5 років [1-3]. Дитяча смертність у зазначеній віковій категорії становить близько 1,5 млн дітей на рік [4, 5]. Останніми роками відзначається тенденція до зростання захворюваності на ГКІ й у нашій країні. Так, в Україні щорічно офіційно реєструється 45-50 тис. випадків ГКІ серед дітей, причому близько 40 дітей помирають через тяжкий і/або ускладнений перебіг [6]. У структурі дитячої смертності у нашій країні інфекційні захворювання традиційно посідають п’яте місце, а серед летальних випадків від інфекційних причин ГКІ займають перше місце (частка становить 30-35% [7]). Причинами значної поширеності ГКІ є збільшення спектра мікроорганізмів, що спричиняють інфекційні процеси, несприятливі соціально-економічні умови, недостатній рівень санітарної освіти населення, інколи – несвоєчасна та нераціональна антибіотикотерапія [8-11].
Згідно з Протоколом лікування гострих кишкових інфекцій у дітей, затвердженим наказом Міністерства охорони здоров’я (МОЗ) України від 10.12.2007 № 803 [12], показаннями до призначення антибактеріальної терапії при інвазивних діареях є:
- Тяжкі та середньотяжкі форми захворювання.
- Вік молодше 3 місяців; імунна скомпрометованість, зокрема у дітей з імунодефицітними станами, ВІЛ-інфікованих; дітей, які перебувають на імуносупресивній терапії (хімічна, променева), довготривалій терапії кортикостероїдами; гемолітичні анемії, гемоглобінопатії незалежно від віку дитини і тяжкості захворювання.
- Гемоколіт незалежно від віку дитини і тяжкості захворювання.
- Наявність вторинних бактеріальних ускладнень у дітей всіх вікових груп.
Показаннями до призначення антибактеріальної терапії при секреторних діареях є:
- Тяжкий та середньотяжкий перебіг ГКІ у немовлят.
- Імунодефіцитні стани (у ВІЛ-інфікованих дітей, дітей, яким проводять імуносупресивну (хімічну, променеву), довготривалу терапію кортикостероїдами, гемолітичні анемії, гемоглобінопатії у дітей).
- Холера, паразитарні діареї незалежно від віку дитини і тяжкості захворювання.
- Наявність вторинних бактеріальних ускладнень у дітей всіх вікових груп.
Слід зауважити, що при ГКІ антибактеріальна терапія не показана:
- Хворим із легкими, стертими та середньотяжкими формами інфекцій, окрім тих, що зазначені вище.
- При бактеріальному носійстві будь-якої етіології (транзиторному, постінфекційному).
- Хворим із дисфункцією шлунково-кишкового тракту (ШКТ), яка пов’язана з наслідками ГКІ (дисбіоз кишечника, лактазна недостатність, целіакія, вторинна ферментопатія та ін.).
Не доведена ефективність антибіотиків при ГКІ, спричинених такими збудниками:
– Campylobacter jejuni;
– Yersinia enterocolitica;
– ентерогеморагічними штамами E. coli;
– ентеротоксигенними штамами E. coli.
Згідно з протоколом МОЗ України [12], препаратами першого ряду, які призначають при ГКІ, є ентеросептики нітрофуранового ряду (ніфуроксазид).
Антибіотики другого ряду (найчастіше – цефалоспорини ІІІ покоління) призначають при тяжких і середньотяжких формах інвазивної діареї, неефективності препаратів першого ряду та пізній госпіталізації хворого.
Препарати третього ряду застосовуються при тяжких і середньотяжких формах захворювання у пацієнтів групи ризику на тлі імунодефіцитних станів, неефективності препаратів другого ряду та виникненні вторинних бактеріальних ускладнень (як правило, це амінопеніциліни, цефалоспорини ІV покоління, карбапенеми) [13-16].
Антимікробна активність нітрофуранів проявляється щодо грампозитивних і грамнегативних бактерій, окремих найпростіших і грибів.
Нітрофурани блокують клітинне дихання мікроорганізмів за рахунок пригнічення активності ряду дихальних ферментів (піруватоксидази, глютатіонредуктази, альдегіддегідрогенази). Ці препарати також блокують біосинтез ДНК і, меншою мірою, РНК мікроорганізмів. Водночас вони не пригнічують імунний захист, а стимулюють його за рахунок посилення фагоцитарної активності лейкоцитів, підвищення адсорбційно-поглинальної здатності ретикуло-ендотеліальної системи печінки та селезінки.
Введення нітрофуранів не викликає системних побічних ефектів. Після перорального застосування вони практично не абсорбуються зі ШКТ, справляють антибактеріальну дію винятково у просвіті кишечника, повністю виводяться з калом, не чинять негативного впливу на облігатну мікрофлору кишок, тобто зберігають їх біоценоз у гострий період ГКІ. У терапевтичних дозах нітрофурани виявляють бактеріостатичний ефект, у максимальних – бактерицидний.
Провідне місце серед нітрофуранових ентеросептиків посідає ніфуроксазид.
На фармацевтичному ринку України міцні позиції займає ніфуроксазид виробництва компанії Gedeon Richter (Угорщина). Однак, враховуючи його вартість, актуальним залишається пошук еквівалентної заміни імпортного препарату на вітчизняний. Така заміна дозволить здійснювати ефективну ерадикацію збудників ГКІ на більш економічно вигідних умовах.
Матеріали та методи
У 2015-2016 рр. проведено клінічне дослідження з вивчення ефективності та переносимості препарату Ніфуроксазид, суспензія оральна 220 мг/5 мл виробництва ПАТ НВЦ «Борщагівський ХФЗ». Дослідження розпочато після отримання дозволу Державного експертного центру МОЗ України та позитивного рішення локальних етичних комісій. Воно проводилося з дотриманням вимог чинного законодавства, принципів Належної клінічної практики (GCP) та Гельсінської декларації на двох клінічних базах. У відділенні кишкових інфекцій Комунальної медичної установи «Обласна дитяча клінічна лікарня» м. Чернівці проведено комплексне обстеження та лікування 100 дітей, хворих на ГКІ. В інфекційно-боксованому відділенні Комунальної установи «Вінницька обласна клінічна дитяча інфекційна лікарня» комплексно обстежено та проліковано 20 дітей з тією самою патологією. Розподіл пацієнтів на групи здійснювався шляхом рандомізації.
До першої (основної) групи увійшли 60 пацієнтів, які приймали Ніфуроксазид (суспензія оральна 220 мг/5 мл виробництва ПАТ НВЦ «Борщагівский ХФЗ») протягом 5 днів. Другу (контрольну) групу сформували 60 дітей, які отримували референтний препарат – Ніфуроксазид Ріхтер (суспензія оральна 220 мг/5 мл виробництва компанії Gedeon Richter). Діти віком від 1 до 2 років отримували по 2,5 мл препарату 4 рази на добу*; від 2 до 7 років – по 5 мл 3 рази на добу; від 7 до 12 років – по 5 мл 4 рази на добу (згідно з інструкцією для медичного застосування).
* Станом на 16.04.2015, коли розпочато проведення дослідження, згідно з інструкцією для медичного застосування референтного препарату, в Україні ніфуроксазид було дозволено для застосування у дітей від 2 міс. Після перереєстрації виробник референтного препарату вніс зміни у розділи інструкції «Показання», «Спосіб застосування та дози», «Діти» (наказ МОЗ України від 29.12.2015 № 915), що обмежують застосування суспензії ніфуроксазиду у дітей віком до 2 років. Проведення вказаного дослідження завершено згідно із затвердженим протоколом, за його результатами дозування та вік пацієнтів не були змінені.
За статтю та віком основна та контрольна групи статистично значущо не відрізнялись. До основної групи увійшли 22 хлопчики (36,7%) та 38 дівчаток (63,3%); середній вік хворих становив 2,7±2,4 року. Контрольна група складалася з 28 хлопчиків (46,7%) та 32 дівчаток (53,3%); середній вік пацієнтів – 3,3±2,5 року.
У всіх дітей оцінювали основні клінічні симптоми захворювання: наявність і тривалість гіпертермії, патологічних змін шкіри, слизових оболонок і ШКТ, а також наявність діареї та характер випорожнень.
Головною змінною дослідження був дихотомічний показник ефективності терапії (категорії: «терапія ефективна», «терапія неефективна»), віднесення до категорій якої здійснювалося за таким алгоритмом:
- якщо на 6-й день лікування (візит 6) відбулася повна інволюція основних симптомів захворювання (частота, характер випорожнень, патологічні домішки в калі), терапію вважали ефективною;
- якщо на 6-й день лікування (візит 6) не настала повна інволюція основних симптомів захворювання (частота, характер випорожнень, патологічні домішки в калі) та/або є необхідність у призначенні додаткової антибактеріальної терапії, терапія вважалася неефективною.
Вторинних змінних ефективності не було.
Первинний критерій ефективності: 95% довірчий інтервал для різниці часток пацієнтів в обох групах, терапія в яких була ефективна, мав перебувати в межах зони терапевтичної еквівалентності (20%). У такому випадку терапевтична еквівалентність вважалася доведеною.
Вторинних критеріїв ефективності не було.
Переносимість досліджуваного та референтного препаратів оцінювалася на підставі скарг пацієнтів та об’єктивних даних, отриманих у процесі лікування, динаміки лабораторних показників, а також частоти виникнення та характеру побічних ефектів.
Результати та їх обговорення
 У 59 пацієнтів, які отримували препарат Ніфуроксазид, суспензія оральна 220 мг/5 мл виробництва ПАТ НВЦ «Борщагівський ХФЗ», на 6-й день лікування (візит 6) відбулася повна інволюція основних симптомів захворювання (частота, характер випорожнень, патологічні домішки в калі). Таким чином, у 98,3% пацієнтів основної групи терапія була ефективною, а в 1,7% (1 пацієнта) – неефективною.
У 59 пацієнтів, які отримували препарат Ніфуроксазид, суспензія оральна 220 мг/5 мл виробництва ПАТ НВЦ «Борщагівський ХФЗ», на 6-й день лікування (візит 6) відбулася повна інволюція основних симптомів захворювання (частота, характер випорожнень, патологічні домішки в калі). Таким чином, у 98,3% пацієнтів основної групи терапія була ефективною, а в 1,7% (1 пацієнта) – неефективною.
У 59 пацієнтів контрольної групи, які отримували референтний препарат, на 6-й день лікування (візит 6) також відбулася повна інволюція основних симптомів захворювання (частота, характер випорожнень, патологічні домішки в калі). Таким чином, у 98,3% пацієнтів контрольної групи терапія була ефективною, а в 1,7% (1 пацієнта) – неефективною.
95% довірчий інтервал для різниці часток пацієнтів, у яких терапія була ефективною, в основній та контрольній групах становив від –7,32 до 7,32%. Оскільки він перебував у межах діапазону терапевтичної еквівалентності (від –20 до 20% згідно з протоколом дослідження), то можна зробити висновок, що препарат Ніфуроксазид, суспензія оральна 220 мг/5 мл виробництва ПАТ НВЦ «Борщагівський ХФЗ» терапевтично еквівалентний референтному препарату при використанні у дітей з ГКІ.
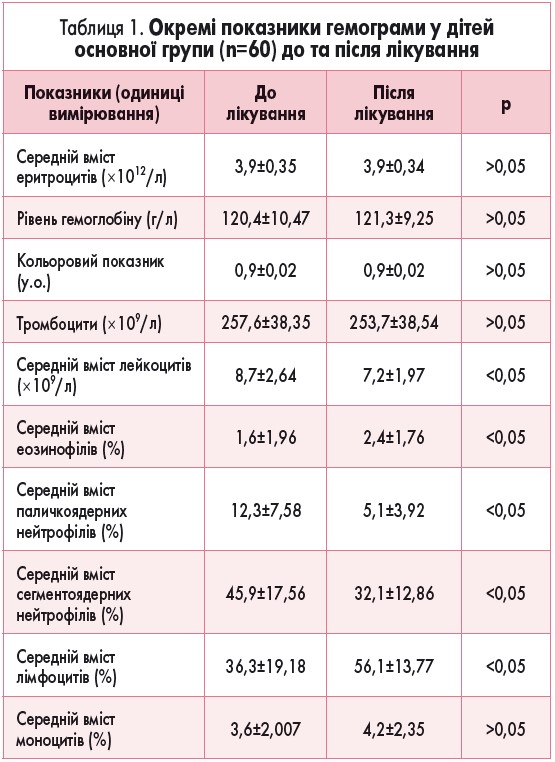
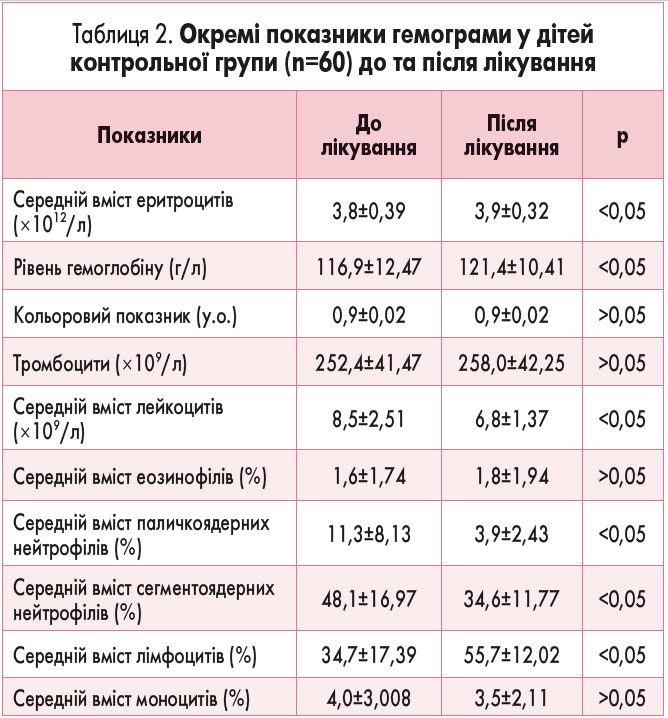
Результати дослідження окремих показників загального аналізу крові у пацієнтів основної групи подано у таблиці 1, контрольної групи – у таблиці 2.
Згідно з отриманими даними, на фоні лікування ГКІ з використанням Ніфуроксазиду виробництва ПАТ НВЦ «Борщагівский ХФЗ» і референтного препарату закордонного виробництва відзначалися статистично значущі зміни окремих показників гемограми, що свідчило про ерадикацію бактеріального запального процесу в організмі: зменшення середнього вмісту лейкоцитів у крові, а також відносного вмісту паличкоядерних і сегментоядерних лейкоцитів; це підтверджувало ефективність призначеної терапії.
 У пацієнтів як основної, так і контрольної груп під час дослідження не виявлено негативної клінічно значущої дії препаратів на показники загального та біохімічного аналізу крові та загального аналізу сечі.
У пацієнтів як основної, так і контрольної груп під час дослідження не виявлено негативної клінічно значущої дії препаратів на показники загального та біохімічного аналізу крові та загального аналізу сечі.
Результати об’єктивного дослідження показали, що зміни вітальних даних (артеріального тиску, частоти серцевих скорочень, температури тіла), а також стану шкіри та слизових оболонок і органів черевної порожнини в пацієнтів основної та контрольної груп свідчили про позитивну динаміку основного захворювання.
Під час дослідження в 1 пацієнта зареєстровано 2 випадки виникнення побічної реакції/побічного явища (ПР/ПЯ), а саме: появу ацетону в сечі та підвищення температури тіла вище 38 °C. Цей пацієнт приймав референтний препарат. Ці ПЯ характеризуються як несерйозні, непередбачувані, сумнівні, пов’язані з перебігом захворювання, вони не потребували відміни препарату та спеціальної терапії, завершились одужанням без наслідків.
Водночас при застосуванні препарату Ніфуроксазид, суспензія оральна 220 мг/5 мл виробництва ПАТ НВЦ «Борщагівський ХФЗ», ніяких ПР/ПЯ не спостерігалося.
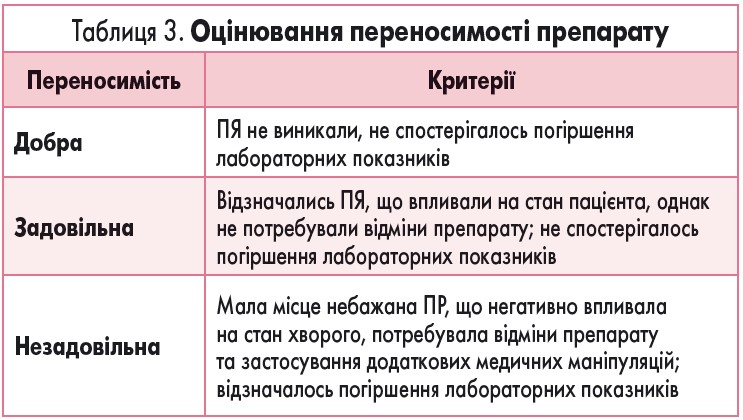 Загальна переносимість препарату оцінювалась за критеріями, поданами у таблиці 3.
Загальна переносимість препарату оцінювалась за критеріями, поданами у таблиці 3.
Загальна переносимість препаратів була оцінена як добра у 100% пацієнтів основної групи та у 98,3% – контрольної групи. В 1 пацієнта контрольної групи переносимість була оцінена як задовільна, що зумовлено виникненням у нього ПР/ПЯ.
Висновки
- Досліджуваний препарат Ніфуроксазид, суспензія оральна 220 мг/5 мл виробництва ПАТ НВЦ «Борщагівський ХФЗ», є терапевтично еквівалентним референтному препарату.
- Досліджуваний і референтний препарати характеризуються однаково доброю переносимістю у дітей з ГКІ.
Література
1. Complete Proteome of a Quinolone-Resistant Salmonella Typhimurium Phage Type DT104B Clinical Strain / S. Correia, J.D. Nunes-Miranda, L. Pinto [et al.] // Int. J. Mol. Sci. – 2014. – Vol. 15 (8). – P. 14191-14219.
2. Ross K. Reducing Risk of Salmonellosis through Egg Decontamination Processes by Thilini Piushani Keerthirathne / K. Ross, H. Fallowfield, H. Whiley // Int. J. Environ. Res. Public Health. – 2017. – Vol. 14 (3). – P. 335-341.
3. Cunill-De Sautu B. Acute Gastroenteritis Deise Granado-Villar / B. Cunill-De Sautu, A. Granados // Pediatrics in Review. – 2012. – № 33. – Р. 487-497.
4. Brade K.D. Oritavancin: A New Lipoglycopeptide Antibiotic in the Treatment of Gram-Positive Infections / K.D. Brade, J.M. Rybak, M.J. Rybak // Infectious Diseases and Therapy. – 2016. – Vol. 5 (1). – P. 1-15.
5. Гострі кишкові інфекції: захворюваність, етіологічна структура, біологічні властивості збудників / Н.Г. Малиш, М.Д. Чемиш, С.І. Доан [та ін.] // Профілактична медицина. – 2012. – № 3-4 (19). – С. 45-50.
6. Whiley H. Knowledge and Attitudes towards Handling Eggs in the Home: An Unexplored Food Safety Issue? / H. Whiley, B. Clarke, K. Ross // Int. J. Environ. Res. Public Health. – 2017. – Vol. 14 (1). – P. 48-56.
7. Незгода І.І. Гострі кишкові інфекції – актуальні проблеми сьогодення / І.І. Незгода, О.В. Боднарюк // Дитячий лікар. – 2012. – № 8 (21). – С. 34-36.
8. Усенко Д.В. Острые кишечные инфекции у детей в практике педиатра: возможности диагностики и терапии / Д.В. Усенко, А.А. Плоскирева, А.В. Горелов // Вопросы современной педиатрии. – 2014. – 13 (3). – С. 12-20.
9. Clinical and Laboratory Assessment of Dehydration Severity in Children With Acute Gastroenteritis / P.C. Parkin, A. Khambalia, R.D. Goldman [et al.] // Clinical pediatrics. – 2010. – Vol. 49 (3). – P. 235-239.
10. Сміян О.І. Сучасний погляд на клінічну картину гострих кишкових інфекцій у дітей / О.І. Сміян, Т.П. Бинда, К.О. Сміян // Вісник Сумського державного університету. – 2012. – № 2. – С. 142-152.
11. Степанова Ю.Ю. Роль ротавірусної інфекції, що потребує лікування в стаціонарних умовах, при діарейному синдромі у дітей / Ю.Ю. Степанова, О.Л. Кривуша, Л.Л. Петренко // Гастроентерологія. – 2013. – № 4 (50). – С. 74-77.
12. Протокол лікування гострих кишкових інфекцій у дітей / Наказ МОЗ України № 803 від 10.12.2007 р. «Про внесення змін до наказу МОЗ від 09.07.04 р. № 354. – К., 2007. – 22 с.
13. Guarino А.A. Ведение детей с острым гастроэнтеритом на педиатрическом участке / А.A. Guarino, И.Н. Захарова, Н.Г. Сугян // Медицинский совет. – 2016. – № 1. – С. 148-156.
14. Тактика педиатра при лечении острых гастроэнтеритов у детей: что нового? / И.Н. Захарова, А.В. Есипов, Е.А. Дорошина [и др.] // Вопросы современной педиатрии. – 2013. – Т. 12, № 4. – С. 120-125.
15. Managing Acute Gastroenteritis Among Children Oral Rehydration, Maintenance, and Nutritional Therapy / C.K. King, R. Glass, J.S. Bresee [et al.] // Recommendations and Reports. – 2003. – Vol. 52 (16). – Р. 1-16.
16. Treatment of acute gastroenteritis in children: an overview of systematic reviews of interventions commonly used in developed countries / S.B. Freedman, S. Ali, M. Oleszczuk [et al.] // Based Child Health. – 2013. – № 8. – Р. 1123-1137.
Тематичний номер «Педіатрія» №2 (45), червень 2018 р.


