Осінньо-зимовий період – час профілактики не лише респіраторних, а й кардіоваскулярних захворювань
Серцево-судинні захворювання (ССЗ) є основною причиною смерті в усьому світі. За даними Всесвітньої організації охорони здоров’я (ВООЗ), 2019 року від ССЗ померло близько 17,9 млн осіб, що становило майже 32% загальної смертності. У 85% цих випадків їхнє життя переривалося через інфаркт міокарда (ІМ) та інсульт (WHO, 2021). Доведено, що ССЗ мають сезонні коливання щодо частоти захворюваності та рівня смертності – із піком у холодні місяці року, це зумовлено складною взаємодією фізіологічних особливостей організму пацієнта та чинників навколишнього середовища (Stewart et al., 2017).
Таким фізіологічним показникам, як артеріальний тиск (АТ), частота серцевих скорочень, рівень холестерину, маса тіла, параметри запалення та коагуляції, притаманний сезонний характер змін (Ockene et al., 2004; Barnett et al., 2007; Dopico et al., 2015).
Більшість із них є прямим наслідком сезонних коливань тривалості світлового дня, температури та вологості повітря (Dopico et al., 2015; Stewart et al., 2017). Чинники навколишнього середовища можуть мати опосередкований вплив на фізіологічні параметри – через сезонні зміни харчової поведінки та фізичної активності (Ma et al., 2006; Barnett and Dobson, 2010).
Cезонні коливання захворюваності на ССЗ та смертності від них
Ще Гіппократ визнавав, що загальний показник смертності є вищим у прохолодніші місяці, ніж у теплі (Chadwick et al., 1983). У Європі через сезонність загальної смертності трапляється на 16% більше смертей узимку, ніж улітку, що робить це проблемою охорони здоров’я (Healy, 2003). Чітка сезонність щодо кількості смертельних випадків від респіраторних захворювань простежується і через підвищення частоти грипу та інших інфекцій у холодну пору року (von Klot et al., 2012). Подібна картина характерна і для смертності внаслідок ССЗ (Kysely et al., 2009; Reavey et al., 2013).
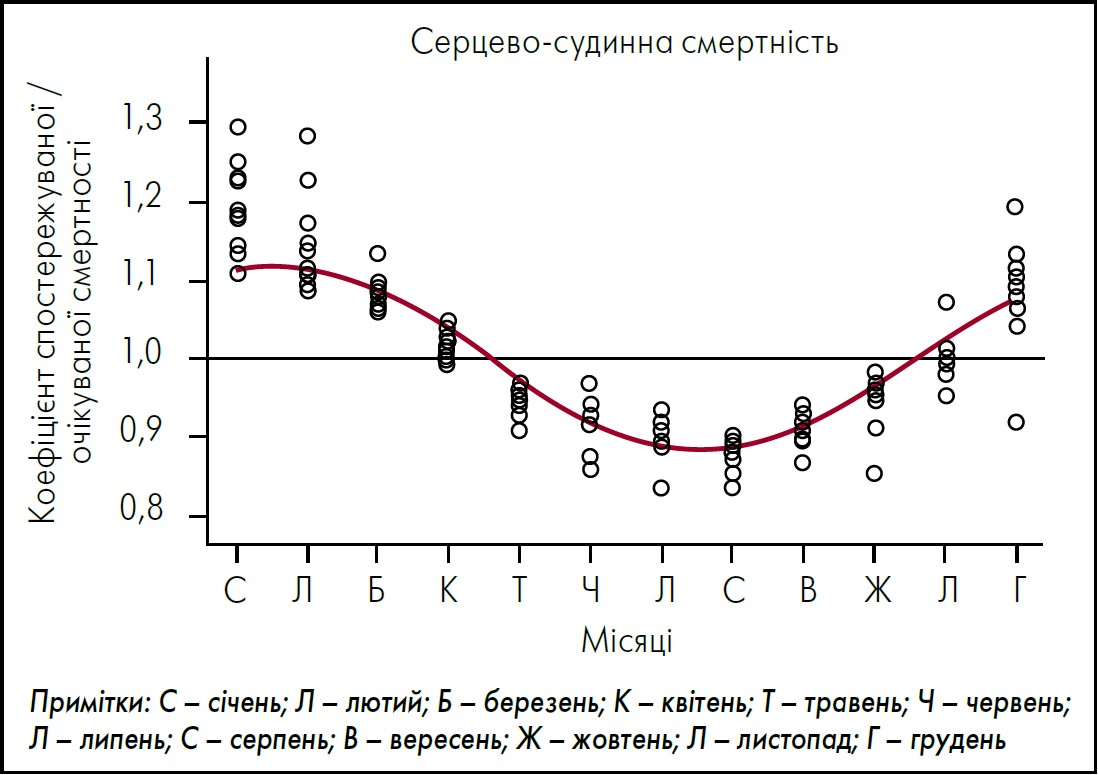
Масштабне дослідження H. Marti-Soler et al. (2014) було присвячене вивченню сезонних коливань загальної та серцево-судинної (СС) смертності в країнах із різним географічним положенням. На підставі аналізу даних про майже 54 млн випадків смертей у 19 країнах світу підтверджено, що СС смертність має стабільну сезонну закономірність. Зокрема, в обох півкулях фіксували вищу кількість смертей у холодний період року, проте така тенденція була суттєво виразнішою в Північній півкулі (рис.). Чинник зниження температури є неєдиним, що зумовлює збільшення показника смертності від ССЗ у холодний період. J.D. Healy (2003), досліджуючи сезонність загальної смертності в 14 європейських країнах, описав «парадокс надмірної кількості смертей узимку»: у найпівнічніших країнах із найхолоднішим кліматом фіксували менш виразну сезонність смертності, ніж у деяких країнах тієї ж півкулі на менш екстремальних широтах. Автор дійшов висновку, що, окрім холоду, на сезонність смертності мають вплив соціально-економічні та житлові умови. Цю гіпотезу підтверджують дані дослідження, у якому встановлено значну нерівність житлових умов у європейських країнах та вибудовано концепцію «залежності від палива» («fuel poverty») (Clinch and Healy, 2000). Суть її полягає в тому, що вплив зовнішньої температури на здоров’я модулюється на індивідуальному рівні різними чинниками, як-от теплоізоляція будинків і якість одягу для захисту від холоду. Тому мешканці країн із дуже низькою температурою взимку (як-от Канада чи скандинавські країни) можуть менше страждати від зимових холодів, ніж ті, хто мешкає в теплих країнах, де будинки менш захищені від холоду (наприклад, у Португалії). Сезонний вплив на АТ також підтверджено результатами багатьох досліджень за участю пацієнтів різного віку, а також здорових осіб і гіпертоніків (Ansa et al., 2008; Sinha et al., 2010; Takenaka et al., 2010). Зокрема, пікові значення як систолічного (САТ), так і діастолічного (ДАТ) АТ припадають на зимовий період, тоді як улітку спостерігається їх спад. Подібні коливання АТ дослідники пов’язують зі змінами таких чинників, як температура повітря, фізична активність, сезонність рівнів вітаміну D, холестерину, норадреналіну, катехоламіну та вазопресину в організмі людини.
Рис. Сезонні коливання співвідношення спостережуваної та очікуваної серцево-судинної смертності в країнах Північної півкулі
Адаптовано за H. Marti-Soler et al. «Seasonal variation of overall and cardiovascular mortality: a study in 19 countries from different geographic locations». PLoS One. 2014 Nov 24; 9 (11): e113500.
Утім, причини підвищення частоти госпіталізації та смертності внаслідок серцевої недостатності (СН) у зимовий період натепер точно не встановлено. Відомо, що похолодання (серед інших чинників) призводить до посилення периферичної вазоконстрикції, що може спричиняти набряк легень унаслідок СН, а також зумовлювати аномальне згортання крові. Наприклад, у пацієнтів із симптоматичною хронічною СН низька температура повітря посилює системну адренергічну активацію. Підвищені концентрації норадреналіну в плазмі крові пов’язані зі збільшенням ризику смерті внаслідок прогресування СН, чим можна частково пояснити зростання показника смертей від ССЗ узимку.
До того ж чинниками ризику сезонного погіршення стану хворих із СН вважаються підвищення АТ, нестача вітаміну D, знижена фізична активність, сезонні вірусні інфекції та забруднення повітря (Barnett et al., 2008).
Також підтверджено наявність сезонних коливань частоти фібриляції передсердь (ФП). Наприклад, за даними популяційного дослідження, проведеного в Данії за участю майже 33 тис. хворих із пароксизмами ФП, встановлено обернено пропорційний вплив температури повітря на частоту проявів ФП (Frost et al., 2002).
Результати дослідження захворюваності на ФП у Японії засвідчили, що її показники є максимальними восени і значно знижуються влітку (Watanabe et al., 2007). Дані низки досліджень у країнах Європи та Ізраїлі продемонстрували залежність ФП від сезонності, підтвердивши, що пік захворюваності припадає на зимові місяці (Viskin et al., 1999; Kupari et al., 1990, Gluszak et al., 2008, 2009; Murphy et al., 2004; Kiu et al., 2004).
Підвищення рівня смертності від ІМ у зимовий період A.M. Masters et al. фіксували ще 1937 року. Сезонність захворюваності та смертності від ІМ особливо притаманна особам літнього віку, причому вона виразніша у чоловіків, ніж у жінок (Manfredini et al., 2008; Abrignani et al., 2009). Коливання таких показників, як АТ, вазоконстрикція, рівні кортизолу та катехоламінів у плазмі крові, агрегація тромбоцитів, гематологічні параметри, асоційовані із сезонним ритмом. Окрім того, потенційними чинниками ризику розвитку ІМ є чинники навколишнього середовища (як-от вологість і температура повітря, атмосферний тиск) та способу життя (фізична активність, режим харчування тощо).
Ще в одному дослідженні, здійсненому в Китаї, вивчали сезонність ризику СС смерті серед госпіталізованих осіб. З’ясувалося, що хворим літнього віку, госпіталізованим у холодну пору року (з листопада до лютого), був притаманний майже на 30‑50% вищий ризик смерті порівняно з пацієнтами, госпіталізованими в теплий сезон. Для хворих молодшого віку подібної сезонної залежності не виявлено. Підвищений показник смертності у холодний період серед літніх пацієнтів був пов’язаний з ішемічною хворобою серця (ІХС), аритміями, СН, ішемічним інсультом та іншими ССЗ. Ризик смерті був вищим взимку, ніж навесні, незалежно від наявності респіраторних захворювань (Beibei et al., 2013).
Можливості підтримки кардіоваскулярної системи та профілактики ССЗ у холодний період року
Вплив кліматичних чинників, передусім зниження температури навколишнього середовища, є вірогідним поясненням спостережуваної сезонності для захворюваності на ССЗ та СС смертності. Також важливим чинником є кількість сонячного світла, від якого залежить рівень вітаміну D (Zittermann et al., 2005). Проте й інші чинники, пов’язані з географічною широтою, також відіграють певну роль, зокрема: звички та особливості харчової поведінки; схильність до інфекційних захворювань; рівень фізичної активності (Faure et al., 2006; Guernier et al., 2004; Matthews et al., 2001).
Очевидно, що на сезонні природні чинники неможливо мати вплив. Тому з настанням холодної пори року слід звертати пильну увагу на чинники ризику ССЗ, які підлягають модифікації. Адекватні фізичні навантаження, належне харчування, контроль АТ, підтримка судинного гомеостазу, контроль рівня холестерину та реологічних параметрів крові, зниження оксидативного стресу – усе це невід’ємні складові сезонної (і не лише) профілактики кардіоваскулярних подій. Важливою умовою такої профілактики є поповнення дефіциту життєво важливих мікро- і макроелементів в організмі людини, оскільки їх нестача призводить до дисбалансу фізіологічних процесів із формуванням патологічних станів і захворювань. Недостатність такого важливого макроелемента, як калій, призводить до порушення електролітного балансу. Результати низки досліджень акцентують увагу на значущості профілактики та корекції дефіциту одного з важливих нутрієнтів через його потенційну роль у патогенезі таких захворювань, як артеріальна гіпертензія (АГ), ІМ, аритмії, церебральний інсульт тощо.
Роль калію у функціонуванні серцево-судинної системи
Калій відіграє ключову роль у багатьох фізіологічних процесах організму людини, його іони залучені до формування клітинних потенціалів дії, скорочення кардіоміоцитів, регуляції та підтримки функції сечовидільної системи. До того ж калій є основним внутрішньоклітинним катіоном, вміст якого в клітині в нормі становить 150‑160 ммоль/л, а в плазмі крові – 3,5‑5,5 ммоль/л. До організму він надходить з їжею та абсорбується через шлунково-кишковий тракт (ШКТ), а його надлишок екскретується нирками; добова потреба дорослої людини у калії – 40‑100 ммоль/л (Федорова, 2014).
Потенційними причинами клінічно значущої гіпокаліємії (<3,6 ммоль/л) є сечогінна терапія, недостатнє надходження калію з їжею, дієта з високим вмістом натрію та гіпомагніємія. Дискаліємія (як гіпо-, так і гіперкаліємія) може перешкоджати ефективному лікуванню, а також підвищувати ризик розвитку аритмій (Komajda et al., 2016).
Гіпокаліємія, зумовлена прийманням тіазидних і петльових діуретиків, яка може призвести до раптової СС смерті пацієнтів з АГ та застійною СН, є незалежним чинником ризику летальних шлуночкових аритмій на тлі гострого ІМ (Gettes, 1992). За даними прогностичного впливу дискаліємії в реальних клінічних умовах, серед 142 087 пацієнтів із нещодавно діагностованою СН гіпокаліємію (<3,5 ммоль/л) на початковому рівні виявлено у 3,0%, гіперкаліємію (≥5,5 ммоль/л) – у 0,9%; 20,4 і 5,7% мали незначну гіпо- і гіперкаліємію (3,5‑3,9 і 5,0‑5,4 ммоль/л відповідно). Підтверджено, що зв’язок зі смертністю відображає U-подібний графік: ризик є найнижчим для значень 4,0‑4,5 ммоль/л. Стійка (>50% вимірювань), періодична (1‑50% вимірювань) і транзиторна (поодинокі вимірювання) дискаліємія впродовж року після діагностування СН також були пов’язані з підвищеним ризиком смерті (Matsushita et al., 2019).
P. Caravaca Perez et al. (2022) також вивчали поширеність дискаліємії, її динамічні зміни та віддалений вплив у госпіталізованих пацієнтів із гострою СН.
Було проаналізовано дані 1779 осіб, розділених на три групи відповідно до рівня калію на момент госпіталізації та в разі виписки: пацієнти з гіпо-, нормо- та гіперкаліємією. Вчені дійшли висновку, що в пацієнтів із гострою СН гіперкаліємія є незалежним предиктором вищої внутрішньолікарняної смертності, а стійка гіпокаліємія та транзиторна гіперкаліємія на момент госпіталізації є незалежними предикторами смерті впродовж року.
Отже, моніторинг та корекція рівня калію є невід’мною частиною стратегії зменшення ризику летальних клінічних подій у коротко- та довгостроковій перспективі.
Препарати для корекції рівня калію
Низький рівень калію у плазмі крові (3,5‑4,0 ммоль/л) потребує відповідної корекції, особливо у пацієнтів із ризиком розвитку аритмії. Шляхи подолання калієвого дефіциту: зниження доз діуретиків без ефекту збереження калію; обмеження споживання натрію; підвищене споживання калієвмісних продуктів; приймання препаратів, діючими речовинами яких є солі калію.
Цитрат калію – ефективний залужнювальний агент, при застосуванні якого збільшується екскреція калію, а його рівень у плазмі практично не змінюється. Його застосування ефективне для залуження сечі за гомозиготної цистинурії (якщо немає тяжкої ниркової недостатності), а також для профілактики нефролітіазу за дистального ниркового тубулярного ацидозу (Fjellstedt et al., 2001; Domrongkitchaiporn et al., 2002). Серед побічних ефектів застосування цитрату калію – нудота, блювання, діарея, біль у шлунку, головний біль і запаморочення.
Аспарагінат калію використовують як для профілактики, так і для лікування ішемічних, гіпоксичних і некротичних процесів; він підвищує витривалість та опірність організму до різних стресових чинників; сприяє надходженню іонів K+ та Mg2+ усередину клітини, відновлюючи адекватну роботу іонних насосів в умовах гіпоксії (Агеев и соавт., 2012). Протипоказанням для його застосування є метаболічний ацидоз, тяжка міастенія, гемоліз, ниркова недостатність. Одночасне приймання з калієзберігальними діуретиками та/або інгібіторами ангіотензинперетворювального ферменту, β-адреноблокаторами, нестероїдними протизапальними препаратами підвищує ризик розвитку гіперкаліємії. Відносно невеликий вихід чистого елементарного калію іноді потребує високого дозування (до 6 таблеток на добу), що підвищує вартість лікування.
Хлорид калію (KCl) використовують для лікування гіпокаліємії, спричиненої як недостатнім споживанням цього елемента, так і різноманітними захворюваннями. Ефективність KCl підтверджено результатами багаторічної практики і відповідних досліджень (Shye, 2018). Приймання замінників харчової солі, які містять KCl, є потенційною стратегією зменшення споживання Na, а отже, зниження АТ. Доведено, що часткове заміщення NaCl такими замінниками сприяє зниженню САТ і ДАТ у середньому на 5,58 і 2,88 мм рт. ст. відповідно, не спричиняючи при цьому гіперкаліємії (Greer et al., 2020).
Як зазначають дослідники, вище споживання калію з їжею пов’язане з нижчою частотою інсультів, зменшенням ризику розвитку ІХС і ССЗ загалом (D’Elia et al., 2011; Jayedi et al., 2019).
Надмірне вживання Na, недостатнє споживання K та низьке співвідношення Na/K є важливими чинниками ризику АГ (Binia et al., 2015; Xu et al., 2020). За рекомендацією ВООЗ, добове споживання Na має становити ≤85 ммоль/добу, а K – ≥90 ммоль/добу (WHO, 2012).
N. Sun et al. (2021) у дослідженні за участю 9501 пацієнта з АГ виявили, що на кожну одиницю збільшення співвідношення Na/K САТ і ДАТ підвищувалися на 0,46 і 0,24 мм рт. ст. відповідно. Отже, зниження коефіцієнта Na/K завдяки зниженню вмісту Na і підвищенню K може сприяти контролю АТ.
Результати низки досліджень свідчать, що обмеження вживання харчової солі та приймання добавок K сприяє зниженню АТ і поліпшенню клінічного прогнозу для пацієнтів із ССЗ (Binia et al., 2015; Filippini et al., 2017; Poorolajal et al., 2017; Sun et al., 2021).
Скоригувати вміст К та інших мікроелементів, які поліпшують роботу судин і серця, допомагає застосування дієтичної добавки Корамаг® (фармацевтична компанія «Асіно»), кожна капсула якого містить 286 мг KCl, а також є додатковим джерелом Mg, коензиму Q10, вітамінів Р і Е. Приймання двох капсул препарату Корамаг® забезпечує організм такою самою кількістю K, як шести таблеток препарату аспарагінату K-Mg, при цьому вартість добавки є суттєво нижчою. Серед поширених побічних ефектів застосування хлориду калію – розлади травлення, проте форма випуску Корамагу (капсули) допомагає уникнути подразнення ШКТ.
Із настанням холодів потреба в підтримці метаболізму та сприянні нормальному обміну речовин стає особливо актуальною через зростання частоти респіраторних інфекцій, до яких додалася останніми роками інфекція SARS-CoV‑2. Підтверджено, що гіпокаліємія підвищує ризик розвитку гострого респіраторного дистрес-синдрому і гострої серцевої травми при COVID‑19 (Lippi et al., 2020; Kumar et al., 2021).
Крім того, українці вже другий пік поспіль живуть в умовах хронічного стресу (постійне відчуття тиску та перевантаження протягом тривалого періоду часу), спричиненого повномасштабним вторгненням РФ і воєнним станом. Як відомо, стресові ситуації (фізичні або емоційні навантаження) в 20‑30% випадках передують загрозливим для життя шлуночковим порушенням ритму. Є припущення, що в умовах хронічного стресу стимуляція симпато-адреналової системи може призводити як до прямого впливу катехоламінів на міокард, так і до опосередкованого – через гіпокаліємію, що отримало назву «стрес-гіпокаліємія» (Батьянова и Иванова, 2011). Тож зміцнення імунітету, приймання вітамінів і мікроелементів, збалансована дієта та підтримка гомеостазу й електролітного балансу набувають додаткової вагомості.
Висновки
Електролітні аномалії, зокрема гіпокаліємія, є потенційними етіологічними чинниками широкого спектра ССЗ. Застосування препаратів і добавок, які сприяють відновленню нормального рівня електролітів, є високоефективною стратегією як профілактики, так і лікування пацієнтів з АГ, ІМ, ІХС, застійною СН та шлуночковими аритміями, а також підтримки нормального обміну речовин в усіх клітинах організму людини.
Препарат Корамаг® може бути рекомендований не лише як дієтична добавка до раціону харчування з метою профілактики ССЗ, особливо актуальної в осінньо-зимовий період, а й для лікування пацієнтів із кардіоваскулярними захворюваннями.
Підготувала Наталія Купко
Тематичний номер «Кардіологія. Ревматологія. Кардіохірургія» № 5 (90) 2023 р.
СТАТТІ ЗА ТЕМОЮ Кардіологія
Як відомо, кальцій бере участь у низці життєво важливих функцій. Хоча більшість досліджень добавок кальцію фокусувалися переважно на стані кісткової тканини та профілактиці остеопорозу, сприятливий вплив цього мінералу є значно ширшим і включає протидію артеріальній гіпертензії (передусім у осіб молодого віку, вагітних та потомства матерів, які приймали достатню кількість кальцію під час вагітності), профілактику колоректальних аденом, зниження вмісту холестерину тощо (Cormick G., Belizan J.M., 2019)....
Торакалгія – симптом, пов’язаний із захворюваннями хребта. Проте біль у грудній клітці може зустрічатися за багатьох інших захворювань, тому лікарям загальної практики важливо проводити ретельну диференційну діагностику цього патологічного стану та своєчасно визначати, в яких випадках торакалгії необхідна консультація невролога. В березні відбувся семінар «Академія сімейного лікаря. Біль у грудній клітці. Алгоритм дій сімейного лікаря та перенаправлення до профільного спеціаліста». Слово мала завідувачка кафедри неврології Харківського національного медичного університету, доктор медичних наук, професор Олена Леонідівна Товажнянська з доповіддю «Торакалгія. Коли потрібен невролог»....
Рівень ліпопротеїну (a) >50 мг/дл спостерігається в ≈20-25% населення і пов’язаний із підвищеним ризиком серцево-судинних захворювань (ССЗ) [1]. Ліпопротеїн (a) задіяний в атерогенезі та судинному запаленні, а також може відігравати певну роль у тромбозі через антифібринолітичну дію і взаємодію із тромбоцитами [2, 3]. Дієта та фізична активність не впливають на рівень ліпопротеїну (a); специфічної терапії для його зниження також не існує. Підвищений ризик ССЗ, пов’язаний з ліпопротеїном (а), залишається навіть у пацієнтів, які приймають статини [4]. Саме тому існує критична потреба в терапії для зниження цього ризику, особливо в первинній профілактиці. ...
Запалення відіграє важливу роль у розвитку багатьох хронічних захворювань, зокрема атеросклерозу. Нещодавно було встановлено, що гіперурикемія спричиняє запалення ендотеліальних клітин судин, ендотеліальну дисфункцію та, зрештою, атеросклероз. Експериментальна робота Mizuno та співавт. (2019), у якій було продемонстровано здатність фебуксостату пригнічувати запальні цитокіни, привернула увагу дослідників до протизапальних ефектів уратзнижувальних препаратів. Кількість лейкоцитів – надійний маркер запалення, пов’язаний із різними кардіоваскулярними захворюваннями, як-от ішемічна хвороба серця; у багатьох попередніх дослідженнях його використовували для оцінки протизапального ефекту терапевтичного втручання. Мета нового аналізу дослідження PRIZE – вивчити вплив фебуксостату на кількість лейкоцитів у пацієнтів із безсимптомною гіперурикемією....