Bacillus clausii – пробиотик выбора для лечения диареи
Пробиотики представляют собой живые микроорганизмы, которые при приеме в адекватном количестве полезны для здоровья человека [1]. Штаммы Bacillus, являющиеся спорообразующими бактериями, активно применяются в качестве пробиотиков на протяжении пяти последних десятилетий. Преимущество спорообразующих пробиотиков перед неспорообразующими (штаммами Lactobacillus) заключается в том, что они являются термостабильными и могут храниться при комнатной температуре без потери жизнеспособности. Спорообразующие бактерии устойчивы к воздействию кислого содержимого желудка (низкому рН) и, следовательно, могут выжить во время транзита к тонкому кишечнику [2, 3]. Данные экспериментальных исследований свидетельствуют, что и споры, и клетки Bacillus clausii (B. clausii) могут прикрепляться к кишечной стенке и колонизировать слизистую оболочку [4]. Три основополагающих обзора предусматривают возможность применения штаммов B. clausii в качестве пробиотиков [5-7]. Наиболее интенсивно исследуются такие штаммы B. clausii, как B. subtilis, B. clausii, B. cereus, B. coagulans и B. licheniformis [8].
Клинические исследования B. clausii
B. clausii представляет собой пробиотик, широко применяющийся в Италии с 1960 г. для лечения вирусной диареи у детей и нивелирования побочных эффектов антибиотикотерапии [9]. Ранее нами было проведено исследование антидиарейной активности штамма UBBC‑07 B. clausii у пациентов с острой диареей (ОД) [10].
В нашем исследовании мы изучали антидиарейную активность штамма UBBC07 B. clausii у пациентов с ОД. В проспективном клиническом исследовании II фазы приняли участие 27 пациентов (средний возраст 35,44±8,08 лет), страдавших ОД. Критерием включения был ≥3-кратный жидкий стул в течение 24 ч на протяжении >7 дней. Всем пациентам рекомендовали принимать одну капсулу, содержавшую штамм UBBC07 B. clausii (2×109 КОЕ), 2 р/сут на протяжении 10 дней. Эффективность терапии оценивали по продолжительности диарейного синдрома, частоте дефекации, интенсивности абдоминальной боли и консистенции каловых масс на 1, 3, 6 и 10 день. Результаты проведенного нами исследования убедительно доказали, что средняя длительность диареи у пациентов, получавших пробиотик, снизилась с 34,81±4,69 до 9,26±3,05 мин/сут (р<0,0001). Кроме того, сократилась частота актов дефекации с 6,96±1,05 до 1,78±0,5 раз/сут (р<0,0001), уменьшилась интенсивность абдоминальной боли с 3,22±0,93 (сильная) до 0,74±0,71 (отсутствие; р<0,0001), улучшилась консистенция кала с 3,93±0,38 (жидкая) до 1,22±0,42 (мягкая; р<0,0001). Значимые статистические межгрупповые различия в безопасности лечения не наблюдались. Наше исследование доказало, что штамм UBBC07 B. clausii представляет собой эффективное средство для нивелирования симптомов диареи, не вызывающее появления каких-либо нежелательных реакций.
Исследования, проведенные другими учеными, подтвердили эффективность и безопасность B. clausii в уменьшении распространенности диареи.
По данным рандомизированного двойного слепого плацебо-контролируемого исследования, терапия B. clausii снижала вероятность появления побочных действий при проведении эрадикации Helicobacter pylori (H. pylori) [20]. В данном трайле изучалось влияние B. clausii на распространенность (основной показатель) и выраженность антибиотикассоциированных побочных действий при проведении антихеликобактерной терапии. Пациенты, инфицированные H. pylori (n=120), были рандомизированы для назначения одной из двух схем лечения. Часть больных получали стандартную 7-дневную тройную терапию рабепразолом (20 мг 2 р/сут), кларитромицином (500 мг 2 р/сут), амоксициллином (1000 мг 2 р/сут) и B. clausii (2×109 КОЕ) начиная с первого дня лечения на протяжении 14 дней. Другим больным была назначена эта же 7-дневная тройная терапия, но с применением плацебо (3 р/сут) также в течение 14 дней. Побочные действия оценивались при помощи валидизированного опросника и регистрировались на протяжении 4 недель после начала лечения. Установлено, что распространенность тошноты, диареи и эпигастральной боли у пациентов, получавших B. clausii, была значительно меньше, чем в группе плацебо.
Таким образом, бактериотерапия с применением B. clausii уменьшает частоту возникновения наиболее распространенных побочных действий (тошноты, диареи, эпигастральной боли), вызванных приемом антибактериальных препаратов при проведении эрадикации H. pylori, по сравнению с плацебо.
Клиническое исследование, анализировавшее эффективность B. clausii в профилактике антибиотикассоциированной диареи (ААД) у филиппинских младенцев и детей младшего возраста, доказало снижение распространенности диареи в группе пациентов, принимавших B. clausii [22]. В этом многоцентровом рандомизированном открытом клиническом исследовании сравнивались две параллельные группы, состоявшие из младенцев и детей младшего возраста, которых рандомизировали для приема пробиотических штаммов B. clausii или отсутствия данного назначения (контрольная группа) одновременно с проведением антибактериальной терапии. Пациенты основной группы получали 2 р/сут по одному флакону, содержавшему споры B. clausii (2×109 КОЕ), в течение 24 ч после начала терапии антибиотиками и продолжали прием пробиотика до последнего дня лечения антибактериальными препаратами. В контрольной группе только наблюдали за результатами лечения. Длительность терапии колебалась от 7 до 21 дня. Состояние пациентов оценивали ежедневно с момента начала антибиотикотерапии и на протяжении еще 45 дней после ее завершения. В контрольной группе было зарегистрировано 7 случаев диареи, в группе B. clausii – 3 (межгрупповые различия статистически недостоверны: р=0,22). Зафиксированная тенденция, хоть и не была статистически значимой, подтверждает уменьшение распространенности ААД на фоне приема B. clausii.
В многоцентровом исследовании, проведенном в Индии, изучалась эффективность вспомогательной терапии B. clausii ОД в педиатрической популяции [23, 24]. В этом проспективном исследовании приняли участие дети, страдавшие ОД и находившиеся на лечении в индийском частном высокоспециализированном госпитале. Пациентов разделили на две группы: первую составили дети, получавшие пероральную регидратационную терапию (ПРТ), цинк и B. clausii (2×109 КОЕ); в состав второй вошли больные, принимавшие только ПРТ и цинк.
Длительность диареи у пациентов первой группы, которые дополнительно принимали пробиотик, составила 22,64 ч, тогда как у больных второй группы, получавших ПРТ и цинк, этот показатель был равен 47,05 ч (р<0,01).
Частота диареи в первой и второй группах уменьшилась, соответственно, через 24 и 60 ч (р<0,001). Средняя длительность стационарного лечения пациентов первой группы составила 2,78 дня, второй – 4,3 дня. Стоимость лечения также значительно снизилась. Вывод, сформулированный в этом исследовании, гласит: «B. clausii сокращают длительность и частоту диареи, а также продолжительность стационарного лечения, уменьшая тем самым стоимость лечения и социальные издержки».
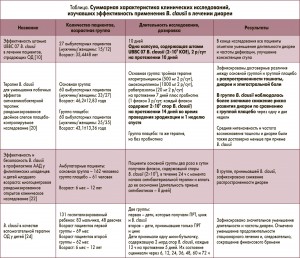
Результаты всех перечисленных исследований приведены в таблице.
Выводы
Клинические преимущества приема пробиотиков связывают в основном с синтезом антимикробных веществ и иммуномодулирующим действием.
B. clausii могут ингибировать рост патогенных микроорганизмов в гастроинтестинальном тракте с помощью трех различных механизмов [21]: колонизации свободных экологических ниш, которые становятся недоступными для роста других микроорганизмов; конкуренции за адгезию к эпителиальным клеткам, что особенно значимо для спор в инициальной или промежуточной фазе роста; синтеза антибиотиков и ферментов, секретируемых в просвет кишечника, в том числе пептидных антибиотиков, активных преимущественно в отношении грамположительных бактерий, и ферментов, проявляющих литическую активность против Pseudomonas aeruginosa. М. Urdaci и соавт. [25] доказали, что B. clausii обладают противомикробными и иммуномодулирующими свойствами. Установлено, что штаммы B. clausii выделяют антимикробные субстанции в окружающую среду. Высвобождение антибактериальных веществ происходит во время фазы стационарного роста и продолжается при спорообразовании. Эти субстанции активны в отношении грамположительных бактерий, в частности Staphylococcus aureus, Enterococcus faecium и Clostridium difficile. Антимикробные вещества устойчивы к действию субтилизина, протеиназы К, химотрипсина, но чувствительны к воздействию проназы. Изучение иммуносупрессивных свойств штаммов B. clausii проводилось в условиях in vitro в культуре клеток мышей швейцарской линии и линии C57 Bl/6j. Ученые [25] доказали, что штаммы B. clausii, находясь в вегетативной форме, способны индуцировать активность NOS II синтетазы, увеличивать синтез интерферона-γ и пролиферацию CD4+ Т-клеток.
На основании вышеупомянутых исследований можно сделать такие выводы: B. clausii – это эффективный пробиотик, который является препаратом выбора для лечения диареи, профилактики ААД и побочных действий, ассоциированных с проведением антихеликобактерной терапии. Этот пробиотик имеет дополнительное преимущество: способность B. clausii образовывать споры делает его весьма устойчивым и стабильным пробиотиком, который может храниться при комнатной температуре.
Печатается в сокращении.
Jayanthi N., Ratna Sudha M. (2015) Bacillus clausii – The Probiotic of Choice in the Treatment of Diarrhoea. J Y Phys Ther 5: 211.
Список литературы находится в редакции.
Перевела с англ. Лада Матвеева
СТАТТІ ЗА ТЕМОЮ Гастроентерологія
Метаболічноасоційована жирова хвороба печінки (МАЖХП) є однією з найактуальніших проблем сучасної гепатології та внутрішньої медицини в цілому. Стрімке зростання поширеності ожиріння та цукрового діабету (ЦД) 2 типу в популяції призвело до істотного збільшення кількості хворих на МАЖХП, яка охоплює спектр патологічних станів від неускладненого стеатозу до алкогольної хвороби печінки та цирозу, що розвиваються на тлі надлишкового нагромадження ліпідів у гепатоцитах. ...
Інфекція Helicobacter pylori (H. pylori) офіційно визнана інфекційним захворюванням і включена до Міжнародної класифікації хвороб (МКХ) 11-го перегляду, тому рекомендовано лікувати всіх інфікованих пацієнтів. Проте, зважаючи на широкий спектр клінічних проявів, пов’язаних із гастритом, викликаним H. pylori, лишаються специфічні проблеми, які потребують регулярного перегляду для оптимізації лікування. ...
Відтворення майбутнього здорової нації – один з найважливіших сенсів існування теперішнього покоління. День боротьби з ожирінням нагадує нам про поширеність цього проблемного явища і важливість попередження його наслідків. Ожиріння може мати вплив на різні аспекти здоров'я, включаючи репродуктивне....
Вивчення клініко-патогенетичних особливостей поєднаного перебігу остеоартрозу (ОА) у хворих із метаболічними розладами, які характеризують перебіг метаболічного синдрому (МС), зокрема цукровим діабетом (ЦД) 2 типу, ожирінням (ОЖ), артеріальною гіпертензією (АГ), є актуальним, оскільки це пов’язано з неухильним збільшенням розповсюдженості цього захворювання, недостатньою ефективністю лікування, особливо за коморбідності з іншими захворюваннями, які патогенетично пов’язані з порушеннями метаболічних процесів. ...