Особливості лікування артеріальної гіпертензії у хворих із хронічною хворобою нирок
За матеріалами XVII Національного конгресу кардіологів (21-23 вересня, м. Київ)
Пацієнти з артеріальною гіпертензією (АГ) і хронічною хворобою нирок (ХХН) належать до категорії найскладніших: відомо, що цільові рівні артеріального тиску (АТ) у них є більш жорсткими, а досягти зниження АТ доволі складно. Отже, ці хворі потребують ретельного вибору антигіпертензивної терапії, яка не тільки має забезпечувати ефективний контроль АТ, а й уповільнювати прогресування порушення ниркової функції.
Як вирішити ці питання, розповіла під час свого виступу завідувач кафедри кардіології та функціональної діагностики Харківської медичної академії післядипломної освіти, доктор медичних наук, професор Віра Йосипівна Целуйко.
Згідно із сучасним визначенням ХХН — це захворювання, яке діагностують у разі, якщо 1) протягом понад 3 міс наявне захворювання нирок із відповідними змінами в аналізах сечі, незалежно від того, спостерігається зниження функції нирок чи ні; 2) протягом понад 3 міс наявне зниження функції нирок при швидкості клубочкової фільтрації (ШКФ) <60 мл/хв незалежно від наявності змін в аналізах сечі.
Нині для лікарів є звичним термін «кардіоренальний континуум»; концепція, завдяки якій він з’явився, продовжує розвиватися, а кількість пацієнтів із ХХН і серцево-судинними (СС) захворюваннями щороку збільшується.
За даними літературних джерел, частота ХХН серед хворих з АГ становить не менш ніж 17-22% (з урахуванням лише ШКФ). Це підтверджують і результати українських досліджень, згідно з якими виразна ниркова дисфункція (стадія ХХН III і вище) трапляється в когорті пацієнтів з АГ у 17% випадків (дослідження «СИСТЕМА», 2015); а серед госпіталізованих пацієнтів з АГ цей показник є ще вищим — 22%.
Слід зауважити, що такі хворі можуть мати вазоренальну гіпертензію, діабетичну нефропатію, вторинну АГ при захворюваннях нирок і, навпаки, ХХН може виникнути внаслідок ураження нирок на тлі АГ.
Іще частіше ХХН діагностують у пацієнтів із «рефрактерною» АГ. За даними G. Thomas і співавт. (2016), 54% хворих на АГ, які не відповідають або погано відповідають на антигіпертензивну терапію, мають виразну ниркову дисфункцію (ШКФ <30 мл/хв). Отже, ХХН — поширений фактор «рефрактерної» АГ, і доволі часто таким хворим досить призначити більш інтенсивну антигіпертензивну терапію, щоб покращити контроль АТ. Згідно із сучасними рекомендаціями всім пацієнтам з АГ слід визначати рівень сироваткового креатиніну, здійснювати оцінку ШКФ, виконувати тест на виявлення білка в сечі за допомогою тест-смужки й оцінювати екскрецію креатиніну із сечею та мікроальбумінурію (клас рекомендацій І, рівень доказовості В).
Не менш часто ХХН діагностують у хворих із клінічними ознаками атеросклерозу: з ішемічною хворобою серця (ІХС), хронічною серцевою недостатністю, хворобою периферичних артерій. У дослідженні EUROPA, у якому взяли участь пацієнти з ІХС, 52% хворих мали ШКФ <75 мл/хв, а частота ниркової дисфункції різного ступеня становила 34-82%. Отже, ураження нирок спричиняє прискорення прогресування атеросклеротичного процесу й кардіоваскулярного континууму, скорочуючи час до розвитку тяжких СС-подій і смерті.
У Практичних клінічних рекомендаціях KDIGO (Kidney Disease: Improving Global Outcomes) з діагностики, класифікації та лікування ХХН (2013) зазначено, що життєвий прогноз пацієнтів із ХХН визначають ступенем виразності альбумінурії та рівнем ШКФ (табл.).
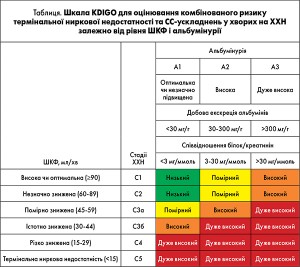
Як можна бачити, частота розвитку СС-ускладнень у пацієнтів із ХХН прогресивно зростає одночасно зі зниженням ШКФ: хворі із ШКФ 30-60 мл/хв мають високий ризик, із ШКФ <30 мл/хв — дуже високий, а кінцева стадія хронічної ниркової недостатності (ХНН) асоціюється з надзвичайно високим ризиком СС-смерті. Ці висновки зроблені на підставі результатів великих рандомізованих контрольованих досліджень та їхніх субаналізів, наприклад дослідження HOT, у якому було встановлено, що частота СС-ускладнень зворотно пропорційна показнику кліренсу креатиніну крові (Jardine et al., 2010). Чітку залежність між ШКФ та ризиком смерті, частотою СС-ускладнень і госпіталізацій встановлено також і в роботі A.S. Go, M. Glenn і співавт. (2004), у котрій аналізували дані, отримані за період із 1996 до 2000 року. В аналіз були включені 1 120 295 пацієнтів, які не отримували гемодіаліз і яким не було виконано трансплантацію нирок. У масштабному дослідженні NHAHES II продемонстровано, що, порівняно з результатами стосовно рівня смертності в групі осіб із ШКФ <90 мл/хв, зниження ШКФ до рівня <70 мл/хв асоційовано з підвищенням ризику смерті від усіх причин на 68%, СС-смерті — на 51%.
На підставі накопичених даних можна стверджувати, що хворі з ХХН мають у 6-12 разів більший ризик померти від СС-ускладнень, аніж дожити до термінальної стадії ниркової недостатності. Серед хворих із ХХН III стадії щороку помирає близько 5% (за 5 років кожний четвертий), а ризик СС-смерті в них є вищим, аніж летального наслідку від ниркової недостатності.
З огляду на це особливу увагу привертають до себе пацієнти з цукровим діабетом (ЦД), для яких є характерною висока частота розвитку нефропатії. Мікроальбумінурія, визнана предиктором розвитку СС-ускладнень, за умови наявності ЦД набуває ще більшого прогностичного значення, у декілька разів підвищуючи ризик ІХС та інсульту, і цей зв’язок посилюється зі збільшенням виразності альбумінурії (Н. Mielton et al., Stroke, 1996). Сучасні рекомендації з лікування хворих на ЦД включають щорічне визначення ступеня альбумінурії: у разі ЦД 1 типу — за умови тривалості захворювання ≥5 років; у разі ЦД 2 типу — від моменту встановлення діагнозу з метою оцінки відповіді на терапію й прогресування хвороби. Незалежно від ступеня виразності альбумінурії в усіх хворих на ЦД рекомендують також щорічно оцінювати рівень креатиніну сироватки крові та ШКФ. При ШКФ <60 мл/хв слід оцінювати й корегувати можливі ускладнення ХХН.
Отже, пацієнти з ХХН належать до категорії високого та дуже високого кардіоваскулярного ризику, і на цьому наголошується в усіх рекомендаціях як із лікування ХХН, так і з лікування СС-захворювань. Зокрема, на цьому акцентують увагу експерти KDIGO і ESH/ESC (Європейського товариства гіпертензії та Європейського товариства кардіологів), які зазначають, що поєднання ХХН і АГ зумовлює необхідність інтенсифікації антигіпертензивної терапії. При цьому цільовий рівень систолічного АТ для пацієнтів із протеїнурією є більш жорстким (<130 мм рт. ст.), аніж для загальної популяції (<140 мм рт. ст.). Антигіпертензивну терапію у цих хворих проводять під контролем ШКФ. Доцільність цих рекомендацій іще раз підтвердили результати нещодавнього метааналізу Х. Xie і співавт. (2016), які продемонстрували зниження частоти як СС-подій, так і ниркових ускладнень на тлі інтенсивної антигіпертензивної терапії.
Відомо, що чим вищий рівень АТ у пацієнтів із ХХН, тим швидше прогресує кардіоваскулярний континуум і вищий ризик виникнення ускладнень. Тож забезпечення ефективного контролю АТ сприяє покращенню прогнозу в пацієнтів з АГ і ХХН.
Проте, крім досягнення цільових рівнів АТ у пацієнтів з АГ і ХНН, ми прагнемо покращити ниркову функцію за рахунок призначення препаратів із доведеним ренопротекторним ефектом.
Згідно з рекомендаціями ESH/ESC 2013 року з лікування АГ для цього слід застосовувати блокатори ренін-ангіотензинової системи (РАС) — інгібітори ангіотензинперетворювального ферменту (ІАПФ) або блокатори рецепторів ангіотензину ІІ (БРА). Крім того, цим хворим із самого початку лікування доцільно призначати раціональні комбінації антигіпертензивних препаратів.
Сучасні рекомендації щодо лікування АГ у хворих із ХХН містять такі положення:
– хворим із ХХН притаманний більш тяжкий перебіг АГ, що часто має рефрактерний характер;
– є докази, що інтенсивна антигіпертензивна терапія має більш відчутний вплив на прогноз цих пацієнтів;
– обов’язковим є призначення інгібіторів РАС (ІАПФ або БРА), які чинять позитивний вплив на функцію нирок;
– для досягнення цільового рівня АТ слід призначати найбільш ефективні препарати та їх комбінації;
– у пацієнтів із вихідним високим АТ слід призначати не менш ніж два антигіпертензивні препарати вже на перших етапах терапії.
У рекомендаціях також вказується на схожий нефропротекторний ефект ІАПФ і БРА, і це підтверджують, зокрема, результати метааналізу Кокранівської бази даних досліджень (2004-2014) щодо ефективності ІАПФ, БРА та інгібіторів реніну в профілактиці СС-ускладнень і термінальної стадії ниркової недостатності. Зазначений метааналіз охопив 85 досліджень за участю 103 120 пацієнтів і продемонстрував схожий вплив ІАПФ та БРА на частоту виникнення ниркових та СС-ускладнень.
Важливий момент, на який, до речі, вказується в Уніфікованому клінічному протоколі первинної, екстреної та вторинної (спеціалізованої) медичної допомоги «Артеріальна гіпертензія» (2016), — необхідність зменшення дози антигіпертензивних препаратів, що екскретуються нирками у пацієнтів із ХХН. До таких препаратів належать бета-адреноблокатори (атенолол, ацебутолол, бетаксолол, бісопролол), а також більшість ІАПФ (за винятком моексиприлу, фозиноприлу, трандолаприлу, спіраприлу). Між іншим, ІАПФ, які найбільш широко призначають в Україні, — каптоприл, лізиноприл, периндоприл, еналаприл, на 90% екскретуються нирками. Згідно з інструкціями щодо застосування лізиноприл не рекомендовано призначати при ХХН, еналаприл слід у таких випадках використовувати з обережністю й у невеликих дозах, периндоприл і раміприл — із корекціями доз залежно від ШКФ. Блокатори кальцієвих каналів (БКК) і БРА не потребують корекції дози під час лікування хворих на ХНН, оскільки виводяться переважно печінкою. Можливість використання цих препаратів у повних дозах значно підвищує шанси на досягнення цільових рівнів АТ у хворих на АГ і ХХН.
Різноманітні клінічні дослідження свідчать про те, що дія ІАПФ та БРА за діабетичної нефропатії абсолютно ідентична, але є думка експертів, що пацієнтам із ЦД 1 типу доцільно призначати ІАПФ, тоді як у пацієнтів із ЦД 2 типу більш виправданим є призначення БРА (J. Lewis et al., 2004). Отже, з метою ефективної нефропротекції цілком виправдано призначати БРА, тим більше що вони забезпечують кращу прихильність хворих до лікування (Clinic Mayo, 2016).
Обираючи препарат для лікування пацієнтів з АГ і ХХН у групі БРА, слід віддавати перевагу представникам останнього покоління, яким характерний виразний і тривалий антигіпертензивний ефект. Серед представників останнього покоління БРА звертає на себе увагу азилсартан (Едарбі), який не тільки продемонстрував більший вплив на АТ порівняно з іншими сартанами (валсартан, олмесартан, кандесартан), а й показав переваги щодо виразності ренопротекторного ефекту навіть у пацієнтів із кінцевою стадією ХХН.
У ході дослідження T. Kusuyama і співавт. (2014) було встановлено, що азилсартан ефективніше знижував АТ, ніж інші БРА, у пацієнтів із ХХН, які отримували гемодіалізну терапію. Згодом цю перевагу було підтверджено й порівняно з іншим БРА останнього покоління — олмесартаном у зниженні АТ у пацієнтів із неконтрольованою АГ, які перебували на гемодіалізі (A. Ukimura et al., 2015). Крім того, у цьому дослідженні встановлено, що азилсартан не впливає на рівень натрію у плазмі крові й не посилює гіперкаліємію.
У ході дослідження K. Kusumoto і співавт. (2011) переведення пацієнтів із нирковою дисфункцією з олмесартану на отримання азилсартану сприяло зменшенню протеїнурії.
Важливо, що пацієнти з будь-яким ступенем ХНН не потребують корекції дози азилсартану, оскільки ступінь ниркової недостатності не впливає на динаміку концентрації в плазмі препарату, хоча подовжує виведення його неактивного метаболіту.
Загалом дані, отримані щодо азилсартану (Едарбі), дають змогу зробити висновок, що цей препарат є більш ефективним порівняно з іншими БРА в лікуванні пацієнтів зі значними труднощами у зниженні АТ, зокрема хворих на ХХН, у тому числі з термінальною стадією ниркової недостатності. Цей ефект може реалізуватися у посиленні прогноз-модифікуючої дії, а також сприяти зниженню ризику смерті у цих хворих.
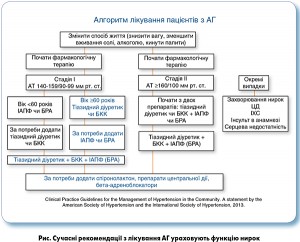
Що стосується раціональних антигіпертензивних комбінацій, які у хворих на АГ із супутньою ХХН рекомендовано застосовувати з перших кроків лікування, то як другий компонент препаратами вибору є тіазидні діуретики та БКК. Це відображено як у европейських, так і в американських і міжнародних рекомендаціях (рис.).
Канадські експерти в оновленому керівництві 2016 року з лікування АГ як адитивну антигіпертензивну терапію у пацієнтів із недіабетичною ХХН рекомендують додавати до блокаторів РАС тіазидні діуретики.
Необхідно пам’ятати, що призначення гідрохлортіазиду й тіазидоподібного діуретика інадапаміду, як і петльового діуретика фуросеміду, обмежено у хворих із тяжкою ХХН. Торасемід протипоказано за наявності порушення функції нирок, що супроводжується анурією. На відміну від них хлорталідон протипоказано лише у разі гострої ниркової недостатності. Цей діуретик у складі фіксованої комбінації, яка містить також азилсартан, найближчим часом буде доступний в Україні (препарат Едарбіклор).
У разі, коли пацієнт із ХХН потребує призначення бета-блокаторів (за спеціальними показаннями), перевагу мають бісопролол і бетаксолол (при кліренсі креатиніну <20 мл/хв максимальна добова доза становить 10 мг). Призначення небівололу таким хворим не рекомендують у зв’язку з відсутністю даних щодо його застосування у пацієнтів із тяжкою ХХН.
Якщо розглянути засоби другого ряду, зокрема групу препаратів центральної дії, то вибір за наявності ХХН може бути зроблено на користь урапіділу, який не має протипоказань у вигляді порушень функції нирок. Моксонідин, що на 90% виводиться нирками, потребує індивідуального підбору дози при ХХН, тому його застосування в цих ситуаціях обмеженіше.
Під час виступу професор В. І. Целуйко озвучила декілька дискусійних питань щодо контролю АТ і навела дані, отримані під час докладного їх вивчення. Одне з них — доцільність призначення інтенсивної антигіпертензивної терапії в осіб без АГ або з АГ легкого ступеня з помірним СС-ризиком. Дослідження HOPE‑3 мало на меті визначення можливостей зниження ризику СС-ускладнень у пацієнтів із помірним ризиком їх розвитку. У ході цього дослідження було встановлено, що призначення комбінованої терапії БРА і тіазидним діуретиком сприяло зниженню ризику СС-смерті і СС-подій, і особливо виразним цей ефект був у пацієнтів із рівнем систолічного АТ >143 мм рт. ст. Крім того, зазначено, що на тлі лікування антигіпертензивними препаратами прогресування ХХН відбувалося дещо рідше (2,1 проти 0,8% у групі плацебо).
Результати дослідження продемонстрували доцільність раннього застосування комбінації БРА і тіазидного діуретика в лікуванні пацієнтів із помірним СС-ризиком, серед яких можуть бути й хворі з початковими стадіями АГ і ХХН.
На завершення виступу професор В. І. Целуйко озвучила декілька основних висновків, які допоможуть лікарю визначитися з тактикою ведення пацієнтів з АГ і ХНН:
1. Порушення функції нирок істотно впливає на розвиток СС-ускладнень, а ризик СС-смерті у пацієнтів із ХХН значно перевищує ризик смерті від ниркової недостатності.
2. Контроль АТ не тільки поліпшує прогноз стосовно СС-ускладнень, а й забезпечує покращення перебігу ХНН.
3. Інтенсивна антигіпертензивна терапія у хворих з АГ і ХХН має переваги над стандартною терапією.
4. Під час лікування хворих на ХХН слід віддавати перевагу препаратам, які сприяють зниженню активності РАС.
5. З-поміж БРА азилсартан (Едарбі) чинить найістотніший позитивний вплив на АТ, у тому числі у пацієнтів із ХХН.
6. Азилсартан продемонстрував вищу ефективність у контролі АТ порівняно з іншими БРА у найтяжчих хворих, яким проводять гемодіаліз.
Підготувала Наталя Очеретяна
Статтю надруковано за сприяння
ТОВ «Такеда Україна».
UA/AZI/1216/0021
СТАТТІ ЗА ТЕМОЮ Кардіологія
Як відомо, кальцій бере участь у низці життєво важливих функцій. Хоча більшість досліджень добавок кальцію фокусувалися переважно на стані кісткової тканини та профілактиці остеопорозу, сприятливий вплив цього мінералу є значно ширшим і включає протидію артеріальній гіпертензії (передусім у осіб молодого віку, вагітних та потомства матерів, які приймали достатню кількість кальцію під час вагітності), профілактику колоректальних аденом, зниження вмісту холестерину тощо (Cormick G., Belizan J.M., 2019)....
Торакалгія – симптом, пов’язаний із захворюваннями хребта. Проте біль у грудній клітці може зустрічатися за багатьох інших захворювань, тому лікарям загальної практики важливо проводити ретельну диференційну діагностику цього патологічного стану та своєчасно визначати, в яких випадках торакалгії необхідна консультація невролога. В березні відбувся семінар «Академія сімейного лікаря. Біль у грудній клітці. Алгоритм дій сімейного лікаря та перенаправлення до профільного спеціаліста». Слово мала завідувачка кафедри неврології Харківського національного медичного університету, доктор медичних наук, професор Олена Леонідівна Товажнянська з доповіддю «Торакалгія. Коли потрібен невролог»....
Рівень ліпопротеїну (a) >50 мг/дл спостерігається в ≈20-25% населення і пов’язаний із підвищеним ризиком серцево-судинних захворювань (ССЗ) [1]. Ліпопротеїн (a) задіяний в атерогенезі та судинному запаленні, а також може відігравати певну роль у тромбозі через антифібринолітичну дію і взаємодію із тромбоцитами [2, 3]. Дієта та фізична активність не впливають на рівень ліпопротеїну (a); специфічної терапії для його зниження також не існує. Підвищений ризик ССЗ, пов’язаний з ліпопротеїном (а), залишається навіть у пацієнтів, які приймають статини [4]. Саме тому існує критична потреба в терапії для зниження цього ризику, особливо в первинній профілактиці. ...
Запалення відіграє важливу роль у розвитку багатьох хронічних захворювань, зокрема атеросклерозу. Нещодавно було встановлено, що гіперурикемія спричиняє запалення ендотеліальних клітин судин, ендотеліальну дисфункцію та, зрештою, атеросклероз. Експериментальна робота Mizuno та співавт. (2019), у якій було продемонстровано здатність фебуксостату пригнічувати запальні цитокіни, привернула увагу дослідників до протизапальних ефектів уратзнижувальних препаратів. Кількість лейкоцитів – надійний маркер запалення, пов’язаний із різними кардіоваскулярними захворюваннями, як-от ішемічна хвороба серця; у багатьох попередніх дослідженнях його використовували для оцінки протизапального ефекту терапевтичного втручання. Мета нового аналізу дослідження PRIZE – вивчити вплив фебуксостату на кількість лейкоцитів у пацієнтів із безсимптомною гіперурикемією....