Пероральные антикоагулянты при фибрилляции предсердий: из исследований – в повседневную практику
В августе этого года медицинской общественности были представлены обновленные практические рекомендации Европейского общества кардиологов (ЕОК) по ведению пациентов с фибрилляцией предсердий (ФП), и, безусловно, в этом руководстве обязательным компонентом стратегии лечения пациентов с ФП остается продолжительная антикоагулянтная терапия с целью предотвращения кардиоэмболического инсульта и других системных эмболий.
В течение почти 10 лет кардиологи имеют возможность назначать инновационные пероральные антикоагулянты (НОАК), которые по многим свойствам превосходят препараты класса антагонистов витамина К (АВК), и сегодня мы задаемся вопросом: как за это время изменилась клиническая практика?
Модератор рубрики, член-корреспондент НАМН Украины, руководитель отдела реанимации и интенсивной терапии ННЦ «Институт кардиологии им. Н.Д. Стражеско» НАМН Украины, доктор медицинских наук, профессор Александр Николаевич Пархоменко:
– Ровно 10 лет назад Управление по контролю за продуктами питания и лекарственными средствами США (FDA) выразило обеспокоенность недостаточным назначением АВК пациентам с ФП и высоким риском развития инсульта. По данным исследования Euro Heart Survey, около 40% больных не получали антитромботическую терапию или принимали только антиагреганты, которые не обеспечивают должной защиты (R. Nieuwlaat et al., 2006). В следующие 5-6 лет параллельно несколько компаний вывели на фармацевтический рынок четыре препарата нового класса прямых пероральных антикоагулянтов: ингибитор тромбина дабигатран и ингибиторы Xa-фактора ривароксабан, апиксабан и эдоксабан. В международных рандомизированных исследованиях все НОАК не уступали варфарину по эффективности профилактики инсульта и вызывали меньше опасных кровотечений, кроме того, их применение ассоциировалось со снижением общей смертности, в результате чего все они были одобрены по показанию профилактики инсульта у пациентов с ФП в США и Европе.
Регистр ORBIT-AF развеял миф о пациенте со стабильным МНО (международное нормированное отношение) при приеме варфарина. Даже если в течение 6 мес 100% значений МНО находились в терапевтическом диапазоне (что наблюдалось лишь у 1 пациента из 4), это не гарантировало такой же стабильности антикоагулянтного эффекта в последующий год наблюдения: у 92% этих пациентов по крайней мере 1 измерение МНО не попало в терапевтический диапазон. Действительно, на практике очень трудно проконтролировать, как пациент принимает варфарин, его взаимодействие с другими препаратами при одновременном приеме, фактор питания. Кроме того, дополнительный анализ результатов исследований ARISTOTLE, ROCKET-AF, RE-LY показал, что стабильное МНО не предотвращает развитие больших кровотечений при приеме варфарина. Повышение качества терапии с достижением высокого процента времени в терапевтическом диапазоне антикоагуляции (до 75%) уменьшало частоту тромбоэмболических событий, но не число больших кровотечений. Эти данные еще раз заставляют нас обратить внимание на преимущества НОАК.
Справедливо было ожидать, что врачи будут активно использовать НОАК как эффективный инструмент для того, чтобы кардинально изменить ситуацию в области антикоагулянтной защиты пациентов с ФП к лучшему. Однако один из крупнейших в мире регистров ФП PINNACLE, содержащий данные почти полумиллиона пользователей медицинских услуг в США, показал, что и на сегодняшний день лишь каждый второй пациент с риском развития инсульта 3 балла и выше по шкале CHA2DS2-VASc принимает пероральные антикоагулянты, а половина пациентов не получают тромбопрофилактику вообще или принимают только ацетилсалициловую кислоту (АСК). В настоящее время продолжаются проспективные наблюдательные исследования и регистры, которые специально спланированы для оценки качества терапии ФП в условиях рутинной практики. В международном регистре GARFIELD с 2011 г. участвуют и украинские клинические центры, а всего насчитывается 35 стран-участниц. В Украине были набраны 1340 пациентов, и совокупный анализ данных участников трех когорт регистра с 2011 по 2016 г. дает возможность сравнивать особенности терапии ФП в украинской популяции с мировыми тенденциями.
В Европе в среднем 70% пациентов назначают АВК, ингибиторы Xa-фактора или дабигатран в сочетании или без антитромбоцитарных средств. В Украине около 50% пациентов с ФП принимают лишь антитромбоцитарные препараты, и только у 45% в схему терапии входят пероральные антикоагулянты. Мировые показатели – в среднем 65 и 25% соответственно. По сравнению с мировыми данными регистра наши пациенты моложе, среди них больше лиц имеют проявления сердечной недостаточности (СН) и ишемической болезни сердца (ИБС). По риску развития инсульта и кровотечений украинская популяция не выделяется на фоне общемировых данных. Оказалось, что процент назначений пероральных антикоагулянтов украинским пациентам не зависит от величины риска (баллов по шкале CHA2DS2-VASc), хотя во всем мире прослеживается логика назначений: чем выше риск, тем больше пациентов принимают антикоагулянты. Обратная закономерность выявлена в зависимости от риска кровотечений: чем он выше у украинских пациентов, тем реже врачи назначают антикоагулянты. При оценке в 4 и более баллов по шкале HAS-BLED антикоагулянты вообще не назначаются. В мировой практике повышенный геморрагический риск не мешает применять пероральные антикоагулянты у большинства пациентов с риском инсульта. Таким образом, в Украине профиль назначений антитромботической терапии при ФП несколько отличается от мирового опыта более осторожным и консервативным подходом. Но высокий балл по шкале HAS-BLED – не повод отказываться от антикоагулянтной защиты, а лишь сигнал о необходимости более внимательного отношения к индивидуальным факторам риска.
Для нас большую ценность представляют результаты пострегистрационных исследований НОАК, которые могут помочь врачам пересмотреть свои взгляды на антикоагулянтную терапию при ФП и адекватно защитить от инсульта больше пациентов. Так, результаты рандомизированного исследования ROCKET-AF относительно профиля безопасности и эффективности ривароксабана хорошо согласуются с данными разных типов исследований в условиях реальной практики, которые были проведены позднее, а также продолжаются в настоящее время. Это проспективное наблюдательное исследование XANTUS, регистр GARFIELD, Дрезденский регистр НОАК, а также ретроспективные исследования и анализы баз данных страховых компаний (US PMSS, RELIEF, REVISIT US). Они подтверждают правильность схемы дозирования ривароксабана, выбора сниженной дозы 15 мг/сут для пациентов с дисфункцией почек, ценность однократного приема для обеспечения высокой приверженности пациентов и показывают, что в случае соблюдения этих правил и рекомендаций можно достигать результатов, полученных в идеальных условиях клинического исследования, – высокой эффективности тромбопрофилактики при минимальном риске геморрагических осложнений.
Большую актуальность сегодня приобретают вопросы применения пероральных антикоагулянтов у пациентов с ФП и коморбидными состояниями. В Украине постепенно накапливается опыт в области лечения таких больных, о чем свидетельствуют представленные ниже клинические примеры из реальной практики.
Клинические примеры: принципы выбора пероральных антикоагулянтов для пациентов с ФП и коморбидными состояниями

Доктор медицинских наук, профессор Андрей Владимирович Ягенский (Волынский областной центр кардиоваскулярной патологии, г. Луцк):
– Мерцательная аритмия редко бывает изолированной, и сочетание ФП с фоновыми заболеваниями – это реальность повседневной практики. По данным зарубежных исследователей, в популяции пациентов с ФП распространенность СН составляет 50%, артериальной гипертензии (АГ) – 72%, ИБС – 32%, сахарного диабета – 21%, почечной недостаточности – 15%, цереброваскулярных заболеваний – 11% (J. Camm et al., 2010).
ФП и СН – это взаимообусловливающие состояния со сложными и не всегда очевидными патогенетическими связями. У таких пациентов ограничен выбор антиаритмических препаратов, но антикоагулянтная терапия должна стать обязательным компонентом стратегии лечения. Согласно новым рекомендациям ЕОК по ведению ФП (ЕОК-2016) без антитромботической терапии можно оставить только пациентов с оценкой «0» по шкале риска развития инсульта CHA2DS2-VASc, а у пациентов с оценкой в 1 балл следует рассмотреть возможность назначения перорального антикоагулянта на длительный срок. Наличие СН уже обеспечивает этот балл.
В связи с наличием коморбидных заболеваний возникает вопрос: какой из антикоагулянтов будет оптимальным для данного конкретного пациента? Кроме того, вопрос рационального выбора и применения пероральных антикоагулянтов всегда актуален с учетом необходимости лечения самой ФП (проведения кардиоверсии, приема антиаритмических препаратов для удержания синусового ритма) и возможных лекарственных взаимодействий.
В исследовании ROCKET-AF, в ходе которого сравнивали эффективность и безопасность ривароксабана с варфарином у пациентов с ФП, СН или сниженная фракция выброса левого желудочка (ФВ ЛЖ) была диагностирована у 63,7% популяции (9033 пациента). Среди пациентов с СН эффективность ривароксабана в профилактике инсульта и системной эмболии не зависела от ФВ (<40% или ≥40%) и функционального класса (ФК) по NYHA (I-II против III-IV). Во всех подгруппах ривароксабан по безопасности и эффективности тромбопрофилактики не уступал варфарину. Эти данные подтверждают, что назначение ривароксабана является альтернативой варфарину у пациентов с СН и ФП (S. van Diepen et al., 2013).
Комментируя алгоритм тромбопрофилактики согласно новым рекомендациям ЕОК-2016, профессор А.В. Ягенский напомнил, что варфарин остается безальтернативным антикоагулянтом только для пациентов с механическими клапанами сердца или митральным стенозом средней и высокой степени. Остальные заболевания клапанов сердца, например пороки аортального клапана, не должны быть препятствием к назначению НОАК. В связи с этим термин «неклапанная» ФП в контексте показаний к антикоагулянтной терапии выглядит не совсем корректно, несмотря на то что традиционно применяется.
Клинический пример № 1
Пациентка С., 69 лет. Перенесла инфаркт миокарда (ИМ) 4 года назад. СН II-III ФК по NYHA. Персистирующая ФП, за последний год перенесла 4 эпизода. Восстановление синусового ритма достигалось амиодароном. Постоянно принимает амиодарон по 200 мг/сут в течение последних 3 мес. Поступила с ухудшением СН (усиление одышки, отеки), которое наступило после физической перегрузки. Во время госпитализации сохраняется синусовый ритм с частотой сердечных сокращений (ЧСС) 88 уд/мин, артериальное давление (АД) – 130/88 мм рт. ст.
При выборе дальнейшей стратегии ведения пациентки необходимо ответить на следующие вопросы:
– нужно ли назначать антикоагулянты всем пациентам с персистирующей формой ФП и нечастыми пароксизмами?
– влияет ли частота пароксизмов на выбор антикоагулянта?
– влияет ли степень тяжести СН на выбор антикоагулянта?
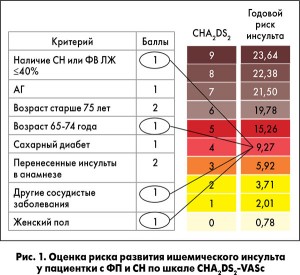
Профессор А.В. Ягенский напомнил, что антикоагулянтная терапия для профилактики инсульта необходима независимо от клинической формы ФП. По данным ряда исследований, риски развития инсульта существенно не различаются у пациентов с постоянной, персистирующей, пароксизмальной формами и при впервые выявленной ФП (R. Nieuwlaat et al., 2008). Значение частоты пароксизмов остается дискуссионным, однако у данной пациентки играет роль не столько частота пароксизмов ФП, сколько общая оценка риска инсульта с учетом наличия СН и ИБС. При оценке по шкале CHA2DS2-VASc пациентка набирает 4 балла, что соответствует высокому риску развития инсульта – 9% в год и является абсолютным показанием к назначению профилактики антикоагулянтами (рис. 1).
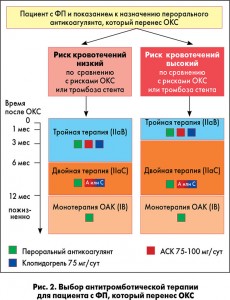
Согласно новым рекомендациям ЕОК-2016 о проведении антитромботической терапии у пациентов с ФП, перенесших острый коронарный синдром (ОКС), пациентке С. показан только пероральный антикоагулянт. Необходимости в дополнительном назначении антитромбоцитарных препаратов нет, поскольку ИМ она перенесла 4 года назад (рис. 2).
Ввиду того что пациентка постоянно принимает амиодарон для профилактики пароксизмов ФП, варфарин не является оптимальным выбором. Известно, что амиодарон с варфарином вступает в нежелательные фармакокинетические взаимодействия, в результате чего повышается концентрация последнего в плазме крови и увеличивается риск кровотечения. Еще в 1980-х годах было установлено, что при совместном приеме этих препаратов дозу варфарина следует уменьшать пропорционально дозе амиодарона: на 35% при суточной дозе амиодарона 200 мг и на 50% при суточной дозе амиодарона 400 мг (A. Hamer et al., 1982; S. Almog et al., 1985; C.A. Sanoski et al., 2002). И безусловно, необходимо регулярно контролировать МНО на фоне приема варфарина и амиодарона.
Лекарственные взаимодействия инновационных пероральных антикоагулянтов показаны в таблице 1.
Из таблицы видно, что для пациентов, принимающих амиодарон или блокаторы кальциевых каналов, оптимальным вариантом является ривароксабан, поскольку у пациентов без почечной недостаточности он практически не взаимодействует с указанными препаратами.
Клинический пример № 2
Пациент 45 лет с дилатационной кардиомиопатией. Постоянная форма ФП 4 года. СН III ФК по NYHA, признаки застоя в малом круге кровообращения. АД – 100/74 мм рт. ст., ЧСС – 122 уд/мин. На момент осмотра принимает рамиприл 2,5 мг, бисопролол 5 мг, спиронолактон 25 мг, торасемид 20 мг.
В данном случае обращает на себя внимание высокая частота сокращения желудочков (ЧСЖ) на фоне постоянной ФП у относительно молодого пациента. Перспектива восстановления синусового ритма сомнительна ввиду большой давности мерцательной аритмии и миопатической этиологии заболевания. Возникают следующие вопросы:
– что дополнительно назначить для уменьшения ЧСЖ: дигоксин или амиодарон?
– влияет ли ЧСЖ при постоянной ФП на выбор антикоагулянта?
Дигоксин в данном случае является оптимальным выбором для контроля ЧСЖ, поскольку при исходно низких показателях АД вряд ли удастся увеличить дозу бета-блокатора.
Сама по себе ЧСЖ не является критерием выбора антикоагулянта, однако если пациенту дополнительно назначен дигоксин, то следует учитывать лекарственные взаимодействия. Дигоксин влияет на концентрацию варфарина, а для НОАК показано отсутствие значимых взаимодействий с дигоксином. Дальнейший выбор конкретного препарата из этого класса зависит от степени тяжести СН и поражения органов-мишеней.
У многих пациентов с СН встречается нарушение функции почек, распространенность которого пропорциональна функциональному классу: от 15-25% у пациентов с ФК II до 40-70% в популяции ФК IV. Профессор А.В. Ягенский обратил внимание на то, что почечная дисфункция у пациентов с СН часто недооценивается на фоне успехов диуретической терапии и других, доминирующих в клинической картине симптомов и признаков. Печень также вовлечена в патофизиологические процессы при СН, поэтому нарушения функции печени, определяемые по уровню билирубина, активности трансаминаз и гамма-глутамилтранспептидазы, у данной категории больных встречаются почти так же часто, как и почечная недостаточность: от 10-20% при ФК СН II до 30-50% при ФК IV. Нарушение работы печени приводит не только к ослаблению путей ферментативной метаболизации препаратов, но и к нарушению синтеза белков, в частности белков системы свертывания крови. Таким образом, пациент с тяжелой СН и печеночной недостаточностью находится в состоянии хронической гипокоагуляции со склонностью к развитию кровотечений.
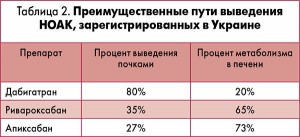
В связи с нарушением функции почек и печени у пациентов с ФП и СН особое значение приобретают пути метаболизации антикоагулянтов и вопросы контроля свертываемости крови. В данном случае достаточно сложно обеспечить удержание терапевтического диапазона МНО на фоне приема варфарина, поэтому оптимальным решением станет назначение НОАК. Для трех НОАК, доступных в Украине, пути выведения показаны в таблице 2.
Ривароксабан характеризуется наиболее сбалансированным соотношением путей выведения, поэтому он может быть предпочтительным для пациентов с тяжелой СН. У лиц с сохранной функцией почек и признаками печеночной недостаточности теоретически обосновано применение дабигатрана (кроме пациентов, у которых уровень трансаминаз не превышает 2 верхние границы нормы и отсутствует цирроз печени, влияющий на выживаемость больных). Но в реальной практике такие пациенты встречаются редко.
В заключительной части лекции профессор А.В. Ягенский напомнил о необходимости регулярного контроля функции почек по клиренсу креатинина (CrCl) на фоне терапии НОАК. При исходном CrCl >60 мл/мин достаточно повторных визитов 1 раз в год, при CrCl 30-60 мл/мин – раз в 6 мес, при CrCl <30 мл/мин – каждые 3 мес. Для пациентов с СН не разработано особых рекомендаций по мониторированию функции почек на фоне приема НОАК, однако докладчик предложил сократить указанные выше интервалы в 2 раза, поскольку при СН состояние почек может динамично меняться и требует более тщательного контроля.
Подготовил Дмитрий Молчанов
СТАТТІ ЗА ТЕМОЮ Кардіологія
Як відомо, кальцій бере участь у низці життєво важливих функцій. Хоча більшість досліджень добавок кальцію фокусувалися переважно на стані кісткової тканини та профілактиці остеопорозу, сприятливий вплив цього мінералу є значно ширшим і включає протидію артеріальній гіпертензії (передусім у осіб молодого віку, вагітних та потомства матерів, які приймали достатню кількість кальцію під час вагітності), профілактику колоректальних аденом, зниження вмісту холестерину тощо (Cormick G., Belizan J.M., 2019)....
Торакалгія – симптом, пов’язаний із захворюваннями хребта. Проте біль у грудній клітці може зустрічатися за багатьох інших захворювань, тому лікарям загальної практики важливо проводити ретельну диференційну діагностику цього патологічного стану та своєчасно визначати, в яких випадках торакалгії необхідна консультація невролога. В березні відбувся семінар «Академія сімейного лікаря. Біль у грудній клітці. Алгоритм дій сімейного лікаря та перенаправлення до профільного спеціаліста». Слово мала завідувачка кафедри неврології Харківського національного медичного університету, доктор медичних наук, професор Олена Леонідівна Товажнянська з доповіддю «Торакалгія. Коли потрібен невролог»....
Рівень ліпопротеїну (a) >50 мг/дл спостерігається в ≈20-25% населення і пов’язаний із підвищеним ризиком серцево-судинних захворювань (ССЗ) [1]. Ліпопротеїн (a) задіяний в атерогенезі та судинному запаленні, а також може відігравати певну роль у тромбозі через антифібринолітичну дію і взаємодію із тромбоцитами [2, 3]. Дієта та фізична активність не впливають на рівень ліпопротеїну (a); специфічної терапії для його зниження також не існує. Підвищений ризик ССЗ, пов’язаний з ліпопротеїном (а), залишається навіть у пацієнтів, які приймають статини [4]. Саме тому існує критична потреба в терапії для зниження цього ризику, особливо в первинній профілактиці. ...
Запалення відіграє важливу роль у розвитку багатьох хронічних захворювань, зокрема атеросклерозу. Нещодавно було встановлено, що гіперурикемія спричиняє запалення ендотеліальних клітин судин, ендотеліальну дисфункцію та, зрештою, атеросклероз. Експериментальна робота Mizuno та співавт. (2019), у якій було продемонстровано здатність фебуксостату пригнічувати запальні цитокіни, привернула увагу дослідників до протизапальних ефектів уратзнижувальних препаратів. Кількість лейкоцитів – надійний маркер запалення, пов’язаний із різними кардіоваскулярними захворюваннями, як-от ішемічна хвороба серця; у багатьох попередніх дослідженнях його використовували для оцінки протизапального ефекту терапевтичного втручання. Мета нового аналізу дослідження PRIZE – вивчити вплив фебуксостату на кількість лейкоцитів у пацієнтів із безсимптомною гіперурикемією....