Запальні захворювання кишечнику: експертна думка та практичні аспекти
Щороку 19 травня у світі вже традиційно відзначається Міжнародний день боротьби з запальними захворюваннями кишечнику (ЗЗК), на які, згідно з експертними оцінками, лише в Європі хворіє не менше ніж 3 млн осіб. Символом підтримки людей, котрі живуть із ЗЗК, стала фіолетова стрічка. 18 травня в м. Києві відбулася науково-практична конференція «Запальні захворювання кишечнику: сучасні підходи до діагностики та лікування», у рамках якої вітчизняні експерти у сфері лікування ЗЗК поділилися своїм досвідом ведення таких хворих та обговорили останні досягнення в діагностиці та лікуванні цієї патології.
Роботу конференції розпочав доцент кафедри гастроентерології, дієтології та ендоскопії Національної медичної академії післядипломної освіти імені П.Л. Шупика, кандидат медичних наук Ігор Ярославович Лопух. Спираючись на сучасні рекомендації Європейської організації з вивчення хвороби Крона та виразкового коліту (ЕССО) й інших профільних товариств, він розповів про шляхи подолання труднощів у діагностиці ЗЗК.
 – Основними документами, що сьогодні регламентують ведення пацієнтів із ЗЗК в Україні, є Уніфікований клінічний протокол первинної, вторинної (спеціалізованої) та третинної (високоспеціалізованої) медичної допомоги «Запальні захворювання кишечнику (хвороба Крона, виразковий коліт)», затверджений наказом МОЗ України від 11.02.2016 № 90, а також видані у 2017 р. рекомендації ЕССО.
– Основними документами, що сьогодні регламентують ведення пацієнтів із ЗЗК в Україні, є Уніфікований клінічний протокол первинної, вторинної (спеціалізованої) та третинної (високоспеціалізованої) медичної допомоги «Запальні захворювання кишечнику (хвороба Крона, виразковий коліт)», затверджений наказом МОЗ України від 11.02.2016 № 90, а також видані у 2017 р. рекомендації ЕССО.
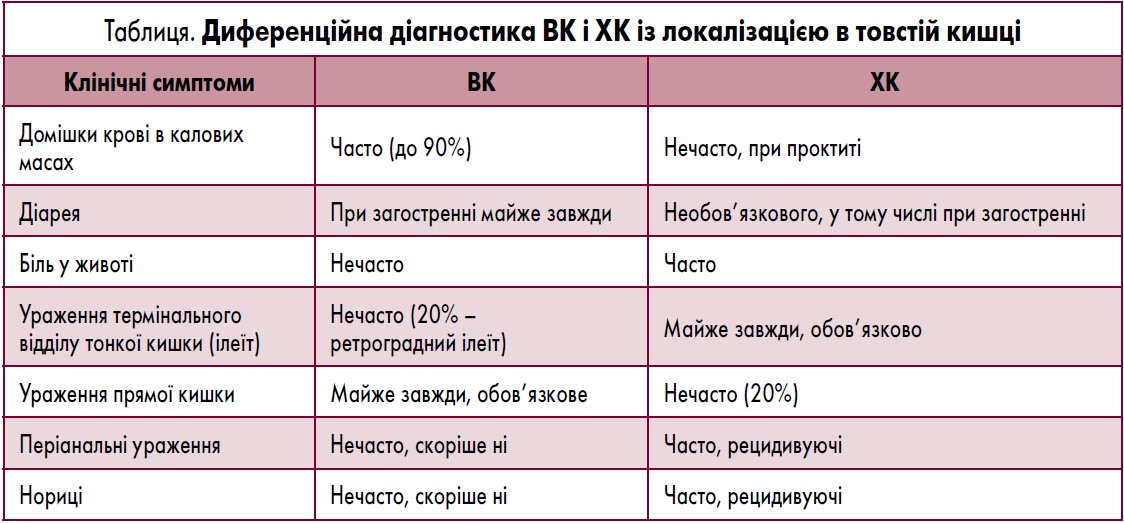
Симптоми виразкового коліту (ВК) залежать від протяжності й тяжкості ураження і, як правило, включають криваву діарею, ректальні кровотечі, невідкладні позиви до дефекації, тенезми, нетримання калу. Часто наявні нічні симптоми, що особливо важливо в осіб молодого віку при проведенні диференційної діагностики з синдромом подразненого кишечнику. Натомість симптоми хвороби Крона (ХК) є дуже гетерогенними і часто включають абдомінальний біль, немотивовану втрату маси тіла та хронічну діарею. Такі симптоми повинні викликати підозру щодо ХК, особливо в молодих осіб. Частими проявами ХК є слабкість, анорексія, лихоманка. Складним клінічним завданням є диференційна діагностика ВК і ХК, що перебігає з ураженням товстої кишки, проте можна виділити низку ознак, які допомагають правильно спрямувати подальший процес верифікації діагнозу (табл.).
Також усім клініцистам обов’язково слід пам’ятати про цілу низку позакишкових проявів та ускладнень, які можуть виявлятися у пацієнтів із ЗЗК одночасно з ознаками ураження кишечнику, а в деяких випадках навіть домінувати у клінічній картині, змушуючи пацієнта спочатку звертатися не до гастроентеролога, а до лікарів інших спеціальностей (алергологів, дерматологів, неврологів, ревматологів, офтальмологів та ін.). До них, зокрема, належать:
- ураження шкіри: вузлувата еритема, гангренозна піодермія, васкуліти;
- ураження суглобів: артрит, сакроілеїт, анкілозуючий спондиліт;
- ураження очей: склерит, епісклерит, іридоцикліт, увеїт;
- захворювання печінки (первинний склерозуючий холангіт).
Крім того, для перебігу ЗЗК характерний розвиток таких небезпечних кишкових ускладнень, як гостра токсична дилатація товстої кишки, перфорація кишки, кишкова кровотеча, нориці, абсцеси, стриктури та стеноз, а також колоректальний рак.
При підозрі на ЗЗК вкрай важливим є ретельний збір анамнезу, особливо відомостей щодо частоти дефекацій, консистенції калу та наявності в ньому патологічних домішок. Згідно з рекомендаціями ЕССО (2017) повний медичний анамнез у пацієнта з підозрою на ВК має включати детальні дані щодо симптомів, обставин їх появи, вираженості кровотечі, консистенції калу й частоти дефекацій, невідкладних позивів, тенезмів, абдомінального болю, нетримання калу, нічної діареї, а також позакишкових проявів. Слід з’ясовувати інформацію про нещодавні подорожі, можливі контакти з інфекційними хворими, прийом медикаментів (антибіотиків, нестероїдних протизапальних засобів – НПЗЗ), куріння, сексуальні контакти, сімейний анамнез і відомості про перенесену апендектомію. При підозрі на ХК, окрім вищезазначеної інформації, доцільно розпитати пацієнта про наявність харчової непереносимості та приділити особливу увагу виявленню доведених факторів ризику (куріння, сімейний анамнез ХК, перенесений інфекційний гастроентерит).
Об’єктивна діагностика ЗЗК включає проведення низки лабораторних та інструментальних досліджень. Обов’язково виконується загальний аналіз крові з формулою та визначається швидкість осідання еритроцитів і рівень С-реактивного білка (СРБ). Останні 2 показники в подальшому також можна застосовувати для оцінки в динаміці відповіді на лікування, а при ХК, крім того, СРБ є маркером активності захворювання. У біохімічному аналіз крові визначають рівень сечовини, креатиніну, електролітів, печінкових ферментів, загального білка й альбуміну тощо. Згідно з рекомендаціями ЕССО (2017) при підозрі на ЗЗК також слід визначати у сироватці крові рівень заліза, вітамінів С, В12 та фолатів, а також виключати можливість інфекційної діареї (у тому числі викликаної Clostridium difficile), при цьому враховуючи, що в деяких випадках вона може перебігати одночасно з ВК. У пацієнтів із підозрою на ХК слід додатково оцінити ознаки гострого/хронічного запалення, анемії, втрати рідини, а також синдромів мальнутриції та мальабсорбції. Також доцільно визначати рівень фекального кальпротектину (ФК), що є маркером органічного ураження кишечнику.
Серед методів інструментальної діагностики ЗЗК, безперечно, пріоритетним є виконання ілеоколоноскопії з подальшим морфологічним дослідженням біоптатів, взятих з усіх відділів товстої кишки та термінального відділу здухвинної кишки. Також додатково за показаннями можуть бути використані відеокапсульна ендоскопія, іригографія, магнітно-резонансна томографія (МРТ), ультразвукове дослідження (УЗД) кишечнику, а також комп’ютерна томографія (КТ) з контрастуванням (у разі підозри на ХК). Проте саме ендоскопічне дослідження кишечнику відіграє ключову роль у встановленні діагнозу ЗЗК, веденні хворих, прогнозуванні перебігу захворювання та в динамічному спостереженні за пацієнтами. Відповідно до Європейського доказового консенсусу з ендоскопії при ЗЗК (2013) для належної морфологічної оцінки (встановлення ініціального діагнозу ХК і ВК) слід брати щонайменше по 2 біоптати з усіх 5 відділів товстої кишки і з термінального відділу здухвинної кишки. Для ВК найбільш характерними є такі ендоскопічні дані, як неперервне ураження з чіткою лінією припинення запалення з ураженням прямої кишки, а для ХК – фокальні, переривчасті ділянки уражень, наявність стриктур, фістул і періанальних уражень. Також існують основні ендоскопічні показники ВК і ХК, які лікар-ендоскопіст оцінює під час дослідження та вказує у висновку. При ВК до них належать стан судинного малюнку (при цьому захворюванні він згладжений або відсутній), грануляції, гіперемія, рихлість, кровоточивість (контактна, спонтанна), ерозії та виразки слизової оболонки товстої кишки. При ХК важливого значення набуває виявлення виразок різного розміру та форми (за типом «слідів равлика») на фоні незміненої слизової оболонки навколо них, оцінка площі поверхні з виразками, тип звуження кишечнику (інфільтративно-запальне, рубцеве) у всіх відділах товстої кишки та в термінальному відділі здухвинної кишки.
Що ж стосується морфологічної діагностики взятих під час ілеоколоноскопії біоптатів, то при ВК найбільш ранньою діагностичною ознакою з найвищим прогностичним значенням є базальний плазмоцитоз. Гістологічна оцінка ВК ґрунтується на поєднанні поширеного спотворення архітектоніки крипт, атрофії слизової оболонки, зменшення кількості слизу та дифузної трансмукозної запальної інфільтрації з базальним плазмацитозом при активному запаленні, що викликає розвиток криптитів та крипт-абсцесів. До числа мікроскопічних ознак ХК відноситься фокальне, неоднорідне хронічне лімфоплазмоцитарне запалення; неоднорідна, переривчаста дерегуляція, спотворення крипт, а також не пов’язані з ураженням крипт гранульоми. Згідно з чинними клінічними протоколами у діагностиці ЗЗК також використовують візуалізаційні методи, такі як КТ, МРТ та УЗД. Вони є додатковими до ендоскопії методами діагностики, що допомагають виявити та визначити ступінь і протяжність запалення, а також наявність кишкової непрохідності та нориць при ХК. Капсульна ендоскопія тонкої кишки (КЕТК) повинна розглядатися як метод обстеження лише в тому випадку, якщо отримані негативні результати ілеоколоноскопії та візуалізаційних досліджень, проте залишаються підозри на наявність ХК (за відсутності обструктивних синдромів або відомих стенозів). Водночас є дані про те, що під час КЕТК майже у 10% здорових осіб виявляють незначні ураження слизової оболонки кишечнику та невеликі ерозії, поява яких найчастіше спричинена прийомом НПЗЗ. МРТ, КТ-ентерографія та трансабдомінальне УЗД кишечнику також розглядаються як додаткові до ендоскопії методи інструментального обстеження, які дають можливість виявляти та стадіювати запальну, обструктивну та фістулізуючу ХК. МРТ, КТ та УЗД мають високу інформативність щодо виявлення тонкокишкових стенозів, пенетруючих ускладнень, а також допомагають у диференційній діагностиці запальних і фібротичних стриктур.
Таким чином, правильне встановлення діагнозу ЗЗК на сьогодні є результатом тісної взаємодії клініциста-аналітика з лікарями суміжних спеціальностей, фахівцями з інструментальної діагностики (ендоскопістом, рентгенологом, лікарем УЗ-діагностики) та патоморфологами.
Основні положення європейських рекомендацій щодо УЗД кишечнику та його інформативності в діагностиці ЗЗК проаналізував у своєму виступі завідувач відділення рентгенологічної діагностики лікарні «Медбуд» (м. Київ) Максим Миколайович Жайворонок.
 – У реальній клінічній практиці при оглядовому УЗД органів черевної порожнини кишечник доволі часто залишається без уваги фахівців. Проте в жовтні 2014 р. Європейська федерація товариств фахівців з УЗД в медицині та біології (EFSUMB) сформувала рекомендації щодо УЗД кишечнику з метою стандартизації та сприяння використанню цієї методики в клінічній практиці лікарями УЗ-діагностики та гастроентерологами. У цьому документі висвітлюються технічні особливості виконання дослідження та УЗ-ознаки нормальної анатомічної будови кишечнику. Згодом, у 2017 р., були надруковані рекомендації стосовно виконання УЗД шлунково-кишкового тракту (ШКТ) саме при ЗЗК. Згідно з ними для комплексного УЗД кишечнику необхідно використовувати як високо-, так і низькочастотні датчики. При цьому для вимірювання товщини стінки кишки слід застосовувати лінійний датчик із частотою не менше 5 мГц. З метою оцінки патологічної васкуляризації кишкової стінки має застосовуватися кольорове доплерівське картування, а для диференційної діагностики васкулярних і аваскулярних уражень (у тому числі абсцесів) має застосовуватися УЗД із контрастним підсиленням. Для оцінки жорсткості патологічно потовщеної стінки кишки може використовуватися ультразвукова еластографія.
– У реальній клінічній практиці при оглядовому УЗД органів черевної порожнини кишечник доволі часто залишається без уваги фахівців. Проте в жовтні 2014 р. Європейська федерація товариств фахівців з УЗД в медицині та біології (EFSUMB) сформувала рекомендації щодо УЗД кишечнику з метою стандартизації та сприяння використанню цієї методики в клінічній практиці лікарями УЗ-діагностики та гастроентерологами. У цьому документі висвітлюються технічні особливості виконання дослідження та УЗ-ознаки нормальної анатомічної будови кишечнику. Згодом, у 2017 р., були надруковані рекомендації стосовно виконання УЗД шлунково-кишкового тракту (ШКТ) саме при ЗЗК. Згідно з ними для комплексного УЗД кишечнику необхідно використовувати як високо-, так і низькочастотні датчики. При цьому для вимірювання товщини стінки кишки слід застосовувати лінійний датчик із частотою не менше 5 мГц. З метою оцінки патологічної васкуляризації кишкової стінки має застосовуватися кольорове доплерівське картування, а для диференційної діагностики васкулярних і аваскулярних уражень (у тому числі абсцесів) має застосовуватися УЗД із контрастним підсиленням. Для оцінки жорсткості патологічно потовщеної стінки кишки може використовуватися ультразвукова еластографія.
Стандартне УЗД кишечнику не потребує спеціальної підготовки пацієнта. Проте слід пам’ятати, що дослідження судин черевної порожнини слід проводити не раніше ніж через 6 год після їди, а оцінку перистальтики кишечнику – натщесерце (прийом їжі більше ніж 8 год тому). Вкрай важливим є системний підхід до проведення трансабдомінального УЗД товстого кишечнику. На першому етапі виконується оглядове сканування (доцільно за принципом «косіння газону»), на другому – поперечне сканування, на третьому – повздовжнє сканування.
Що ж стосується УЗД тонкої кишки, то для його проведення рекомендується використовувати розчини поліетиленгліколю (які зазвичай застосовуються для підготовки кишечнику перед ендоскопічними дослідженнями), що «розправляють» тонку кишку та дають можливість добре вивчити її просвіт і стан стінки. У нормі товщина кишкової стінки не перевищує 2 мм (за винятком дванадцятипалої та прямої кишки). Товщину стінки кишечнику слід вимірювати перпендикулярно від точки між серозною оболонкою та власним м’язовим шаром до точки між слизовою оболонкою та просвітом. Потовщення стінки кишечнику, виміряне при УЗД, може бути ознакою ХК, зокрема при локалізації уражень у тонкій кишці. Згідно з даними нещодавно проведеного метааналізу проспективних досліджень потовщення стінки кишечнику >3 мм слід розглядати як порогове значення для виявлення ХК (у цій ситуації чутливість складає 89%), тимчасом як потовщення стінки >4 мм характеризується високою специфічністю – 96% (J. Dong et al., 2014). Клінічна активність при ХК також корелює з товщиною стінки кишечнику і може бути оцінена за допомогою УЗД. Крім того, УЗД може продемонструвати збережену чи зруйновану пошарову будову потовщеної стінки кишечнику при ХК. Локальне чи поширене руйнування шарів стінки кишечнику свідчить про наявність значних деструктивних змін.
Під час проведення УЗД може бути виявлена інфільтрація вісцеральної жирової клітковини у вигляді підвищення ехогенності, що відображає клінічні та біохімічні показники захворювання. За допомогою УЗД може бути виявлена вільна рідина у черевній порожнині, проте її наявність являє собою неспецифічний критерій, який не має чіткого діагностичного значення при ХК. Може спостерігатися залучення апендиксу до патологічного процесу при ХК, зазвичай у поєднанні з термінальним ураженням здухвинної та сліпої кишки.
Стенози можуть візуалізуватися при УЗД у вигляді сегментів кишечнику з потовщенням стінки, звуженням просвіту й передстенотичним розширенням. Порушення пошарової будови, підсилений кровотік вказують на запальний характер процесу. Порушення пошарової будови та гіповаскуляризація стінки кишечнику на рівні стриктури вказує на більш високий ступінь фіброзу. Для оцінки жорсткості стенозу при ХК може використовуватися еластографія. Фістули при ХК можуть візуалізовуватися як гіпоехогенні ділянки з пухирцями газу чи без них.
Слід зазначити, що застосування УЗД із метою виявлення нориць при ХК може характеризуватися високими показниками чутливості (67-87%) та специфічності (90-100%), зіставними з такими у КТ і МРТ. Абсцеси можуть бути виявлені у вигляді скупчення рідини, що може містити пухирці газу. Для їх виявлення при ХК УЗД може використовуватися з високою чутливістю (81-100%) та специфічністю (92-94%).
УЗД кишечнику можна використовувати для оцінки потовщення стінки товстої кишки, котре зазвичай визначається при активному ВК. Пошарова структура стінки кишки за активного ВК, як правило, збережена (за винятком тяжких випадків), тимчасом як при ХК вона часто порушена. Посилені доплерівські сигнали в потовщеній стінці кишечнику при ВК, котрі можна спостерігати при УЗД, слід інтерпретувати як ознаку активного запалення. УЗД можна використовувати для діагностики ВК і ХК, спираючись на локалізацію ушкодження, ступінь потовщення стінки, збереженість пошарової будови, ураження вісцеральної жирової клітковини та наявність ускладнень. УЗД може виявити специфічні зміни кишечнику (переважно ділянку ураження та параколітичні зміни), які можуть бути використані для диференціації ХК і ВК та інших патологічних змін кишечнику.
Отже, при кваліфікованому проведенні УЗД кишечнику можна оцінити його анатомію, васкуляризацію та ширину просвіту кишки, а також перистальтику та вміст кишечнику. Крім того, за допомогою УЗД можна оцінити стан лімфатичних вузлів і брижі, виявити патологічні зміни, у тому числі й при ЗЗК. Висновок фахівця з УЗД має ґрунтуватися на ступені візуалізації кишечнику, певних технічних аспектах і результатах дослідження, пов’язаних із його клінічним контекстом.
Практичні алгоритми лікування ЗЗК з урахуванням можливих індивідуальних нюансів докладно розглянула у своїй доповіді з наведенням клінічних прикладів доцент кафедри хірургії № 1 Національного медичного університету імені О.О. Богомольця, кандидат медичних наук Тетяна Георгіївна Кравченко.
 – Як відомо, перебіг ВК і ХК є прогресуючим і характеризується чергуванням рецидивів та ремісій. При цьому відсутність клінічних симптомів не виключає наявності запальних змін у кишечнику, а персистуюче запалення закономірно призводить до анатомічних змін у кишечнику та до порушення його функцій. Мета сучасного лікування ЗЗК, яке має проводитися мультидисциплінарною командою фахівців, полягає у модифікації перебігу хвороби. Для цього потрібно «взяти під контроль» запалення на максимально ранній стадії, коли ще не сформувалися незворотні структурні зміни кишечнику та не виникли небезпечні ускладнення. При ЗЗК слід намагатися досягти поєднання ендоскопічної та клінічної ремісії. При цьому також дуже бажано досягти й нормалізації біомаркерів запалення – СРБ та ФК. Сучасна таргетна терапія ЗЗК базується на оцінці тяжкості перебігу хвороби й обов’язковому врахуванні наявних у конкретного пацієнта факторів ризику, а не лише власне активності патологічного процесу. Обов’язковим має бути регулярний моніторинг стану пацієнта після досягнення ремісії зі своєчасним коригуванням лікування.
– Як відомо, перебіг ВК і ХК є прогресуючим і характеризується чергуванням рецидивів та ремісій. При цьому відсутність клінічних симптомів не виключає наявності запальних змін у кишечнику, а персистуюче запалення закономірно призводить до анатомічних змін у кишечнику та до порушення його функцій. Мета сучасного лікування ЗЗК, яке має проводитися мультидисциплінарною командою фахівців, полягає у модифікації перебігу хвороби. Для цього потрібно «взяти під контроль» запалення на максимально ранній стадії, коли ще не сформувалися незворотні структурні зміни кишечнику та не виникли небезпечні ускладнення. При ЗЗК слід намагатися досягти поєднання ендоскопічної та клінічної ремісії. При цьому також дуже бажано досягти й нормалізації біомаркерів запалення – СРБ та ФК. Сучасна таргетна терапія ЗЗК базується на оцінці тяжкості перебігу хвороби й обов’язковому врахуванні наявних у конкретного пацієнта факторів ризику, а не лише власне активності патологічного процесу. Обов’язковим має бути регулярний моніторинг стану пацієнта після досягнення ремісії зі своєчасним коригуванням лікування.
Важливо розуміти різницю між поняттями «активність» і «тяжкість перебігу» захворювання. Якщо активність захворювання відображає стан пацієнта на момент поточного загострення (симптоми, біологічні маркери запалення, ендоскопічна та гістологічна картина), то при оцінюванні ступеня тяжкості захворювання враховується перебіг хвороби з моменту встановлення діагнозу та фактори ризику, тобто картина захворювання в цілому та прогностичні фактори (госпіталізація, хірургічні втручання, позакишкові прояви, рефрактерність до терапії, вплив на якість життя тощо).
До несприятливих прогностичних факторів ХК відносять вік молодше 30 років на момент дебюту захворювання, наявність фістул, абсцесів і стриктур, ураження термінального відділу здухвинної кишки, тонкої кишки, верхніх відділів ШКТ, періанальні/ректальні ураження, симптоми, підвищені рівні СРБ і ФК, зниження концентрації гемоглобіну й альбуміну, глибокі виразки, трансмуральне запалення, необхідність лікування (особливо ініціального) кортикостероїдами (КС), хірургічні втручання, великий обсяг ураження, зниження індексу маси тіла (ІМТ), куріння.
Ризик несприятливого перебігу ВК підвищують такі фактори, як вік молодше 30 років, великий обсяг ураження кишечнику, високі рівні СРБ і ФК, анемія, гіпоальбумінемія, виражені клінічні симптоми, глибокі виразки слизової оболонки, госпіталізація, зниження ІМТ та необхідність використання КС.
Дуже цікавою є історія медикаментозного лікування ЗЗК. Вона розпочалася у 50-х роках минулого століття з застосування сульфасалазину та КС, у 1980 р. почали застосовувати препарати 5-аміносаліцилової кислоти (5-АСК), через 10 років – будесонід. У 1998 р. з появою інфліксимабу розпочалася ера біологічної терапії ЗЗК: у 2007 р. стали призначати наталізумаб та адалімумаб, у 2008 р. – цертолізумаб, у 2014 р. – голімумаб і ведолізумаб, у 2016 р. – устекінумаб. У 2018 р. з’явився потужний селективний інгібітор родини янус-кіназ – тофацитиніб.
Сьогодні в лікуванні ВК легкого/середнього ступеня тяжкості (низький ризик) застосовують 5-АСК і будесонід. При цьому, незважаючи на майже 40-річний «стаж», 5-АСК залишається стандартом у лікуванні ВК легкого та середнього ступеня тяжкості (а це близько 60% пацієнтів). Лікування пацієнтів із ВК 5-АСК забезпечує швидку й ефективну індукцію ремісії та її підтримання, досягнення ендоскопічної ремісії, профілактику розвитку ускладнень, дисплазії та колоректального раку, підвищує якість життя пацієнтів та не асоціюється з ризиком виникнення інфекцій або малігнізацією. Терапія 5-АСК характеризується високим профілем безпеки, дозволена до застосування у дітей та може призначатися навіть у період вагітності та грудного вигодовування. Проте в реальній клінічній практиці терапія 5-АСК може бути недостатньо ефективною при ВК. Передусім це зумовлено призначенням її в субоптимальних дозах, недостатньою тривалістю прийому 5-АСК у фазі загострення (лише до зменшення вираженості симптомів, але не до досягнення ендоскопічної ремісії), відмовою від застосування препарату у ректальних формах, а також нерегулярним прийомом препарату.
Середній ступінь тяжкості ВК за умови високого ризику або тяжкий його перебіг вимагають призначення системних КС. Можлива терапія імуносупресорами (азатіоприном та 6-меркаптопурином). З засобів біологічної терапії можуть бути обрані інфліксимаб, адалімумаб, голімумаб, ведолізумаб, тофацитиніб. Можливості застосування у пацієнтів із ВК устекінумабу сьогодні вивчаються у клінічних дослідженнях третьої фази.
При легкій та середній формі перебігу ХК (за умови низького ризику) препаратами вибору є будесонід, а за його неефективності – системні КС. Дані досліджень щодо ефективності 5-АСК при цій патології є суперечливими. Середньої тяжкості (високий ризик) і тяжкий перебіг ХК вимагають терапії системними КС, імуносупресорами (азатіоприн, 6-меркаптопурин) і препаратами для біологічної терапії (інфліксимаб, адалімумаб, цертолізумаб, ведолізумаб, устекінумаб тощо).
Якщо розглянути ієрархію потреб пацієнтів із ЗЗК і лікарів, які займаються їх веденням, то можна констатувати певну розбіжність: для лікаря найбільш важливим є досягнення клінічної та ендоскопічної ремісії, а пацієнти оцінюють успіх лікування передусім як можливість жити звичним життям (ходити на роботу, вчитися, самостійно харчуватися, зберігати масу тіла), уникати госпіталізацій та хірургічних втручань.
На жаль, терапія КС не є панацеєю при ЗЗК, незважаючи на їх достатньо високу ініціальну терапевтичну ефективність. Дійсно, КС забезпечують досягнення повної симптоматичної відповіді через 30 діб лікування у 58 і 54% пацієнтів із ХК і ВК відповідно і часткової відповіді у 26 і 30% відповідно. Проте через 1 рік лікування КС тривала відповідь зберігається лише у 28% пацієнтів із ХК і в 49% хворих на ВК, тимчасом як у 32 і 22% пацієнтів відповідно формується стероїдзалежний перебіг хвороби. Крім того, через 1 рік терапії КС оперативне втручання доводиться виконувати в 38% пацієнтів з ХК і в 29% з ВК (W.A. Faubios, E.J. Sandbom, 2001). Токсичні ефекти системних КС, серед яких формування місяцеподібного обличчя, акне, екхімози, гіпертензія, гірсутизм, петехіальні крововиливи, стриї на шкірі, стероїдні васкуліти, цукровий діабет, остеопороз, остеонекроз, міопатія, катаракта, глаукома, психоз, інфекції тощо, також обмежують їх тривале використання.
Що ж стосується застосування при ЗЗК азатіоприну в режимі монотерапії, то, на жаль, воно характеризується мінімальною ефективністю порівняно з плацебо. До того ж імуносупресори (азатіоприн, 6-меркаптопурин) також мають несприятливий профіль токсичності, який включає підвищення ризику розвитку опортуністичних інфекцій, 4-кратне підвищення ризику розвитку лімфоми, асоційованої з інфікуванням вірусом Епштейна–Барр, та немеланомного раку шкіри, а також супресії кісткового мозку (лейкопенія, що розвивається у 2-5% хворих).
За умови неефективності стандартної терапії необхідно приєднувати до лікування препарати для біологічної терапії. Першою групою таких препаратів стали інгібітори фактора некрозу пухлини. У дослідженнях інфліксимабу, адалімумабу, голімумабу та цертолізумабу було встановлено, що вони забезпечують швидке досягнення та тривале підтримання клінічної ремісії, проте їх застосування обмежується можливістю розвитку таких небажаних явищ, як:
- імуногенність;
- інфузійні реакції;
- реакції сповільненої гіперчутливості;
- запальні реакції у місці введення;
- формування аутоантитіл;
- медикаментозно-індукований вовчак;
- неходжкінська лімфома;
- опортуністичні інфекції (у тому числі туберкульоз, гістоплазмоз).
Високу ефективність при ВК і ХК продемонстрував ведолізумаб (B.G. Feagan et al., 2013; W.J. Sandborn et al., 2013), який відноситься до нової групи препаратів для біологічної терапії – антиінтегринів. У пацієнтів із ВК терапія ведолізумабом забезпечує високі показники частоти досягнення клінічної відповіді, клінічної ремісії (у тому числі стійкої), загоєння слизової оболонки та, що вкрай важливо, безстероїдної ремісії. При ХК терапія ведолізумабом також забезпечує високу частоту досягнення клінічної ремісії (у тому числі стійкої та безстероїдної) та клінічної відповіді. Ведолізумаб має сприятливий профіль безпеки. У пацієнтів, які застосовували ведолізумаб, кількість серйозних чи опортуністичних інфекцій, онкологічної патології не відрізняється від такої серед загальної популяції хворих на ЗЗК, хоча, безумовно, слід пам’ятати про те, що токсичність нових препаратів часто виявляється вже на етапі постреєстраційних досліджень.
Таким чином, хоча ЗЗК залишаються невиліковною патологією, тим не менш лікарі мають інструменти, використання яких може попередити прогресування ЗЗК і розвиток пов’язаних із хворобою ускладнень. І ці інструменти можна використовувати в Україні вже сьогодні.
Підготувала Олена Терещенко
За підтримки ТОВ «Такеда Україна».
UA/IBDD/0518/0018
Тематичний номер «Гастроентерологія. Гепатологія. Колопроктологія» № 2 (48), травень 2018 р.
СТАТТІ ЗА ТЕМОЮ Гастроентерологія
Метаболічноасоційована жирова хвороба печінки (МАЖХП) є однією з найактуальніших проблем сучасної гепатології та внутрішньої медицини в цілому. Стрімке зростання поширеності ожиріння та цукрового діабету (ЦД) 2 типу в популяції призвело до істотного збільшення кількості хворих на МАЖХП, яка охоплює спектр патологічних станів від неускладненого стеатозу до алкогольної хвороби печінки та цирозу, що розвиваються на тлі надлишкового нагромадження ліпідів у гепатоцитах. ...
Інфекція Helicobacter pylori (H. pylori) офіційно визнана інфекційним захворюванням і включена до Міжнародної класифікації хвороб (МКХ) 11-го перегляду, тому рекомендовано лікувати всіх інфікованих пацієнтів. Проте, зважаючи на широкий спектр клінічних проявів, пов’язаних із гастритом, викликаним H. pylori, лишаються специфічні проблеми, які потребують регулярного перегляду для оптимізації лікування. ...
Відтворення майбутнього здорової нації – один з найважливіших сенсів існування теперішнього покоління. День боротьби з ожирінням нагадує нам про поширеність цього проблемного явища і важливість попередження його наслідків. Ожиріння може мати вплив на різні аспекти здоров'я, включаючи репродуктивне....
Вивчення клініко-патогенетичних особливостей поєднаного перебігу остеоартрозу (ОА) у хворих із метаболічними розладами, які характеризують перебіг метаболічного синдрому (МС), зокрема цукровим діабетом (ЦД) 2 типу, ожирінням (ОЖ), артеріальною гіпертензією (АГ), є актуальним, оскільки це пов’язано з неухильним збільшенням розповсюдженості цього захворювання, недостатньою ефективністю лікування, особливо за коморбідності з іншими захворюваннями, які патогенетично пов’язані з порушеннями метаболічних процесів. ...