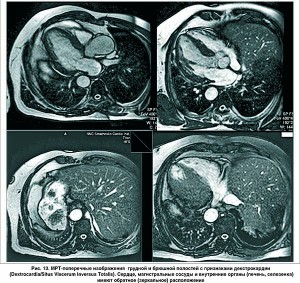
Декстрокардия с транспозицией органов (situs inversus)
Впервые аномальное расположение сердца в грудной клетке научно описал итальянский анатом и хирург Иероним Фабриций в 1606 году. Марко Аурелио Северино применил термин «декстрокардия» в 1643 году при описании у пациента зеркального расположения внутренних органов. Более века спустя Мэтью Бейли описал транспозицию органов как полный поворот органов грудной и брюшной полости в зеркальном изображении [1].
В настоящее время под декстрокардией понимают редкую врожденную аномалию развития сердечно-сосудистой системы, при которой сердце расположено в грудной клетке справа, соответственно все входящие и исходящие сосуды сердца расположены зеркально своему обычному положению. С помощью генетических исследований установлено, что декстрокардия ассоциируется с мутацией генов HAND, ZIC3Shh, ACVR2, Pitxz, и доказан аутосомно-рецессивный тип наследования этой патологии. Мутации происходят в первом триместре беременности, когда осуществляется закладка всех органов и систем.
Частота указанных аномалий достигает 1,5-5% среди всех врожденных пороков сердца и, как правило, сочетается с транспозицией магистральных сосудов [2-4]. Наиболее распространенным среди них являются правосформированное праворасположенное сердце (изолированная декстрокардия) – 54% и левосформированное праворасположенное сердце («зеркальная декстрокардия») – 33%. В первом случае расположение других органов грудной клетки и топография органов брюшной полости соответствуют физиологической норме, во втором случае отмечают полное обратное расположение внутренних органов (situs inversus) [5].
В зависимости от ориентации внутренних органов выделяют [6]:
– situs inversus cordis – простая декстрокардия, при которой зеркально расположено только сердце; встречается очень редко;
– situs viscerum inversus partialis – сердце и некоторые органы дыхательной или пищеварительной системы расположены зеркально;
– situs viscerum inversus totalis – все внутренние органы имеют зеркальное расположение.
Два последних вида декстрокардии называются зеркальными. При декстрокардии нередко встречаются и другие врожденные пороки сердца, в том числе эндокардиальные дефекты, стеноз легочной артерии, дефект межжелудочковой перегородки (МЖП), двухместный желудочковый выход, транспозиция магистральных сосудов, тетрада Фалло [1, 6, 7], а также может обнаруживаться двух-, трехкамерное сердце [6].
В редких случаях встречается неопределенное разнонаправленное положение внутренних органов, которое называется гетеротаксией, или situs ambiguous. При этом у пациентов печень может быть расположена по срединной линии, селезенка может отсутствовать или может быть не одна, структура предсердий неопределенная, кишечник перевернут; как правило, односторонние структуры дублируются или отсутствуют [2, 8, 9, 10].
Клиника и диагностика
Простая декстрокардия, которая не сопровождается врожденными пороками развития сердца и внутренних органов, может не проявляться клинически и часто обнаруживается случайно во время медицинского осмотра или проведения электрокардиографии (ЭКГ) и рентгеновского исследования [11]. Такие пациенты могут не предъявлять никаких жалоб, и лишь чаще других страдают заболеваниями дыхательной системы. Декстрокардию клиницист довольно легко может заподозрить при физикальном обследовании: при пальпации верхушечный толчок обнаруживается справа, также при перкуссии смещается сердечная тупость.
Расположение сердца определяется положением предсердий [12]. При транспозиции органов морфологически правое предсердие (ПП) находится слева, а левое предсердие (ЛП) – справа. При этом структурно легкие повернуты таким образом, что левое легкое имеет 3 доли и правое легкое – 2 доли. Кроме того, печень и желчный пузырь расположены с левой стороны брюшной полости, в то время как селезенка и желудок расположены справа.
При отсутствии сопутствующих патологий аномальное расположение сердца не влияет на продолжительность и качество жизни. У таких людей рождаются здоровые дети с нормальным расположением всех внутренних органов, хотя считается, что вероятность рождения ребенка с декстрокардией у них все же несколько выше.
При сочетании декстрокардии с другими аномалиями внутренних органов на ранних стадиях заболевания могут проявиться следующие симптомы: задержка в росте и наборе веса, быстрая утомляемость, склонность к инфекционным заболеваниям дыхательных органов, выраженная слабость, затрудненное или учащенное дыхание, учащенное сердцебиение, бледность, цианоз кожных покровов и/или желтушность кожи и склер.
При возникновении первых клинических проявлений заболевания лечащий врач в обязательном порядке должен выполнить комплекс диагностических обследований:
• объективный осмотр, перкуссию и аускультацию;
• рентгенологическое исследование;
• ЭКГ ;
• ультразвуковое исследование (УЗИ) сердца и сосудов;
• компьютерную томографию (КТ);
• магнитно-резонансную томографию (МРТ);
• при необходимости ангиокардиографию и катетеризацию сердца.
Клинический случай
Пациент Р. был госпитализирован в отдел некоронарных болезней сердца и ревматологии ГУ ННЦ «Институт кардиологии им. Н.Д. Стражеско» НАМН Украины с жалобами на боль за грудиной длительностью 5-30 мин без четкой связи с физической нагрузкой, одышку при умеренной физической нагрузке, ощущение перебоев в работе сердца, нитраты не принимал. Пациент отмечал повышение артериального давления (АД) до 170/100 мм рт. ст. при «рабочем» АД 160/90 мм рт. ст. на протяжении 10 лет.
Пациент также сообщил о наличии у него обратного расположения внутренних органов (situs inversus), что было выявлено во время выполнения плановой аппендэктомии в детстве. Обратное расположение внутренних органов также было у родного брата пациента и отсутствовало у дочери. На догоспитальном этапе больной принимал бисопролол в дозе 2,5 мг/сут и ацетилсалициловую кислоту в дозе 75 мг/сут.
При пальпации сердечный толчок располагался в пятом межреберье справа по среднеключичной линии, перкуторно тупость сердца обнаруживалась в правой половине грудной клетки. Аускультативно тоны сердца максимально прослушивались справа соответственно общепринятым аускультативным точкам, симметрично смещенным на правую половину грудной клетки. При пальпации внутренних органов печень и селезенка имели зеркальное расположение.
Общий анализ крови не продемонстрировал отклонений от референтных величин. В биохимическом анализе: калий – 4,2 ммоль/л, натрий – 144 ммоль/л, билирубин – 17 мкмоль/л, креатинин – 67 ммоль/л, глюкоза – 4,6 ммоль/л, общий холестерин – 5,8 ммоль/л, триглицериды – 1,7 ммоль/л.
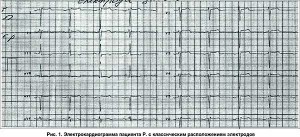
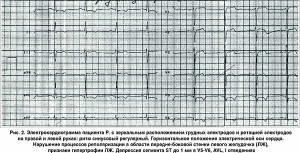
На ЭКГ, записанной с классическим расположением электродов (рис. 1), в I стандартном отведении регистрировался отрицательный зубец Р, а основной зубец комплекса QRS направлен вниз от изолинии. Вследствие такой ориентации средних векторов QRS зубец RIII становится выше зубца RII. Зубец РII сглаженный, РIII – положительный. В грудных отведениях V1-V6 в комплексе QRS преобладает зубец S. В правых грудных отведениях зубец Р положительный, в левых – отрицательный. По этим признакам в общепринятых отведениях дается заключение о декстрокардии.
Для выявления изменений миокарда при декстрокардии нами была проведена запись ЭКГ с зеркальным расположением грудных электродов и ротацией электродов на правой и левой руках (рис. 2). Для этого красный электрод был перемещен с правой руки на левую, а желтый – на правую руку. Грудные отведения были записаны с левой и правой половин грудной клетки в следующем порядке: V2, V1, V3R-V6R. В этих отведениях направление зубцов и возрастание их амплитуды соответствует нормальным взаимоотношениям зубцов в отведениях V1-V6 при обычном расположении сердца [13].
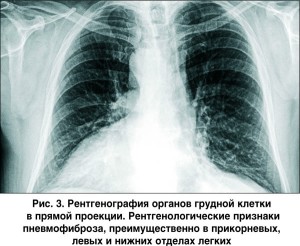
При рентгенологическом исследовании обнаружено аномальное расположение сердца: тень сердца находится преимущественно в правой половине грудной клетки, верхушка сердца ориентирована вправо (рис. 3).
Эхокардиография (ЭхоКГ) позволяет морфологически визуализировать структурные элементы сердца, положение ЛП и ПП, клапаны, оценить кровоток в сосудах [14].
При ЭхоКГ в В-режиме выявлены следующие изменения: створки аортального клапана фиброзированы, клапан трехстворчатый, в режиме цветной допплерографии визуализируется поток эксцентрической аортальной регургитации умеренной степени (поток регургитации выходит за переднюю створку митрального клапана, vena contracta – 5,2 мм).
Правый желудочек (ПЖ) не увеличен, размеры соответствуют верхней границе нормы (продольный размер – 8,7 см, поперечный размер в базальном отделе – 3,9 см, площадь в диастолу – 25 см2 [норма – до 24 см2], индекс площади ПЖ – 12,2 см2/м2 [норма – до 12,5 см2/м2]). Систолическая функция ПЖ не нарушена (фракционная смена площади ПЖ – 40%, систолическая скорость движения трикуспидального кольца (S`) – 15,9 см/с, TAPSE – 21 мм). ЛП увеличено (площадь – 24,2 см2, индекс объема – 39,7 мл/м2).
При оценке ЛЖ в М- и В-режимах выявлена умеренная дилатация (конечно-диастолический размер – 5,8 см, конечно-диастолический объем – 166 мл, индекс конечно-диастолического объема – 81,4 мл/м2 [норма – <74 мл/м2]), незначительное снижение глобальной систолической функции – фракция выброса ЛЖ – 49,1% (норма – ≥52%), эксцентрическая гипертрофия миокарда (индекс массы миокарда ЛЖ – 185 г/ м2, толщина МЖП – 1,4 см, толщина задней стенки ЛЖ – 1,1 см, относительная толщина стенки ЛЖ – 0,38), нарушение диастолической функции ЛЖ, псевдонормальный тип наполнения (E/A – 1,65, DcTime – 200 мс, ранне-диастолическая скорость смещения кольца митрального клапана на латеральной стенке – 9,6 см/с и 6,4 см/с на медиальной стенке).
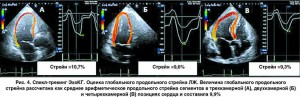
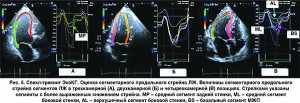
При оценке состояния ЛЖ были выявлены сегменты с нарушением локальной сократимости: гипокинез среднего и верхушечного сегментов боковой стенки ЛЖ, гипокинез базального сегмента МЖП и среднего сегмента задней стенки ЛЖ. При проведении спекл-трекинг ЭхоКГ было обнаружено более выраженное уменьшение величины продольного стрейна (от англ. strain, деформация волокон миокарда при его сокращении) указанных выше сегментов, а также снижение глобального продольного стрейна ЛЖ (рис. 4, 5). Уменьшение глобального и сегментарного стрейна является очень чувствительным маркером систолической дисфункции ЛЖ, однако не позволяет установить нозологическую причину этих изменений.
При проведении холтеровского (24 ч) мониторирования (ХМ) ЭКГ выявлено на фоне синусового ритма с частотой сердечных сокращений 48-68-98 уд/мин частые (4,9%) политопные желудочковые экстрасистолы с периодами аллоритмии по типу бигеминии, тригеминии, вставочные экстрасистолы, нечастые суправентрикулярные экстрасистолы. Значимых пауз, нарушений проводимости не обнаружено. Зарегистрированы фоновые нарушения реполяризации в виде отрицательных зубцов Т.
При УЗИ сосудов головы и шеи выявлено утолщение комплекса интима-медиа до 1,5 мм. В области бифуркации общей сонной артерии слева визуализируется атеросклеротическая бляшка, суживающая до 20% просвета сосуда.
Результаты проведенных инструментальных исследований продемонстрировали поражения миокарда ЛЖ, которые проявлялись его дилатацией, нарушением глобальной и сегментарной систолической функции. Правостороннее расположение сердца в грудной клетке несколько усложняло качество визуализации сердца при проведении ЭхоКГ. Был составлен список вероятных нозологических причин обнаруженных изменений ЛЖ: гипертоническая болезнь с развитием гипертензивного сердца, хронический миокардит неуточненной этиологии или постинфарктный кардиосклероз как следствие ишемической болезни сердца (ИБС).
Учитывая неангинальный тип боли за грудиной, мужской пол и возраст пациента, претестовая вероятность ИБС у больного составила 44%, что требовало проведения дальнейшего неинвазивного обследования для верификации или исключения ИБС. У пациента невозможно 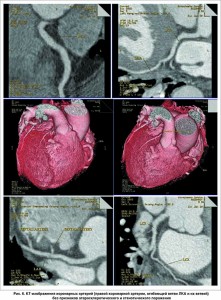 было провести нагрузочный ЭКГ-тест (признаки гипертрофии ЛЖ на ЭКГ и депрессия сегмента ST в покое) и стресс-ЭхоКГ (неудовлетворительное акустическое окно), поэтому для данной цели использовалась КТ сердца с контрастированием коронарных артерий. Метод КТ является предпочтительным для постановки окончательного диагноза при транспозиции органов с декстрокардией, обеспечивает хорошую анатомическую детализацию расположения висцеральных органов, положение верхушки сердца и отхождение магистральных сосудов [15].
было провести нагрузочный ЭКГ-тест (признаки гипертрофии ЛЖ на ЭКГ и депрессия сегмента ST в покое) и стресс-ЭхоКГ (неудовлетворительное акустическое окно), поэтому для данной цели использовалась КТ сердца с контрастированием коронарных артерий. Метод КТ является предпочтительным для постановки окончательного диагноза при транспозиции органов с декстрокардией, обеспечивает хорошую анатомическую детализацию расположения висцеральных органов, положение верхушки сердца и отхождение магистральных сосудов [15].
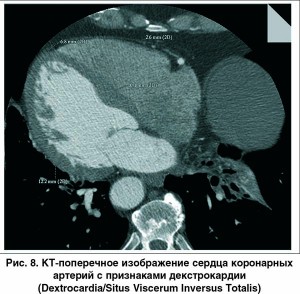
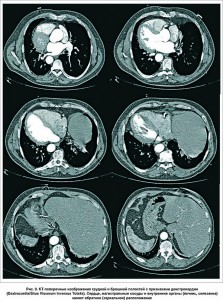
При мультиспиральной КТ-коронарографии сердце и крупные сосуды являются зеркальным отражением их нормальной анатомии; обнаружены признаки начальных атеросклеротических изменений коронарных артерий и локального кальциноза (единичная стабильная коронарная бляшка) (рис. 6). В проксимальном сегменте передней межжелудочковой ветви (ПМЖВ) левой коронарной артерии (ЛКА) атеросклеротическая бляшка без признаков гемодинамически значимого стеноза – 20% (рис. 7). Полости сердца – без особенностей (рис. 8). Транспозиция внутренних органов (рис. 9). Левая половина грудной клетки содержит трехдолевое легкое, правая половина грудной клетки – две доли легкого; печень и желчный пузырь находятся в левой половине брюшной полости, селезенка и желудок – справа. Частичный ателектаз средней доли левого легкого и сегментов S7, S8. Жировой гепатоз. Расширение восходящего отдела аорты.
Для уточнения характера поражения миокарда и проведения дифференциальной диагностики было принято решение провести МРТ сердца. МРТ с высокой степенью достоверности позволяет получить точную информацию об анатомическом строении и расположении отдельных внутренних органов, этот метод визуализации имеет особое значение при диагностике положения предсердий [16-18].
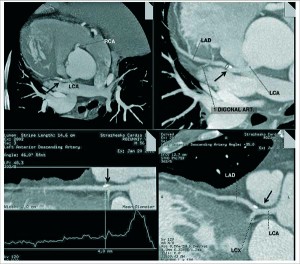 Рис. 7. КТ-изображения ПМЖВ ЛКА (МСКТ2
Рис. 7. КТ-изображения ПМЖВ ЛКА (МСКТ2постпроцессинговая обработка). КТ-признаки локального кальциноза в проксимальном сегменте ПМЖВ ЛКА, без гемодинамически значимого стеноза на указанном уровне (стрелка)
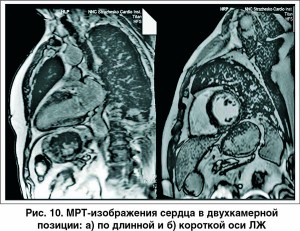
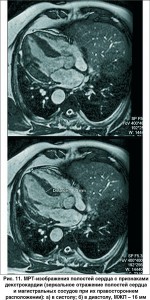
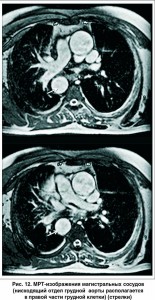
У нашего пациента при МРТ сердца c внутривенным болюсным контрастированием (гадолиниевый контраст, 20 мл) не было выявлено признаков кардиофиброза и воспалительных изменений миокарда ЛЖ (рис. 10). Обнаружено незначительное снижение глобальной сократительной функции ЛЖ, локальную гипертрофию базального отдела МЖП. Левые отделы сердца незначиельно расширены. Выявлено транспозицию органов грудной клетки и брюшной полости (рис. 11-13).
МРТ-признаков воспалительного поражения миокарда ЛЖ и кардиофиброза ЛЖ не обнаружено.
Таким образом, проведенные исследования позволили установить пациенту следующие диагнозы:
• Гипертоническая болезнь сердца, II стадия, 2 степень. Гипертензивное сердце. Риск 4 (очень высокий).
• ИБС: атеросклероз коронарных артерий (стеноз ПМЖВ ЛКА – 20%, МСКТ-коронарография 20.01.16). Частая желудочковая экстрасистолическая аритмия (4,9%), нечастая суправентрикулярная экстрасистолическая аритмия (ХМЭКГ 21.01.16). Сердечная недостаточность I стадии.
• Гиперхолестеринемия.
• Транспозиция внутренних органов (situs inversus).
Назначено следующее лечение: бисопролол – 2,5 мг 1 раз в сутки; фиксированная комбинация индапамид 2,5 мг/периндоприл 5 мг 1 раз в сутки; амлодипин – 2,5 мг/сут; ацетилсалициловая кислота 75 мг/сут; аторвастатин – 20 мг/сут; пропафенон – 150 мг 2 раза в сутки.
Больной был выписан с улучшением.
Литература
1. Gutgesell H.P. Cardiac malposition and heterotaxy. Garson AG Jr, Fisher DJ, Neish SR, eds. Science and Practice of Pediatric Cardiology. 2nd ed. Baltimore, Md: Williams & Wilkins; 1998. Vol 2: 1539-61.
2. Lee S.E., Kim H.Y., Jung S.E. et al. Situs anomalies and gastrointestinal abnormalities. J Pediatr Surg. 2006 Jul. 41(7): 1237-42.
3. Maldjian P.D., Saric M. Approach to dextrocardia in adults: review. AJR Am J Roentgenol. 2007 Jun. 188(6 suppl):S39-49; quiz S35-8.
4. Fung T.Y., Chan D.L., Leung T.N. et al. Dextrocardia in pregnancy: 20 years' experience. J Reprod Med. 2006 Jul. 51(7): 573-7.
5. Руководство по кардиологии / Под ред. В.Н. Коваленко. – К.: Морион, 2008. – 922 с.
6. Hagler D.J., O'Leary P.W. Cardiac malpositions and abnormalities of atrial and visceral situs. Emmanouilides GC, Riemenschneider T.A., Allen H.D., Gutgesell H.P., eds. Moss and Adams' Heart Disease in Infants, Children, and Adolescents: Including the Fetus and Young Adult. 5th ed. Baltimore, Md: Williams & Wilkins; 1995. Vol 2: 1307-36.
7. Silverman N.H. An ultrasonic approach to the diagnosis of cardiac situs, connections, and malpositions.Cardiol Clin. 1983 Aug. 1(3): 473-86.
8. Winer-Muram H.T. Adult presentation of heterotaxic syndromes and related complexes. J Thorac Imaging. 1995. 10(1): 43-57.
9. Applegate K.E., Goske M.J., Pierce G. et al. Situs revisited: imaging of the heterotaxy syndrome.Radiographics. 1999 Jul-Aug. 19(4): 837-52; discussion 853-4.
10. Winer-Muram H.T., Tonkin I.L. The spectrum of heterotaxic syndromes. Radiol Clin North Am. 1989 Nov. 27(6): 1147-70.
11. Janchar T., Milzman D., Clement M. «Situs Inversus: Emergency Evaluations of Atypical Presentations» American Journal of Emergency Medicine 18, no. 3 (May 2000): 349-50.
12. Partridge J. The radiological evaluation of atrial situs. Clin Radiol. 1979 Jan. 30(1): 95-103.
13. Орлов В.Н. Руководство по электрокардиографии. – М.: Медицина, 1984. – 528 с.
14. Tonkin I.L., Tonkin A.K. Visceroatrial situs abnormalities: sonographic and computed tomographic appearance. AJR Am J Roentgenol. 1982 Mar. 138(3): 509-15.
15. Oui H., Kim J., Bae Y. et al. Computed Tomography Angiography of Situs Inversus, Portosystemic Shunt and Multiple Vena Cava Anomalies in a Dog. J Vet Med Sci. 2013 Jul 9.
16. Yoo S.J., Kim Y.M., Choe Y.H. Magnetic resonance imaging of complex congenital heart disease. Int J Card Imaging. 1999 Apr. 15(2): 151-60.
17. Rossi A.C., Pluijmert M., Bovendeerd P.H. et al. Assessment and comparison of left ventricular shear in normal and situs inversus totalis hearts by means of magnetic resonance tagging. Am J Physiol Heart Circ Physiol. 2015 Mar 1. 308 (5): H416-23.
18. Kouwenhoven J.W., Bartels L.W., Vincken K.L. et al. The relation between organ anatomy and pre-existent vertebral rotation in the normal spine: magnetic resonance imaging study in humans with situs inversus totalis. Spine. 2007 May 1. 32(10): 1123-8.
СТАТТІ ЗА ТЕМОЮ Кардіологія
Як відомо, кальцій бере участь у низці життєво важливих функцій. Хоча більшість досліджень добавок кальцію фокусувалися переважно на стані кісткової тканини та профілактиці остеопорозу, сприятливий вплив цього мінералу є значно ширшим і включає протидію артеріальній гіпертензії (передусім у осіб молодого віку, вагітних та потомства матерів, які приймали достатню кількість кальцію під час вагітності), профілактику колоректальних аденом, зниження вмісту холестерину тощо (Cormick G., Belizan J.M., 2019)....
Торакалгія – симптом, пов’язаний із захворюваннями хребта. Проте біль у грудній клітці може зустрічатися за багатьох інших захворювань, тому лікарям загальної практики важливо проводити ретельну диференційну діагностику цього патологічного стану та своєчасно визначати, в яких випадках торакалгії необхідна консультація невролога. В березні відбувся семінар «Академія сімейного лікаря. Біль у грудній клітці. Алгоритм дій сімейного лікаря та перенаправлення до профільного спеціаліста». Слово мала завідувачка кафедри неврології Харківського національного медичного університету, доктор медичних наук, професор Олена Леонідівна Товажнянська з доповіддю «Торакалгія. Коли потрібен невролог»....
Рівень ліпопротеїну (a) >50 мг/дл спостерігається в ≈20-25% населення і пов’язаний із підвищеним ризиком серцево-судинних захворювань (ССЗ) [1]. Ліпопротеїн (a) задіяний в атерогенезі та судинному запаленні, а також може відігравати певну роль у тромбозі через антифібринолітичну дію і взаємодію із тромбоцитами [2, 3]. Дієта та фізична активність не впливають на рівень ліпопротеїну (a); специфічної терапії для його зниження також не існує. Підвищений ризик ССЗ, пов’язаний з ліпопротеїном (а), залишається навіть у пацієнтів, які приймають статини [4]. Саме тому існує критична потреба в терапії для зниження цього ризику, особливо в первинній профілактиці. ...
Запалення відіграє важливу роль у розвитку багатьох хронічних захворювань, зокрема атеросклерозу. Нещодавно було встановлено, що гіперурикемія спричиняє запалення ендотеліальних клітин судин, ендотеліальну дисфункцію та, зрештою, атеросклероз. Експериментальна робота Mizuno та співавт. (2019), у якій було продемонстровано здатність фебуксостату пригнічувати запальні цитокіни, привернула увагу дослідників до протизапальних ефектів уратзнижувальних препаратів. Кількість лейкоцитів – надійний маркер запалення, пов’язаний із різними кардіоваскулярними захворюваннями, як-от ішемічна хвороба серця; у багатьох попередніх дослідженнях його використовували для оцінки протизапального ефекту терапевтичного втручання. Мета нового аналізу дослідження PRIZE – вивчити вплив фебуксостату на кількість лейкоцитів у пацієнтів із безсимптомною гіперурикемією....