2 липня, 2023
Сечова кислота та серцево-судинні захворювання: докази і терапевтичні підходи
Патофізіологічні процеси, спричинені сечовою кислотою (СК), у т. ч. запалення та окислювальний стрес, відіграють ключову роль у патогенезі низки серцево-судинних захворювань (ССЗ). Крім того, чимало епідеміологічних досліджень продемонстрували зв’язок між рівнем СК у плазмі та багатьма факторами ризику ССЗ. Звіт дослідницького центру Національної асоціації лікарів-кардіологів (ANMCO, Італія) надає оновлену інформацію щодо зв’язку між підвищеним рівнем СК у плазмі крові та ризиком ССЗ, а також безпеки й ефективності препаратів, що знижують рівень СК. Узагальнено практичні показання до застосування уратзнижувальних препаратів в осіб групи ризику чи в пацієнтів із ССЗ.
СК – кінцевий продукт катаболізму пуринів. Підвищення показників СК у плазмі крові може відбуватися внаслідок її збільшеного синтезу чи зменшення виведення. З патофізіологічного погляду найвідомішим наслідком стійкої гіперурикемії є типове накопичення кристалів уратів у суглобах із подальшим розвитком подагри. Підвищення рівня СК у плазмі також може зумовити розвиток подагричного артриту та сечокам’яної хвороби. Крім того, патофізіологічні процеси, спричинені підвищенням рівня СК, як-от запалення та окислювальний стрес, відіграють важливу роль у патогенезі багатьох ССЗ [1-3]. Хоча за результатами проведення численних клінічних досліджень задокументовано зв’язок між підвищеним рівнем СК і факторами серцево-судинного ризику, як-от артеріальна гіпертензія, ожиріння, метаболічний синдром, дисліпідемія, хронічна хвороба нирок, епідеміологічні дослідження з оцінки потенційного впливу гіперурикемії на серцево-судинний ризик надали суперечливі результати [4]. З огляду на високу поширеність подагри та гіперурикемії серед дорослого населення (1-4 та до 20% відповідно в популяції США), поширеність яких поступово зростала впродовж останніх десятиліть, важливо надати оновлену інформацію про наявні дані щодо зв’язку між високими концентраціями СК у плазмі та ризиком ССЗ, а також про ефективність і безпеку фармакологічних засобів, що застосовуються для зниження рівня СК у крові [7].
СК і серцево-судинний ризик: патофізіологічні механізми
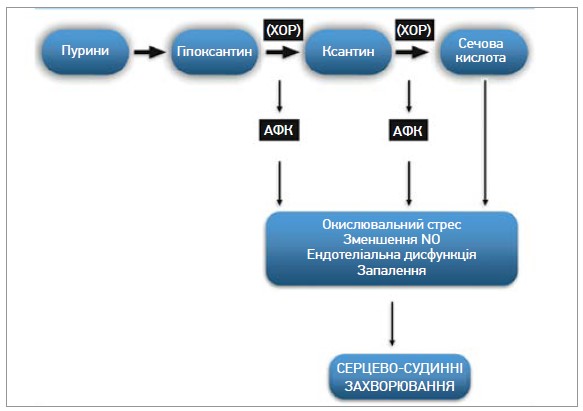
Синтез СК регулюється ферментом ксантиноксидоредуктазою (КОР), який перетворює гіпоксантин на ксантин, а ксантин – на СК (рис. 1).
Рис. 1. Роль СК у патогенезі ССЗ
КОР існує у двох взаємоперетворюваних формах: ксантиндегідрогеназа, яка використовує як акцептор електронів нікотинамідаденіндинуклеотид (NAD+), і ксантиноксидаза, що використовує як акцептор електронів молекулярний кисень, спричиняючи в такий спосіб утворення активних форм кисню (АФК). Отже, з підвищенням активності ксантиноксидази й утворенням СК відбувається супутнє продукування АФК, які, сприяючи окисленню ліпідів і знижуючи біодоступність оксиду азоту, чинять шкідливий вплив на функцію ендотелію [1]. Крім того, КОР також зумовлює поглинання холестерину ліпопротеїдів низької щільності макрофагами, що сприяє їхньому перетворенню на пінисті клітини, а також має вирішальне значення в патогенезі атеросклеротичних уражень [8] (рис. 2).
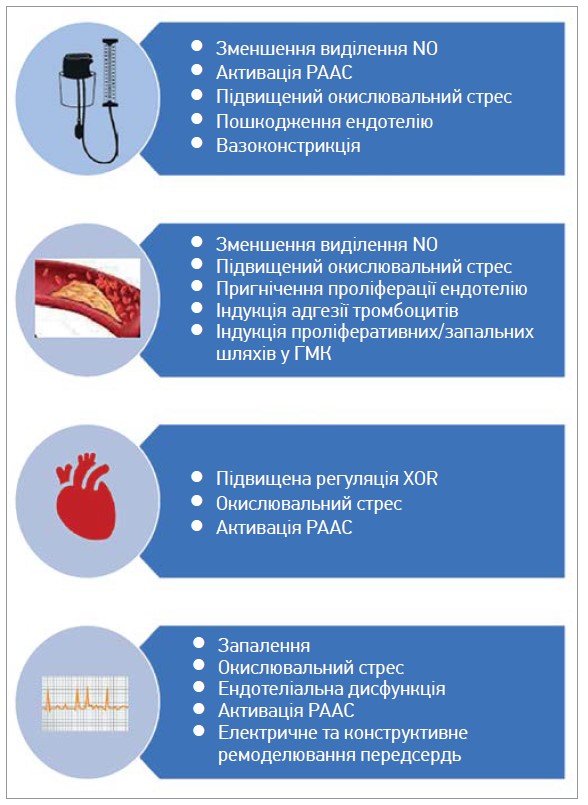
Рис. 2. Основні механізми впливу СК на патогенез ССЗ
Примітка: ГМК – гладком’язові клітини.
Крім того, експериментальні дослідження свідчать про те, що СК під час проникнення до ендотеліальних клітин завдяки відповідним транспортерам зумовлює ендотеліальну дисфункцію [1]. Ще одним потенційним механізмом, який пояснює зв’язок між гіперурикемією та ССЗ, є спричинена відкладеннями уратів активація запалення [12].
З іншого боку, СК має антиоксидантні властивості. Епідеміологічні дослідження показали, що ризик ССЗ є більшим у популяціях з особливо низьким або дуже високим рівнем СК [1, 13]. Також було висунуто гіпотезу, що в пацієнтів із ССЗ підвищення рівня СК можна вважати компенсаторним механізмом підвищеного окисного стресу, наявного за цих станів [1].
Нижче наведено деякі доступні клінічні докази зв’язку між СК та основними ССЗ.
Артеріальна гіпертензія
За результатами декількох досліджень повідомлено про кореляцію між гіперурикемією та артеріальною гіпертензією [2]. У великій популяції осіб (n=96 606) без факторів ризику чи ССЗ підвищення показників СК у крові асоціювалося зі зростанням ризику розвитку гіпертензії [14]. Згідно з результатами аналізу даних 1720 осіб з артеріальною гіпертензією та без ССЗ, внесених до Проєкту амбулаторного моніторингу гіпертензії в Умбрії (Італія), виявлено, що зв’язок між рівнями СК у плазмі та серцево-судинними подіями, серцево-судинною смертю, смертю від усіх причин має вигляд J‑подібної кривої з найбільшою частотою подій у квартилях із найнижчими й найвищими рівнями СК у плазмі [15]. Метааналіз, який включав 55 607 пацієнтів (середній вік складав 44 роки), продемонстрував, що ризик розвитку артеріальної гіпертензії зростає на 13% із кожним збільшенням рівня СК на 1 мг/дл [16].
Експериментальні дослідження показують, що СК пригнічує вивільнення оксиду азоту з ендотелію та активує ренін-ангіотензин-альдостеронову систему (РААС), що спричиняє вазоконстрикторний ефект. Цей вплив можна усунути призначенням препаратів, що знижують рівень СК у плазмі. На пізнішій стадії СК, проникаючи до клітин гладких м’язів судин, індукує проліферативну відповідь та сприяє атерогенезу. Загалом дослідження на тваринних моделях і клінічні випробування показали, що наявність гіперурикемії (після поправки на інші незалежні фактори ризику) передує розвитку артеріальної гіпертензії [1, 18]. Дослідження генетичних варіантів гена SLC2A9, який кодує білок-транспортер СК і бере участь у забезпеченні гомеостазу СК, продемонстрував, що зниження рівня СК на кожні 0,44 мг/дл у сироватці крові пов’язане зі зниженням систолічного артеріального тиску 2,2 або 1,5 мм рт. ст. залежно від високого чи низького споживання натрію [19].
Із 2018 року до рекомендацій Європейського товариства кардіологів і Європейського товариства гіпертензії СК внесено до факторів, що впливають на серцево-судинний ризик пацієнтів з артеріальною гіпертензією, а також у цих рекомендаціях надано пораду оцінювати рівень СК як складову скринінгу гіпертонічної хвороби [20].
Ішемічна хвороба серця
Численні дослідження свідчать про те, що гіперурикемія корелює з ризиком ішемічної хвороби серця (ІХС). Роттердамське дослідження, проведене за участю пацієнтів без судинних захворювань, продемонструвало, що гіперурикемія пов’язана з підвищеним ризиком інфаркту міокарда й інсульту [21]. Подальший метааналіз показав, що збільшення рівня СК на кожні 1 мг/дл зумовлює зростання ризику ІХС і смертності від усіх причин на 20 і 9% відповідно [22].
Гіперурикемія також є незалежним фактором ризику розвитку субклінічного коронарного атеросклерозу в популяції здорових молодих осіб [23].
У хворих, які вже страждають на ІХС, гіперурикемія асоціюється з підвищеною смертністю та ризиком несприятливих подій [24]. У великому дослідженні пацієнтів із критичним коронарним стенозом (≥75%) було виявлено, що гіперурикемія – незалежний предиктор розвитку серцево-судинних подій і смертності від усіх причин [25]. Гіперурикемія також пов’язана з наявністю коронарних бляшок і підвищеним умістом ліпідів [26, 27].
Аналіз даних італійського реєстру START (STable coronary Artery disease RegisTry), проведений на пацієнтах із хронічним коронарним синдромом, показав, що вищі показники СК у сироватці крові пов’язані з більшим тягарем ССЗ [28].
Отже, гіперурикемія є станом, пов’язаним із підвищеним ризиком ІХС і несприятливішим прогнозом її перебігу.
Серцева недостатність
Гіперурикемія часто зустрічається в пацієнтів із серцевою недостатністю (СН). У когорті з 1869 пацієнтів, госпіталізованих у зв’язку із СН, більше половини (56%) мали підвищений рівень СК (≥7,4 мг/дл) [29].
Декілька досліджень показали, що гіперурикемія пов’язана із СН. У дослідженні Framingham Offspring частота СН була в 6 разів вищою в пацієнтів із рівнем СК у верхньому квартилі (>6,3 мг/дл), ніж в осіб із рівнем СК у нижньому квартилі (<3,4 мг/дл) [30]. Подальший метааналіз продемонстрував, що зі збільшенням рівня СК на кожні 1 мг/дл спостерігається зростання ймовірності розвитку СН на 19%, а серед пацієнтів із СН – підвищення показників смертності на 4% [30]. Гіперурикемія також асоціюється з гіршим функціональним класом СН за класифікацією Нью-Йоркської кардіологічної асоціації, нижчою фізичною здатністю, підвищеним споживанням кисню, діастолічною дисфункцією та кахексією [32-34].
Найімовірніше, в основі зв’язку між гіперурикемією та СН є посилення КОР, активація РААС і застосування діуретиків, які можуть зменшити виведення СК.
Миготлива аритмія
Останні дослідження продемонстрували чіткий зв’язок між гіперурикемією та ризиком фібриляції передсердь (ФП) [37]. Дослідження ARIC показало, що підвищений рівень СК у крові асоціюється зі зростанням ризику ФП у 1,16 раза, сильнішим зв’язком між рівнем СК та ФП у жінок [38].
Патогенетичний механізм такого зв’язку остаточно не вивчено, втім, було продемонстровано, що гіперурикемія може відігравати певну роль у ремоделюванні передсердь (як електричного – з укороченням рефрактерного періоду передсердь, так і структурного – з уповільненням провідності), сприяючи створенню контурів повторного входу [39]. Вважають, що ремоделюванню сприяють через запалення, окислювальний стрес, ендотеліальну дисфункцію та активацію РААС.
Зниження серцево-судинного ризику за допомогою уратзнижувальних препаратів
З огляду на зв’язок між гіперурикемією та серцево-судинним ризиком було проведено чимало клінічних досліджень, спрямованих на вивчення впливу препаратів, які знижують рівень СК, на серцево-судинний ризик [21, 27, 29, 40-42]. Більшість з них було присвячено вивченню інгібіторів ксантиноксидази (фебуксостат, алопуринол), які здатні зменшувати синтез СК.
Результати клінічних досліджень продемонстрували, що алопуринол, крім зниження синтезу СК, зменшує окислювальний стрес і завдяки цьому покращує ендотеліальну функцію [42]. У пацієнтів з артеріальною гіпертензією алопуринол поліпшував потокзалежну вазодилатацію [43].
Селективний інгібітор ксантиноксидази фебуксостат, нещодавно введений у клінічну практику, виявився ефективнішим за алопуринол щодо зниження рівня СК у плазмі [48]. В першому рандомізованому подвійному сліпому дослідженні було показано, що фебуксостат не поступається алопуринолу щодо частоти серцево-судинних подій, але пов’язаний з підвищенням загальної та серцево-судинної смертності [49]. Втім, цей результат не був підтверджений подальшими клінічними дослідженнями. Зокрема, рандомізоване відкрите сліпе дослідження FAST (Febuxostat versus Allopurinol Streamlined Trial) не повідомляло про підвищений ризик смерті на тлі застосування фебуксостату. Навпаки, частка смертей у групі фебуксостату виявилася нижчою, ніж у групі алопуринолу [50]. В рандомізованому відкритому сліпому дослідженні кінцевої точки FREED (Febuxostat for Cerebral and CaRdiorenovascular Events PrevEnTy Study) призначення фебуксостату зумовило значне зниження частоти комбінованої кінцевої точки – церебральних, серцево-судинних, ниркових подій та загальної смертності [51]. Продемонстровано, що фебуксостат сприяє уповільненню прогресування ураження нирок. Результати метааналізу 16 клінічних випробувань (загалом 257 851 пацієнт) свідчать про те, що лікування фебуксостатом асоціюється із кращим загальним результатом без статистично значущої різниці щодо серцево-судинної смертності та смертності від усіх причин [52]. Інше велике обсерваційне випробування продемонструвало, що терапія фебуксостатом порівняно з алопуринолом не спричиняє підвищення ризику ССЗ або показників смертності в пацієнтів із подагрою та серцево-судиною патологією або без неї [53].
Практичні настанови щодо управління серцево-судинним ризиком
З огляду на те що серцево-судинний ризик прогресивно зростає зі збільшенням рівня СК, у клінічній практиці визначення порогових її значень може бути корисним для виявлення пацієнтів підвищеного ризику. В обсерваційному дослідженні URRAH (Uric Acid Right for Heart Health), яке включало дані 22 714 осіб, рівень СК >5,6 мг/дл (що нижче за терапевтичну ціль, зазначену в європейських рекомендаціях із лікування подагри <6 мг/дл) асоціювався з підвищеним ризиком смертності від ССЗ [54, 55].
Згідно з європейськими рекомендаціями з лікування подагри, застосування препаратів, що знижують рівень СК, показано всім пацієнтам із рецидивувальними епізодами подагри (>2/рік), уратною артропатією або літіазом сечовивідних шляхів, обумовленим відкладанням уратів. Ранній початок терапії показаний також молодим пацієнтам (віком <40 років) з особливо високим рівнем СК (>8 мг/дл) або супутніми ССЗ (артеріальна гіпертензія, хронічна хвороба нирок, ІХС, СН) [55]. Як підкреслюється в останніх рекомендаціях Європейської протиревматичної ліги (EULAR), відтермінування початку лікування гіперурикемії спричиняє постійне зростання рівня СК, що може мати шкідливий вплив на серцево-судинну систему та нирки. Під час лікування слід проводити періодичний моніторинг рівня СК, який варто підтримувати на рівні <6 мг/дл. Із метою пришвидшення розчинення уратних відкладень слід розглянути жорсткішу терапевтичну ціль (<5 мг/дл) [55].
Прийом усіх препаратів, що знижують рівень СК, варто розпочинати з найнижчої дози та титрувати до цільової. Значення СК <6 мг/дл необхідно підтримувати впродовж усього життя.
Відповідно до міжнародних рекомендацій за нормальної функції нирок препаратом першого вибору є алопуринол. Його призначення розпочинають з дози 100 мг/добу, збільшуючи її за потреби на 100 мг/добу кожні 2-4 тиж (середня доза – 300 мг) [55, 56].
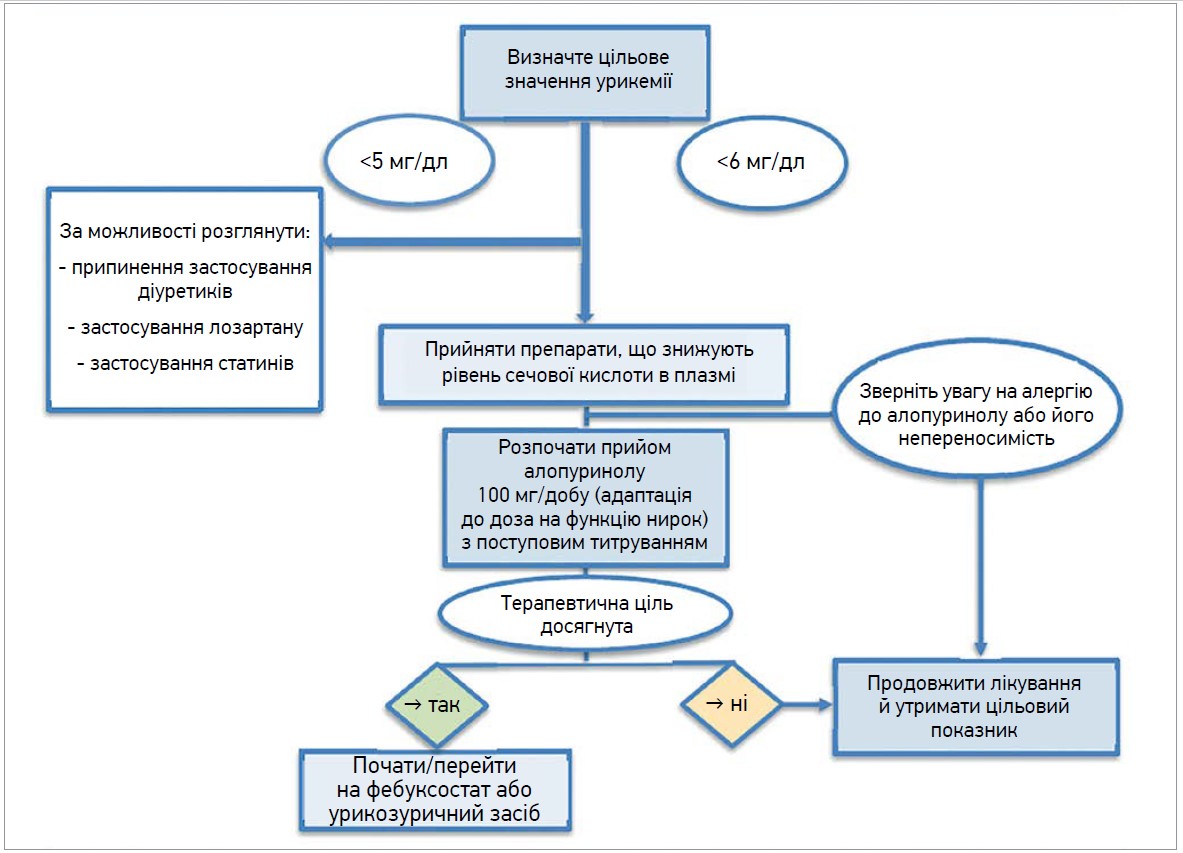
Якщо за допомогою алопуринолу цільових рівнів СК досягти не вдається, препарат слід замінити фебуксостатом або іншим урикозуричним засобом (рис. 3).
Рис. 3. Алгоритм призначення препаратів, що знижують рівень СК
Фебуксостат також показаний за поганої переносимості алопуринолу. Що стосується зниження рівня СК у сироватці крові, то добова доза фебуксостату в 40 мг порівнюється з дозою в 300 мг алопуринолу, досягаючи вираженішого (порівняно з алопуринолом) зниження при терапевтичних дозах 80 та 120 мг/день [57].
Висновки
СК може активувати різні патофізіологічні механізми, які беруть участь у патогенезі ССЗ. Наявність доказів зв’язку між високим рівнем СК і факторами ризику / ССЗ свідчить про можливу причинну роль СК у генезі / прогресуванні серцево-судинної патології. Сьогодні медикаментозна корекція рівня СК показана лише за наявності гіперурикемії або її клінічних проявів в анамнезі. Втім, уратзнижувальну терапію слід розглядати на ранніх стадіях у пацієнтів із ССЗ, а також в осіб із факторами ризику.
Довідка «ЗУ»
На вітчизняному фармацевтичному ринку фебуксостат представлений препаратом Подафеб виробництва АТ «Київський вітамінний завод». Це єдиний фебуксостат українського виробництва. Подафеб випускається в таблетках із дозуванням по 80 та 120 мг, що полегшує титрування. Препарат показаний для лікування пацієнтів із хронічною гіперурикемією при захворюваннях, які супроводжуються відкладанням кристалів уратів, у т. ч. за наявності тофусів та/або подагричного артриту на цей час чи в анамнезі, а також для терапії та профілактики гіперурикемії в дорослих пацієнтів, котрі отримують хіміотерапію щодо гематологічних злоякісних новоутворень із помірним або високим ризиком синдрому лізису пухлини. Слід зазначити, що Подафеб є біоеквівалентним оригінальному фебуксостату.
Згідно з останніми міжнародними рекомендаціями, фебукостат є препаратом другої лінії уратзнижувальної терапії при гіперурикемії та подагрі. Він також може використовуватися при непереносимості алопуринолу (FitzGerald J.D. et al., 2020). Варто зауважити, що фебуксостат дозволено приймати пацієнтам із хронічною хворобою нирок, оскільки він метаболізується печінкою. Крім того, фебуксостат має доведені ренопротективні властивості (Kim S. et al., 2017).
Di Fusco S.A., Castello L., Marino G. et al. Statement ANMCO:
Acido urico e malattiecardiovascolari: evidenze e approccio terapeutico.Gital Cardiol/VOL 24/Giungo 2023.
Адаптований переклад з італ. Наталії Александрук
Медична газета «Здоров’я України 21 сторіччя» № 10 (546), 2023 р.